David Castro C. 1
Rev Chil Anest Vol. 40 Núm. 3 pp. 192-202|doi:
PDF|ePub|RIS
ANTECEDENTES
Para producir anestesia regional (AR) es necesario depositar anestésico local (AL) en la proximidad de las fibras nerviosas que se desea anestesiar. Ello requiere conocer el trayecto y la localización de esas fibras en cada paciente específico.
El avance de la AR ha buscado desarrollar nuevas técnicas que permitan localizar las estructuras nerviosas de modo de aumentar la tasa de éxito de los procedimientos y reducir sus complicaciones asociadas.
Durante la segunda mitad del siglo pasado pudimos observar, en primer lugar, el paso de la técnica basada en reparos anatómicos a la técnica basada en la provocación de parestesias 1 . Este paso fue considerado un avance con el que se esperaba mejorar la tasa de éxito, sin embargo, siguió habiendo reportes y casuísticas que daban cuenta de fracasos de la técnica y casos de complicaciones neurológicas asociadas.
Algunos años después, asistimos al paso de la técnica basada en provocación de parestesias a la técnica basada en la neuroestimulación (NE) 2 . Con ello se esperaba aumentar aún más la tasa de éxito y muy especialmente se esperaba reducir la tasa de complicaciones neurológicas. El aumento en la tasa global de éxito (sin distinguir entre distintos territorios nerviosos) pudo ser documentado 3 llegando a alrededor de 95% (cuando los procedimientos eran realizados por expertos). La reducción en la tasa de complicaciones, sin embargo, nunca fue adecuadamente demostrada.
Hacia fines del siglo, la comunidad anestesiológica reconocía a la NE como “gold standard” para la realización de anestesia de plexos nerviosos y nervios periféricos 4 .
La literatura médica siguió informando de un cierto número de fracasos, reportes de intoxicación por AL y casos de complicaciones neurológicas 5 .
A comienzos del presente siglo, el desarrollo científico y tecnológico permitió empezar a usar el ultrasonido (US) para visualizar las estructuras nerviosas, las agujas y la inyección de AL en la proximidad de los nervios. Esta nueva posibilidad fue seguida de un gran número de publicaciones ensayando la técnica y reportando prometedores resultados 6 , 7 , 8 (Figura 1).
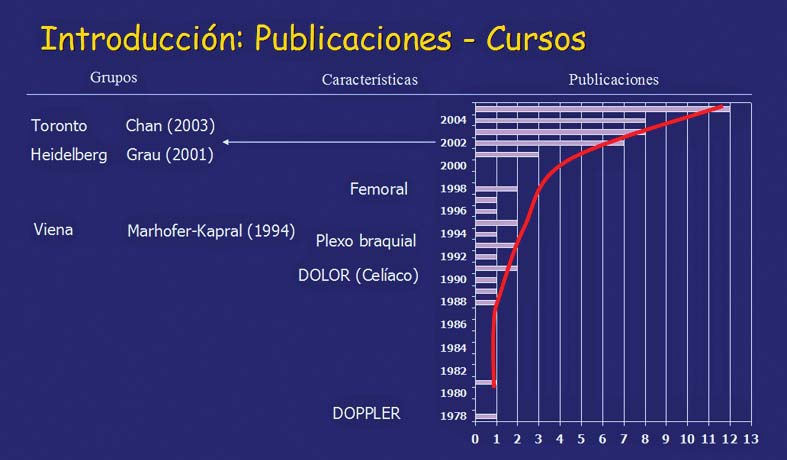
Figura 1 El gráfico muestra la progresión del número de publicaciones que refieren el uso de US para procedimientos de AR desde el año 1978 hasta el año 2004 (Tomado del Dr. Sala Blanch, Barcelona, 2007).
En el año 2006, la Sociedad Americana de Anestesiología (ASA) publicó su primer texto de introducción a la AR guiada por US 9 ; el mismo año, la Universidad de Barcelona editó su primer texto de ecografía (ECO) para anestesiólogos 10 . En el año 2007, el British Journal of Anaesthesia (BJA) publicó un editorial en que por primera vez se planteó la posibilidad de que la técnica guiada por US sea el nuevo “gold standard” en AR 11 ; luego, en diciembre del año 2007 la revista Regional Anesthesia and Pain Medicine (RAPM) anunció la creación de una nueva sección de AR guiada por US en sus contenidos. En abril del año 2008 el Acta Anaesthesiologica Scandinavica dio cuenta de la introducción del US en la práctica de la AR 12 .
No obstante, el mismo mes de abril del año 2008 la revista Anesthesiology publicó dos casos de inyección intravascular durante procedimientos de AR guiada por US 13 , 14 y en el editorial del mismo número, los Drs. Hadzic y Sala Blanch, advirtieron que “sería un error descansar en la tecnología y descuidar las estrategias habituales de seguridad”. A lo anterior se han ido sumando paulatinamente reportes aislados de casos de intoxicación por AL y de casos de complicaciones neurológicas postoperatorias.
Las exigencias actuales de ajustar la práctica clínica a la medicina basada en evidencia, han exigido a la técnica guiada por US la demostración de una mayor tasa de éxito y una menor tasa de complicaciones que las obtenidas por la técnica guiada por NE. Teniendo esta última tasas muy altas de éxito y muy bajas de complicaciones, no ha sido fácil para el US mostrar los resultados exigidos, lo cual ha sido fuente de un interesante debate sobre las exigencias impuestas al desarrollo de nuevas herramientas.
Con todo, a la luz de los meta-análisis de los últimos años, la AR guiada por US ha mostrado ya, en algunas áreas, superioridad a las técnicas anteriores, ha puesto en duda la interpretación de la respuesta a la NE y ha puesto en jaque las teorías sostenidas hasta comienzos de este siglo sobre las causas del daño neurológico asociado a las técnicas anestésicas 4 , 15 , 16 , 17 .
Las exigencias actuales de ajustar la práctica clínica a la medicina basada en evidencia, han exigido a la técnica guiada por US la demostración de una mayor tasa de éxito y una menor tasa de complicaciones que las obtenidas por la técnica guiada por NE. Teniendo esta última tasas muy altas de éxito y muy bajas de complicaciones, no ha sido fácil para el US mostrar los resultados exigidos, lo cual ha sido fuente de un interesante debate sobre las exigencias impuestas al desarrollo de nuevas herramientas.
Con todo, a la luz de los meta-análisis de los últimos años, la AR guiada por US ha mostrado ya, en algunas áreas, superioridad a las técnicas anteriores, ha puesto en duda la interpretación de la respuesta a la NE y ha puesto en jaque las teorías sostenidas hasta comienzos de este siglo sobre las causas del daño neurológico asociado a las técnicas anestésicas4,15,16,17.
Estado del arte
En el año 2008, la Sociedad Americana de Anestesia Regional (ASRA) encargó a un grupo de 12 expertos un análisis con metodología de medicina basada en evidencia de todos los trabajos publicados en los últimos 20 años sobre AR guiada por US. Los resultados de este estudio fueron publicados en un suplemento especial de RAPM, en su edición de marzo-abril de 2010 15 . Para la graduación de la evidencia se usó la escala propuesta por la Agencia de Políticas de Salud e Investigación del Departamento de Salud y Servicios Humanos de los Estados Unidos 18 .
En este análisis, de 211 trabajos preseleccionados, sólo 25 superaron los estrictos criterios de exclusión. Tras el análisis global de los datos, los expertos concluyeron que la AR guiada por US es superior a las otras técnicas por cuanto mejora las características de los bloqueos, aunque de manera diferente dependiendo de cada tipo de bloqueo regional. Del mismo modo, la evidencia para sostener que la técnica es más segura está “aún restringida a fenómenos indirectos asociados con las complicaciones graves”.
Al analizar separadamente el resultado de los bloqueos regionales de extremidad superior, encontraron evidencia de grado A, nivel I-b que permite sostener una disminución en la latencia de los bloqueos y con el mismo grado de evidencia, una mayor tasa de éxito medida sólo a través de fenómenos indirectos. El análisis de los resultados de los bloqueos regionales de extremidad inferior encontraron también con una evidencia de grado A, nivel I-b una mayor tasa de éxito medida en forma directa, una menor latencia de los bloqueos y la necesidad de menor volumen de solución anestésica. El estudio no tuvo potencia suficiente para sostener otras ventajas.
El análisis de los resultados de los bloqueos de pared torácica y abdominal llegó a menos conclusiones por falta de datos suficientes.
El análisis de los datos relacionados con bloqueos neuroaxiales halló diversos grados de evidencia de que el US es superior a la palpación para determinar el nivel intervertebral y de que el US es muy fidedigno para determinar la distancia desde la piel al espacio peridural. Un estudio permitió tener evidencia que, en pacientes obstétricas, la técnica ecográfica requiere menos intentos para encontrar el espacio peridural que la técnica convencional, aunque la tasa de éxito fue igual.
En población pediátrica se halló evidencia grado A, nivel I-b de mayor tasa de éxito de la técnica guiada por US sobre la tradicional para los bloqueos de pared abdominal anterior y en particular, para los bloqueos de nervios iliohipogástrico-ilioinguinal.
El estudio analiza también la evidencia existente en relación al uso de la técnica guiada por US para procedimientos empleados en el tratamiento del dolor crónico. Los estudios de factibilidad han mostrado la utilidad del US para realizar bloqueos de raíces cervicales específicas y bloqueos de ganglio estrellado. No obstante, no existe hasta esa fecha estudios comparativos con fluoroscopía. El único estudio aleatorizado y controlado publicado que compara el US con la tomografía computarizada para la realización de bloqueos facetarios lumbares, halla evidencia grado I-b de que el US se asocia con menor tiempo de procedimiento y menor exposición a la radiación, pero similares resultados en el alivio del dolor del paciente.
Respecto de las complicaciones, el análisis no halló evidencia de una menor tasa de complicaciones neurológicas. Sí encontró evidencia I-a de disminución del número de punciones vasculares pero, como era de esperar, datos insuficientes para hallar menor frecuencia de intoxicación por AL.
Los expertos concluyen su estudio sosteniendo que el US es un gran avance en el progreso de la AR, que la mayoría de los estudios encontró que la técnica ecográfica es superior o igual a las otras y que ningún estudio mostró inferioridad del US al compararlo con otras. Sostienen que es posible que nunca se evidencie si efectivamente produce una disminución en la frecuencia de daño neurológico puesto que esta ya es muy baja y que la técnica anestésica es sólo uno de los factores que conllevan al daño neurológico. Creen que sí es factible que en el futuro se evidencie disminución de otros riesgos. Por último, enfatizan que la técnica es sólo uno de los factores que inciden en el resultado de la AR y que no sustituye al conocimiento, entrenamiento, criterio, experiencia y responsabilidad del especialista.
Después de la publicación de este estudio, varios trabajos y editoriales publicados en revistas de alto impacto, concuerdan en que hasta hoy no se ha demostrado una disminución en la tasa de complicaciones y han avanzado en nuevos desafíos 4 . Las publicaciones de los años 2010 y lo que ha trascurrido del 2011 se avocan a estudiar las dosis de AL, la ahora “real posibilidad” de disminuirlas y la conveniencia teórica de hacerlo. Actualmente se profundiza en analizar la significación de la inyección subepineural, la dificultad de prevenirla (incluso la incierta necesidad de prevenirla), y su “no demostrada” peligrosidad.
Un editorial del BJA de mayo de 2010 escrito por P. Marhofer, uno de los precursores de la técnica guiada por US, sostiene que esta no ha sido diseñada para ser practicada por un pequeño grupo de anestesiólogos expertos sino para aumentar el número de especialistas que puedan practicarla 19 . Esta afirmación, no obstante ser solo la aspiración del autor, pone de relieve la posibilidad, ya enunciada por algunos expertos 4 de un nuevo despertar del interés de muchos anestesiólogos por las técnicas de AR, lo que, de ser real, podría incidir no sólo en el bienestar de los pacientes sino también en las tendencias, resultados, tasas de éxito y complicaciones. El autor enfatiza la necesidad de un adecuado entrenamiento en el uso de la técnica.
La misma editorial referida analiza las implicancias económicas de la introducción de la técnica ecográfica. Pocos estudios han aportado evidencia que permita pronunciarse sobre esta materia. El último trabajo sistemático al respecto es el realizado por S. Liu, publicado en RAPM en febrero de 2010 4 , que mediante un trabajo de simulación compara la neuroestimulación con la ecografía en cuatro escenarios clínicos en que se pueden realizar bloqueos nerviosos. El estudio concluye que la implementación de la técnica ecográfica es, financieramente hablando, altamente competitiva en un escenario de cirugía ambulatoria pero que su competitividad desaparece en los pacientes hospitalizados. Pocos meses después, Marhofer, en el volumen de octubre de 2010 del Current Opinion in Anesthesiology 20 argumenta la necesidad de incluir todos los costos perioperatorios en el análisis económico asociado a la técnica.
Los artículos publicados en los últimos meses aportan nueva evidencia sobre el menor volumen de solución anestésica con la técnica ecográfica 20 . Mc Naught en la edición de enero de 2011 del BJA muestra en un trabajo bien realizado la necesidad de menores volúmenes de AL y menor número de avances de la aguja con US que con NE 21 .
Recomendaciones para el aprendizaje
Bastante ha sido escrito sobre el proceso de enseñanza-aprendizaje para la anestesia regional guiada por US 22 – 33 .
La literatura especializada ha mostrado (y la práctica clínica lo confirma) que el acercamiento al aprendizaje es distinto entre los anestesiólogos con experiencia y los residentes de anestesiología 32 . Los primeros tienden a observar a un experto hacer algunos procedimientos, luego tratan de reproducir en sus pacientes lo observado y luego comparten su experiencia con otros colegas 34 . Los residentes, en cambio, sometidos a un programa de estudio, suelen hacer primero un estudio teórico, luego practicar en tejido animal o fantoma y luego iniciar una práctica clínica supervisada hasta lograr algún “expertise” mínimo preestablecido 31 . Es significativo que, después de un período de entrenamiento, ambos grupos de aprendices cometen un significativo número de errores en sus procedimientos 28 . ASRA, ESRA y los expertos más prestigiosos en el tema, coinciden en recomendar que el aprendizaje comprenda la mayor parte posible de las siguientes etapas 30 – 32 , 35 – 37 :
- Aprendizaje Preclínico:
- Nociones de ultrasonido.
- Manejo de la ergonomía.
- Manejo del ecógrafo.
-
Conocimiento de imágenes ecográficas de anatomía normal.
-
Adquisición de destreza de la mano que hace examen ecográfico.
-
Adquisición de destreza de la mano que punciona.
-
Integración cerebro-manual: guiarse por 2D para moverse en 3D.
- Aprendizaje Clínico:
- Realizar algún número de casos.
- Realizar alguna variedad de bloqueos.
Aprendizaje preclínico
-
Nociones de ultrasonido
No es el objetivo de este artículo describir los conceptos de la física del ultrasonido. El tema ha sido amplia y detalladamente abordado en la literatura 25 – 27 . Sin embargo, la experiencia recomienda insistir en que el conocimiento de la base física del ultrasonido permite entender y superar problemas cotidianos de la práctica clínica, por ejemplo: no lograr ver estructuras profundas; desaparición de la imagen de un nervio tras un movimiento mínimo del transductor; imágenes sugerentes de ser nervios debajo de las arterias; ausencia de imagen debajo de una línea hiperecogénica; o, al usar Doppler, la ausencia de color o color confuso en una estructura que parece vaso sanguíneo 26 . El conocimiento de los conceptos de frecuencia, amplitud, atenuación, anisotropía, refuerzo posterior, sombra acústica, ángulo de incidencia, frecuencia de tren de pulsos (prf) 26 , 38 , puede permitir comprender y resolver los problemas de imágenes en el teclado del ecógrafo (Figuras 2 a 6).
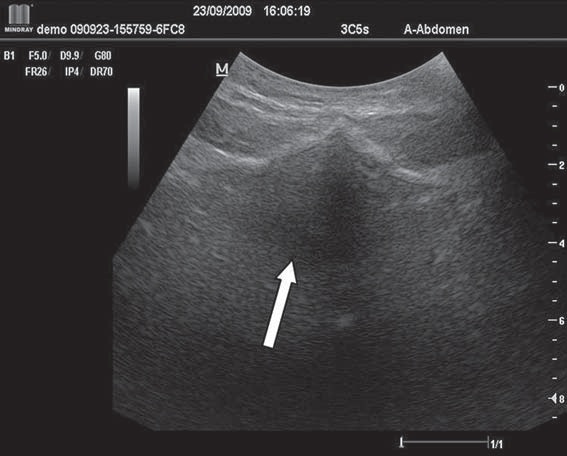
Figura 2 Sombra acústica bajo el hueso sacro.
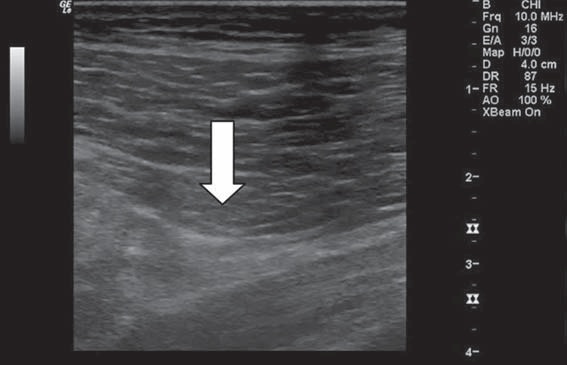
Figura 3 Anisotropía: el mismo nervio ciático subglúteo visto con distinta angulación del transductor.
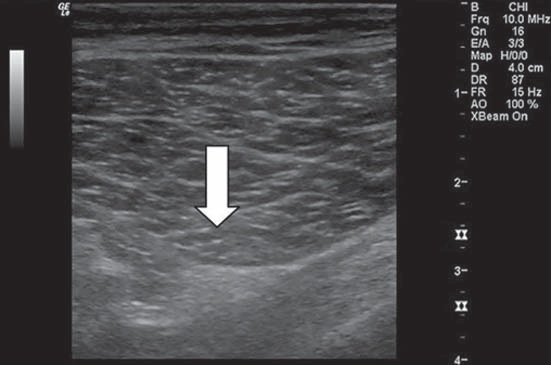
Figura 4 Anisotropía: el mismo nervio ciático subglúteo visto con distinta angulación del transductor.
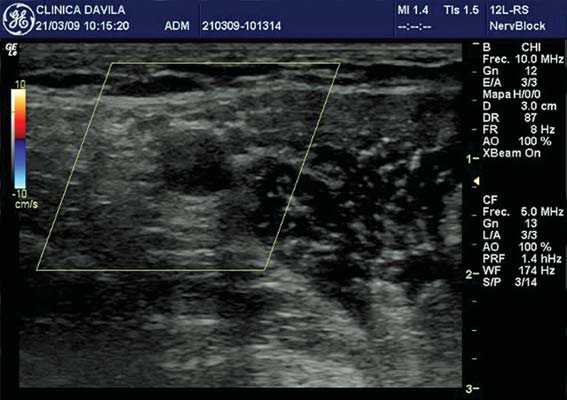
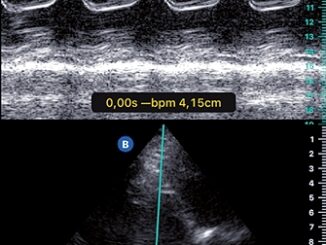
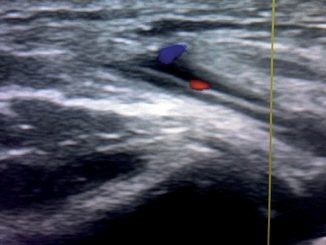
Figura 5 Doppler; los mismos vasos cambiando el ángulo de incidencia del haz de US.
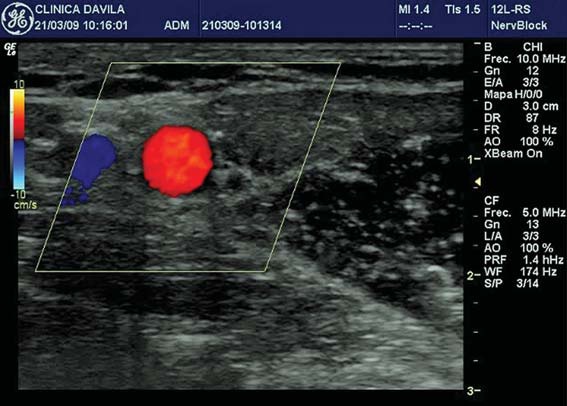
Figura 6 Doppler; los mismos vasos cambiando el ángulo de incidencia del haz de US.
-
Manejo de la ergonomía
La AR y, en particular la guiada por US, requiere movimientos de alta precisión que se realizan con ambas manos 33 . Para ello es necesario elegir la altura de la camilla del paciente, la ubicación espacial del ecógrafo, la ubicación espacial del operador y la postura corporal, del mismo de modo que la tensión muscular de su cuerpo sea la adecuada para evitar que realice movimientos y vibraciones involuntarios que dificulten el procedimiento. Es frecuente observar en el operador una inconveniente rotación del cuello, mala posición de antebrazos y espalda y, por ello, cansancio y movimientos involuntarios del transductor
-
Manejo del ecógrafo
Los distintos modelos y marcas de ecógrafo ofrecen la posibilidad de modificar los diversos parámetros del US para obtener las mejores imágenes posibles. Para lograrlo es necesario conocer sus características básicas y así poder manejarlas en las funciones que ofrece cada equipo 25 , 26 .
Existen diversos modelos de ecógrafo (Figura 7).

Figura 7 Algunos modelos de ecógrafos.
Antes de iniciar un procedimiento 30 , 33 , 39 , es recomendable elegir en el equipo los siguientes parámetros:
-
Tipo de tejido.
-
Frecuencia de US.
-
Profundidad de las estructuras a buscar.
-
Ubicación de la profundidad del/los focos.
-
Determinar una ganancia general.
-
Verificar la disposición de las ganancias temporales.
-
Conocimiento de imágenes ecográficas de anatomía normal
También es necesario conocer y aprender lo que ha sido llamado “sono-anatomía”, es decir, cómo son las imágenes ecográficas de la anatomía normal. Hoy existe en diversos libros, revistas y sitios web (www.asra.com; www.usra.ca; www.nysora.com, etc.) bancos de imágenes ecográficas de las diferentes estructuras nerviosas.
La práctica racional es conocer primero las imágenes digitales y luego ir a reconocer en el modelo humano vivo las imágenes que ya se tiene en la memoria 12 ,30 . (Figuras 8 y 9).
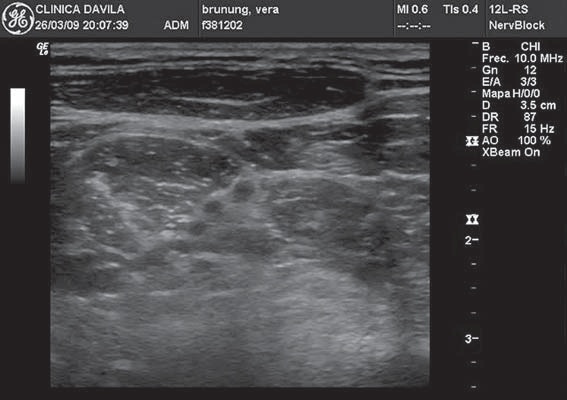
Figura 8 Plexo braquial a nivel interescalénico.
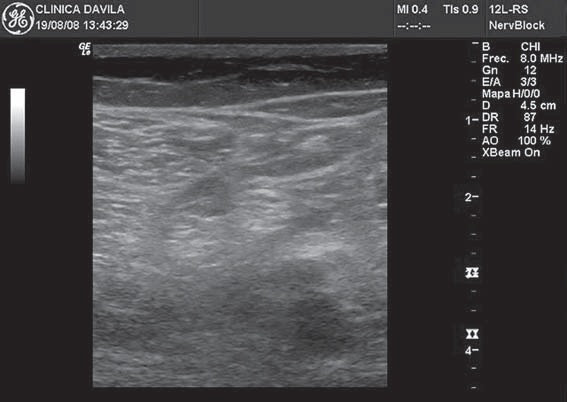
Figura 9 División del nervio ciático poplíteo en los nervios tibial y peroneo.
-
Adquisición de la mano que sostiene y maneja el transductor
La técnica de manejo del transductor también ha sido descrita en la literatura 33 .
Para facilitar la comprensión de los textos puede ser útil recordar los términos utilizados. “Eje corto o transversal” (son lo mismo) o “eje largo o longitudinal” (son lo mismo) se refieren a la relación entre el eje del haz de US (el transductor) y la estructura nerviosa. Los términos “en plano” o “fuera de plano” (se verán posteriormente) se refieren a la relación entre el eje de la aguja de punción y la estructura nerviosa.
Parece necesario insistir en algunos detalles. Es aconsejable que el antebrazo y/o la mano que mueve el transductor estén apoyados (sobre el paciente o la camilla) para evitar la vibración y/o movimientos involuntarios 33 . También, que es recomendable tomar el transductor lo más cerca posible de su base (lejos del cable) para evitar el cansancio y movimientos involuntarios.
Los movimientos posibles del transductor son 5 y la búsqueda de las estructuras nerviosas se hace “jugando” con estos 5 movimientos. Los movimientos deben ser lentos, pues un movimiento rápido del transductor puede enfocar la imagen buscada en un instante y luego perderla. Los movimientos también deben ser pequeños, pues un cambio mínimo de ángulo en la superficie se traduce en un gran cambio de ángulo en la profundidad (Figuras 10-17).
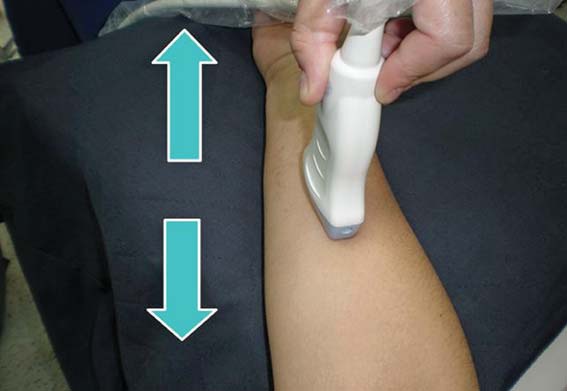
Figura 10 Movimiento 1: desplazamiento en el mismo eje del transductor.
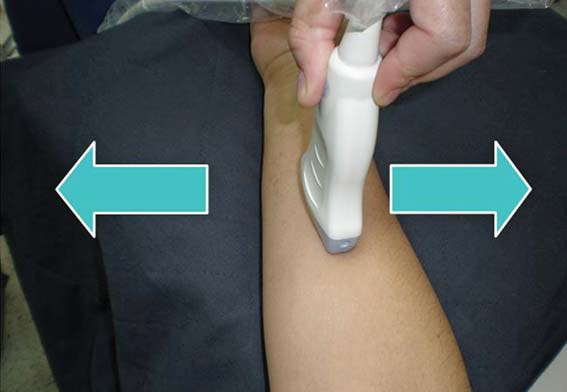
Figura 11 Movimiento 2: desplazamiento perpendicular al eje del transductor.
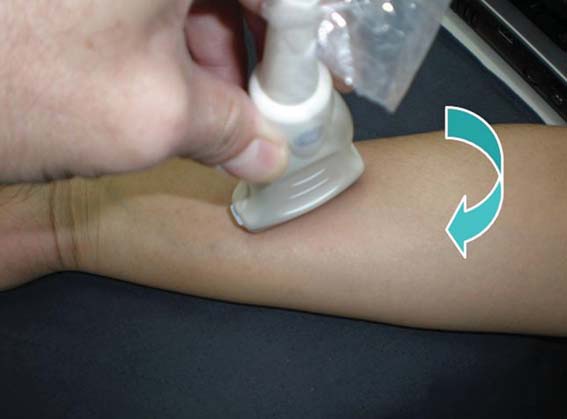
Figura 12 Movimiento 3a: rotación en el sentido de los punteros del reloj.
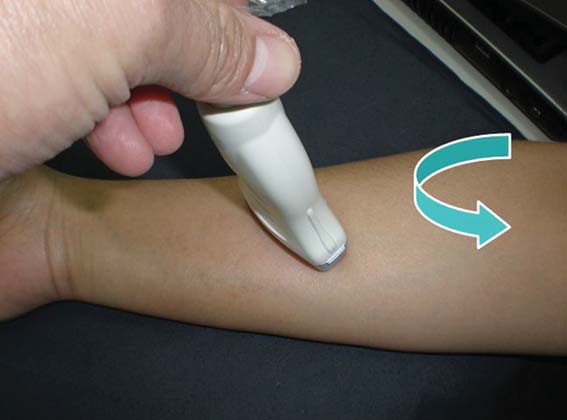
Figura 13 Movimiento 3b: rotación contraria al sentido de los punteros del reloj.
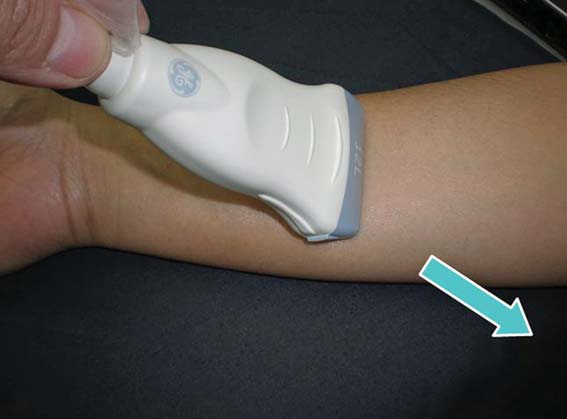
Figura 14 Movimiento 4a: inclinación (tilt) en un sentido.
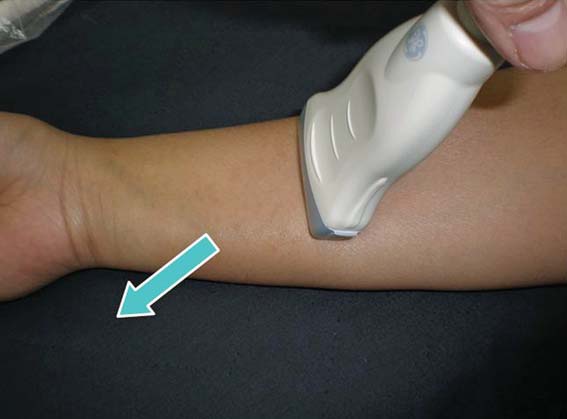
Figura 15 Movimiento 4b: Inclinación (tilt) en sentido contrario.
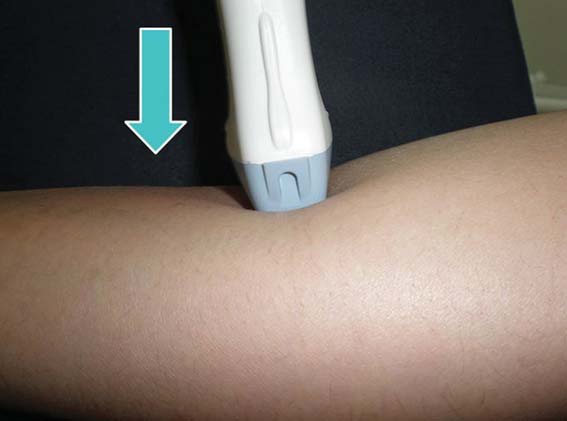
Figura 16 Movimiento 5a: compresión.
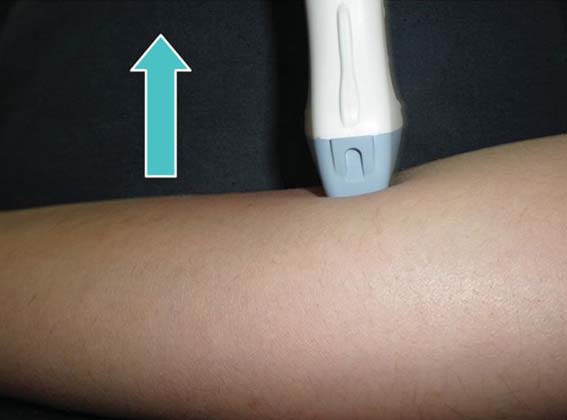
Figura 17 Movimiento 5b: relajación.
-
Adquisición de destreza de la mano que punciona
Como hemos señalado, el abordaje de la punción puede ser “en plano” o “fuera de plano”, decisión que toma el operador antes de puncionar (Figuras 18 y 19).

Figura 18 Punción “en plano”.

Figura 19 Punción “fuera de plano”.
No hay hasta hoy evidencia que permita recomendar en forma categórica un abordaje por sobre el otro 19 . No obstante, existe “un cierto consenso” en que para la anestesia de estructuras profundas puede ser preferible el abordaje fuera de plano. Varios expertos recomiendan también que los operadores que estén recién aprendiendo comiencen por la anestesia de estructuras superficiales y con abordaje en plano 33 . La literatura especializada sí es unánime en insistir en que, durante el avance de la aguja en dirección hacia la estructura nerviosa, se debe procurar saber en todo momento dónde está la punta de la aguja y ver siempre el avance de la punta 28 ,32 . Como métodos coadyuvantes para saber dónde está la punta se describen diversas técnicas 40 ,41 :
Técnicas de acercamiento ecográfico de la aguja al nervio:
-
Visión permanente del cuerpo y punta de la aguja.
-
Hidrolocalización.
-
Movimiento de partes blandas.
-
Avance “paso a paso”.
-
Apoyo de neuroestimulación.
-
Integración cerebro-manual
La integración es una habilidad que es necesario adquirir. El grado de facilidad o dificultad para adquirirla es multifactorial y muy personal 32 .
Se requiere:
-
Interpretar la imagen de la pantalla en 2D para mover las manos en 3D.
-
Trasladar la atención desde la piel del paciente hacia la pantalla del ecógrafo.
-
Coordinar y sumar las técnicas descritas.
Para el proceso de aprendizaje pre-clínico las recomendaciones de ASRA-ESRA sugieren la utilización de las siguientes herramientas 30 :
- Estudio de bibliografía.
- Análisis de material audiovisual.
- Talleres de manejo de ecógrafo.
- Talleres de examen de voluntarios.
- Práctica de punción en fantomas de gel.
- Práctica de punción en tejido animal.
- Práctica de punción en cadáver.
- Colaboración con radiólogo.
APRENDIZAJE CLÍNICO
En la última década, los expertos coincidieron en que para el aprendizaje de las técnicas de anestesia neuroaxial los residentes deben realizar un cierto número mínimo de procedimientos 42 ,43 . Los números considerados mínimos fueron distintos en Estados Unidos y en Europa y también fueron distintos para la anestesia subaracnoídea y epidural. En la misma época hubo intentos de establecer números mínimos para cada uno de los bloqueos de plexos y nervios periféricos, pero no hubo consenso al respecto. Una evaluación entre los residentes encontró que el número de cada bloqueo que cada uno realizaba era muy diferente y algunos bloqueos eran realizados con muy poca frecuencia 43 ,44 . Las comisiones de expertos reconocieron la dificultad de establecer números mínimos de cada tipo de bloqueo para la formación de los residentes.
Las recomendaciones clínicas para el aprendizaje de AR guiada por US redactadas por las comisiones conjuntas de ASRA y ESRA vigentes, eludieron mencionar números mínimos para el aprendizaje 32 .
Al estudiar las dificultades del aprendizaje se han identificado los errores más frecuentes cometidos por los residentes y los especialistas 28 . Estos son, en orden de frecuencia:
-
-
Avanzar sin ver aguja.
-
Movimientos involuntarios del transductor.
-
Mala programación del equipo.
-
Equivocar el lado de la pantalla.
-
Mala ergonomía.
-
Mal diagnóstico del sitio de depósito del anestésico local.
-
Los expertos han aludido al distinto grado de entrenamiento necesario según el objetivo deseado. El caso es distinto si se quiere adquirir habilidad, competencia, desempeño, etc. Unos conceptos más exigentes que otros. Además, el entrenamiento necesario es distinto para cada individuo dependiendo de múltiples factores, entre ellos, la experiencia previa del aprendiz, la variedad de bloqueos a aprender y las capacidades personales 32 .
Las recomendaciones de ASRA y ESRA resumen señalando lo siguiente 32 :
-
Debe haber un aprendizaje teórico.
-
Debe haber un aprendizaje experimental.
-
El aprendizaje debe incluir varios nervios.
-
El número de casos para dominar las habilidades dependerá inevitablemente de la experiencia y habilidades de cada uno.
-
La autorización para realizar procedimientos de AR guiados por US debe resolverse en cada hospital en forma interna.
RERERENCIAS
- Winnie AP. Interscalene brachial plexus block. Anesth Analg 1970; 49: 455-466.
- Greenblatt GM, Denson JS. Needle nerve-locator: nerve blocks with a new instrument for locating nerves. Anesth Analg 1962; 41: 599-601.
- Liguori GA, Zayas VM, YaDeau JT, et al. Nerve localization techniques for interscalene brachial plexus blockade: a prospective, randomized comparison of mechanical paresthesia versus electrical stimulation. Anesth Analg 2006; 103: 761-767.
- Liu S, Ngeow J, YaDeau J. Ultrasound-guided regional anesthesia and analgesia a qualitative systematic review. Reg Anesth Pain Med 2009; 34: 47-59.
- Nielsen KC, Steele SM. Outcome after regional anesthesia in the ambulatory setting-is it really worth it? Clin Anaesthesiol 2002; 16: 145-157.
- Denny NM. Location, location, location! Ultrasound imaging in regional anaesthesia. Editorial I: Br J Anaesth 2005; 94: 1-3.
- Kessler J, Gray AT. Sonography of scalene muscle anomalies for brachial plexus block. Reg Anesth Pain Med 2007; 32: 172.
- Kapral S, Krafft P, Eibenberger K, et al. Ultrasound-guided supraclavicular approach for regional anesthesia of the brachial plexus. Anesth Analg 1994; 78: 507-513.
- Sites B. Introduction to Ultrasound-Guided Regional Anesthesia: Seeing is Believing. ASA Refresher Courses in Anesthesiology, Vol 34, Chapter 14, 151-163, 2006.
- Sala-Blanch X. Curso de Ecografía para Anestesiólogos. Aula Clinic, Universidad de Barcelona, 2006 – 2007.
- Hopkins PM. Ultrasound Guidance as a Gold Standard in Regional Anaesthesia. Editorial. Br Journal Anaesth 2007; 98: 299 301.
- Sites B, Spence BC, Gallagher J, et al. Regional anaesthesia meets ultrasound: a specialty in transition. Acta Anaesthesiol Scand 2008; 52: 456-566.
- Zetlaoui P, Labbe JPh, Benhamou D. Ultrasound Guidance for Axillary Plexus Block Does Not Prevent Intravascular Injection. Anesthesiology 2008; 108: 761.
- Loubert C, Williams SR, Hélie F, et al. Complication during Ultrasound-guided Regional Block: Accidental Intravascular Injection of Local Anesthetic. Anesthesiology 2008; 108: 759-760.
- Neal J, Brull R, Chan V, et al. The ASRA Evidence-Based Medicine Assessment of Ultrasound-Guided Regional Anesthesia and Pain Medicine-Executive Summary. Reg Anesth Pain Med 2010; 35: 325.
- Bigeleisen PE. Nerve puncture and apparent intraneural injection during ultrasound-guided axillary block does not invariably result in neurologic injury. Anesthesiology 2006; 105: 779-783.
- Bigeleisen PE, Moayeri N, Groen GJ. Extraneural versus intraneural stimulation thresholds during intraneural ultrasound-guided supraclavicular block. Anesthesiology 2009; 110: 1235-1243.
- US Department of Health and Human Services Agency for Health Care Policy and Research Acute Pain Management: Operative or Medical Procedures and Trauma. Clinical Practice Guideline 1. Rockville, MD: AHCPR; 1993. AHCPR Publication 92-0023-0107.
- Marhofer P, Harrop-Griffiths W, Kettner1 SC, et al. Fifteen years of ultrasound guidance in regional anaesthesia: Part 1. Br J Anaesth 2010; 104: 538-546.
- Marhofer P, Willschke H, Kettner S. Current concepts and future trends in ultrasound-guided regional anesthesia. Curr Opin Anaesthesiol 2010; 23: 632-636.
- McNaught A, Shastri U, Carmichael1 NY, et al. Ultrasound reduces the minimum effective local anaesthetic volume compared with peripheral nerve stimulation for interscalene block interscalene block. Br J Anaesth 2011; 106: 1240-1230.
- Sites BD, Gallagher JD, Cravero J, et al. The learning curve associated with a simulated ultrasound guided interventional task by inexperienced anesthesia residents. Reg Anesth Pain Med 2004; 29: 544-548.
- Kessler J, Bolger A, Gray A. An Essential Skill. Reg Anesth Pain Med 2006; 31: 498-500.
- Adler R. The Use of Compact Ultrasound in Anesthesia: Friend or Foe. Anesth Analg 2007; 105: 1530-1532.
- Sites B, Brull R, Chan V, et al. Artifacts and Pitfall Errors Associated With Ultrasound-Guided. Regional Anesthesia. Part I: Understanding the Basic Principles of Ultrasound Physics and Machine Operations. Reg Anesth Pain Med 2007; 32: 412-418.
- Sites B, Brull R, Chan V, et al. Artifacts and Pitfall Errors Associated With Ultrasound-Guided. Regional Anesthesia. Part II: A Pictorial Approach to Understanding and Avoidance. Reg Anesth Pain Med 2007; 32: 419-433.
- De la Fuente R, Altermatt F, Corvetto M, et al. Conceptos Básicos de Ultrasonografía Aplicada a la Anestesia Regional. Rev Chil Anest 2009; 38: 39-45.
- Sites B, Spence B, Gallagher J, et al. Characterizing Novice Behavior Associated With Learning Ultrasound-Guided Peripheral Regional Anesthesia. Reg Anesth Pain Med 2007; 32:107-115.
- Rodrigues de Oliveira G, Escovedo P, Bruggemann da Conceicao D, et al. Learning Curves and Mathematical Models for Interventional Ultrasound Basic Skills. Anesth Analg 2008;106: 568 -573.
- Smith H, Kopp S, Jacob A, et al. Designing and Implementing a Comprehensive Learner-Centered Regional Anesthesia Curriculum. Reg Anesth Pain Med 2009; 34: 88-94.
- Orebaugh S, Bigeleisen P, Kentor M. Impact of a regional anesthesia rotation on ultrasonographic identification of anatomic structures by anesthesiology residents. Acta Anaesthesiol Scand 2009; 53: 364-368.
- Sites B, Chan V, Neal J, et al. The American Society of Regional Anesthesia and Pain Medicine and the European Society of Regional Anaesthesia and Pain Therapy Joint Committee Recommendations for Education and Training in Ultrasound-Guided Regional Anesthesia. Reg Anesth Pain Med 2009; 34: 40-46.
- Fingerman M, Benonis J, Martin G. A practical guide to commonly performed ultrasound-guided peripheral nerve blocks. Curr Opin Anaesthesiol 2009; 22: 600-607.
- Ramlogan R, Manickam B, Chan V, et al. Challenges and Training Tools Associated With the Practice of Ultrasound- Guided Regional Anesthesia A Survey of the American Society of Regional Anesthesia and Pain Medicine. Reg Anesth Pain Med 2010; 35: 224-226.
- Sites B, Brull R. Ultrasound guidance in peripheral regional anesthesia: philosophy, evidence-based med, and techniques. Curr Opin Anaesthesiol 2006; 19: 630-639.
- Sites BD, Gallagher JD, Cravero J, et al. The learning curve associated with a simulated ultrasound-guided interventional task by inexperienced anesthesia residents. Reg Anesth Pain Med 2004; 29: 544-548.
- Chapman GA, Johnson D, Bodenham AR. Visualisation of needle position using ultrasonography. Anaesthesia 2006; 61: 148-158.
- Dang CP. Some Additional Insight into Ultrasound Imaging for Successful Ultrasound-Guided Placement of Catheters. Reg Anesth Pain Med 2010; 35: 565.
- Manickam B, Perlas A, Chan V, et al. The Role of a Preprocedure Systematic Sonographic Survey in Ultrasound-Guided Regional Anesthesia. Reg Anesth Pain Med 2008; 33: 566-570.
- Bloc S, Ecoffey C, Dhonneur D. Controlling Needle Tip Progression During Ultrasound-Guided Regional Anesthesia Using the Hydrolocalization Technique. Reg Anesth Pain Med 2008; 33: 382-383.
- Chin K, Perlas A, Chan V, et al. Needle Visualization in Ultrasound-Guided Regional Anesthesia: Challenges and Solutions. Reg Anesth Pain Med 2008; 33: 532-544.
- ACGME Accreditation Council for Graduate Medical Education Program Requirements for Graduate Medical Education in Anesthesiology. Anesthesiology Program Requirements. (Acceso el 16 de septiembre de 2011 en: http://www.acgme.org/acWebsite/RRC_040/040_prIndex.asp).
- Kopacz DJ, Neal JM. Regional anesthesia and pain medicine: Residency training The year 2000. Reg Anesth Pain Med 2002; 27: 9-14.
- Schupfer K, Gerber W. Learning manual skills in anesthesiology: Is there a recommended number of cases for anesthetic procedures? Anesth Analg 1998; 86: 635-639.


 Creative Commons Attribution
Creative Commons Attribution