Florence Gazabatt S. 1
Rev Chil Anest Vol. 39 Núm. 2 pp. 167-173|doi:
PDF|ePub|RIS
La extubación es un proceso complejo donde intervienen múltiples variables tanto de la vía aérea como de la mecánica respiratoria, estados de conciencia, cardiovasculares, metabólicos, efecto residual de drogas anestésicas, etc. Cualquiera de estas variables pueden por si sola afectar el éxito de la extubación convirtiendo el post-operatorio en un período de máxima vulnerabilidad 1 – 3 .
Por otro lado, las complicaciones pueden ocurrir en la sala de recuperación 4 o lejos de ella y en forma inesperada, por lo que en términos relativos es el momento de mayor riesgo perioperatorio, superando en frecuencia e importancia a los problemas de la inducción anestésica 5 .
Las complicaciones de la extubación son muy variadas 6 , como obstrucción respiratoria, hipoventilación, apnea, broncoespasmo, laringoespasmo, edema pulmonar por presión negativa 7 , edema laríngeo o supraglótico, aspiración de contenido gástrico, etc. Algunas, por su gravedad, requerirán reintubación (en condiciones adversas) agregando mayor morbilidad. La incidencia de reintubación en la población general es menor a 0,2%, pero en cirugías maxilofaciales o de columna cervical puede ser tan alta como un 10 a 15%.
No existen claras recomendaciones o algoritmos, como los dados por la ASA para la intubación difícil, por lo que este artículo pretende dar algunas pautas de manejo y sensibilizar a los anestesiólogos para reconocer factores de riesgo y condiciones que pudieran favorecer una extubación difícil y/o reintubación con el fin de prevenir complicaciones y optimizar su tratamiento.
Aspectos generales de la extubación
La extubación es un acto deliberado y planificado por el anestesiólogo, por lo que éste debe elegir el momento más apropiado para efectuarla, considerando varios factores:
-
Estado de conciencia: Es preferible la extubación vigil, donde el paciente obedezca órdenes, tenga reflejos conservados y con la menor concentración posible de halogenados o de propofol. En ocasiones esto no se logra, por ejemplo cuando el paciente presenta daño neurológico previo o perioperatorio, lo que retarda la extubación y aumenta el riesgo de aspiración o de hipoventilación.
-
Reversión neuromuscular: Aquellos pacientes que requirieron relajantes neuromusculares, deben ser monitorizados con estimulador de nervio periférico y asegurar una relación T4/T1 mayor a 90% al término de la cirugía 8 . Actualmente se dispone de sugammadex, que asegura una reversión completa y en escasos minutos, a diferencia de la neostigmina, que tiene efectos colaterales y puede afectar el músculo glosofaríngeo y diafragma, lo que podría traducirse en una menor capacidad ventilatoria en el despertar 9 , 10 . Se ha demostrado que la curarización residual (que puede tener una incidencia de un 20-40%) aumenta la frecuencia de complicaciones respiratorias como hipoventilación, obstrucción respiratoria, reintubación y aspiración de contenido gástrico 11 .
-
Analgesia: Una buena analgesia regional permite un despertar más tranquilo, disminuir los opiáceos sistémicos y una mejor mecánica respiratoria. El uso de remifentanil hasta el momento de la extubación, en concentraciones de TCI de 1,5 a 2 µg·ml-1, ha logrado mejorar la calidad del despertar, disminuyendo considerablemente la tos y el laringoespasmo, junto a una mayor estabilidad cardiovascular 12 , 13 .
-
Optimización ventilatoria: El reclutamiento alveolar seguido de PEEP, disminuye la incidencia de atelectasias, en especial en pacientes de riesgo como el obeso mórbido. El uso de CPAP nasal evita el colapso de la vía aérea superior en pacientes con apnea del sueño. En estos casos también se recomienda una extubación con el paciente en posición semisentada 14 . Los pacientes con patología bronquial secretora se favorecen de una prolija aspiración de secreciones previo a la extubación.
-
Otros: Un adecuado control metabólico, hemodinámico y térmico, facilitan el proceso de despertar.
Clasificación
Con fines didácticos, la extubación difícil puede subdividirse arbitrariamente en tres grupos según patología de base:
1. Pacientes que presentan vía aérea difícil en la inducción anestésica:
Obviamente, estos pacientes pueden presentar problemas en la extubación especialmente aquellos que son difíciles de ventilar, con apnea obstructiva, edema de laringe de cualquier etiología, tumores orofaríngeos o laríngeos (Figura 1), abscesos maxilofaciales y de cuello como lo es la Angina de Ludwig (Figura 2). En todos estos pacientes debemos tomar las medidas necesarias para evitar las complicaciones del despertar.
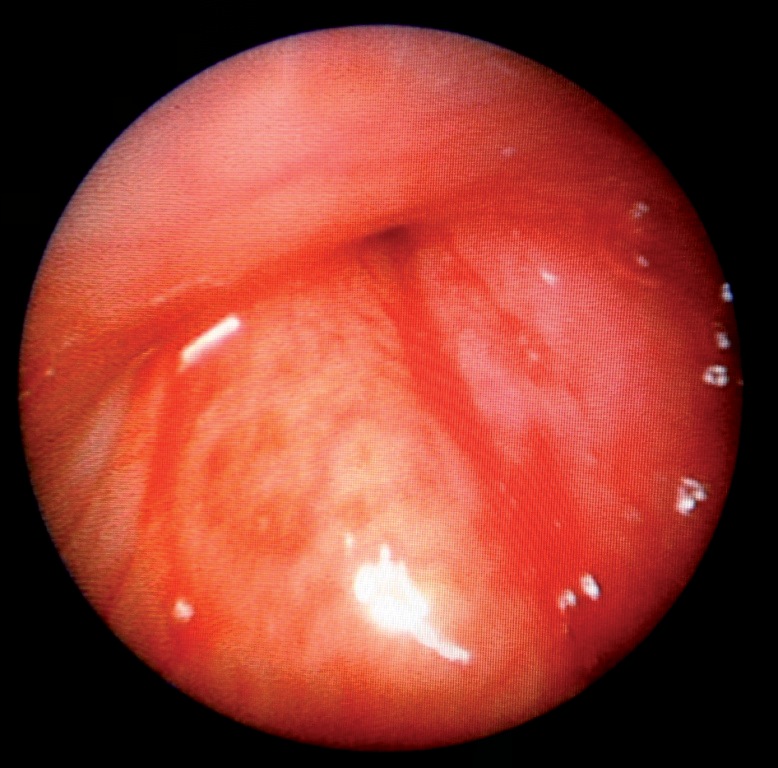
Figura 1 Edema laríngeo por cáncer.
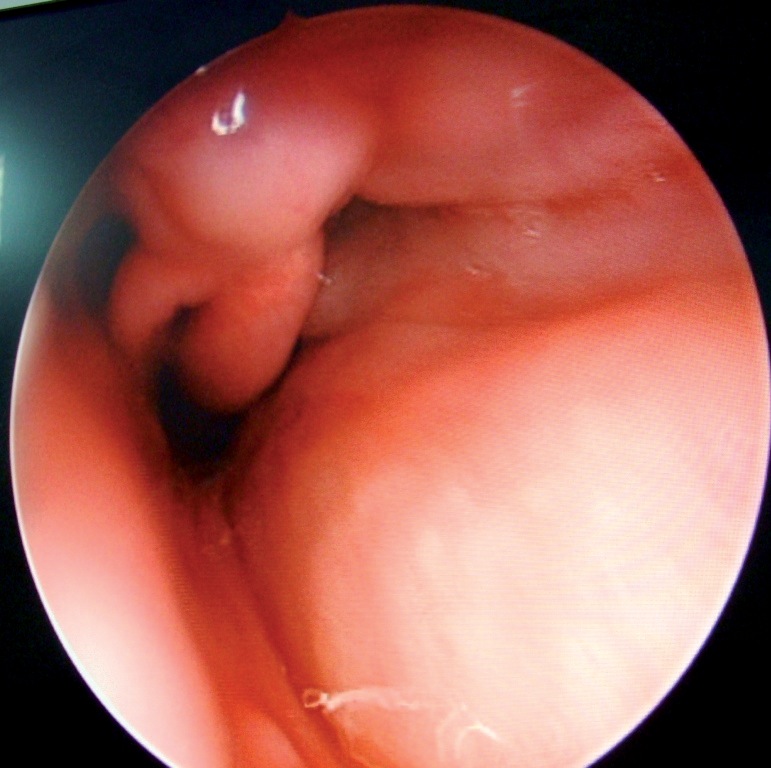
Figura 2 Edema de faringe y glotis por Angina de Ludwig.
2. Pacientes con vía aérea normal en la inducción, pero que sufren modificaciones en el transcurso de la cirugía:
-
De origen anestésico: Múltiples intentos de intubación puede provocar trauma en la vía aérea 15 , 16 , destacando la subluxación de aritenoides, edema laríngeo o subglótico, flap de mucosa traqueal, ruptura traqueal, enfisema subcutáneo, pneumotórax, etc. También se ha descrito parálisis de cuerdas vocales (incluso bilateral) con el uso de máscaras laríngeas reutilizables, especialmente cuando se ha empleado óxido nitroso, que permea el cuff provocando altas presiones en su interior.
-
De origen quirúrgico: Clásicamente la cirugía de columna cervical, endarterectomía carotídea, tiroidectomía, disección radical de cuello y la cirugía máxilo-facial son las que originan mayor tasa de morbilidad relacionada al manejo de la vía aérea.
– La cirugía de columna cervical, especialmente la fijación de columna por vía anterior, presenta alto riesgo de complicaciones en especial cuando son varios los segmentos a fijar, muchas horas de cirugía, politransfusión, obesidad, etc. 17 – 18 . La posición prona y en Trendelenburg por varias horas suele ocasionar edema laríngeo y de lengua 19 . Estos pacientes suelen requerir de una extubación diferida y aproximadamente un 10% necesitan una reintubación. Es importante considerar que la inmovilidad cervical postoperatoria cambia el escenario, pudiendo hacer difícil una intubación que originalmente no lo fue 20 .
– Toda gran cirugía de cuello puede comprometer el drenaje venoso y linfático, especialmente en cirugía oncológica, agravándose aún más si previamente el paciente ha recibido radioterapia 21 . Estos pacientes tienen riesgo de edema laríngeo que puede dificultar la extubación.
– Se ha observado que una simple endarterectomía carotídea genera edema de vía aérea asintomático 22 . Distinta es la situación cuando existe un hematoma secundario a dicha cirugía que tiene una incidencia de 1 a 2%. Este hematoma deforma la glotis y produce edema laríngeo dificultando la reintubación 23 , 24 (Figura 3). El edema suele persistir una vez corregido el problema quirúrgico por lo que se recomienda una extubación diferida.
– La cirugía de tiroides también puede provocar un hematoma post operatorio que ponga en riesgo vital al paciente (incidencia 0,6-1%) 25 , aunque la lesión del nervio laríngeo recurrente es lo más típico de esta cirugía, con una incidencia de parálisis definitiva de 1% y temporal del 5% 26 . Esto es de mayor relevancia cuando se efectúa una tiroidectomía total con disección de cuello, alcanzando un 10% de frecuencia la lesión del nervio laríngeo recurrente 27 .
– La cirugía del tiroides retroesternal 28 también es importante mencionarla, porque suele comprometer tráquea, comprimir grandes vasos, etc. El porcentaje de lesión del nervio laríngeo recurrente es mayor, y la intubación post operatoria es más prolongada (Figura 4).
– En cirugía maxilofacial es importante considerar el edema post operatorio, el cambio de ejes en cirugía ortognática 29 y si el paciente es extubado con una fijación de arco dental que impida una reintubación por vía oral.
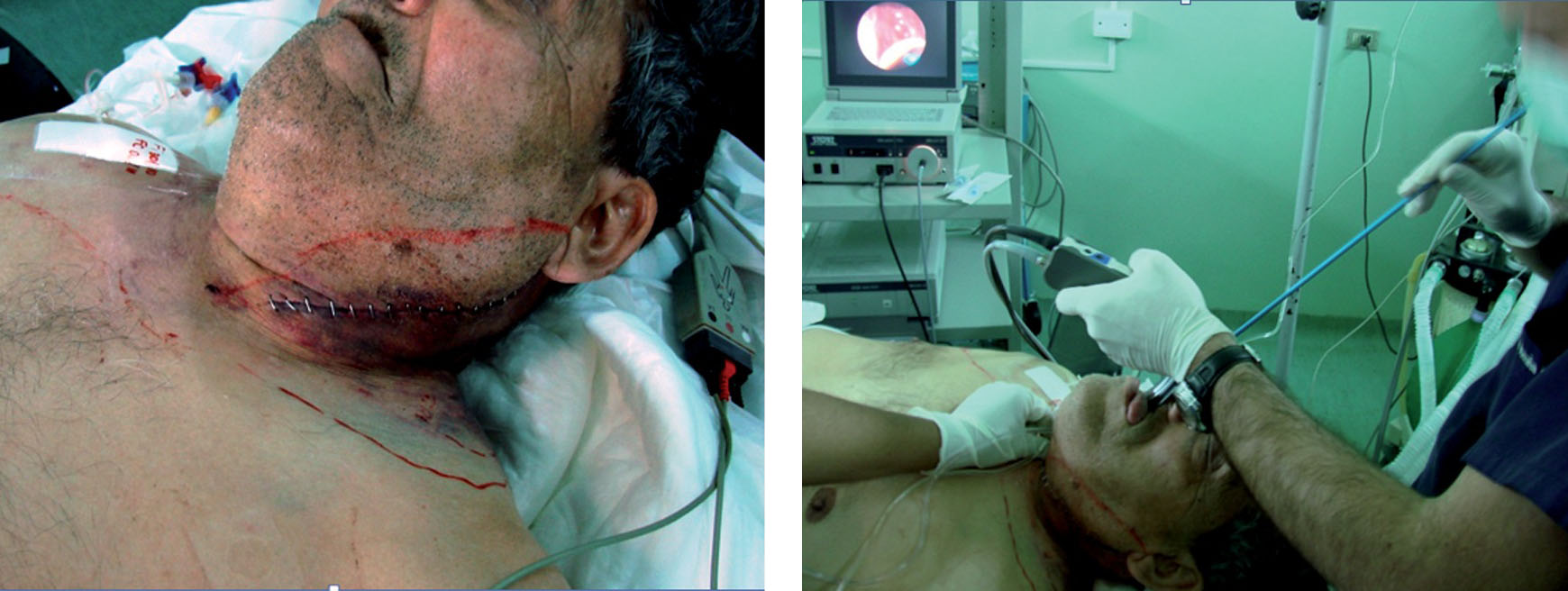
Figura 3 Hematoma post endarterectomía carotídea. Intubación con videolaringoscopio V-MAC® y Frova®.
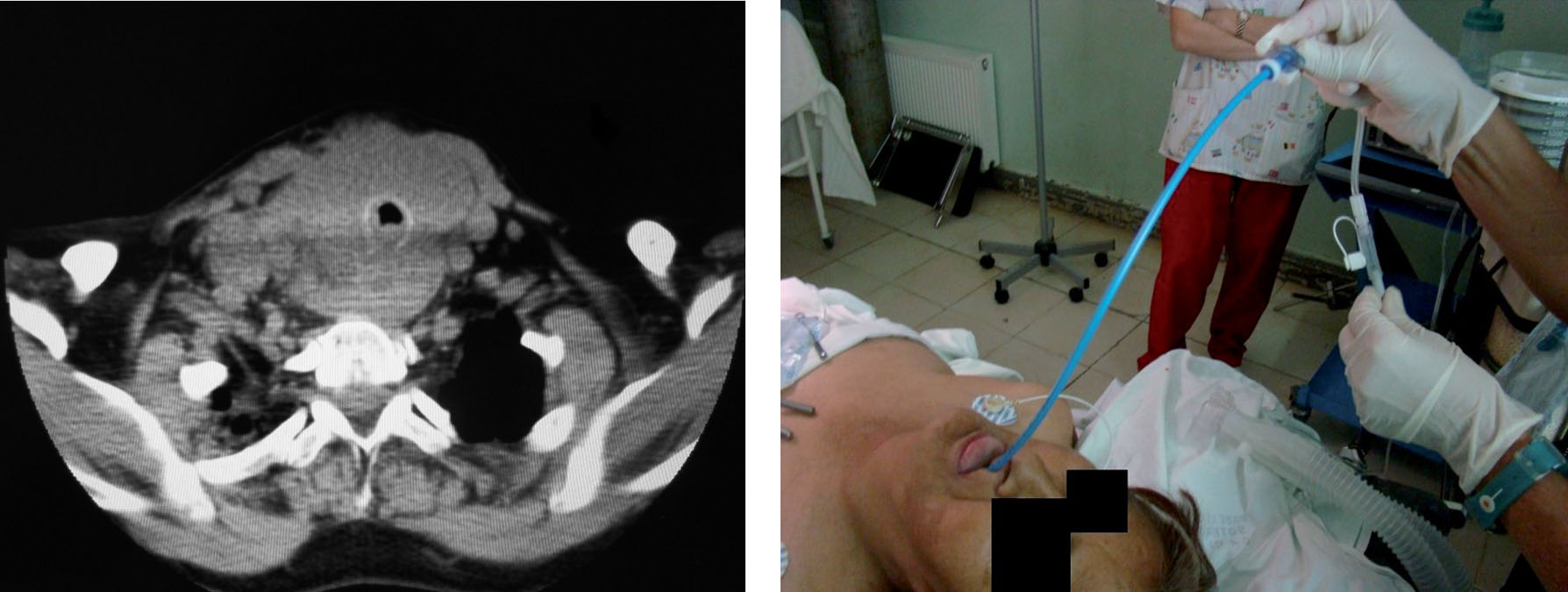
Figura 4 Carcinoma de tiroides retroesternal con edema de tráquea. Paciente intubada con Frova® y ventilada con modulador de flujo de oxígeno ENK®.
3. Pacientes con vía aérea normal pero con patología médica sobreagregada:
Numerosas patologías médicas pueden dificultar la extubación o generar una reintubación. Destaca el compromiso neurológico central dado por un accidente vascular encefálico perioperatorio o bien el agravamiento de éste, enfermedades neuro-musculares como la miastenia gravis o encefalopatía tóxico-metabólica. Descompensaciones del sistema cardiovascular, como insuficiencia cardíaca o isquemia miocárdica con edema pulmonar, pueden hacer necesaria una intubación prolongada en UCI. Pacientes con reserva pulmonar disminuida también son muy frágiles y pueden descompensarse por aspiración de contenido gástrico, atelectasias, distress respiratorio, broncoespasmo, efecto directo de la cirugía (en especial de tórax y abdomen alto), etc.
Este tipo de pacientes, con patología médica asociada, suelen encontrarse en unidades de cuidados intensivos y por lo general son complejos, ya que se conjuga el edema laríngeo y la patología pulmonar, dificultando la desconexión al ventilador y la extubación. Los criterios de destete son múltiples y con una tasa de fracaso cercana al 20-30%. La reintubación en este tipo de pacientes se asocia a un franco aumento de la morbilidad y mortalidad. Lamentablemente el análisis de este problema escapa al lineamiento central de este artículo.
Cómo enfrentar una extubación difícil o reintubación
El anestesiólogo debe tener clara conciencia que la extubación es un proceso que exige una preparación tanto previa como posterior al retiro del tubo traqueal. Las complicaciones pueden aparecer minutos o varias horas después. Se debe tener un alto índice de sospecha dependiendo del tipo de cirugía y deben existir protocolos de manejo, tanto en pabellón como en recuperación, para la adecuada prevención o tratamiento de las complicaciones.
Es fundamental la evaluación visual y funcional de la vía aérea. Se recomienda el uso rutinario de fibrobroncoscopía en cirugías de alto riesgo para valorar el grado de edema glótico, subglótico y la movilidad de las cuerdas vocales. De no contar con un fibrobroncoscopio (FBC), la laringoscopía directa o indirecta (videolaringoscopio) pueden ser de utilidad.
Paralelo a la evaluación por fibrobroncoscopía puede hacerse el “cuff-leak test” para verificar si existe un espacio entre la mucosa y el tubo traqueal con su cuff desinflado. Debiera filtrar aproximadamente más de 110-140 cc de aire o al menos un 20% del volumen corriente 30 . Este test tiene una alta sensibilidad y especificidad. Su valor predictivo negativo es superior al 95% y el valor predictivo positivo varía entre un 40 a 80%, por lo que es posible efectuar con bastante seguridad una extubación si la filtración es mayor a 140 ml.
En el caso de existir edema laríngeo, la utilización de corticoides como dexametasona o metilprednisolona y epinefrina racémica han demostrado utilidad, aunque con bajo grado de evidencia. Trabajos más recientes sugieren que se debe utilizar corticoides (metilprednisolona 20 mg c/4 horas o dexametasona 5 mg c/6 horas) e iniciarse el tratamiento 12 horas antes de la extubación. Esto logra disminuir significativamente el estridor y la necesidad de reintubación 31 – 34 .
Frente a la sospecha de una extubación difícil se recomienda que se inserte un intercambiador de tubo y una vez confirmada su adecuada posición y funcionamiento, proceder a retirar el tubo traqueal 35 . Se sugiere que el intercambiador de tubo se exteriorice por vía nasal lo que permite una mejor tolerancia del paciente. De lo contrario, existe la alternativa de dejar in situ una guía de alambre flexible que viene en algunos de estos equipos, para poder deslizar un intercambiador y luego un tubo traqueal de ser necesario.
1.- Catéteres de intercambio
Existen distintos diseños de catéteres de intercambio, pero los más aceptados y que se encuentran en nuestro medio son los de la empresa Cook: Cook Airway Exchange Catheters. Tienen la particularidad de tener lumen y dos adaptadores específicos para su extremo proximal con el sistema “Rapi-Fit®” (Figura 5); uno de éstos permite ventilación jet por tener una conexión “luer-lock” y el otro ventilación con Ambú o máquina de anestesia por disponer de un conector universal de 15 mm (Figura 6). En su extremo distal se encuentran 2 pequeños orificios paralelos y uno terminal, además posee un sistema graduado en cm, hasta los 35 cm, que permite cuantificar la profundidad de inserción.
Existen 4 tamaños: 8, 11, 14 y 19 French. Los más utilizados en adultos son los de 11 y 14 F, que tienen 83 cm de largo y 2,3 y 3 mm de diámetro interno, permitiendo el intercambio de tubos a partir de 4 y 5 mm de diámetro interno respectivamente.
La empresa Cook ha desarrollado un catéter de intercambio llamado “Arndt Airway Exchange Catheter Set”, con un diámetro externo de 14 F y 70 cm de largo. Este catéter tiene 6 orificios en su extremo distal, el que a su vez ha sido aguzado (Figura 7). Este set contiene los adaptadores Rapi-Fit, una guía de alambre flexible de 0,97 mm de diámetro y 160 cm de largo. Además, posee un conector de 15 mm que contiene un adaptador para fibrobroncoscopio. Este catéter de Arndt está diseñado para la intubación y extubación difícil cuando se necesita el uso de un fibrobroncoscopio y la utilización de una guía metálica a través de su canal de trabajo.
También puede utilizarse en extubación difícil el catéter que viene en el set de intubación retrógrada. Al igual que el anterior, posee un extremo aguzado y 6 orificios latero-distal, pero viene en la presentación de 11 F, 70 cm de largo y trae una guía metálica flexible de 0,97 mm de diámetro y 110 cm de largo.

Figura 5 Catéter de intercambio de tubo traqueal 14 French y adaptadores Rapi-Fit®.
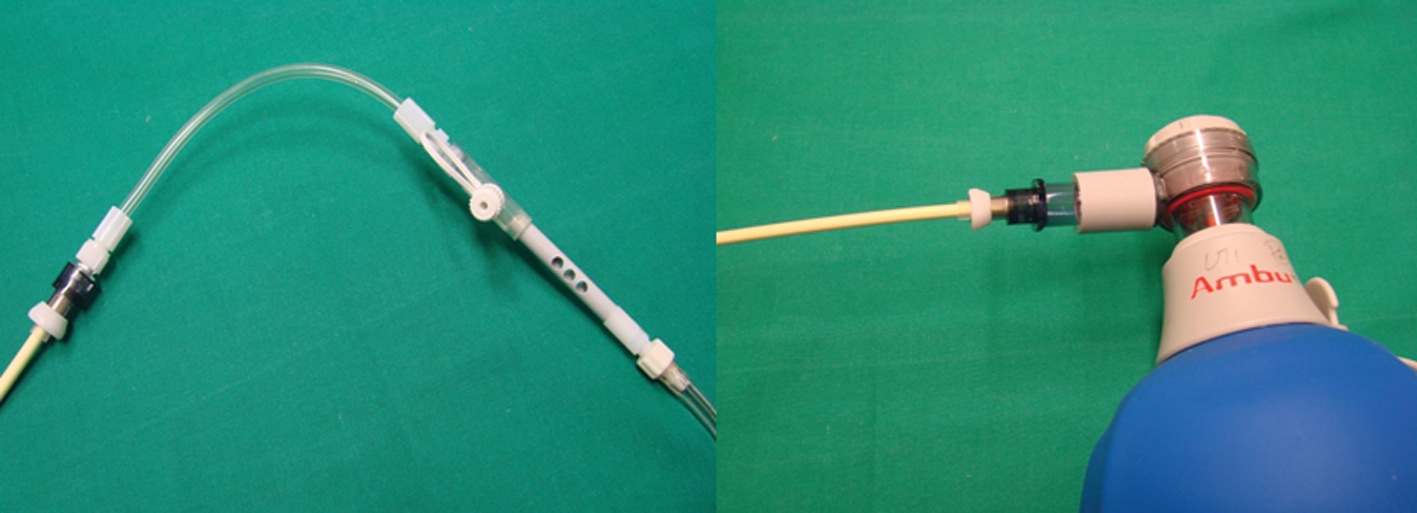
Figura 6 CAEC conectado a un modulador de flujo de oxígeno ENK® y a una bolsa de Ambu® respectivamente.
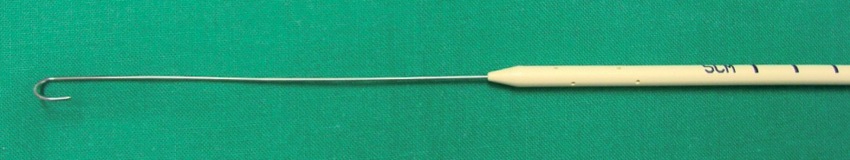
Figura 7 CAEC tipo Arndt®, 14 French y guía metálica flexible.
2.- Recomendaciones Generales en el Uso de Catéteres de Intercambio.
Los diámetros más recomendados son los de 11 y 14 F; un catéter más delgado tenderá a acodarse y uno más grueso a ser poco aceptado por el paciente.
Según la tolerancia y la patología asociada, estos catéteres pueden permanecer in situ desde un par de horas a dos o tres días 36 – 38 . Existe la opción de reemplazar el catéter por una guía metálica flexible; tiene la ventaja de ser mejor tolerada y permite avanzar un fibrobroncoscopio por su canal de trabajo con el fin de evaluar la vía aérea y/o intubar bajo visión directa.
Otra de las ventajas de estos catéteres de intercambio es que permiten ventilar u oxigenar. Se recomienda utilizar bajas presiones de ventilación como las dadas por el “modulador de flujo de oxígeno ENK”; de utilizarse el Manujet III, se sugiere no sobrepasar los 15 o 20 PSI, con el fin de evitar el barotrauma 39 . Pacientes con edema laríngeo severo están en riesgo de ello porque el escape de aire a través de la glotis está dificultado produciéndose fácilmente una hiperinsuflación.
Nunca se debe forzar el avance de un catéter de intercambio, y su extremo distal debe quedar pre-carinal, evitando así el trauma directo que pueden producir estos catéteres. Cuando se desliza un tubo traqueal, se debe lubricar tanto el catéter como el tubo. De existir dificultad en el avance del tubo, se debe sospechar del choque del extremo distal con el aritenoide derecho; para vencer esta resistencia se debe rotar el tubo traqueal en 90° contra el sentido de los punteros del reloj y ayudarse de una laringoscopía. Se debe privilegiar un tubo flexible y atraumático, resultando muy útil el tubo desechable diseñado para LMA Fastrach, ya que es flexible, reforzado y con una punta de silicona aguzada que se adapta mejor al catéter de intercambio (Figura 8) disminuyendo la posibilidad de pellizcamiento.

Figura 8 CAEC tipo Arndt® y tubo traqueal N° 7 LMA.
La probabilidad de lograr la intubación a través de un catéter de intercambio es cercana al 90% al primer intento. Cuando se compara la morbilidad de la reintubación es claramente mayor en aquellos pacientes que no tenían acceso expedito a la vía aérea, como lo es un catéter de intercambio o una guía metálica flexible.
La reintubación en un paciente sin catéter de intercambio es compleja ya que la glotis está distorsionada y con edema de magnitud variable. Si existe tiempo suficiente, se dispone de un FBC y un operador con experiencia, se debe intentar una intubación vigil. De lo contrario se podrá intubar utilizando un videolaringoscopio más bougie o algún dispositivo supraglótico. No se recomienda intubar a ciegas a través de una máscara laríngea debido a las razones mencionadas anteriormente y deberá inicialmente ser utilizada sólo como medio de ventilación. Si se cuenta con FBC podrá ser utilizado para guiar la intubación en una LMA Fastrach bajo visión directa; en el caso de LMA Proseal se sugiere recurrir a una guía de intubación Aintre® (Cook) que tiene 19 F, 4,7 mm de diámetro interno y 83 cm de largo. La guía de intubación Aintre sirve para proteger el FBC y luego de posicionada ésta en tráquea se retira la máscara laríngea y se utiliza como un CAEC para tubos traqueales mayor o igual a 7 mm de diámetro interno 40 – 42 .
En el caso de haber utilizado una LMA Supreme como medio de rescate ventilatorio, y se pretende intubar a través de ésta, se recomienda utilizar FBC más guía metálica, para luego retirar la máscara y avanzar el FBC por su canal de trabajo o un CAEC tipo Arndt 43 – 44 .
Bibliografía
- Miller KA, Harkin CP, Bailey PL. Postoperative tracheal extubation. Anesth Analg 1995; 80: 149-172.
- Karmarkar S, Varshney S. Tracheal extubation. CEACCP 2008; 8: 214-220.
- Lien CA, Koff H, Malhotra V, Gadalla F. Emergence and extubation: a systematic approach. Anesth Analg 1997; 85: 1177.
- Argalious M. Management of Postanesthesia Care Unit Emergencies. ASA Refresher Courses in Anesthesiology 2009; 37: 1-12.
- Peterson GN, Domino KB, Caplan RA, et al. Management of the difficult airway a closed claims analysis. Anesthesiology 2005; 103: 33-39.
- Asai T, Koga K, Vaughan RS. Respiratory complications associated with tracheal intubation and extubation. Br J Anaesthesia 1998; 80: 767-775.
- Krodel DJ, Bittner EA, Abdulnour R, et al. Anesthesiology. Case scenario: acute postoperative negative pressure pulmonary edema 2010; 113: 200-207.
- Murphy GS, Brull SJ. Residual neuromuscular block: lessons unlearned. Part I: definitions, incidence, and adverse physiologic effects of residual neuromuscular block. Anesth Analg 2010; 111: 120-128.
- Herbstreit F, Peters J, Eikermann M. Impaired upper airway integrity by residual neuromuscular blockade: increased airway collapsibility and blunted genioglossus muscle activity in response to negative pharyngeal pressure. Anesthesiology 2009; 110: 1253-1260.
- Eikermann M, Zaremba S, Malhotra A, et al. Neostigmine but not sugammadex impairs upper airway dilator muscle activity and breathing. Br J Anaesth 2008; 101: 344-349.
- Murphy GS, Szokol JW, Marymont JH, et al. Residual neuromuscular blockade and critical respiratory events in the postanesthesia care unit. Anesth Analg 2008; 107: 130-137.
- Nho J, Lee S, Kang J, et al. Effects of maintaining a remifentanil infusion on the recovery profiles during emergence from anaesthesia and tracheal extubation. Br J Anaesth 2009; 103: 817-821.
- Lee B, Lee J, Na S. Targeting smooth emergence: the effect site concentration of remifentanil for preventing cough during emergence during propofol-remifentanil anaesthesia for thyroid surgery. Br J Anaesth 2009; 102: 775-778.
- Isono S. Obstructive Sleep Apnea of Obese Adults. Pathophysiology and Perioperative Airway Management. Anesthesiology 2009; 110: 908-921.
- Hagberg C. Complications of managing the airway. Best Practice & Research Clinical Anaesthesiology 2005; 19: 641-659.
- Mort T. Emergency Tracheal Intubation: Complications Associated with Repeated Laryngoscopic Attempts. Anesth Analg 2004; 99: 607-613.
- Sagi HC, Beutler W, Carroll E, Connolly PJ. Airway complications associated with surgery on the anterior cervical spine. Spine 2002; 27: 949-953.
- Manninen PH, Jose GB, Lukitto K, et al. Management of the airway in patients undergoing cervical spine surgery. J Neurosurg Anesthesiol 2007; 19: 190-194.
- Sinha A, Agarwal A, Gaur A, Pandey CK. Oropharyngeal swelling and macroglossia after cervical spine surgery in the prone position. J Neurosurg Anesthesiol 2001; 13: 237-239.
- Crosby ET. Considerations for airway management for cervical spine surgery in adults. Anesthesiol Clin 2007; 25: 511-533.
- Burkle CM, Walsh MT, Pryor SG, Kasperbauer JL. Severe postextubation laryngeal obstruction: The role of prior neck dissection and radiation. Anesth Analg 2006; 102: 322-325.
- Carmichael FJ, McGuire GP, Wong DT, et al. Computed tomographic analysis of airway dimensions after carotid endarterectomy. Anesth Analg 1996; 83: 12-17.
- Kwok OK, Sun KO, Ahchong AK, Chan CK. Airway obstruction following carotid endarterectomy. Anaesth Intensive Care 2004; 32: 818-820.
- Shakespeare W, Lanier W, Perkins W, Pasternak J. Airway Management in Patients Who Develop Neck Hematomas After Carotid Endarterectomy. Anesth Analg 2010; 110: 588-593.
- Rosenbaum MA, Haridas M, McHenry CR. Life-threatening neck hematoma complicating thyroid and parathyroid surgery. Am J Surg 2008; 195: 339-343.
- Bhattacharyya N, Fried MP. Assessment of the morbidity and complications of total thyroidectomy. Arch Otolaryngol Head Neck Surg 2002; 128: 389-392.
- Sevim T. Risk factors for permanent laryngeal nerve paralysis in patients with thyroid carcinoma. Clin Otolaryngol 2007; 32: 378-383.
- Shen WT, Kebebew E, Duh QY, Clark OH. Predictors of airway complications after thyroidectomy for substernal goiter. Arch Surg 2004; 139: 656-659.
- Rodrigo C. Anesthetic considerations for orthognathic surgery with evaluation of difficult intubation and technique for hypotensive anesthesia. Anesth Prog 2000; 47: 151-156.
- Antonaglia V, Vergolini A, Pascotto S, et al. Cuff-leak test predicts the severity of postextubation acute laryngeal lesions: a preliminary study. Eur J Anaesthesiol 2010; 27: 534-541.
- McCaffrey J, Farrell C, Whiting P, et al. Corticosteroids to prevent extubation failure: a systematic review and meta-analysis. Intensive Care Med 2009; 35: 977-986.
- Roberts RJ, Welch SM, Devlin JW. Corticosteroids for prevention of postextubation laryngeal edema in adults. Ann Pharmacother 2008; 42: 686-691.
- Bagshaw SM, Delaney A, Farrell C, et al. Best evidence in critical care medicine. Steroids to prevent post-extubation airway obstruction in adult critically ill patients. Can J Anaesth 2008; 55: 382-385.
- François B, Bellissant E, Gissot V, et al. 12-h pretreatment with methylprednisolone versus placebo for prevention of postextubation laryngeal oedema: a randomised double-blind trial. Lancet 2007; 369: 1083-1089.
- Mort T. Continuous Airway Access for the Difficult Extubation: The Efficacy of the Airway Exchange Catheter. Anesthesia Analgesia 2007; 105: 1357-1362.
- Loudermilk EP, Hartmannsgruber M, Stoltzfus DP, Langevin PB. A prospective study of the safety of tracheal extubation using a pediatric airway exchange catheter for patients with a known difficult airway. Chest 1997; 111: 1660-1666.
- Dosemeci L, Yilmaz M, Yegin A, et al. The routine use of pediatric airway exchange catheter after extubation of adult patients who have undergone maxillofacial or major neck surgery: a clinical observational study. Crit Care 2004; 8: R385-390.
- Benumof JL. Airway exchange catheters for safe extubation: The clinical and scientific details that make the concept work. Chest 1997; 111: 1483-1486.
- Benumof JL. Airway exchange catheters: Simple concept, potentially great danger. Anesthesiology 1999; 91: 342-344.
- Avitsian R, Doyle DJ, Helfand R, et al. Successful reintubation after cervical spine exposure using an Aintree intubation catheter and a Laryngeal Mask Airway. J Clin Anesth 2006; 18: 224-225.
- Cook TM, Silsby J, Simpson TP. Airway rescue in acute upper airway obstruction using a ProSealTM Laryngeal mask airway and an Aintree CatheterTM – a review of the ProSealTM Laryngeal mask airway in the management of the difficult airway. Anaesthesia 2005; 60: 1129-1136.
- Cook TM, Seller C, Gupta K, et al. Non-conventional uses of the Aintree Intubating catheter in management of the difficult airway: fourteen reports. Anaesthesia 2007; 62: 169-174.
- Matioc A. Use of Arndt airway exchanger catheter set with the laryngeal mask airway Supreme. J Clin Anesth 2009; 21: 152-153.
- Micaglio M, Ori C, Parotto M, Feltracco P. Three different approaches to fibreoptic-guided intubation via the Laryngeal Mask Airway Supreme. J Clin Anesth 2009; 21: 153-154.


 Creative Commons Attribution
Creative Commons Attribution