Rodrigo Gazmuri1, Florence Gazabatt1, Magdalena Estefó1, Felipe Miranda1, Constanza Rivera2, Dagoberto Ojeda1
Recibido: 2025-05-20
Aceptado: 2025-07-06
©2026 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 55 Núm. 2 |https://doi.org/10.25237/revchilanestv55n2-05
PDF
Opioid free anesthesia. Lowers postoperative nausea and vomiting?
Abstract
Introduction: Bariatric surgery is frequently associated with postoperative nausea and vomiting (NVPO). This study evaluated whether an opioid-free anesthetic regimen (OFA) reduces the incidence of PONV compared with reduced-opioid balanced general anesthesia (OLA), within an Enhanced Recovery After Surgery (ERAS) protocol. Methods: A single-center, prospective, single-blind, randomized clinical trial was designed with 134 ASA II-III patients with a BMI between 35 and 59.9 kg/m2 undergoing elective laparoscopic bariatric surgery. The OFA and OLA groups were compared regarding PONV, postoperative pain, morphine consumption, urinary retention, and length of hospital stay during the first 24 hours after surgery. Results: No significant differences were found in the incidence of vomiting (OLA: 4.8% vs. OFA: 5.9%; p = 0.996). The incidence of nausea was higher in the OFA group (13.4% vs. 9.1%), but not statistically significant (p = 0.055). The OFA group showed greater postoperative pain (area under the curve, p = 0.008) and higher morphine consumption (p = 0.0053), although both were clinically low. There were no differences in urinary retention or length of hospital stay. Conclusion: Within an optimized ERAS protocol, the OFA regimen offered no significant advantage over OLA in reducing NVPO. Although she experienced increased pain and opioid use, no additional analgesia was required beyond 12 hours. OLA is a viable alternative, but requires adjustments to optimize pain control.
Resumen
Introducción: La cirugía bariátrica se asocia frecuentemente con náuseas y vómitos posoperatorios (NVPO). Este estudio evaluó si un régimen anestésico libre de opioides (ALO) reduce la incidencia de NVPO comparado con anestesia general balanceada reducida en opioides (ARO), dentro de un protocolo de Recuperación Acelerada Después de Cirugía (Enhanced Recovery After Surgery (ERAS)). Métodos: Se diseñó un ensayo clínico aleatorizado, simple ciego, prospectivo y unicéntrico, con 134 pacientes ASA II-III y un IMC entre 35 y 59,9 kg/m2, sometidos a cirugía bariátrica laparoscópica electiva. Se compararon los grupos ALO y ARO en cuanto a NVPO, dolor posoperatorio, consumo de morfina, retención urinaria y duración de hospitalización, durante las primeras 24 h tras la cirugía. Resultados: No se hallaron diferencias significativas en la incidencia de vómitos (ARO: 4,8% vs. ALO: 5,9%; p = 0,996). La incidencia de náuseas fue mayor en el grupo ALO (13,4% vs. 9,1%), sin significancia estadística (p = 0,055). El grupo ALO mostró mayor dolor posoperatorio (área bajo la curva, p = 0,008) y mayor consumo de morfina (p = 0,0053), aunque ambos fueron clínicamente bajos. No hubo diferencias en la retención urinaria ni en el tiempo de hospitalización. Conclusión: Dentro de un protocolo ERAS optimizado, el régimen ALO no ofreció ventajas significativas sobre ARO en la reducción de NVPO. Aunque presentó mayor dolor y consumo de opioides, no se requirió analgesia adicional más allá de las 12 h. La ALO es una alternativa viable, pero necesita ajustes para optimizar el control del dolor.
Introducción
La anestesia libre de opioides (ALO; Opioid-Free Anesthesia (OFA) en inglés) es una técnica anestésica emergente cuyo principio se basa en evitar el uso de opioides durante el intraoperatorio[1]. Esta estrategia busca mejorar los resultados posoperatorios, dado que los opioides se asocian a efectos adversos a corto plazo, como náuseas y vómitos posoperatorios (NVPO), depresión respiratoria, retención urinaria, prurito y constipación[1],[2]. A largo plazo, su uso clínico también puede contribuir al desarrollo de dependencia y adicción[2],[3]. La crisis de opioides en países desarrollados, como Estados Unidos y varios países europeos, evidencia este riesgo: solo en EE.UU., más de 42.000 personas murieron por sobredosis de opioides en 2016, muchas de las cuales iniciaron su consumo en contextos médicos[4].
La ALO permite evitar el uso de opioides en el perioperatorio, reemplazándolos con una combinación de fármacos que garantizan una anestesia general de calidad[1]. Entre estos se incluyen antagonistas del receptor NMDA (como ketamina, lidocaína y sulfato de magnesio), bloqueadores de los canales de sodio (anestésicos locales), antiinflamatorios (AINES, dexametasona y anestésicos locales) y agonistas alfa-2 (dexmedetomidina y clonidina)[1],[2].
La ALO se ha utilizado por más de una década y su aplicación ha ganado respaldo en diversas áreas quirúrgicas[5],[6]. En combinación con protocolos de recuperación acelerada (ERAS), puede reducir el uso de opioides sin comprometer el control del dolor perioperatorio[7],[8]. Desde 2011, el equipo del Dr. Mulier en Bélgica, ha implementado la ALO en cirugía bariátrica con resultados positivos, reportando una drástica disminución en el uso de opioides posoperatorios, menos complicaciones y una reducción en la estadía hospitalaria[9]. El protocolo propuesto por este equipo incluye una dosis de carga de dexmedetomidina (0,25 mcg/kg) administrada 15 minutos antes de la inducción, junto con ketamina (0,5 mg/kg), lidocaína (1,5 mg/ kg) y magnesio (40 mg/kg) durante la inducción como reemplazo de opioides. Durante la cirugía, se mantiene una infusión continua de dexmedetomidina, ketamina y lidocaína, y se administran AINES como ketorolaco (0,5 mg/kg) o diclofenaco (150 mg), además de dexametasona (10 mg) para controlar la inflamación[9].
El ensayo clínico aleatorizado, controlado y doble ciego de Mullier et al., evaluó el dolor posoperatorio en pacientes sometidos a cirugía bariátrica laparoscópica electiva comparando ALO versus anestesia basada en opioides, en el que demostraron que ALO tiene menor consumo de opioides en la unidad de recuperación postanestésica (URPA) y una mejor calidad de recuperación[8]. La evidencia muestra que ALO en cirugía bariátrica laparoscópica, es superior a la anestesia basada en opioides en el control del dolor durante las primeras 24 h posoperatorias, menor requerimiento de opioides, mejor recuperación posoperatoria y una menor incidencia de NVPO[8],[10],[11].
Según el equipo de Mulier, las principales indicaciones para la ALO son: obesidad, apnea obstructiva del sueño (SAOS), adicción a opioides y síndromes de hiperalgesia o dolor crónico, como el síndrome de dolor regional complejo[9].
Esto adquiere especial relevancia en cirugía bariátrica, ya que la mayoría de los pacientes presentan obesidad mórbida, con alto riesgo de depresión respiratoria en el posoperatorio debido a la elevada prevalencia de SAOS[12], así como una alta incidencia de NVPO. La incidencia reportada en la literatura de NVPO en cirugía bariátrica es variable, por ejemplo, ZiemmanGimmel et al., reportan una incidencia de NVPO de 37,3% en pacientes que recibieron anestesia basada en opioides[5]. Mientras que el estudio prospectivo de Clanet et al., donde se evaluó el uso de ALO versus anestesia basada en opioides en cirugía bariátrica, demostró una incidencia de NVPO de 59% en anestesia basada en opioides y 37% en el grupo sin opioides, durante las primeras 24 h posoperatorias[13]. Existen otros protocolos anestésicos, como TIVA, para intentar reducir la incidencia de NVPO en pacientes con obesidad[14].
En abril de 2024, fue publicado el SOFA Trial cuya hipótesis era que un protocolo ALO mejoraría la calidad de recuperación temprana para pacientes sometidos a una cirugía mayor electiva bajo anestesia general[15]. Este ensayo clínico concluye que el protocolo sin opioides mejoró la calidad de la recuperación después de una cirugía electiva mayor de una manera estadística, pero no clínicamente significativa, en comparación con la anestesia estándar[15].
Desde 2021, en Clínica Dávila se implementó un protocolo de anestesia general balanceada con reducción de opioides (ARO; Opioid Low Anesthesia (OLA) en inglés), basado en los principios ERAS, para pacientes sometidos a cirugía bariátrica. Este protocolo consiste en limitar la dosis de opioides durante la inducción -utilizando únicamente 250 mcg de fentaniloe incorpora coadyuvantes analgésicos como ketamina, dexmedetomidina y sulfato de magnesio, con el objetivo de lograr un enfoque de analgesia multimodal.
El objetivo principal de este estudio fue evaluar si ALO reduce la incidencia de NVPO en pacientes sometidos a cirugía bariátrica, comparado con nuestro protocolo de anestesia general balanceada reducida en opioides utilizado en nuestra institución. Se evaluó la incidencia de NVPO durante las primeras 24 h postquirúrgicas. Como objetivos secundarios, se evaluó el dolor posoperatorio mediante la escala visual análoga (EVA) de 0 a 10, el uso de opioides de rescate, la incidencia de retención urinaria, el tiempo quirúrgico y la duración de la hospitalización en ambos grupos. El seguimiento posoperatorio se realizó a las 2, 4, 6, 12 y 24 h posteriores a la cirugía.
Materiales y Métodos
Diseño del estudio
Se realizó un ensayo clínico aleatorizado, prospectivo, unicéntrico y simple ciego, llevado a cabo entre marzo y noviembre de 2024 en Clínica Dávila, Santiago de Chile. El objetivo principal fue comparar la incidencia de NVPO durante las primeras 24 h tras cirugía bariátrica laparoscópica entre dos regímenes anestésicos: ALO versus ARO, ambos en el contexto de un protocolo ERAS. Los desenlaces secundarios incluyeron la intensidad del dolor posoperatorio, el consumo de opioides de rescate, la incidencia de retención urinaria y la duración de la estadía hospitalaria.
Participantes
Se incluyeron pacientes entre 18 y 65 años, clasificados ASA
II a III según la escala de la American Society of Anesthesiologists (ASA), con un índice de masa corporal (IMC) entre 35 y 59,9 kg/m2, sometidos a cirugía bariátrica laparoscópica electiva (bypass gástrico o manga gástrica). Se excluyeron pacientes con antecedentes de uso crónico de opioides, dolor crónico no oncológico, alergias o contraindicaciones a los fármacos del protocolo (fentanilo, ketamina, dexmedetomidina, lidocaína o sulfato de magnesio), cardiopatía coronaria con uso crónico de betabloqueadores, electrocardiograma alterado o procedimientos quirúrgicos adicionales planificados.
Se registraron las características demográficas y clínicas basales de los participantes al momento de su inclusión, incluyendo: sexo, edad, IMC, tipo de cirugía bariátrica (manga gástrica obypass gástrico), antecedentes mórbidos relevantes (hipertensión arterial, diabetes mellitus tipo 2 insulinorrequirente o no insulinorrequirente, dislipidemia, hipotiroidismo y SAOS con o sin uso de CPAP, puntuación en el cuestionario STOP-BANG, clasificación ASA y puntuación de riesgo de NVPO según la escala de Apfel[16]. La escala de Apfel considera 4 predictores de NVPO: género femenino, antecedentes previos de NVPO o mareo, no fumadores y uso de opioides perioperatorios; asignando un punto a cada factor presente[16].
Aleatorización y cegamiento
La asignación de los pacientes a los grupos de intervención se realizó mediante una secuencia aleatoria generada por computador, utilizando un algoritmo de aleatorización simple. La secuencia fue aplicada por un investigador externo, independiente del equipo clínico y del personal encargado de recolectar los datos. El estudio fue simple ciego: tanto los pacientes como el recolector de datos desconocían el grupo asignado. Por razones técnicas relacionadas con la administración anestésica, el equipo anestesiológico no fue cegado.
Intervenciones
Ambos protocolos (ALO y ARO) se enmarcaron en guías de recuperación acelerada para cirugía bariátrica, con indicaciones estandarizadas tanto para la preparación preoperatoria como para el manejo posoperatorio, incluyendo una estrategia de analgesia multimodal con opioides de rescate.
Todos los pacientes recibieron premedicación 4 h antes de la cirugía con paracetamol 1 g y etoricoxib 120 mg vía oral, además de 300 ml de bebida isotónica. El manejo intraoperatorio incluyó monitoreo estándar (presión arterial no invasiva, electrocardiografía de tres derivaciones, pulsioximetría continua y capnografía), manteniéndose en todo momento normotermia, normoglicemia y normovolemia. Se empleó ventilación protectora con flujos bajos (1 L/min), desflurano como agente anestésico (ET-MAC 0,8-1,0) con FIO2 al 50%, y ventilación controlada por volumen (6-8 ml/kg) con PEEP de 5-8 cmH2O. Todos los fármacos se dosificaron según peso ideal (kg = talla2 x 25).
Grupo ARO:
Inducción anestésica con fentanilo (máximo 250 mcg), lidocaína (1-1,5 mg/kg), propofol (2-2,5 mg/kg), rocuronio (0,6 mg/kg; repetir si TOF > 40%), sulfato de magnesio (2,5 g), ketamina (0,5 mg/kg), dexametasona (8 mg), ketoprofeno (100 mg), metamizol (2 g), metoclopramida (10 mg) y cefazolina (2-3 g según peso). Se administró una infusión continua de dexmedetomidina (0,2-0,6 mcg/kg/h) hasta el final de la cirugía. Al cierre de piel, se infiltraron los puertos laparoscópicos con bupivacaína al 0,25 % (5-10 ml por puerto), y se administraron paracetamol 1 g y ondansetrón 0,1 mg/kg (máximo 8 mg).
Grupo ALO:
No se utilizó fentanilo. Se administró una dosis de carga de dexmedetomidina (0,25 mcg/kg) en bolo lento 15 minutos previo a la inducción, además de lidocaína (1,5 mg/kg) y ketamina (0,5 mg/kg). La infusión continua consistió en una solución de 50 ml de suero fisiológico con lidocaína 500 mg, ketamina 50 mg y dexmedetomidina 50 mcg, a una velocidad de 0,1 ml/ kg/h, ajustada según las variables hemodinámicas.
El manejo posoperatorio fue estandarizado en ambos grupos, incluyendo paracetamol 1 g cada 8 h EV, bomba de infusión con metamizol (4 g), ketoprofeno (300 mg) y droperidol (2 mg) administrados durante 24 h. Se indicó morfina 1 mg EV como analgesia de rescate en la unidad de recuperación.
Determinación de resultados
El desenlace primario fue la incidencia de NVPO en las primeras 24 h posoperatorias. Náuseas y vómitos fueron evaluados por separado: náuseas en una escala de 0 a 5 (0 = sin náuseas, 1 = náuseas previstas, 2 = náuseas leves, 3 = náuseas moderadas, 4 = náuseas severas y 5 = náuseas intensas), y vómitos en formato dicotómico (presencia/ausencia).
Los desenlaces secundarios incluyeron:
Los datos fueron registrados en la URPA y en la ficha clínica electrónica, mediante formularios estandarizados.
Análisis estadístico
El tamaño muestral fue calculado con base en la comparación de proporciones para dos grupos independientes, considerando como variable principal la incidencia de náuseas y vómitos posoperatorios en pacientes sometidos a cirugía bariátrica. De acuerdo con la literatura, la incidencia promedio de NVPO en anestesia convencional basada en opioides en cirugía bariátrica se estima en 37%[5]. Se planteó como objetivo una reducción clínica significativa de dicha incidencia al 10% mediante el uso de anestesia libre de opioides (ALO/OFA), con un nivel de confianza del 95% (a = 0,05) y una potencia del 80% (P = 0,20), obteniéndose un tamaño muestral mínimo de 124 pacientes (62 por grupo). Para compensar posibles pérdidas de seguimiento, datos incompletos o exclusiones, se planificó incluir un total de 140 pacientes.
Las variables categóricas se expresaron en frecuencias y porcentajes; las variables continuas, en medias y desviación estándar. Para comparar las tasas de NVPO entre los grupos ALO/ OFA y ARO/OLA se utilizó la prueba de chi-cuadrado. El nivel de significancia se estableció en p < 0,05. Los intervalos de confianza se calcularon al 95%. El análisis estadístico se realizó con elsoftware STATA versión 18.
Consideraciones éticas
El estudio fue aprobado por el Comité de Ética de la Clínica Dávila. Todos los participantes firmaron consentimiento informado. Ambos grupos recibieron analgesia multimodal efectiva y acceso a opioides de rescate, garantizando que no se expusieran a riesgos adicionales. La confidencialidad de los datos fue resguardada conforme a la normativa vigente.
Resultados
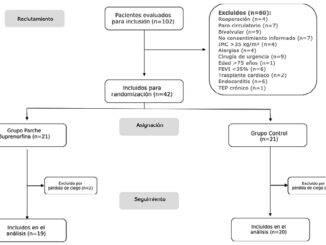
Durante el período comprendido entre marzo y octubre de 2024, se reclutaron un total de 134 pacientes, de los cuales 66 fueron asignados al grupo ALO y 68 al grupo ARO. El reclutamiento fue detenido anticipadamente en noviembre de 2024, debido a la falta de disponibilidad de ketamina a nivel nacional, lo que imposibilitó continuar aplicando el protocolo. No obstante, dado que todos los pacientes reclutados completaron el seguimiento y no se registraron pérdidas, se decidió cerrar el proceso de reclutamiento con esa muestra.
Las características basales de ambos grupos fueron comparables en cuanto a edad, sexo, IMC, tipo de cirugía realizada (manga gástrica obypass gástrico), y comorbilidades relevantes (HTA, diabetes mellitus tipo 2, dislipidemia, hipotiroidismo y SAOS, además de las puntuaciones en las escalas STOP-BANG, ASA y Apfel[16]; éstas se representan en la Tabla 1.
Respecto al desenlace primario, no se observaron diferencias estadísticamente significativas en la incidencia de vómitos posoperatorios (5,9% en ALO [CI 3,7-9,0] vs. 4,8% en ARO [CI 2,8-7,8]; p = 0,996) ni de náuseas (13,4% en ALO vs. 9,1% en grupo ARO; p = 0,055), con una mediana de náuseas de 0 en ambos grupos según la escala de 0 a 5. Los resultados se presentan en la Figura 1.
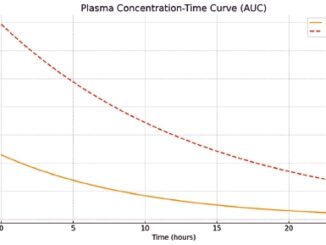
En cuanto a los desenlaces secundarios, el área bajo la curva (AUC) del dolor posoperatorio fue mayor en el grupo ALO (AUC 33 vs. 20; p = 0,008), aunque las puntuaciones EVA no superaron los 3 puntos en ninguno de los grupos (Figura 2).
El consumo de morfina posoperatoria fue significativamente mayor en el grupo ALO (AUC 0,88 vs. 0,42 mg; p = 0,0053), aunque limitado en términos absolutos y sin requerimientos adicionales después de las 12 h posoperatorias (Figura 3).
No hubo diferencias significativas en la duración de la hospitalización (p = 0,8376), representado en la Figura 4. No se evidenció diferencias en la incidencia de retención urinaria entre los grupos (p = 0,597).
Tabla 1. Características de la población
| ARO n = 68 | ALO n = 66 | |
|---|---|---|
| Mujeres n (%) | 51 (75,0) | 45 (68,2) |
| Edad (años)* | 40,8 ± 10,7 | 38,2 ± 11,0 |
| IMC ((kg • m-2)* | 38,2 ± 4,3 | 39,5 ± 4,8 |
| Manga/Bypass gástrico (%) | 58,2/41,2 | 57,6/42,4 |
| HTA n (%) | 31 (42,9) | 26 (41,4) |
| DM2NIR n (%) | 6 (8,8) | 4 (6,1) |
| DM2IR n (%) | 3 (4,4) | 0 (0,0) |
| DLP n (%) | 50 (73,5) | 38 (57,6) |
| Hipotiroidismo n (%) | 8 (11,8) | 8 (12,1) |
| Insulino-resistencia n (%) | 51 (75,0) | 54 (81,8) |
| SAOS CON C-PAP n (%) | 14 (20,6) | 11 (16,7) |
| SAOS SIN C-PAP* n (%) | 5 (7,4) | 11 (16,7) |
| Hígado graso n (%) | 25 (36,7) | 28 (42,4) |
| STOP-BANG** | 3,0 (2) | 3,0 (2) |
| ASA n (%) | ||
| II | 47 (69,1) | 33 (50,0) |
| III | 21 (30,9) | 33 (50,0) |
| Escala de Apfel n (%) | ||
| I | 17 (25,0) | 21 (31,8) |
| II | 49 (72,1) | 42 (63,6) |
| III | 2 (2,9) | 3 (4,6) |
| Duración cirugía (min)** | 105 (59) | 103 (61) |
Figura 1. Incidencia de náuseas y vómitos según tipo de anestesia.
Figura 2. Dolor posoperatorio según grupo.
Figura 3. Consumo de morfina posoperatoria según grupo.
Figura 4. Estadía hospitalaria.
Discusión
Las náuseas y vómitos posoperatorios tienen una etiología multifactorial y representan la causa más frecuente de readmisión en pacientes sometidos a cirugía bariátrica[17],[18]. Su incidencia está determinada por factores propios del paciente, el tipo de cirugía y los fármacos utilizados, especialmente los opioides. En pacientes con obesidad mórbida sometidos a cirugía bariátrica, la incidencia de NVPO es mayor que en la población general. Según la literatura, el uso de anestesia general basada en opioides se asocia con incidencias de NVPO que varían entre el 30% y el 60% [5],[8],[10],[14],[18].
En nuestro estudio, la incidencia de NVPO en ambos grupos fue considerablemente menor que la reportada en la literatura. El grupo control (ARO) presentó una incidencia de náuseas inferior al 10% y de vómitos menor al 5%. En el grupo intervención (ALO), no se observaron diferencias estadísticamente significativas en comparación con el grupo control, lo que contrasta con lo descrito en estudios previos[5],[10],[18]. Una posible explicación para esta discrepancia es la forma en que se midió la NVPO: los estudios mencionados evalúan la incidencia de NVPO como una entidad única, mientras que en nuestro trabajo se midieron por separado las náuseas y los vómitos. Además, nuestros protocolos ALO y ARO están integrados dentro de un enfoque ERAS, lo que podría contribuir a la baja incidencia de efectos adversos como la NVPO. Esto sugiere que la simple eliminación de opioides no garantiza, por sí sola, una reducción en la incidencia de NVPO, especialmente en el contexto de la cirugía bariátrica, donde confluyen múltiples factores de riesgo.
La baja incidencia de NVPO en el grupo ARO podría limitar el margen de mejora atribuible al uso de ALO en nuestro centro. Entre los factores que podrían haber influido en estos resultados, destaca el tamaño muestral, el cual fue calculado en base a una incidencia del 30% reportada en la literatura. Sin embargo, esta cifra no se reflejó en nuestro grupo control, lo que podría haber afectado la capacidad del estudio para detectar diferencias en el desenlace primario.
Respecto a los desenlaces secundarios, nuestros resultados muestran que el grupo ALO presentó mayor dolor posoperatorio y un mayor consumo acumulado de morfina, ambos con significancia estadística. No obstante, en términos absolutos, ambos grupos mostraron niveles bajos: el dolor posoperatorio
en las primeras 24 h fue menor a 3 en la escala EVA y no se requirió analgesia con opioides más allá de las primeras 12 h posoperatorias.
Estos hallazgos difieren del metaanálisis publicado recientemente por Yichan et al.[19], que no evidenció diferencias significativas en dolor posoperatorio ni en el consumo de morfina entre los grupos ALO, ARO y anestesia basada en opioides en cirugía bariátrica. Asimismo, el metaanálisis de Hung et al.[10], reportó una reducción significativa en el dolor en el grupo ALO durante las primeras 24 h, aunque la diferencia en la escala EVA no superó un punto, lo cual podría no ser clínicamente relevante. La mayor intensidad de dolor y el mayor consumo de morfina observados en nuestro grupo ALO han sido también descritos en otras series[13], lo que sugiere que los esquemas libres de opioides podrían requerir ajustes o estrategias complementarias para garantizar un control analgésico adecuado.
Entre las fortalezas de este estudio destacan su diseño aleatorizado y ciego, así como la evaluación en un entorno clínico real, lo que favorece su aplicabilidad externa. La homogeneidad de la población y la estandarización de los procedimientos también fortalecen su validez interna. Además, no contamos con estudios randomizados que comparen ALO y anestesia basada en opioides en población chilena, lo que constituye una contribución novedosa y relevante para la práctica anestésica local, aportando evidencia contextualizada que puede guiar futuras decisiones clínicas y de investigación.
No obstante, deben considerarse algunas limitaciones. En primer lugar, el carácter unicéntrico del estudio podría restringir la generalización de los resultados. En segundo lugar, el tamaño muestral podría no haber tenido el poder estadístico suficiente para detectar diferencias sutiles en otros desenlaces. Además, la evaluación del dolor y de los NVPO puede estar influida por factores subjetivos no controlados, como la tolerancia individual, el umbral de percepción o las expectativas del paciente. Finalmente, el período de observación limitado a 24 h podría haber omitido eventos adversos o efectos analgésicos tardíos.
En conjunto, los hallazgos de este estudio sugieren que la elección entre ALO y ARO en cirugía bariátrica debe considerar múltiples dimensiones clínicas, más allá de la incidencia de NVPO, como el control del dolor, la experiencia del equipo clínico y la disponibilidad de recursos. La tendencia a un mayor dolor posoperatorio en el grupo ALO resalta la necesidad de protocolos analgésicos cuidadosamente ajustados para asegurar una analgesia efectiva.
La ALO en nuestro estudio mantuvo la baja incidencia de NVPO del grupo control y se presenta también como una alternativa válida a usar en algunas poblaciones de pacientes en que el uso de opioides no es aconsejable.
Este estudio abre la brecha para la realización de estudios multicéntricos con muestras más amplias, que permitan evaluar distintas combinaciones de fármacos y enfoques anestésicos. Esto podría contribuir a optimizar los regímenes ALO y a mejorar el manejo del dolor posoperatorio en pacientes sometidos a cirugía bariátrica.
Conclusiones
Los resultados mostraron una incidencia muy baja de NVPO en ambos grupos, menor a lo reportando en la literatura. No evidenciaron diferencias estadísticamente significativas entre ambos grupos en cuanto a la incidencia de vómitos, se observó una tendencia mayor a náuseas en el grupo ALO.
Respecto a los desenlaces secundarios, el grupo ALO presentó mayor dolor posoperatorio (ninguno superando EVA 3) y mayor consumo de morfina de forma limitada. No hubo diferencias en tiempo de hospitalización ni retención urinaria.
La ALO puede constituir una alternativa válida en determinados contextos, siempre que se implemente dentro de un protocolo cuidadosamente ajustado que garantice un adecuado control del dolor posoperatorio.
Referencias
1. Beloeil H. Opioid-free anesthesia. Best Pract Res Clin Anaesthe- siol. 2019 Sep;33(3):353-60. https://doi.Org/10.1016/j.bpa.2019.09.002 PMID:31785720
2. Egan TD. Are opioids indispensable for general anaesthesia? Br J Anaesth. 2019 Jun;122(6):e127-35. https://doi.Org/10.1016/j.bja.2019.02.018 PMID:31104756
3. Koepke EJ, Manning EL, Miller TE, Ganesh A, Williams DG, Manning MW. The rising tide of opioid use and abuse: the role of the anesthesiologist. Perioper Med (Lond). 2018 Jul;7(1):16. https:// doi.org/10.1186/s13741-018-0097-4 PMID:29988696
4. Hedegaard H, Warner M, Minino AM. Drug Overdose Deaths in the United States, 1999-2016. NCHS Data Brief. 2017 Dec;(294):1-8. PMID:29319475
5. Ziemann-Gimmel P, Goldfarb AA, Koppman J, Marema RT. Opioid-free total intravenous anaesthesia reduces postoperative nausea and vomiting in bariatric surgery beyond triple prophylaxis. Br J Anaesth. 2014 May;112(5):906-11. https://doi.org/10.1093/bja/aet551 PMID:24554545
6. Barakat H, Al Nawwar R, Abou Nader J, Aouad M, Yazbeck Karam V, Gholmieh L. Opioid-free versus opioid-based anesthesia in major spine surgery: a prospective, randomized, controlled clinical trial. Minerva Anestesiol. 2024 Jun;90(6):482-90. https://doi.org/10.23736/S0375-9393.24.17962-X PMID:38869262
7. Ulbing S, Infanger L, Fleischmann E, Prager G, Hamp T. The Performance of Opioid-Free Anesthesia for Bariatric Surgery in Clinical Practice. Obes Surg. 2023 Jun;33(6):1687-93. https://doi.org/10.1007/s11695-023-06584-5 PMID:37106268
8. Mulier JP, Wouters R, Dillemans B, Dekock M. A randomized controlled, double-blind trial evaluating the effect of opioid-free versus opioid general anaesthesia on postoperative pain and discomfort measured by the QoR-40. J Clin Anesth Pain Med. 2018;6:2.
9. Mulier J. Opioid free general anesthesia: A paradigm shift? Rev Esp Anestesiol Reanim. 2017 Oct;64(8):427-30. https://doi. org/10.1016/j.redar.2017.03.004 PMID:28431750
10. Hung KC, Chiu CC, Hsu CW, Lin CM, Liao SW, Teng IC, et al. Impact of Opioid-Free Anesthesia on Analgesia and Recovery Following Bariatric Surgery: a Meta-Analysis of Randomized Controlled Studies. Obes Surg. 2022 Sep;32(9):3113-24. https://doi.org/10.1007/s11695-022-06213-7 PMID:35854095
11. Cheng L, Liu J, Qin S, Geng X, Jing L, Fang S. Safety and effectiveness of multimodal opioid-free anaesthesia for pain and recovery after laparoscopic surgery: a systematic review and meta-analysis. BMJ Open. 2025 Mar;15(3):e085988. https://doi.org/10.1136/bmjopen-2024-085988 PMID:40122555
12. Kositanurit W, Muntham D, Udomsawaengsup S, Chirakalwasan N. Prevalence and associated factors of obstructive sleep apnea in morbidly obese patients undergoing bariatric surgery. Sleep Breath. 2018 Mar;22(1):251-6. https://doi.org/10.1007/s11325- 017-1500-y PMID:28396972
13. Clanet M, Touihri K, El Haddad C, Goldsztejn N, Himpens J, Fils JF, et al. Effect of opioid-free versus opioid-based strategies during multimodal anaesthesia on postoperative morphine consumption after bariatric surgery: a randomised doubleblind clinical trial. BJA Open. 2024 Feb;9:100263. https://doi.org/10.1016/j.bjao.2024.100263 PMID:38435809
14. Domene SS, Fulginiti D, Thompson A, et al. Regímenes de anestesia inhalatoria y anestesia intravenosa total (TIVA) en pacientes con obesidad: una revisión sistemática actualizada y un metaa- nálisis de ensayos controlados aleatorizados. J Anesth Analg Crit Care. 2025;5:15. https://doi.org/10.1186/s44158-025-00234-1 PMID:40098208
15. Léger M, Perrault T, Pessiot-Royer S, Parot-Schinkel E, Costerousse F, Rineau E, et al. Opioid-free Anesthesia Protocol on the Early Quality of Recovery after Major Surgery (SOFA Trial): A Randomized Clinical Trial. Anesthesiology. 2024 Apr;140(4):679-89. https://doi.org/10.1097/ALN.0000000000004840 PMID:37976460
16. Apfel CC, Läärä E, Koivuranta M, Greim CA, Roewer N. A simplified risk score for predicting postoperative nausea and vomiting: conclusions from cross-validations between two centers. Anesthesiology. 1999 Sep;91(3):693-700. https://doi.org/10.1097/00000542-199909000-00022 PMID:10485781
17. Mieszczanski P, Kotacz M, Trzebicki J. Opioid-Free Anesthesia in Bariatric Surgery: Is It the One and Only? A Comprehensive Review of the Current Literature. Healthcare (Basel). 2024 May;12(11):1094. https://doi.org/10.3390/healthcare12111094 PMID:38891169
18. Groene P, Eisenlohr J, Zeuzem C, Dudok S, Karcz K, HofmannKiefer K. Postoperative nausea and vomiting in bariatric surgery in comparison to non-bariatric gastric surgery. Wideochir Inne Tech Malo Inwazyjne. 2019 Jan;14(1):90-5. https://doi.org/10.5114/wiitm.2018.77629 PMID:30766634
19. Ao Y, Ma J, Zheng X, Zeng J, Wei K. Opioid-Sparing Anesthesia Versus Opioid-Free Anesthesia for the Prevention of Postoperative Nausea and Vomiting after Laparoscopic Bariatric Surgery: A Systematic Review and Network Meta-Analysis. Anesth Analg. 2025 Feb;140(2):385-96. https://doi.org/10.1213/ANE.0000000000006942 PMID:38578868

 ORCID
ORCID