Karina Ortega A.1, Karol N. Cabeza Díaz2, Diego F. Ordoñez Tellez3, Ximena Cediel Carrillo2
Recibido: 2025-08-14
Aceptado: 2025-12-04
©2026 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 55 Núm. 2 |https://doi.org/10.25237/revchilanestv55n2-01
PDF
Functional approach to the pathophysiology of chronic pain, a narrative review of the literature
Abstract
Classical pain mechanisms are categorized into nociceptive, inflammatory, and pathological types. Nociceptive pain arises from tissue injury, inflammatory pain from an exaggerated response to stimuli, and pathological pain from altered neuronal processing, including neuropathic and dysfunctional pain. This review explores lesser-discussed mechanisms of chronic pain to identify new therapeutic targets. An exploratory scoping review was conducted using major databases and university repositories, with consensus on article inclusion. The role of mitochondrial dysfunction, vitamin imbalance, HPA axis alterations and intestinal dysbiosis will allow us to discover new therapeutic targets and improve chronic pain management strategies.
Resumen
Los mecanismos clásicos del dolor se clasifican en tipos nociceptivos, inflamatorios y patológicos. El dolor nociceptivo surge de una lesión tisular, el dolor inflamatorio de una respuesta exagerada a los estímulos y el dolor patológico de un procesamiento neuronal alterado, el cual incluye tanto al dolor neuropàtico cómo al disfuncional. Esta revisión explora mecanismos menos discutidos del dolor crónico para identificar nuevos objetivos terapéuticos. Se realizó una revisión exploratoria del alcance utilizando las principales bases de datos y repositorios universitarios, con consenso sobre la inclusión de artículos. El rol de la disfunción mitocondrial, el desequilibrio vitamínico, las alteraciones del eje HPA y la disbiosis intestinal nos permitirán descubrir nuevos objetivos terapéuticos y mejorar las estrategias de manejo del dolor crónico.
Introducción
La categorización clásica de los tipos de dolor nos muestra tres principales mecanismos fisiopatológicos en los cuales se pueden encasillar las manifestaciones dolorosas. El dolor nociceptivo se da por una lesión tisular continua (estímulo mecánico, térmico o químico)[1],[2]. El segundo tipo de dolor es el inflamatorio en el que el sistema nervioso sufre un cambio profundo en su capacidad de respuesta, volviendo las respuestas a los estímulos exageradas y prolongadas pudiendo activarse mediante estímulos inocuos de bajo umbral. Por lo general, el dolor inflamatorio desaparece después de la resolución de la lesión tisular; sin embargo, en algunas enfermedades como la artritis reumatoide, el dolor puede persistir mientras la inflamación está activa, lo que se conoce cómo dolor patológico, el tercer tipo de dolor. Su principal diferencia es que el inflamatorio representa una reacción de hipersensibilidad a una patología periférica definida, mientras que el patológico resulta de un procesamiento neuronal alterado y aberrante[1],[2]. Este último puede ocurrir mediante dos principales vías: daño al sistema somatosensorial (dolor neuropático), pero también en condiciones en las que no existe tal daño o inflamación (dolor disfuncional)[1].
No obstante, existen una gran variedad de mecanismos moleculares por los cuales se activan estas vías de dolor lo que lleva a que no se entiendan a la perfección. Enfocándose específicamente en los dolores patológicos, no existe una teoría que englobe todas la vías implicadas pero se cree que tanto los cambios en el número de canales iónicos que resulta en sensibilización central y periférica, la reorganización cortical, desinhibición de los circuitos neuronales y cambios moleculares como resultado de la respuesta inmune después del daño nervioso y simpático son los responsables de la perpetuación del dolor[2],[3].
Desde una perspectiva holística se quieren abordar en esta revisión algunos de estos mecanismos poco discutidos en la literatura, desde una enfoque funcional de la fisiopatología del dolor crónico para así encontrar nuevos blancos terapéuticos y alternativas de manejo.
Métodos
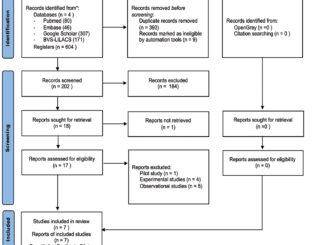
El objetivo de esta publicación fue realizar una revisión narrativa de alcance sobre la literatura disponible acerca de los diferentes enfoques funcionales en la fisiopatología del dolor crónico, con el propósito de ofrecer un abordaje integral y alternativo al paradigma convencional. Para ello, los autores efectuaron de manera independiente una búsqueda en las bases de datos PubMed, Scopus, Google Scholar, LILACS y AccessMedicine, así como en repositorios universitarios. Se emplearon como términos clave:dolor crónico, disfunción mitocondrial, disbiosis intestinal y eje hipotálamo-hipófisis-adrenal, combinados con descriptores relacionados como cortisol y estrés. La selección de artículos se realizó considerando la relevancia clínica y fisiopatológica de los estudios identificados.
Resultados y Discusión
La mitocondria es un sistema complejo de doble membrana que cumple diferentes funciones cómo organelo entre las cuales destacan la producción energética de la célula mediante mecanismos de fosforilación oxidativa (OxPhos), reacciones redox, homeostasis del calcio y regulación del ciclo celular[4],[5],[6],[7]. Pero más allá de estas funciones, la mitocondria cuenta con su propio material genético, codificando hasta para el 5% de las proteínas de los mamíferos[4],[7].
La homeostasis mitocondrial hace referencia al mantenimiento de un número estable de mitocondrias funcionales a lo largo del cuerpo mediante diferentes mecanismos tales cómo la biogénesis, fisión, fusión y autofagia[6]. Actualmente, se cree que existen tres tipos de procesos principales de señalización mitocondrial, que le permiten a este organelo influir directa o indirectamente en una serie de procesos celulares ya mencionados. Estos pueden resumirse conceptualmente como contacto mitocondrial directo, tráfico vesicular especializado y transmisión mediante la producción y liberación de metabolitos de señalización[8]. Son la disrupción de estas vías de señalización las que, al día de hoy, la evidencia muestra están relacionadas con enfermedades neurodegenerativas, autoinmunes y autoinflamatorias[7],[8]. Por ejemplo, se ha demostrado que un disbalance del ambiente intracelular secundario a alteraciones mitocondriales juega un rol primordial en la fisiopatología de la artritis reumatoidea[9].
Ahora bien, la relación que existe entre la disfunción mitocondrial y el dolor no es nueva. Se ha reportado que hasta 70% de los humanos con defectos mitocondriales hereditarios desarrollan dolor crónico así cómo manifestaciones neurodegenerativas a lo largo de su vida[5],[10],[16]. Sin embargo, se cree que existen diferentes mecanismos por los cuales esto se genera, los cuales serán mencionados a continuación.
La respiración celular, o fosforilación oxidativa (OxPhos), se lleva acabo en la membrana mitocondrial interna bajo una estructura de transporte de electrones en cadena conformada por cinco complejos moleculares que permiten la producción del ATP[4]. El 90% de las moléculas de ATP que utilizan las neuronas se producen bajo la OxPhos, lo que significa que una disminución de su actividad se traduce en daño celular, disminución de la plasticidad neuronal y muerte debido al alto requerimiento energético que conllevan las células del sistema nervioso[5]. Modelos animales muestran que diferentes estados de dolor crónico, especialmente los mediados por quimioterapéuticos, evidencian una disminución en la OxPhos por diferentes mecanismos, incluyendo las citoquinas proinflamatorias cómo el TNF o IFNy[16],[5]. Esto se puede evidenciar de igual forma en una larga lista de enfermedades cuya mediación se da por estas señales cómo es la osteoartritis crónica[17].
Se ha sabido por muchos años que la mitocondria funciona cómo un reservorio intracelular de calcio (Ca2+). No obstante, la razón y los mecanismos de su activación no se encuentran claros. Se ha descrito que la saturación intracelular de Ca2+ podría activar poros mitocondriales que conllevan a su acumulación intramitocondrial[5],[15]. En la normalidad, este calcio funciona cómo materia prima en la cadena oxidativa del ciclo del ácido cítrico[4]. Sin embargo, en caso de sobresaturación mitocondrial de Ca2+, los poros mPTP liberan al citoplasma el Ca2+ junto con otras moléculas, tales cómo el citocromo C, lo que induce la apoptosis[5],[15]. De igual forma existe un daño a la cadena respiratoria causando una falla de los mismos procesos que desarrollan y mantienen el potencial debido a la fuga de protones[15].
En modelos animales son muchos los mecanismos que muestran estos aumento citosólicos de Ca2+, siendo las citoquinas proinflamatorias uno de ellos así como el daño neuronal mediado por quimioterapéuticos cómo el cisplatino, oxaliplatino, paclitaxel[5],[7]. Es así como cualquier disfunción en la homeostasis intracelular del Ca2+ genera apoptosis, lo que conlleva a daño neuronal y desmielinización aportando a los mecanismos etiológicos del dolor crónico.
En la neuropatía diabética y en algunas enfermedades neurodegenerativas se ha demostrado que la disfunción mitocondrial y posterior acumulación de ROS son cambios patológicos típicos que podemos encontrar[5],[11]. En las personas sanas, la autofagia mediada por Parkin y P53 permite que las mitocondrias no funcionales sean descartadas, sin embargo, una alteración del equilibrio Parkin/P53 generaría una acumulación de estas, generando a su vez una sobre producción de ROS y de esta forma resultando en daño neuronal irreversible[11]. La razón de esto es la capacidad de las ROS para la generación de estrés oxidativo que supera la capacidad antioxidante máxima de cada célula[4],[5]. La sensibilidad celular que presentan las neuronas frente a tales ambientes intracelulares se debe tanto a su alta tasa metabólica, cómo a su composición (proteínas, lípidos y ácidos grasos sensibles al estrés oxidativo)[5],[12],[13].
Otro ejemplo de esto serían los marcadores de estrés oxidativo que se encuentran presentes cómo uno de los muchos mecanismos fisiopatológicos de la fibromialgia y la osteoartritis y que al usarse cómo blanco terapéutico se ha visto mejoría del dolor[5],[13],[17]. Estos marcadores muestran que un aumento de ROS inhiben la vía PI3K/Akt y activan la vía MEK/ERK favoreciendo el estado proinflamatorio permanente[17]. Finalmente, la administración intraperitoneal de antioxidantes redujo considerablemente la producción de ROS y atenuó los niveles de dolor en los modelos experimentales demostrando que su producción conlleva a disfunción neuronal y dolor crónico[5],[14].
El rol que juegan las vitaminas en el cuerpo es amplio pero no muy claro en su totalidad. Se obtienen de una dieta saludable y balanceada y se sabe que su disbalance, en exceso o déficit, conlleva repercusiones en la salud de diferentes maneras[18]. Son muchos los mecanismos por los cuales se han relacionado las vitaminas con los procesos dolorosos que experimenta el ser humano, sin embargo, son dos las vitaminas principales relacionadas con estas vías: Complejo B y vitamina D.
Los efectos musculoesqueléticos de la vitamina D son ampliamente conocidos, además, se ha relacionado su deficiencia con el dolor muscular difuso y la sarcopenia[19],[20]. Esto se ve evidenciado también en la eficacia de la administración de vitamina D en la mejoría del dolor crónico, mostrando que pacientes con niveles de 25OHD < 20 ng/mL tienen mayor riesgo de perpetuar procesos dolorosos crónicos[19],[23]. Modelosin vitro han mostrado el efecto antiinflamatorio mediante la reducción de la síntesis de prostaglandina E2 y se ha mostrado una relación directa con procesos dolorosos crónicos cómo la fibromialgia[21]. Pero no solo se relaciona con el dolor muscu- loesquelético, múltiples estudios muestran su relación con la deprivación del sueño y cefalea, disminuyendo su intensidad y frecuencia a medida que los niveles de vitamina D aumentaban[22],[23]. Existen otros procesos menos estudiados que involucran los niveles de vitamina D con el dolor crónico, por ejemplo, estas alteraciones vitamínicas tienen una implicación directa en la microbiota intestinal relacionado con procesos cómo el síndrome de intestino irritable, tema que será discutido más adelante[24].
Por otro lado, el complejo B, específicamente las vitaminas neurotrópicas (B1-tiamina, B6-piridoxina, B12-cianocobalamina), son mecanismos neuromoduladores de dolor e inflamación[25]. Se ha demostrado que niveles óptimos de vitamina B12 soportan la regeneración nerviosa que resulta en mejoría del dolor crónico, así cómo un efecto ahorrador de opioides lo que reduciría la necesidad de altas dosis de los mismos[26],[27].
El eje Hipotalamo-Hipofisis-Adrenal (HHA) es uno de los mecanismos con los que cuenta el ser humano para responder ante los estímulos estresores, codificando un conjunto de manifestaciones cognitivas, conductuales y endocrinas al estrés[32]. En condiciones normales, ante el estímulo estresor, el eje HHA conlleva una cascada neuroendocrina que finaliza en la liberación de cortisol, el cual es fundamental en estas situaciones. El eje cuenta con un mecanismo de retroalimentación negativa volviendo el sistema a su estado previo una vez que el estresor desaparece. Se sabe que el HHA juega un rol fundamental en las vías del dolor, sin embargo, no se conoce muy bien, y de hecho se hayan discrepancias en lo reportado por la literatura[35].
La premisa inicial de la relación cortisol/dolor era que en los casos en los que el estrés persiste en el tiempo, la constante liberación de corticosteroides genera una desadaptación del eje, perdiéndose la capacidad de retroalimentación negativa, favoreciendo los efectos nocivos del cortisol en el cuerpo[32],[33],[35]. Existe importante evidencia soportando tal premisa. Ejemplos cómo la reducción en los niveles de cortisol matutino después de terapias, cómo los masajes suecos y su relación con la mejoría en la calidad de vida de los pacientes con fibromialgia nos orientan a pensar esto[34]. En modelos animales esto se evidencia en los roedores en los cuales hipersensibilidad visceral se presenta cuando existen niveles altos de CRH y ACTH en sangre y a nivel glandular[36].
Por otro lado, múltiples estudios demuestran que bajos niveles de cortisol se han reportado en pacientes con fibromialgia, encontrando un impacto de los niveles de estrés en la reducción de la calidad de vida de estos pacientes, pero no relacionado con un aumento en los niveles de glucocorticoides[31]. Otros estudios demuestran que los individuos con una respuesta de cortisol más robusta reportaron menos niveles de dolor y que su secreción regula la respuesta al dolor agudo. De hecho, los pacientes con lesiones agudas que no tienen una respuesta adecuada de cortisol corren el riesgo de desarrollar dolor crónico posterior[30].
Lo que sí está claro es que los pacientes con eventos traumáticos generan disregulación del eje HHA y, aunque no se tenga certeza de cuál es su mecanismo en las vías del dolor, existe evidentemente la relación directa con una respuesta dolorosa crónica. Un ejemplo de esto es la cistitis intersticial, enfermedad comúnmente presentada en mujeres que se caracteriza por dolor pélvico crónico, encontrando una mayor incidencia de eventos traumáticos tempranos en estas pacientes comparadas con el grupo control[29]. Eventos traumáticos se han relacionado con alteraciones neuroendocrinas e inflamatorias, cómo es el caso del síndrome de intestino irritable en quienes se reportan alta incidencia comórbida de estrés, angustia y ansiedad comparados con los pacientes sanos[28].
El término xenobióticos proviene del griegoxenos (extranjero) y bios (vida), significando cosas extranjeras en forma de vida. Los xenobióticos son químicos encontrados pero no producidos en organismos o en el medio ambiente y se encuentran en el aire, suelo, agua, plantas, animales y humanos, y se clasifican como pesticidas, compuestos farmacéuticos, productos de cuidado personal, drogas ilícitas, productos industriales y desechos nucleares. Estos compuestos son difíciles de degradar debido a sus estructuras moleculares complejas.
Los mecanismos mediante los cuales los factores ambientales alteran los procesos biológicos básicos para desencadenar enfermedades autoinmunes continúan siendo estudiados, pero en gran medida son desconocidos. Los humanos están expuestos diariamente a una amplia gama de xenobióticos que pueden incluir diferentes clases de moléculas (por ejemplo, aditivos alimentarios, drogas, pesticidas, contaminantes de procesos y contaminantes ambientales) que pueden ingresar al cuerpo humano a través de múltiples vías, incluyendo contacto con la piel, inhalación e ingestión[37],[38].
Se destacan los métodos de eliminación de xenobióticos, como la biotransformación, biorremediación, fitorremediación, adsorción, procesos avanzados de oxidación, humedales construidos y procesos de membrana. Para minimizar los efectos negativos de los xenobióticos y reducir su uso, organizaciones a nivel mundial han aprobado directivas y regulaciones para monitorearlos. La lista de contaminantes prioritarios y compuestos nocivos se actualiza regularmente con todos los compuestos detectados, junto con el desarrollo y modernización de métodos. Comprender las complejas interacciones en la cadena entre el huésped, el microbioma y el exposoma es esencial para evaluar los impactos ambientales en la salud.
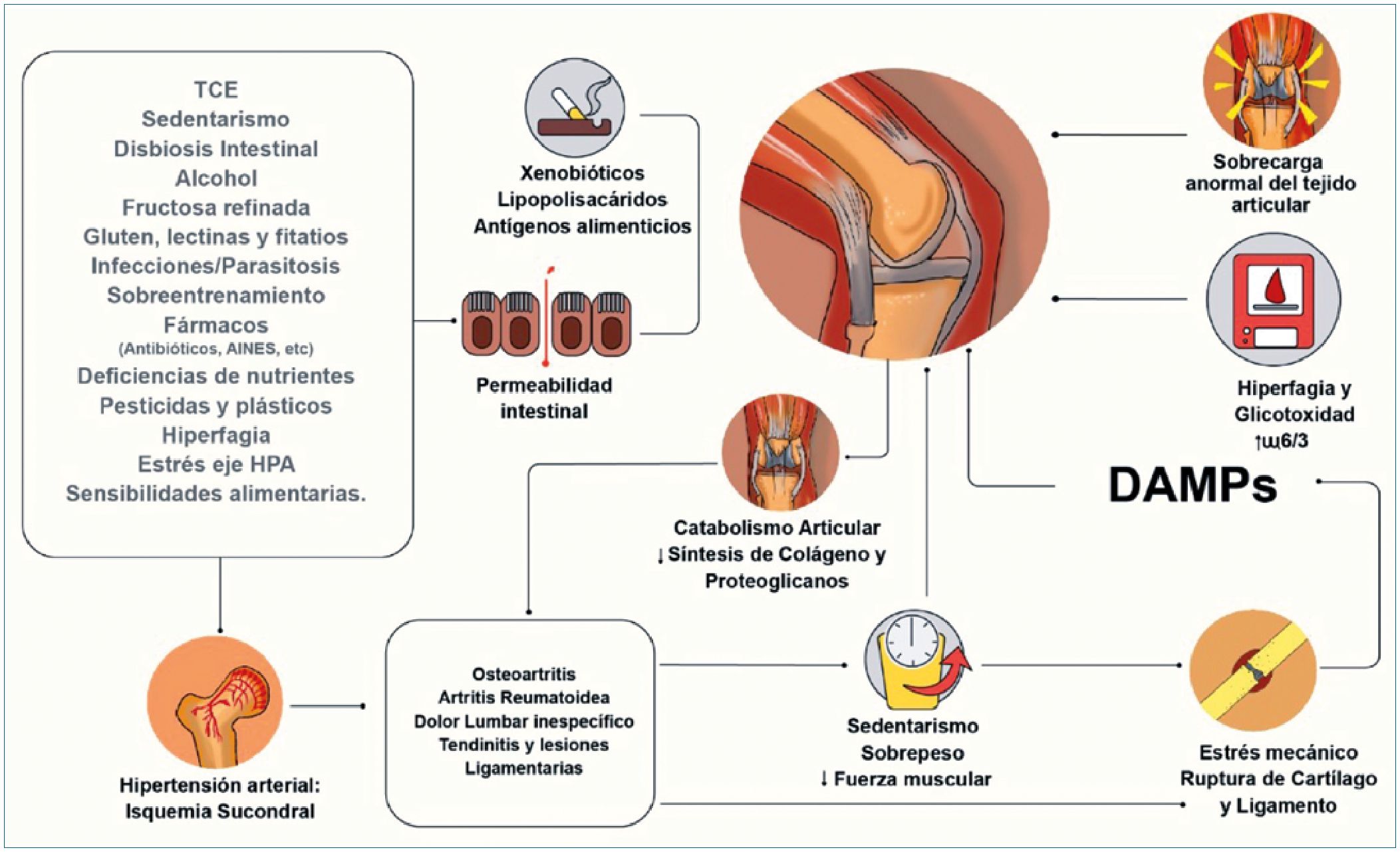
El estudio de revisión de Francesca De Filippis y coautores, confirmó el impacto significativo de los xenobióticos ambientales en las comunidades microbianas, destacando el papel del microbioma intestinal en la degradación de compuestos tóxicos y su potencial en el desarrollo de probióticos para mitigar los efectos negativos de la contaminación en la salud. El estudio examinó cómo la contaminación ambiental afecta la composición y función del microbioma intestinal en una población de una zona altamente contaminada en Campania, Italia. Comparando microbiomas intestinales de áreas con alta, media y baja contaminación, se revelaron adaptaciones microbianas significativas a la contaminación. La alta contaminación se correlacionó con niveles aumentados de dioxinas y PCB en la sangre y una selección de microbiota intestinal capaz de degradar contaminantes orgánicos. Sorprendentemente, se encontraron concentraciones más altas de metales pesados en sujetos de áreas de contaminación media, vinculadas a características geomorfológicas específicas[38] (Figura 1).
Figura 1. Factores metabólicos, dietéticos y mecánicos que contribuyen a la disfunción articular a través de permeabilidad intestinal, catabolismo del cartílago y generación de patrones moleculares asociados a daño (DAMPs).
La microbiota intestinal es un complejo grupo de microbios que interaccionan para participar en procesos fisiológicos como digestión y la defensa inmunitaria, la composición de la microbiota intestinal es variada y debe estar en correcto equilibrio para que las cepas protectoras superen las potencialmente perjudiciales, el desequilibrio entre estas proporciones se denomina disbiosis[39], está perdida de equilibrio se asociada a una amplia gama de trastornos como las enfermedades inflamatorias intestinales, a trastornos dolorosos crónicos y recientemente se ha relacionado con enfermedades neurológicas, como los trastornos cognitivos, trastornos del ánimo y del espectro autista[40].
La disbiosis está caracterizada por una reducción en el número de bacterias que producen los ácidos grasos de cadena corta, los cuales estructuralmente cumplen un papel importante en la formación de la barrera intestinal, lo cual debilita el sistema inmunológico, a su vez, la proporción de microorganismo nocivos aumenta, con un incremento en la producción de lipopolisacáridos, los cuales generan endotoxinas que amplifican la cascada inflamatoria, adicionalmente aumenta la producción de radicales libres de oxígeno generando toxicidad celular y la producción de ácido sulfhidrico a nivel de las células epiteliales, lo que se relaciona con daño celular[39].
Recientemente, se ha identificado el papel de la microbiota gastrointestinal en la fisiopatología del dolor crónico, en particular de tipo no somático, encontrándose interacciones importantes entre la disbiosis intestinal y procesos a nivel del sistema nervioso central como la neuroinflamacion y neuroexcitacion[41]. La mayor cantidad de especies son bacterianas y se localizan predominantemente en el tracto gastrointestinal y contribuyen a las homeostasis del organismo, las familias deFirmicutes, actinobacter y bacteroides son los más abundantes, seguidos de la familias de verrocomicrobia y proteobacterias, se ha encontrado una relación importante en el equilibrio entre estos grupos de bacterias, como lo son las bifibacterias que pertenecen a la familia de actinobacterias, cuentan con propiedades antiinflamatorias, lo que disminuye la permeabilidad intestinal, influyendo en la degradación de polisacaridos complejos y en la degradación de ácidos grasos, lo cual es esencial para la producción de vitaminas y aminoácidos, como la vitamina B y la vitamina K, la composición de la microbiota varía según el nivel de oxígeno disponible, el pH, el estado nutricional e inmunológico del huésped, encontrándose relación estrecha en la presentación de enfermedades metabólicas como la diabetes, la resistencia a la insulina y la dislipidemia y estados proinflamatorios como la enfermedad intestinal inflamatoria, enfermedad celíaca, colon irritable, cáncer de colon y enfermedades inflamatorias a nivel del páncreas e hígado[42].
El cerebro regula la función gastrointestinal por medio del sistema nervioso entérico y en nervio vago, el cual conecta de forma bidireccional por medio del hipotálamo y el sistema nervioso parasimpático, siendo influenciada por la microbiota intestinal para activar vías de secreción de péptidos neuroactivos como lo son la serotonina, la noradrenalina, la dopamina, la acetilcolina y el ácido gamabutirico (GABA), induciendo vías de sensibilización central por medio de la activación de células inflamatorias y mediadores que convergen en las vías efectoras del dolor, por lo que el conocimiento de la estrecha relación que hay entre la microbiota humana, el sistema nervioso y el sistema autoinmune en la regulación de la homeostasis es de gran importancia, por lo que el desarrollo de tecnologías que permites realizar secuenciaciones genéticas de la microbiota propia de cada huésped, busca ser una estrategia alternativa para el manejo del dolor crónico[43].
Conclusiones
De este texto se pueden concluir varios puntos clave sobre los mecanismos fisiopatológicos del dolor y sus implicaciones en el manejo y tratamiento del dolor crónico:
Es evidente que el dolor abarca más de lo que actualmente entendemos sobre sus mecanismos fisiopatológicos. Por lo tanto, un enfoque funcional de los mismos es necesario para abarcar un correcto entendimiento de cómo funcionan estas vías.
Agradecimientos: Ninguno declarado por los autores.
Notas: Conclusiones a modo parrafo para envio a Congreso Chile
De este análisis se desprenden varios puntos clave sobre los mecanismos fisiopatológicos del dolor y sus implicaciones en el manejo del dolor crónico. Las mitocondrias, más allá de ser los “motores” de la célula, cumplen funciones esenciales en la homeostasis neuronal, y aunque su papel como causa del dolor crónico no ha sido estudiado en profundidad, su implicación en procesos de neurodegeneración abre la posibilidad de nuevos blancos terapéuticos. La evidencia indica que los niveles de vitamina D tienen un impacto directo en las vías de transmisión del dolor y en la regulación del ciclo circadiano, observándose mejoría de ambos al normalizar sus valores. La disfunción del eje hipotálamo-hipófisis-adrenal, inducida por estrés crónico, puede favorecer la perpetuación del dolor; aunque existe debate sobre la influencia precisa del cortisol, está claro que los eventos traumáticos y el estrés alteran la respuesta nociceptiva. Por su parte, los xenobióticos representan un desafío ambiental y sanitario debido a su persistencia y capacidad de interacción con sistemas biológicos, y un mayor conocimiento sobre las interacciones entre exposoma, microbioma y huésped permitirá avanzar en estrategias de protección frente a sus riesgos. La microbiota intestinal, fundamental en la regulación inmunológica, la digestión y la señalización neurológica, puede sufrir alteraciones -denominadas disbiosis- que se asocian con patologías autoinmunes, osteomusculares como la osteoartritis, neuroendocrinas y oncológicas. Su relación con la modulación de linfocitos Th1, Th2 y Th17, así como con la producción de citoquinas proinflamatorias, sugiere un impacto directo en la inflamación crónica, la nocicepción y la función neurocognitiva. En conjunto, estos hallazgos muestran que el dolor crónico involucra procesos fisiopatológicos más complejos de lo que se reconoce habitualmente, por lo que un enfoque funcional que integre aspectos meta- bólicos, endocrinos, inmunológicos y ambientales resulta esencial para una comprensión más completa y el desarrollo de estrategias terapéuticas más efectivas.
Referencias
1. Zahid H. Bajwa, R. Joshua Wootton, Carol A. Warfield. Principles and Practice of Pain Medicine, 3e [Internet]. McGraw-Hill Education; 2016. Disponible en: https://accessanesthesiology-mhmedical-com.bibliotecavirtual.uis.edu.co/content.aspx?bookid=1845§ionid=133682578
2.Khelemsky Y, Malhotra A, Gritsenko K, editors. Academic Pain Medicine [Internet]. Springer International Publishing; 2019. Available from: http://dx.doi.org/10.1007/978-3-030-18005-8
3.Stephen B. McMahon, Martin K., Irene T., Dennis T. Wall and Melzack’s Textbook of Pain, 6e. ELSEVIER; 2013.
4.Geoffrey M. Cooper REH. La Célula, 5e. Marbán; 2015.
5.Silva Santos Ribeiro P, Willemen HL, Eijkelkamp N. Mitochondria and sensory processing in inflammatory and neuropathic pain. Front Pain Res (Lausanne). 2022 Oct;3:1013577. https://doi.org/10.3389/fpain.2022.1013577 PMID:36324872
6.Cui L, Weiyao J, Chenghong S, Limei L, Xinghua Z, Bo Y, et al. Rheumatoid arthritis and mitochondrial homeostasis: The crossroads of metabolism and immunity. Frontiers in Medicine [Internet]. 2022 Sep 23;9. Available from: http://dx.doi.org/10.3389/fmed.2022.1017650
7.Doyle TM, Salvemini D. Mini-Review: mitochondrial dysfunction and chemotherapy-induced neuropathic pain. Neurosci Lett. 2021 Aug;760:136087. https://doi.org/10.1016/j.neulet.2021.136087 PMID:34182057
8.Jack J. Collier Monika Oláhová Thomas G. McWilliams Robert W. Taylor. Mitochondrial signalling and homeostasis: from cell biology to neurological disease. Disponible en: https://www.cell.com/trends/neurosciences/fulltext/S0166-2236(22)00239-9#secst0020
9.Barrera MJ, Aguilera S, Castro I, Carvajal P, Jara D, Molina C, et al. Dysfunctional mitochondria as critical players in the inflammation of autoimmune diseases: potential role in Sjögren’s syndrome. Autoimmun Rev. 2021 Aug;20(8):102867. https://doi.org/10.1016/j.autrev.2021.102867 PMID:34118452
10.Fearon U, Canavan M, Biniecka M, Veale DJ. Hypoxia, mitochondrial dysfunction and synovial invasiveness in rheumatoid arthritis. Nat Rev Rheumatol. 2016 Jul;12(7):385–97. https://doi.org/10.1038/nrrheum.2016.69 PMID:27225300
11.Ayahiro Yamashita, Yutaka Matsuoka, Megumi Matsuda, Kenshiro Kawai, Teiji Sawa a and Fumimasa Amaya. Dysregulation of p53 and Parkin Induce Mitochondrial Dysfunction and Leads to the Diabetic Neuropathic Pain. NEUROSCIENCE RESEARCH ARTICLE; 2019.
12.Zhao Y, Liu B, Xu L, Yu S, Fu J, Wang J, et al. ROS-induced mtDNA release: the emerging messenger for communication between neurons and innate immune cells during neurodegenerative disorder progression. Antioxidants. 2021 Nov;10(12):1917. https://doi.org/10.3390/antiox10121917 PMID:34943020
13.Assavarittirong C, Samborski W, Grygiel-Górniak B. Oxidative Stress in Fibromyalgia: From Pathology to Treatment [Internet]. Oxid Med Cell Longev. 2022 Oct;2022(1):1582432. https://doi.org/10.1155/2022/1582432 PMID:36246401
14.Kim HK, Zhang YP, Gwak YS, Abdi S. Phenyl N-tert-butylnitrone, a free radical scavenger, reduces mechanical allodynia in chemotherapy-induced neuropathic pain in rats. Anesthesiology. 2010 Feb;112(2):432–9. https://doi.org/10.1097/ALN.0b013e3181ca31bd PMID:20068451
15.Duchen MR. Mitochondria and calcium: from cell signalling to cell death [Internet]. The Journal of Fisiology; 2000. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2270168/
16.Yoshimoto N, Nakamura Y, Hisaoka-Nakashima K, Morioka N. Mitochondrial dysfunction and type I interferon signaling induce anxiodepressive-like behaviors in mice with neuropathic pain [Internet]. Experimental Neurology; 2023. Available from: https://www.cell.com/neuron/fulltext/S0896-6273(21)00969-7?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0896627321009697%3Fshowall%3Dtrue#secsectitle0040
17.Chiyuen Cheung, Shaoqin Tu, Yi Feng, Chuiming Wan, Hong Ai, Zheng Chen. Mitochondrial Quality Control Dysfunction in Osteoarthritis: Mechanisms, Therapeutic Strategies & Future Prospects. Archives of Gerontology and Geriatrics; 2024.
18.Serrano SG. Vitaminas. Componentes esenciales. FORMACIÓN CONTINUADA; 2002.
19.Lombardo M, Feraco A, Ottaviani M, Rizzo G, Camajani E, Caprio M, et al. The Efficacy of Vitamin D Supplementation in the Treatment of Fibromyalgia Syndrome and Chronic Musculoskeletal Pain. Nutrients. 2022 Jul;14(15):3010. https://doi.org/10.3390/nu14153010 PMID:35893864
20.Benson J, Wilson A, Stocks N, Moulding N. Muscle pain as an indicator of vitamin D deficiency in an urban Australian Aboriginal population. Med J Aust. 2006 Jul;185(2):76–7. https://doi.org/10.5694/j.1326-5377.2006.tb00475.x PMID:16842060
21.Liu X, Nelson A, Wang X, Farid M, Gunji Y, Ikari J, et al. Vitamin D modulates prostaglandin E2 synthesis and degradation in human lung fibroblasts. Am J Respir Cell Mol Biol. 2014 Jan;50(1):40–50. https://doi.org/10.1165/rcmb.2013-0211OC PMID:23941558
22.Kirsten Valebjørg Knutsen, Mette Brekke, Svein Gjelstad, and Per Lagerløv. Vitamin D status in patients with musculoskeletal pain, fatigue and headache: A cross-sectional descriptive study in a multi-ethnic general practice in Norway. Scandinavian journal of primary health care;
23.de Oliveira DL, Hirotsu C, Tufik S, Andersen ML. The interfaces between vitamin D, sleep and pain. J Endocrinol. 2017 Jul;234(1):R23–36. https://doi.org/10.1530/JOE-16-0514 PMID:28536294
24.Abdella M. Habib, Karim Nagi, Nagendra Babu Thillaiappan, VijayaKumar Sukumaran, and Saghir Akhtar. Vitamin D and Its Potential Interplay With Pain Signaling Pathways. Front Immunol. 2020.
25.Paez-Hurtado AM, Calderon-Ospina CA, Nava-Mesa MO. Mechanisms of action of vitamin B1 (thiamine), B6 (pyridoxine), and B12 (cobalamin) in pain: a narrative review. Nutr Neurosci. 2023 Mar;26(3):235–53. https://doi.org/10.1080/1028415X.2022.2034242 PMID:35156556
26.Buesing S. Vitamin B12 as a Treatment for Pain. Pain Physician [Internet]. 2019 Jan 11;1(22;1):E45–52. Available from: http://dx.doi.org/10.36076/ppj/2019.22.e45
27.Corinne G. Jolivalt, Leah M Mizisin, Austin Nelson, Joice M Cunha, Khara M Ramos, Dieter Bonke, Nigel A Calcutt. B vitamins alleviate indices of neuropathic pain in diabetic rats. 2009.
28.Dickhaus B, Mayer EA, Firooz N, Stains J, Conde F, Olivas TI, et al. Irritable bowel syndrome patients show enhanced modulation of visceral perception by auditory stress. Am J Gastroenterol. 2003 Jan;98(1):135–43. https://doi.org/10.1111/j.1572-0241.2003.07156.x PMID:12526949
29.Gupta A, Bhatt RR, Naliboff BD, Kutch JJ, Labus JS, Vora PP, et al.; MAPP Research Network. Impact of early adverse life events and sex on functional brain networks in patients with urological chronic pelvic pain syndrome (UCPPS): A MAPP Research Network study. PLoS One. 2019 Jun;14(6):e0217610. https://doi.org/10.1371/journal.pone.0217610 PMID:31220089
30.Trevino CM, Geier T, Morris R, Cronn S, deRoon-Cassini T. Relationship Between Decreased Cortisol and Development of Chronic Pain in Traumatically Injured. J Surg Res. 2022 Feb;270:286–92. https://doi.org/10.1016/j.jss.2021.08.040 PMID:34717262
31.Fischer S, Doerr JM, Strahler J, Mewes R, Thieme K, Nater UM. Stress exacerbates pain in the everyday lives of women with fibromyalgia syndrome—the role of cortisol and alpha-amylase. Psychoneuroendocrinology. 2016 Jan;63:68–77. https://doi.org/10.1016/j.psyneuen.2015.09.018 PMID:26431802
32.Cristián Fuentes, Lina Ortiz Msc, Álvaro Wolfenson, Gabriela Schonffeldt. Dolor crónico y depresión. Revista Médica Clínica Las Condes. 2019;áginas 459-465. https://doi.org/10.1016/j.rmclc.2019.10.005.
33.Ulrich-Lai YM, Xie W, Meij JT, Dolgas CM, Yu L, Herman JP. Limbic and HPA axis function in an animal model of chronic neuropathic pain. Physiol Behav. 2006 Jun;88(1-2):67–76. https://doi.org/10.1016/j.physbeh.2006.03.012 PMID:16647726
34.de Oliveira FR, Visnardi Gonçalves LC, Borghi F, da Silva LG, Gomes AE, Trevisan G, et al. Massage therapy in cortisol circadian rhythm, pain intensity, perceived stress index and quality of life of fibromyalgia syndrome patients. Complement Ther Clin Pract. 2018 Feb;30:85–90. https://doi.org/10.1016/j.ctcp.2017.12.006 PMID:29389485
35.Wingenfeld K, Nutzinger D, Kauth J, Hellhammer DH, Lautenbacher S. Salivary cortisol release and hypothalamic pituitary adrenal axis feedback sensitivity in fibromyalgia is associated with depression but not with pain. J Pain. 2010 Nov;11(11):1195–202. https://doi.org/10.1016/j.jpain.2010.02.011 PMID:20627822
36.Chang X, Zhang H, Chen S. Neural circuits regulating visceral pain. Commun Biol. 2024 Apr;7(1):457. Available from: https://doi-org.bibliotecavirtual.uis.edu.co/10.1038/s42003-024-06148-y https://doi.org/10.1038/s42003-024-06148-y PMID:38615103
37.Štefanac T, Grgas D, Landeka Dragičević T. Xenobiotics-Division and Methods of Detection: A Review. J Xenobiot. 2021 Oct;11(4):130–41. https://doi.org/10.3390/jox11040009 PMID:34842778
38.De Filippis F, Valentino V, Sequino G, Borriello G, Riccardi MG, Pierri B, et al. Exposure to environmental pollutants selects for xenobiotic-degrading functions in the human gut microbiome. Nat Commun. 2024 May;15(1):4482. https://doi.org/10.1038/s41467-024-48739-7 PMID:38802370
39.Moreno X. Disbiosis en la microbiota intestinal. Rev GEN Soc Venez Gastroenterol [Internet]. 2022;76(1):17–23. Available from: saber.ucv.ve/ojs/index.php/rev_gen/article/view/24183
40.Guarner F. Disbiosis-causas, consecuencias y tratamiento Cuando la microbiota intestinal pierde su equilibrio. GUT Microbiota Heal; 2016. pp. 1–4.
41.Álvarez J, Fernández Real JM, Guarner F, Gueimonde M, Rodríguez JM, Saenz de Pipaon M, et al. Gut microbes and health [Internet]. Gastroenterol Hepatol. 2021;44(7):519–35. https://doi.org/10.1016/j.gastrohep.2021.01.009 PMID:33652061
42.Germ R, de Castro Pérez F. Sedación y analgesia en la emergencia pediátrcia. Med Infant. 1997;4(3):176–86.
43.Garvey M. The Association between Dysbiosis and Neurological Conditions Often Manifesting with Chronic Pain. 2023;1–15. https://doi.org/10.3390/biomedicines11030748.

 ORCID
ORCID