Marcos Bolívar1,*, Amalia del Valle Bolívar1, Marcos José Bolívar1
Recibido: 31-08-2023
Aceptado: 17-11-2023
©2024 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 53 Núm. 2 pp. 151-159|https://doi.org/10.25237/revchilanestv53n2-10
PDF|ePub|RIS
Opioid-free postoperative analgesia. In which patients should we use it and which drugs to use ?: a systematic review
Abstract
Opioids produce hemodynamic stability, analgesia, and reduce the doses of other anesthetics. Its use in some patients produces more risks than benefits. In them, a new analgesic modality is required to achieve the opioid effect, it is opioid-free analgesia. This systematic review was carried out with the research questions: In what clinical conditions were drugs used for opioid-free postoperative analgesia and what were the adjuvants used? PubMed and Scielo were searched for available research from the last 10 years. 426 articles could answer the research questions, finally leaving 31 for review. Patients who benefit from this technique and non-opioid drugs with analgesic properties were identified. Opioid-free analgesia is a technique for a niche of patients who should not receive these drugs.
Resumen
Los opioides producen estabilidad hemodinámica, analgesia y reducción de las dosis de otros anestésicos. Su uso en algunos pacientes produce más riesgos que beneficios. En ellos, se requiere de una nueva modalidad analgésica para lograr el efecto opioide, es la analgesia libre de opioide. Se realizó esta revisión sistemática con las preguntas de investigación: En cuáles condiciones clínicas se usaron fármacos para analgesia posoperatoria libre de opioides y ¿Cuáles fueron los coadyuvantes utilizados?. Se buscó en PubMed y Scielo la investigación disponible los últimos 10 años. 426 artículos podían responder las preguntas de la investigación, quedando finalmente 31 para realizar su revisión. Se identificaron pacientes que se benefician de esta técnica y los fármacos no opioides con propiedades analgésicas. La analgesia libre de opioides es una técnica para un nicho de enfermos que no deben recibir estos fármacos.
-
Introducción
Antes del advenimiento de los opioides, los objetivos de la anestesia general: hipnosis, inmobilidad, y analgesia, se lograban con altas dosis de hipnóticos o agentes inhalatorios, técnicas que generalmente causaban inestabilidad hemodinámica severa[1]. La introducción de los opioides en el año 1960, inicialmente grandes dosis de morfina y posteriormente el fentanilo y otros opioides sintéticos, ofreció mayor estabilidad hemodinámica, excelente analgesia, permitiendo adicionalmente la reducción de las dosis de otros agentes anestésicos. A partir de entonces, se estableció el paradigma de la anestesia balanceada o equilibrada basada en opioides, convirtiéndose la analgesia en una parte esencial de la anestesia equilibrada, junto con la hipnosis y la inmovilidad[1].
Actualmente, la administración de opioides en el período perioperatorio es omnipresente y se estima que el 99% de los pacientes reciben estos fármacos como parte de su atención quirúrgica, tanto por el equipo de anestesia (84% – 100%) como por el personal quirúrgico[2]. En los Estados Unidos de América, al momento del alta hospitalaria, también hay una elevada prescripción de opioides en los pacientes sometidos a cirugía mayor (77% – 87%) y en los sometidos a cirugía menor (90% – 91%)[3]. Sin embargo, los beneficios del uso generoso de opioides han sido cuestionados, con datos que muestran que un mayor consumo de ellos en el perioperatorio se asocia con un aumento en las Reacciones Adversas Medicamentosas (RAM). Adicionalmente, cuanto más opioide administremos en el transoperatorio, mayores serán sus requerimientos posoperatorios: esto se denomina “paradoja de los opioides” y puede explicarse a través de la tolerancia aguda y los procesos de neuro-adaptación causados por los opioides de acción corta o el uso crónico de ellos[3].
Todos los fármacos tienen efectos secundarios y los opioides no escapan a ello[2]. Su uso durante la anestesia no reduce el dolor posoperatorio, pero si aumenta los efectos secundarios, especialmente las náuseas y los vómitos. Causan hiperalgesia y tolerancia dependientes de la dosis, lo que puede resultar en un mayor dolor posoperatorio y eventualmente promueven el desarrollo de dolor posoperatorio persistente[4]. Otras RAM de los opioides son[4],[5],[6]:
1) Sedación, disforia, delirio, constipación, ilio paralítico, retención urinaria, depresión respiratoria, rigidez muscular, somnolencia, delirio y debilidad y flacidez de la musculatura laríngea.
2) Riesgo de dependencia y tolerancia en pacientes que son dados de alta con prescripción de opioides.
3) Prolongación de la estancia hospitalaria y aumento de los costos de atención médica.
4) Inhibición de la inmunidad celular y humoral, lo que podría favorecer la recurrencia tumoral. Este hecho todavía es discutible al día de hoy.
Por todo lo antes mencionado, actualmente el uso de opioides en el perioperatorio es un tema controvertido. Estamos ante la presencia de una moda o un movimiento en anestesiología, con la finalidad de disminuir el uso de estos fármacos, hacer de ellos un uso racional, utilizar la menor dosis que produzca el mejor efecto analgésico y finalmente, proponer una nueva modalidad analgesica sin opioides[6].
En este sentido, la Sociedad Estadounidense de Anestesió- logos (ASA, por sus siglas en inglés) ha solicitado que se reduzca la exposición de los pacientes a los opioides en el entorno quirúrgico, con la finalidad de disminuir otro problema latente del uso de estos fármacos, como lo es la crisis de opioides que afecta a los norteamericanos[2],[25],[29]. Un concepto moderno de anestesia debería eliminar los opioides intraoperatorios, buscando un enfoque equilibrado y sin estos fármacos (anestesia libre de opioides u OFA por sus siglas en inglés). En esta técnica se combinan fármacos y recursos históricamente probadas por su eficacia, bajo un concepto multimodal. Se incluyen allí: el paracetamol, los antiinflamatorios no esteroideos (ketorolaco, ibuprofeno, celecoxib), agonistas alfa-2 (dexmede- tomidina, clonidina, tizanidina), antagonistas de los receptors de N-metil-d-aspartato (NMDA) (ketamina, amantadina, dex- trometorfano), gabapentioides (gabapentina y pregabalina), antidepresivos (amitriptilina, desipramina, duloxetina), esmolol, lidocaína, cafeína, glucocorticoides (dexametasona), relajantes musculares (metocarbamol, ciclobenzaprina) y magnesio[6].
Es importante tener en consideración, que analgesia y anestesia son términos que en ocasiones se confunden dentro del uso común. Analgesia significa aquellos estados en donde sólo participa la modulación de la percepción del dolor y anestesia implica los estados en los que se pierde la conciencia mental y la percepción de otras sensaciones. Se han hecho intentos por dividir la anestesia en diversos componentes, que incluyen analgesia, amnesia, relajación y pérdida de la respuesta refleja al dolor. Desde esta óptica, la analgesia se puede considerar como un componente de la anestesia[6],[7].
En el año 1993, se introduce el concepto de la analgesia multimodal, analgesia balanceada o analgesia equilibrada, como técnica ‘ahorradora de opioides”, la cual tenía por objetivo mejorar la analgesia mediante el empleo de fármacos con efectos sinérgicos o aditivos[1].
Bajo esta idea surge la analgesia libre opioides (ALO) o en inglés Opioid Free Anaesthesia (OFA). Esta modalidad analgésica nace con la hipótesis de que el uso de un adyuvante, reduce los requerimientos de opioides durante y después de la cirugía, lo que hace posible que la combinación de estos fármacos colaboradores, logren evitar el uso de opioides en el transoperatorio. Es así como aparece en el año 2005, con pro y contras esta técnica analgésica, para el tratamiento de pacientes obesos sometidos a cirugía bariátrica[1],[8],[9].
La ALO es una técnica multimodal, en la cual no se utilizan opioides sistémicos, ni por vía neuraxial ni intracavitaria, durante el período perioperatorio[9],[10]. Se utilizan fármacos con diferentes mecanismos de acción, que ejercen sus efectos a distintos niveles del proceso nociceptivo[12]. Los fármacos y procedimientos usados en la analgesia libre de opioides, son los mismos que se utilizan en la anestesia libre de opioides[8],[12].
De manera individual, la mayoría de ellos no son tan potentes analgésicos como los opioides, su uso habitualmente se realiza en el trans-operatorio y no están exentos de RAM. Adicionalmente, no hay suficiente experiencia de su empleo en analgesia posoperatoria, por lo cual algunos autores motivan y sugieren a cada actor, para que haga su propia experiencia con el uso de estos fármacos en el posoperatorio[3],[8],[13].
El objetivo de esta revisión sistemática, es considerar la analgesia posoperatoria libre de opioides como una opción analgésica válida en el tratamiento del dolor posoperatorio, para un nicho de pacientes, en los cuales el uso de los opioides representan más riesgos que beneficios y determinar cuales son esos recursos farmacológicos disponibles para el logro de ese objetivo.
-
Metodología
Se realizó una revisión sistemática para examinar la investigación disponible en los últimos 10 años, sobre la analgesia posoperatoria libre de opioides. Nuestro protocolo siguió las pautas del Preferred Reporting Items for Systematic Review and Meta-Analysis Extension for Scoping Review Protocols (PRISMA) [14]. El método siguió cinco etapas consecutivas:
1) Identificación de la pregunta de investigación.
2) Identificar estudios relevantes.
3) Selección de estudios.
4) Análisis de los datos.
5) Resumen y reporte de los resultados.
Los autores definieron la analgesia libre de opiáceos como cualquier régimen analgésico en el posoperatorio que no implique la acción sobre los receptores de opiáceos. Pudiendo ser ser multimodal o unimodal, y farmacológica o no farmacológica.
Etapa 1: Pregunta de investigación
La formulación de las preguntas obedeció a la mnemotecnia “PICO” (Problema, intervención a analizar, comparación y resultados).
Las preguntas a resolver son:
1) ¿Cuáles son las condiciones clínicas donde se usaron los fármacos para analgesia postoperatoria libre de opioides.
2) ¿Cuáles son los coadyuvantes utilizados como analgésicos en la analgesia postoperatoria libre de opioides?
Etapa 2: Identificación de los estudios relevantes
Esta revisión se planificó para usar datos de revisiones sistemáticas, revisiones narrativas, metaanálisis, ensayos controlados aleatorios y estudios de cohortes. Se realizaron búsquedas en las siguientes bases de datos: MEDLINE (Medical Analysis and Retrieval System Online) a través de PubMed y Scie- lo (Scientific Electronic Library Online), entre los años 2013 a 2023 (10 años). La estrategia de búsqueda fue: “Opioid free postoperative analgesia”, “Opioid free postoperative analgesia and indications”, “Opioid free postoperative analgesia and adjuvants”. La revisión se realizó en humanos, sin restricciones de idioma, ni edad.
Etapa 3. Selección de estudios
Los artículos identificados con posibilidad para responder a nuestras preguntas de investigación fueron elegidos.
Etapa 4. Análisis de los datos
Los estudios identificados y revisados, fueron analizados buscando respuestas a las preguntas de investigación.
Los resultados considerados importantes para esta revisión fueron los siguientes:
1. Resultados primarios: Condiciones clínicas donde se usaron los fármacos para analgesia posoperatoria libre de opioides.
2. Resultados secundarios: Fármacos adyuvantes, no opioides, usados y recomendados para tratar el dolor posoperatorio, características y dosis recomendadas.
Etapa 5: Resumen de datos y síntesis de los resultados
En total, se identificaron 426 artículos a partir de la estrategia de búsqueda. Fueron excluidos 398, por referirse a anestesia posoperatoria libre de opioides, artículos duplicados y otros temas. Quedando 28 artículos. De este grupo de artículos excluidos se seleccionaron 6 que contenían datos relacionados con las preguntas de investigación, quedando finalmente 34 artículos. De ellos, finalmente fueron considerados como relevantes para el desarrollo de la investigación 21 artículos. Se analizó la lista de referencias de los artículos relevantes incluidos para identificar artículos importantes, incluyéndose 10 artículos nue-
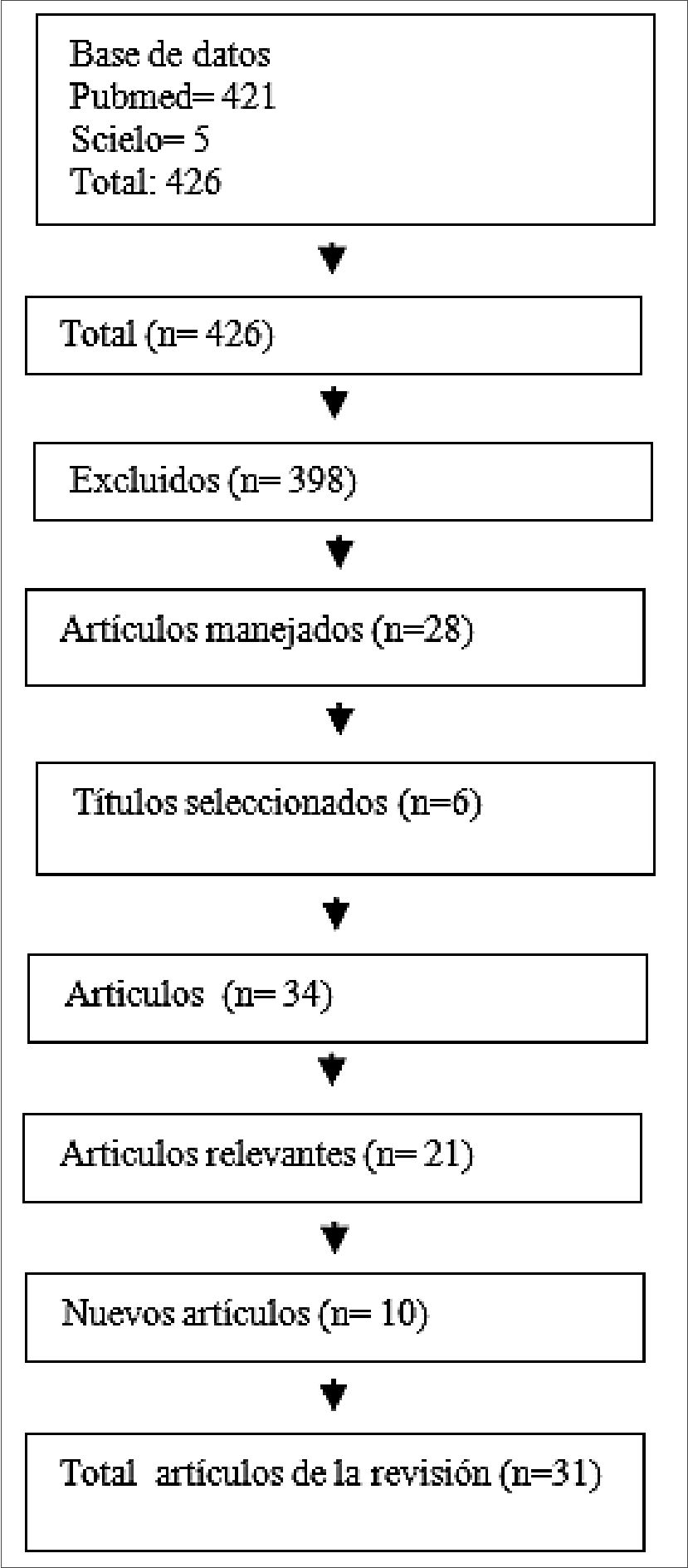
Figura 1. Diagrama de flujo de los artículos incluidos.
vos en este proceso. El total de artículos objeto de esta revisión fue de 31 (Figura 1).
-
Resultados
Luego de eliminar duplicados y seleccionar los artículos enfocados al objetivo a describir, de la analgesia posoperatoria libre de opioides, se seleccionaron 31 artículos que fueron sintetizados en forma de de revisión sistemática. En relación a la primera pregunta formulada.
¿En cuáles condiciones clínicas se deben usar los fármacos no opioides para el tratamiento del dolor agudo posoperatorio (DAPO)?, las respuestas obtenidas fueron las siguientes:
Aunque cualquier paciente puede recibir ALO, hay cierto grupo de pacientes para los cuales la técnica parece más apropiada. Los resultados arrojan:
a) Pacientes obesos y/o con apnea obstructiva del sueño. Los opiodes contribuyen a la debilidad de la musculatura faríngea, lo cual puede generar patrones respiratorios obstructivos y dificultades al momento de la intubación y la extubación (9,1).
b) Pacientes portadores de dolor crónico y/o consumidores de opioides antes de la cirugía. Estos enfermos tienen mayor riesgo de DAPO severo, consumen más opioides posoperatorios y tienen mayor riesgo de desarrollar dolor crónico posterior a la cirugía[18].
c) Pacientes geriátricos. El uso de opioides en el período perioperatorio en este grupo etario, produce delirio (5%-15%) y disfunción cognitiva posoperatoria (25%-40%), especialmente en los pacientes a los cuales se le realizan procedimientos de artroplastia. El delirio se asocia con un mayor deterioro cognitivo que puede conducir a un inicio acelerado de la demencia. Además de prolongar la estancia hospitalaria, el uso de opioides posoperatorios en este segmento de enfermos, es de especial preocupación[20].
d) Enfermos con riesgo de inmunosupresión. Tanto el dolor como los opioides producen inmunosupresión. Los opioides afectan la proliferación celular, la inflamación, la angiogé- nesis y la respuesta inmune. Todo ello podría influir en la evolución del tumor. Sin embargo, los datos no son conclu- yentes[19]. Los estudios han demostrado que los opioides producen una disminución de la actividad de las células asesinas naturales (NK) y un aumento de la apoptosis de las células B y T. Se ha demostrado que la mayoría de los opioides tienen actividad inmunosupresora excepto el tramadol[20].
e) Posibilidad de recurrencia tumoral. El uso de opioides perioperatorios y su vínculo con la recurrencia del cáncer sigue siendo un tema controvertido. La mayoría de los estudios que han tratado de establecer esta relación, son estudios in vitro cuyos resultados no pueden extrapolarse a los humanos. Sin embargo, aunque no hay una evidencia concluyente que asocie el opioide con la recurrencia del cáncer, se recomienda utilizar técnicas libre de opioides en los pacientes oncológicos[21],[22].
f) Otro grupo de enfermos que puede beneficiarse de la ALO son los siguientes[3],[19],[23].
• Pacientes englobados en los Protocolos ERAS (enhanced recovery after surgery), o recuperación acelerada posterior a la cirugía.
• Pacientes con síndrome de dolor regional complejo (SDRC).
• Pacientes adictos o dependientes de los opioides.
• Pacientes con insuficiencia respiratoria.
• Pacientes con apnea obtructiva del sueño
• Pacientes sometidos a cirugía bariátrica.
• Pacientes obesos sometidos a cirugías no bariátricas.
• Pacientes con reserva ventilatoria comprometida.
• Pacientes con dolor crónico preoperatorio tratado con opiáceos.
• Pacientes con trastorno por consumo de sustancias opiáceas.
• Pacientes con apnea obstructiva del sueño relacionada con la obesidad.
• Pacientes con dolor posquirúrgico persistente (PPSP).
Contraindicaciones de la ALO [6],[25]
Las contraindicaciones de la ALO son:
Relativas:
1) Necesidad de hipotensión controlada para evitar el sangrado.
2) Isquemia miocárdica.
3) Pacientes con tratamiento de betabloqueantes.
4) Bloqueos aurúculoventriculares y los trastornos del sistema nervioso autónomo.
5) Hipotensión ortostática.
6) Pacientes hipovolémicos.
7) Pacientes con estenosis coronaria crítica conocida.
8) Pacientes con isquemia coronaria aguda.
9) Pacientes con shock hipovolémico inestable.
10) Pacientes politraumatizados.
11) Pacientes con disfunciones autonómicas.
12) Intolerantes a los opioides.
Absolutas:
1) Alergia a algunos de los fármacos que componen la mezcla analgésica.
2) Bradicardia extrema.
3) Politraumatizado.
4) Lesión arteria coronaria principal.
5) Boqueo cardíaco.
La analgesia libre de opioides tiene varios beneficios, entre ellos:
1) Mayor estabilidad hemodinámica durante la cirugía.
2) Menor incidencia de dolor posoperatorio crónico.
3) Reducción de la exposición a opioides y, por lo tanto menor riesgo de reacciones adversas relacionadas con su uso.
4) Prolongación de la analgesia postoperatoria.
5) Reducción de la tolerancia y la hiperalgesia inducida por opioides.
6) Menor riesgo de adicción a los opioides.
7) Mejores resultados en cirugía ambulatoria.
-
¿Porqué la ALO?
Si bien tenemos muchos años de experiencia con el uso de los opioides, tenemos menos experiencia con los medicamentos individuales utilizados en la anestesia sin ellos, y mucho menos con sus combinaciones. La anestesia sin opiáceos, anteriormente reservada para la cirugía bariátrica, está recibiendo una atención cada vez mayor en la anestesia convencional[24]. La implementación de la ALO sigue siendo difícil debido a la falta de consenso, persistiendo algunas interrogantes sin resolver. Entre ellas, la elección y combinaciones adecuadas de los agentes anti-nociceptivos y el saber si la elección de los agentes debe estar relacionada con el paciente o con el procedimiento quirúrgico.
Algunos fármacos parecen ser la piedra angular del abordaje de la ALO, sea cual sea el tipo de cirugía a realizar[4],[24]. La base de una cirugía rápida y exitosa es el uso de analgesia y anestesia multimodales eficaces, y se recomiendan desde hace más de una década para evitar los posibles efectos nocivos del uso de los opiáceos[8]. Estos regímenes de fármacos multimodales que evitan los opioides, tienen como objetivo disminuir los requisitos de estos medicamentos intraoperatorios y poso
peratorios, disminuir el dolor agudo posoperatorio (DAPO) y, por lo tanto, acelerar la recuperación evitando los posibles efectos secundarios causados por estos fármacos[25]. Los beneficios de cambiar a una anestesia sin opioides se basan en gran medida en evitar los eventos adversos relacionados con ellos. Estos beneficios incluyen beneficios para el paciente, beneficios para los recursos del hospital y beneficios sociales[24].
La anestesia libre de opioides (ALO), OFA por sus siglas en inglés, y la analgesia posoperatoria libre de opioides, (APLO), son prácticas multimodales que utilizan los mismos recursos farmacológicos: hipnóticos, gabapentinoides, antagonistas de los receptores N-metil-D-aspartato (NMDA), anestésicos locales, medicamentos antiinflamatorios, agonistas alfa-2 y procedimientos de anestesia regional[10],[12].
Las combinaciones de los fármacos utilizados y sus dosis, son escasas en la literatura y sus beneficios está por verse[10],[19].
Contestando la seguna pregunta de la investigación, es decir ¿Cuáles son los coadyuvantes utilizados como analgésicos en la analgesia posoperatoria libre de opioides, características y dosis recomendadas?, encontramos lo siguien- te[3],[4],[6],[18],[19],[25],[26],[27],[28]: (Tabla 1).
-
A. Ketamina
• La ketamina es un fármaco antihiperalgésico, que produce analgesia y sedación.
• Reduce el dolor posoperatorio y las necesidades analgésicas, independientemente del tipo de cirugía y la intensidad del dolor.
• Disminuye los requerimientos de opioides y la incidencia de dolor posoperatorio crónico.
• Mecanismo de acción: es un antagonista de los receptores N-metil-D-aspartato (NMDA), evitando así que el glutamato facilite el proceso de la nocicepción.
• Es homeostática para el sistema inmune/inflamatorio, al reducir la producción de citoquinas proinflamatorias después de la lesión.
• Para la ALO se usan dosis subanestésicas, bolo: 0,25-0,5 mg/kg + infusión continua: 0,1-0,25 mg/kg/h. También se puede usar una infusión continua intraoperatoria de 50500 pg /kg/h.
• Las dosis recomendadas para analgesia pueden producir RAM leves y de fácil manejo con benzodiacepinas.
-
B. Alfa2 agonistas
• Los agonistas alfa2 (clonidina y dexmedetomidina) son agentes ideales para la ALO por sus características farmacológicas favorables que incluyen: sedación, hipnosis, ansioli- sis, antiemesis, simpaticolisis y analgesia.
• Su uso en el perioperatorio disminuye la intensidad del dolor, el consumo de opioides, sin prolongar el tiempo de recuperación.
• Actúan como drogas agonistas de los receptores a2 adre- nérgicos, que son proteinas G acopladas al receptor ubicado en el sistema nervios central (SNC) y sistema nervioso periférico (SNP).
• La activación de esta proteina G causa inhibición de la liberación de noradrenalina en el SNC y, por lo tanto, se inhibe la transmisión de señales nociceptivas al cerebro.
• Activan la vía inhibitoria descendente del dolor.
• Se cree que la dexmedetomidina en particular, promueve la liberación de acetilcolina a lo largo de las interneurones espinales, lo que posiblemente contribuya a la liberación de óxido nítrico, que puede ayudar a modular la analgesia.
• Ambas drogas tienen efecto analgésico y sedante e iguales RAM (hipotensión, bradicardia, resequedad bucal).
-
Dexmedetomidina (Dex)
Tabla 1. Fármacos usados en la analgesia libre de opioides. Dosis[10],[15],[16],[17]
| Fármaco | Bolos | Infusión continua |
| Ketamina | 0,25-0,5 mg/kg | 0,05-0,3 mg/kg/h |
| Dexmedetomidina | 1 p.g/kg/10 min | 0,05-0,8 ^g/kg/h |
| Clonidina | 1-4 p.g/kg/20 min 0,5-3mg/kg/h | |
| Lidocaina | 1-2 mg/kg/h (inducción) | (Intra-op) 0,5-2 mg/kg/h (Post-op) |
| Esmolol (ß-1) | 0,5-2 gg/kg | 5-500 p.g/kg/min |
| Magnesio | 30-50 mg/kg/20 min | 8-25 mg/kg/h |
| Gabapentoides PG | 150-300 mg VO pre-op | |
| GP | 600-900 mg VO pre-op | 600 mg TID VO post-op |
| Duloxetina | 60 mg/VO/15 días | |
| Paracetamol/Acetaminofen | 15 mg/kg/IV QID | |
| Dexametasona | 0,1 mg/kg EV | |
| AINE | Ketorolac: 30 mg EV c/6h/5 días Celecoxib:200-400 VO/día |
Pre-op: Preoperatorio; Intra-op: Intraoperatorio; Post-op: Postoperatorio; AINE: antiinflamatorios de origen no esteroideos; PG: Pregabalina; GP: Gabapentina.
• Tiene mejor perfil farmacológico y mayor afinidad por los receptores alfa2 presinápticos que la clonidina (Clo).
• Es aproximadamente 8 veces más selectiva por los receptores adrenérgicos a2 que la clonidina y con una vida media de eliminación mucho más corta (2 h frente a 15 h). Su inicio de acción es rápido (6 minutos) y una vida media más corta (2 h). Lo cual es adecuado para infusión continua.
• Su uso intraoperatorio en infusion continua ha sido asociado en con una menor escala visual analógica (EVA) en el postoperatorio, menor incidencia de náuseas y vómitos y disminución del consumo de opioides, beneficios que pueden prolongarse hasta 3 días después en el postoperatorio.
• Parece producir mayor estabilidad hemodinámica que la clonidina.
• Debe administarse lentamente y en infusión continua.
• Dosis para infusión intravenosa: 0,1-0,8 pg/kg/h. También se ha usado: 0,5 a 1 pg/kg durante 10 minutos antes de la inducción, seguida de una infusión continua de 0,2 a 0,8 pg/kg/h después de la intubación.
-
Clonidina
• Su uso está limitado por su inicio de acción y vida media prolongadas (20 minutos y 15 h respectivamente).
• Dosis: se recomienda una sola dosis en el preoperatorio para disminuir el DAPO: 1-3 pg/kg endovenoso.
-
C. Lidocaina
• Es un anestésico local tipo amida, con múltiples usos: analgésicos, antihiperalgésicos, antiinflamatorios, ahorradores de opioides, antieméticos
• Mecanismo de acción: tradicionalmente se ha dicho que bloquea la transmisión nerviosa en la membrana de la neurona, al bloquear los canales de sodio. Actualmente se dice que bloquea también los canales de potasio y calcio e interactúa con los receptores acoplados a la proteina G.
• El uso perioperatorio de la infusión intravenosa de lidocaí- na, disminuye significativamente los requerimientos anestésicos y de opioides, disminuye la incidencia de náuseas y vómitos postoperatorios, con un retorno más rápido de la función peristáltica y mejora la calidad de la recuperación.
• Los beneficios de la infusión continua de lidocaina se manifiestan en la cirugía abdominal abierta o laparoscópica
• Dosis sugeridas en el perioperatorio:
Dosis bolo (en la inducción anestésica): 1- 2 mg/kg. Infusión continua (durante la cirugía): 0,5-3 mg/kg/h Posoperatorio (continuar infusión): 1,5-2 mg/kg/h (ideal de 8 a 24 h)
• Durante su uso se deben monitorear los signos de toxicidad: tinitus, adormecimiento perioral , arritmias, sabor metálico en la boca.
-
D. Magnesio
• Es un antagonista no competitivo de los receptores NMDA.
• Por sus efectos como ahorrador de opioide y antiinflamatorio se le considera un componente natural de la ALO.
• RAM asociadas a su uso: potenciación de la acción de los relajantes neuromusculares y de los hipnóticos. También puede producir hipotensión secundaria a vasodilatación
• Dosis: bolo de: 30-50 mg/kg/20 minutos, seguido de infusión continua de 8-25 mg/kg/h.
-
E. AINE (antiinflamatorios de origen no esteroideos)
• La inflamación es el componente principal del DAPO, por ello los fármacos con propiedades antiinflamatorias son de uso obligatorio en la ALO.
• Los AINE disminuyen la reacción inflamatoria periférica y central en respuesta al trauma tisular, mediando también un efecto antihiperalgésico.
• Son fármacos analgésicos, antipiréticos, antihiperalgésicos y ahorradores de opioides, de uso obligado en el DAPO.
• Mecanismo de acción: inhibición periférica de las isoformas 1 y 2 de la ciclooxigenasa (COX). Según el tipo de AINE la inhibición puede ser a COX 1 o COX 2 o ambas.
• RAM: toxicidad gástrica (relacionada principalmente con los inhibidores de la COX-1), aumento de la morbilidad cardiovascular (asociada a la COX-2), insuficiencia renal con su uso prolongado y altas dosis.
• Dosis de los más usados: ketorolac: 30 mg IV o celecoxib 200-400 mg VO.
-
F. Esteroides
• Son fármacos que usados en el perioperatorio, tienen un efecto relevante sobre la respuesta inflamatoria, por lo cual siempre deberían formar parte de la ALO.
• Afectan la respuesta de estrés como consecuencia de la cirugía, reduciendo la inflamación, el dolor, las náuseas, vómitos y la fatiga.
• Dosis recomendadas para el dolor y profilaxis de náuseas y vómitos postoperatorios (NVPO): 0,1 mg/kg EV (dexameta- sona).
-
G. Gabapentanoides
• Son fármacos cuyo mecanismo de acción es la inhibición de los canales de calcio a2 delta en la neurona presináptica. El resultado de esto, es la disminución de la liberación de neu- rotransmisores exitatorios como el glutamato, sustancia P y el gen relacionado con el péptido de la calcitonina.
• Los fármacos más usados de este grupo son la gabapentina y la pregabalina. Ellas son drogas de absorción rápida vía oral, tienen alta biodisponibilidad y se excretadas por la orina sin ser metabolizadas.
• La pregabalina parece tener mejor potencial como analgésico en el perioperatorio.
• Dosis: Pregabalina 150 mg VO 2 h antes de la cirugía + 75-300 mg BID en el posoperatorio como acompañante de la analgesia postoperatoria. Gabapentina 600 mg VO 2 h antes de la cirugía o 600-900 mg en el preoperatorio.
-
H. Acetaminofen/Paracetamol
• Su mecanismo de acción parece ser la inhibición central de la ciclooxigenasa (COX), modulación del sistema canabi- noide endógeno y la activación de las vías serotoninérgicas descendientes.
• Se obtiene en formulaciones orales, rectales e inyectables.
• Se requiere suficiente concentración plasmática para que produzca su paso a traves de la barrera sangre/cerebro y así obtener una buena concentración en el líquido cerebro espinal.
• A los 15 minutos de su administración por vía endovenosa (VEV), se obtienen concentraciones en el líquido cerebro espinal de 75% a 142% mayores en comparación con las
formas oral y rectal.
• Es importante recordar que la formulación rectal requiere de 2-3 h para alcanzar su concentración plasmática máxima. Por lo cual, si una cirugía dura de 30 minutos a una hora, no tiene sentido administrar acetaminofen con fines analgésicos transoperatorios por esta vía al momento de la anestesia.
• Dosis: 15 mg/kg/VEV QID.
-
I. Duloxetina
• Es un fármaco inhibidor de oral de la recaptación de seroto- nina-norepinefrina, que se usa comúnmente para el tratamiento de la depresión y la ansiedad.
• Mecanismo de acción: se cree que su efecto analgésico se deriva de un efecto modulador en las vías inhibitorias descendentes del dolor, en el cerebro y la médula espinal.
• La evidencia publicada relacionada con el dolor posquirúrgico sugiere que la duloxetina produce un efecto ahorrador de opioides, sin embargo, no proporciona un alivio consistente.
• Se han usado dosis de 60 mg hasta por 15 días en artroplas- tia de rodilla, cirugía de columna e histerectomía abdominal.
-
J. Esmolol
• Es un bloqueador a-1 selectivo por vía intravenosa, caracterizado por sus tiempos de inicio y eliminación ultracortos. Su capacidad para alcanzar rápidamente el bloqueo a lo convierten en un agente ideal para controlar la respuesta hemodinámica asociada con estímulos nocivos, tales como la intubación endotraqueal y el neumoperitoneo.
• Además de sus efectos simpaticolíticos, el esmolol se ha utilizado para el tratamiento del dolor posquirúrgico.
• Su mecanismo de acción es desconocido, sin embargo, se cree que bloquea los efectos exitatorios de la señalización del dolor en el SNC y SNP. También parece que modula la actividad adrenérgica central.
• Dosis: se han usado dosis para DAPO de 5-500 pg/kg/min con o sin dosis de carga de 0,5-1 mg/kg.
• Estas dosis producen menor consumo de opioides en el posoperatorio (69%) y reducción de la náusaes y vómitos posoperatorios (61%).
-
K. Técnicas regionales
• Son acompañantes destacadas y obligados de la ALO. El bloqueo de las entradas aferentes amortigua la respuesta de estrés a la cirugía y la activación simpática en todo el período perioperatorio. Las técnicas regionales son recursos que deben implementarse en cualquier protocolo de ALO, siempre que sea posible y no estén contraindicadas. Son efectivas tanto las inyecciones de anestésicos locales de duración prolongada en las incisiones y puertos quirúrgicos, como los bloqueos nerviosos periféricos y los bloqueos interfasciales.
• Incluyen los bloqueos de nervios periféricos, bloqueos de planos fasciales, bloqueos paravertebrales y los bloqueos neuroaxiales.
• La incorporación del bloqueo del plano transverso del abdomen (TAP) a los protocolos ERAS ha demostrado disminuir los requerimientos de opioides posoperatorios y la estadía
hospitalaria luego de cirugía abdominal.
• Otros bloqueos de planos faciales como el serrato anterior, el erector de la espina y el cuadrado lumbar, están ganando gran interés como herramientas analgésicas perioperatorias combinadas con anestesia general para evitar los opioides.
• Una limitante del uso de anestésicos locales como la bu- pivacaina es su corta duración. Sin embargo, actualmente se dispone de una forma liposomal del fármaco que tiene una duración más prolongada (2 a 3,5 días), lo cual ha sido probado en analgesia local posquirúrgica, hemorroidecto- mía, reconstrucción mamaria microquirúrgica con bloqueo TAP[30],[31].
Al comentar sobre la analgesia posoperatoria libre de opioides (APLO) se menciona el tema de la analgesia multimodal, pero se desconocen que combinaciones específicas pueden reemplazar por completo y efectivamente a los opioides. Los hospitales que practican OFA tienen sus propias combinaciones para sus pacientes, para ser usadas en el transoperatorio, lo cual sería una verdadera OFA, y en el posoperatorio, lo cual sería una APLO. Es un tema de investigación complejo, determinar cuál o cuáles de estos cocteles serían los más efectivos como técnicas de OFA, ¿para qué procedimientos y/o para qué pacientes? Estas son preguntas difíciles de responder en la actualidad.
-
Conclusiones
Los opioides han sido la piedra angular de la anestesia y la analgesia posoperatoria durante muchos años; sin embargo, están asociados con muchas RAM que pueden retardar la recuperación del paciente después de la cirugía. El uso excesivo de ellos los últimos años en la profesión médica, ha contribuido a la actual epidemia de opioides en los Estados Unidos de América. Estamos obligados a poner en práctica un uso más racional de estos fármacos, en la menor dosis posible que nos produzca el menor efecto analgésico, así como también implementar opciones analgésicas multimodales, con fármacos no opioides pero con propiedad analgésica.
Está bien documentado, donde no se deberían utilizar los opioides, por los efectos de sus RAM. Es allí donde tiene cabida esta nueva modalidad analgésica, con fármacos diferentes con propiedades analgésicas, usados como coadyuvantes.
-
Referencias
1. Mulier J. Opioid free general anesthesia: A paradigm shift? Rev Esp Anestesiol Reanim. 2017 Oct;64(8):427–30. https://doi.org/10.1016/j.redar.2017.03.004 PMID:28431750
2. Boretsky K, Mason K. In the Arms of Morpheus without Morphia; Mitigating the United States Opioid Epidemic by Decreasing the Surgical Use of Opioids. J Clin Med. 2021 Apr;10(7):1472. https://doi.org/10.3390/jcm10071472 PMID:33918296
3. Thota RS, Ramkiran S, Garg R, Goswami J, Baxi V, Thomas M. Opioid free onco-anesthesia: Is it time to convict opioids? A systematic review of literature. J Anaesthesiol Clin Pharmacol. 2019 Oct-Dec;35(4):441-452. https://doi.org/10.4103/joacp.JOACP_128_19.. PMID: 319 20226; PMCID: PMC6939563.
4. Leonard TG. Non-opioid analgesic options. S Afr Fam Pract. 2018;60(4):S17–20. https://doi.org/10.4102/safp.v60i4.4891.
5. Chia PA, Cannesson M, Bui CC. Opioid free anesthesia: feasible? Curr Opin Anaesthesiol. 2020 Aug;33(4):512–7. https://doi.org/10.1097/ACO.0000000000000878 PMID:32530891
6. Kaniyil S, Haley CH. Anestesia Libre de Opioides. https://resources.wfsahq.org/atotw/anestesia-libre-de-opioides/
7. McDonald JS, Chen B, Kwan W. Analgesia y anestesia en obstetricia. In: De Cherney AH, Nathan L, Laufer N, Roman AS. eds. Diagnóstico y tratamiento ginecoobstétricos, 11e. McGraw Hill; 2014. Accessed junio 08, 2023. https://accessmedicina.mhmedical.com/content.aspx?bookid=1494§ionid=98126957
8) Olausson A, Svensson CJ, Andréll P, Jildenstål P, Thörn SE, Wolf A. Total opioid-free general anaesthesia can improve postoperative outcomes after surgery, without evidence of adverse effects on patient safety and pain management: A systematic review and meta-analysis. Acta Anaesthesiol Scand [Internet]. 2022;66(2):17085. Disponible en: https://doi.org/10.1111/aas.13994 ..
9. Sultana A, Torres D, Schumann R. Special indications for Opioid Free Anaesthesia and Analgesia, patient and procedure related: including obesity, sleep apnoea, chronic obstructive pulmonary disease, complex regional pain syndromes, opioid addiction and cancer surgery. Best Pract Res Clin Anaesthesiol. 2017 Dec;31(4):547–60. https://doi.org/10.1016/j.bpa.2017.11.002 PMID:29739543
10. Tauste- Hernández B. Cortiñas-Sáenz M, Fernández Gines FD, Expósio-Lópesz JM. Revisión de mezclas binarias. Terciarias y cuaternarias para inducción y mantenimiento de anestesia libre de opiáceos. Farm Hosp. 2021;45(3):135–41. PMID:33941057
11. Beverly A, Kaye AD, Ljungqvist O, Urman RD. Essential Elements of Multimodal Analgesia in Enhanced Recovery After Surgery (ERAS) Guidelines. Anesthesiol Clin. 2017 Jun;35(2):e115–43. https://doi.org/10.1016/j.anclin.2017.01.018 PMID:28526156
12. Gabriel RA, Swisher MW, Sztain JF, Furnish TJ, Ilfeld BM, Said ET. State of the art opioid-sparing strategies for post-operative pain in adult surgical patients. Expert Opin Pharmacother. 2019 Jun;20(8):949–61. https://doi.org/10.1080/14656566.2019.1583743 PMID:30810425
13. Schenkel L, Vogel Kahmann I, Steuer C. Opioid-Free Anesthesia: Physico Chemical Stability Studies on Multi-Analyte Mixtures Intended for Use in Clinical Anesthesiology. Hosp Pharm. 2022 Apr;57(2):246–52. https://doi.org/10.1177/00185787211016336 PMID:35601712
14. Tricco AC, Lillie E, Zarin W, O’Brien KK, Colquhoun H, Levac D, et al. PRISMA Extension for Scoping Reviews (PRISMA-ScR): checklist and Explanation. Ann Intern Med. 2018 Oct;169(7):467–73. https://doi.org/10.7326/M18-0850 PMID:30178033
15. Gelineau AM, King MR, Ladha KS, Burns SM, Houle T, Anderson TA. Intraoperative Esmolol as an Adjunct for Perioperative Opioid and Postoperative Pain Reduction: A Systematic Review, Meta-analysis, and Meta-regression. Anesth Analg. 2018 Mar;126(3):1035–49. https://doi.org/10.1213/ANE.0000000000002469 PMID:29028742
16. Koepke EJ, Manning EL, Miller TE, Ganesh A, Williams DG, Manning MW. The rising tide of opioid use and abuse: the role of the anesthesiologist. Perioper Med (Lond). 2018 Jul;7(1):16. https://doi.org/10.1186/s13741-018-0097-4 PMID:29988696
17. Ramírez-Paesano C, Juanola Galceran A, Rodiera Clarens C, Gilete García V, Oliver Abadal B, Vilchez Cobo V, et al. Opioid-free anesthesia for patients with joint hypermobility syndrome undergoing craneo-cervical fixation: a case-series study focused on anti-hyperalgesic approach. Orphanet J Rare Dis. 2021 Apr;16(1):172. https://doi.org/10.1186/s13023-021-01795-4 PMID:33849631
18. Forget P, Cata J. Stable anesthesia with alternative to opioids: are ketamine and magnesium helpful in stabilizing hemodynamics during surgery? A systematic review and meta-analyses of randomized controlled trials. Best Pract Res Clin Anaesthesiol. 2017 Dec;31(4):523–31. https://doi.org/10.1016/j.bpa.2017.07.001 PMID:29739541
19. Anamourlis PC. Opioid Free Anaesthesia: a paradigm shift. S Afr Fam Pract. 2019;61(2):S21S24. https://doi.org/10.4102/safp.v61i2.4993.
20. Afsharimani B, Cabot PJ, Parat MO. Morphine use in cancer surgery. Front Pharmacol. 2011 Aug;2:46. https://doi.org/10.3389/fphar.2011.00046 PMID:21852973
21. Ramaswamy S, Langford RM. Antinociceptive and immunosuppressive effect of opioids in an acute postoperative setting: an evidence-based review. BJA Educ. 2017;17(3):105–10. https://doi.org/10.1093/bjaed/mkw030.
22. Kosciuczuk U, Knapp P, Lotowska-Cwiklewska AM. Opioid-induced immunosuppression and carcinogenesis promotion theories create the newest trend in acute and chronic pain pharmacotherapy. Clinics (São Paulo). 2020 Mar;75:e1554. https://doi.org/10.6061/clinics/2020/e1554 PMID:32215455
23. Cozowicz C, Poeran J, Zubizarreta N, Liu J, Weinstein SM, Pichler L, et al. Non-opioid analgesic modes of pain management are associated with reduced postoperative complications and resource utilisation: a retrospective study of obstructive sleep apnoea patients undergoing elective joint arthroplasty. Br J Anaesth. 2019 Jan;122(1):131–40. https://doi.org/10.1016/j.bja.2018.08.027 PMID:30579391
24. Mauermann E, Ruppen W, Bandschapp O. Different protocols used today to achieve total opioid-free general anesthesia without locoregional blocks. Best Pract Res Clin Anaesthesiol. 2017 Dec;31(4):533–45. https://doi.org/10.1016/j.bpa.2017.11.003 PMID:29739542
25. Mugabure-Bujedo B, González-Santos S, Uría-Azpiazu A, Conejero-Morga G, González-Jorrín N. Coadyuvantes farmacológicos con efecto ahorrador de opioides en el periodo perioperatorio. Rev. Soc. Esp. Dolor [Internet]. 2018 Oct [citado 2023 Jun 28]; 25 (5) : 278-290. Disponible en: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1134-80462018000500005&lng=es. https://dx.doi.org/https://doi.org/10.20986/resed.2018.3663/2018.
26. Baboli KM, Liu H, Poggio JL. Opioid-free postoperative analgesia: is it feasible? Curr Probl Surg. 2020 Jul;57(7):100794. https://doi.org/10.1016/j.cpsurg.2020.100794 PMID:32546291
27. Watts R, Thiruvenkatarajan V, Calvert M, Newcombe G, van Wijk RM. The effect of perioperative esmolol on early postoperative pain: A systematic review and meta-analysis. J Anaesthesiol Clin Pharmacol. 2017;33(1):28–39. https://doi.org/10.4103/0970-9185.202182 PMID:28413270
28. Bugada D, Lorini LF, Lavand’homme P. Opioid free anesthesia: evidence for short and long-term outcome. Minerva Anestesiol. 2021 Feb;87(2):230–7. https://doi.org/10.23736/S0375-9393.20.14515-2 PMID:32755088
29. Do U, El-Kefraoui C, Pook M, Balvardi S, Barone N, Nguyen-Powanda P, et al.; McGill Better Opioid Prescribing Collaboration. Feasibility of Prospectively Comparing Opioid Analgesia With Opioid-Free Analgesia After Outpatient General Surgery: A Pilot Randomized Clinical Trial. JAMA Netw Open. 2022 Jul;5(7):e2221430. https://doi.org/10.1001/jamanetworkopen.2022.21430 PMID:35849399
30. Kaye AD, Armstead-Williams C, Hyatali F, Cox KS, Kaye RJ, Eng LK, et al. Exparel for Postoperative Pain Management: a Comprehensive Review. Curr Pain Headache Rep. 2020 Oct;24(11):73. https://doi.org/10.1007/s11916-020-00905-4 PMID:33098008
31. Momeni A, Ramesh NK, Wan D, Nguyen D, Sorice SC. Postoperative analgesia after microsurgical breast reconstruction using liposomal bupivacaine (Exparel). Breast J. 2019 Sep;25(5):903–7. https://doi.org/10.1111/tbj.13349 PMID:31131501

 ORCID
ORCID