Eduardo Martinez Aquino1*, Fausto de la Cruz Benito1, Carla Viridiana Lezcano Lázaro1, Efrén Magallón Arellano1, Adolfo Álvarez Castañeda1, Brenda Janette De La Mora Loa2
Recibido: 16-08-2025
Aceptado: 18-09-2025
©2025 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 54 Núm. 5 pp. 570-580|https://doi.org/10.25237/revchilanestv54n5-12
PDF|ePub|RIS
Ultrasound venous access in pediatrics
Abstract
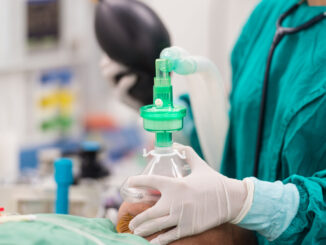
The placement of central venous catheters in pediatric patients represents a clinical challenge due to anatomical and physiological peculiarities and the high risk of complications. The systematic incorporation of ultrasound has transformed this procedure, allowing direct visualization of vascular structures, optimizing technical precision, and reducing adverse events. This review article addresses the physical fundamentals of ultrasound, catheter selection according to age and anatomy, the technical principles of ultrasound guidance, and specific strategies for each anatomical site (internal jugular, subclavian, and femoral). The GAVeCeLT protocol and its integration with advanced clinical practices are analyzed, as well as the ultrasound evaluation of early and late complications associated with the procedure. Tools such as the triangulation principle, the ECHOTIP-Ped protocol, and functional echocardiography with bubble test are highlighted, which improve the safety and efficacy of central venous catheterization in neonates and children. Current evidence supports the use of ultrasound as an international standard in pediatrics, with a positive impact on clinical outcomes and the technical training of medical personnel.
Resumen
La colocación de catéteres venosos centrales en pacientes pediátricos representa un desafío clínico debido a las particularidades anatómicas, fisiológicas y al riesgo elevado de complicaciones. La incorporación sistemática del ultrasonido ha transformado este procedimiento, permitiendo una visualización directa de las estructuras vasculares, optimizando la precisión técnica y reduciendo eventos adversos. Este artículo de revisión aborda los fundamentos físicos del ultrasonido, la selección de catéteres según edad y anatomía, los principios técnicos de orientación ecográfica, y las estrategias específicas por sitio anatómico (yugular interna, subclavia y femoral). Se analiza el protocolo GAVeCeLT y su integración con prácticas clínicas avanzadas, así como la evaluación ecográfica de complicaciones tempranas y tardías asociadas al procedimiento. Se destacan herramientas como el principio de triangulación, el protocolo ECHOTIP-Ped y la ecocardiografía funcional con prueba de burbujeo, que permiten mejorar la seguridad y eficacia de la canalización venosa central en neonatos y niños. La evidencia actual respalda el uso del ultrasonido como estándar internacional en pediatría, con impacto positivo en los resultados clínicos y en la formación técnica del personal médico.
-
Introducción
El catéter venoso central (CVC) se define como aquel cuya porción distal se localiza en una vena central -específicamente en el tercio proximal de la vena cava superior (VCS), la vena cava inferior (VCI) o la aurícula derecha (AD)-, independientemente del sitio de punción o ingreso. Este procedimiento invasivo es ampliamente utilizado en población pediátrica, particularmente en pacientes que requieren transfusiones múltiples, terapias prolongadas o administración de fármacos no compatibles con la vía periférica[1].
En pediatría, la canalización venosa central representa un desafío técnico debido a las particularidades anatómicas y fisiológicas del paciente. La incorporación del ultrasonido (USG) como herramienta médica ha transformado este procedimiento, al ofrecer mayor seguridad, eficacia y precisión en la colocación de los catéteres[2]. Un estudio de cohorte prospectivo realizado en una unidad de cuidados intensivos neonatales (UCIN) de un hospital universitario en México evaluó 100 CVC colocados en la vena yugular interna (VYI) en recién nacidos de bajo peso (94%). Se reportó un tiempo promedio de inserción de 16,8 minutos (rango: 10-40 min) y una mediana de 2 intentos (rango: 1-8), respaldando la eficacia y seguridad del USG en tiempo real para el acceso venoso central en neonatos[2].
La Sociedad Española de Cuidados Intensivos Pediátricos (SECIP) recomienda el uso sistemático de la ecografía en la canalización vascular, dado que incrementa la tasa de éxito al primer intento, reduce fallos de canalización, minimiza punciones arteriales erróneas y previene complicaciones. Además, permite identificar variantes anatómicas, vasos no idóneos (por trombosis, calibre reducido o proximidad arterial) y optimizar la elección del tamaño del catéter[3].
En concordancia, las guías del National Institute for Health and Care Excellence (NICE) establecen desde 2002 el uso del USG en tiempo real como estándar para la colocación de CVC en pediatría. Estas directrices destacan que la ecografía mejora significativamente la seguridad del procedimiento, reduce complicaciones como punciones arteriales inadvertidas y aumenta la tasa de éxito al primer intento, especialmente en accesos yugulares[4].
La Revista Europea de Anestesiología (EJA) propone el uso integral del USG en todas las etapas del procedimiento, incluyendo: evaluación ecográfica previa de las opciones venosas disponibles, detección de patología local que contraindique la punción, punción ecoguiada en tiempo real, verificación del trayecto de la guía metálica y del catéter hacia la VCS o VCI, confirmación de la posición correcta de la punta del catéter, y detección temprana y tardía de complicaciones postprocedimiento[5] (Figura 1).
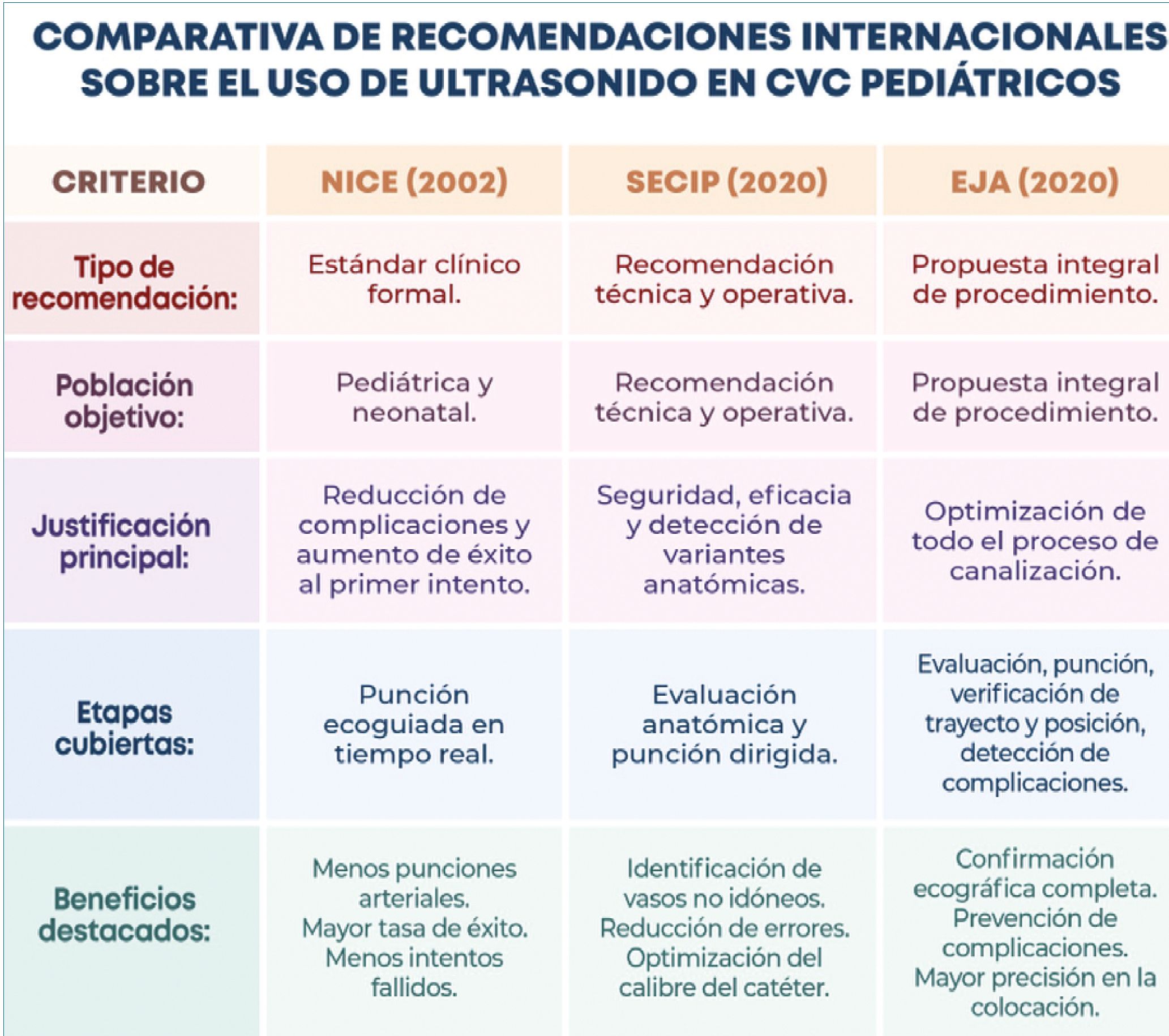
Figura 1. Cuadro comparativo de recomendaciones internacionales.
Complementando estas recomendaciones europeas, la Association for Vascular Access (AVA) y el World Congress on Vascular Access (WoCoVA) han establecido que el uso de USG en tiempo real para la colocación de CVC en pediatría debe considerarse un estándar internacional de atención. AVA enfatiza que la ecografía mejora la precisión de la punción, reduce intentos fallidos y complicaciones, y debe ser realizada por profesionales con formación específica en ecografía vascular pediátrica[6]. Por su parte, WoCoVA promueve el concepto de “uso global del ultrasonido”, que incluye la evaluación preprocedimiento, la canalización ecoguiada, la navegación y localización de la punta del catéter, así como la detección de complicaciones inmediatas y tardías[7]. Ambas organizaciones coinciden en que el USG ha reemplazado a los métodos radiológicos en la canalización venosa pediátrica, mejorando significativamente los resultados clínicos y la seguridad del paciente.
Respecto a los sitios de punción recomendados, la EJA establece indicaciones específicas según edad y contexto clínico (Figura 2). Actualmente, el uso de guía ecográfica se considera obligatorio para la canalización venosa central en neonatos y niños. Los únicos dispositivos que no requieren ecografía para su inserción son el catéter venoso umbilical (UVC) y los catéteres epicutaneocava (CEC) en neonatos. Todos los demás accesos centrales -incluyendo CICC, PICC, FICC y puertos implantables- deben colocarse mediante canalización ecoguiada.
-
Catéteres recomendados en pediatría
La selección del catéter venoso central (CVC) en pacientes pediátricos debe considerar múltiples factores: peso corporal, localización del vaso, tipo de acceso y duración prevista del tratamiento. Actualmente, los dispositivos disponibles están fabricados principalmente de poliuretano, material que ofrece ventajas clínicas relevantes como alta biocompatibilidad, resistencia al acodamiento, buena fuerza de tensión y tolerancia a diversos agentes químicos. Además, presentan una punta suave y flexible que facilita la inserción, son radiopacos y cuentan con tratamiento antiséptico a base de clorhexidina y sulfadiazina de plata, lo que contribuye a la prevención de infecciones asociadas al dispositivo[9].
Los catéteres pueden ser de uno, dos o tres lúmenes, con capacidades de flujo que alcanzan hasta 2.656 ml/h, dependiendo del calibre. En contextos de terapia intensiva pediátrica, se recomienda limitar su uso a un máximo de 21 días[9]. La elección del calibre debe basarse en la evaluación ecográfica del vaso, procurando que el diámetro externo del catéter no exceda un tercio del diámetro interno del vaso, ya que esto incrementa el riesgo de trombosis. El uso del ultrasonido permite medir con precisión el diámetro vascular y seleccionar el calibre más adecuado. Asimismo, la longitud del catéter debe garantizar que la punta se ubique en una posición anatómica segura y funcional[10].
La correcta ubicación de la punta del CVC es esencial para asegurar su funcionamiento óptimo y minimizar complicaciones. En abordajes por vía yugular o subclavia, se recomienda que la punta se sitúe en el tercio inferior de la vena cava superior, idealmente en la unión con la aurícula derecha o en su porción superior. Esta localización permite una adecuada alineación con el eje del vaso, reduce la irritación mecánica del endotelio y favorece la dilución de fármacos en zonas de alto flujo sanguíneo[10].
Las recomendaciones específicas según la edad del paciente son las siguientes:
• Lactantes pequeños: 0,5 cm por encima de la carina.
• Lactantes mayores: 1 cm por encima de la carina.
• Niños mayores: a nivel de la carina.
En el caso de abordajes femorales, la punta del catéter debe quedar por encima del diafragma, evitando su proximidad a la desembocadura de las venas renales, ya que esta ubicación puede inducir trombosis renal y daño funcional[10].
| Vena braquiocefálica. | Uso ecogulado solo por operadores expertos. |
| Vena femoral. | Ecografía aumenta tasa de éxito, con tendencia a reducir complicaciones. |
| Arterias periféricas. | Recomendado uso rutinario de USC. |
| Venas periféricas. | No se recomienda uso rutinario de USG. |
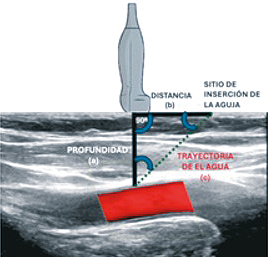
Figura 2. Sitios de punción y grado de recomendación según la EJA.
Cuando el procedimiento se realiza bajo guía ecográfica, es posible confirmar la localización de la punta en tiempo real. En procedimientos quirúrgicos o colocaciones “a ciegas”, se recomienda realizar una radiografía de tórax al finalizar, tanto para verificar la posición como para descartar complicaciones como neumotórax[10].
Una localización demasiado proximal en la vena cava superior puede favorecer la aparición de flebitis por soluciones de alta osmolaridad, mientras que una ubicación excesivamente distal en la aurícula derecha podría inducir arritmias, lesión valvular o taponamiento cardíaco. En pacientes pediátricos, se debe considerar el crecimiento corporal, ya que una punta mal posicionada puede migrar con el tiempo hacia zonas no deseadas como la vena subclavia o las venas renales, generando complicaciones trombóticas o necesidad de recambio prematuro del CVC[10]. Se considera que la localización ideal se encuentra en la unión entre la vena cava superior y la aurícula derecha, donde se optimiza el flujo, se reduce la irritación en- dotelial y se mejora la alineación del catéter con el eje vascular, disminuyendo así los factores predisponentes a trombosis y mal funcionamiento[10].
-
Principios ecográficos para la colocación de catéteres venosos centrales guiados por ultrasonido
La colocación de catéteres venosos centrales (CVC) guiada por ultrasonido se ha consolidado como una técnica estándar en múltiples entornos clínicos, especialmente en unidades de cuidados intensivos y en pacientes pediátricos. Su implementación mejora la seguridad del procedimiento, reduce las complicaciones mecánicas y aumenta la tasa de éxito en la primera punción[11].
-
Fundamentos físicos del ultrasonido
El ultrasonido médico se basa en la emisión de ondas mecánicas de alta frecuencia, generadas por la vibración de un cristal piezoeléctrico contenido en el transductor. Estas ondas se propagan a través de los tejidos corporales y su frecuencia supera los 20.000 Hz (20 kHz), límite superior del sonido audible por el ser humano[12]. Las frecuencias utilizadas en diagnóstico clínico oscilan entre 2 y 30 MHz; las frecuencias altas permiten valorar estructuras superficiales como vasos, piel y ojos, mientras que las bajas se emplean para explorar tejidos profundos[12].
La velocidad de propagación del sonido en tejidos blandos se estima en 1.540 m/s, aunque varía según la densidad y compresibilidad del medio. Los sólidos presentan alta impedancia acústica, mientras que los líquidos y tejidos blandos tienen menor impedancia. No obstante, el aire -a pesar de su baja impedancia- es un mal transmisor del ultrasonido, ya que no cumple con las condiciones de continuidad acuosa necesarias para la propagación eficiente del haz[12].
Cuando el haz ultrasónico encuentra una interfase entre tejidos con diferentes impedancias, parte de la energía se refleja y regresa al transductor como eco. Si la diferencia de impedancia es alta, el reflejo será más intenso; si es baja, el haz se transmitirá en mayor proporción[12]. Este fenómeno es clave para la formación de imágenes en escala de grises.
-
Selección del transductor y modos ecográficos
La elección del transductor depende de la profundidad del vaso y del tamaño del paciente. En accesos venosos centrales, se prefieren transductores lineales de alta frecuencia (5-15 MHz) por su excelente resolución para estructuras superficiales como la vena yugular interna o la femoral[13]. En neonatos y lactantes, los transductores microconvexos permiten una mejor adaptación anatómica[14].
Los modos ecográficos más utilizados en la colocación de CVC son: el modo B (Brightness), que ofrece una imagen bidimensional en escala de grises; el Doppler color, que permite diferenciar venas (flujo continuo) de arterias (flujo pulsátil); y el Doppler pulsado, que cuantifica la velocidad del flujo y confirma su naturaleza venosa[15],[16].
-
Ecogenicidad y artefactos
La ecogenicidad describe la capacidad de los tejidos para reflejar las ondas de ultrasonido. Las estructuras anecoicas (sin ecos) se visualizan en negro, como ocurre en la luz vascular; las hipoecoicas (reflejo débil) en gris oscuro, como el músculo; y las hiperecoicas (reflejo intenso) en blanco brillante, como la aguja o el hueso. Las estructuras isoecoicas presentan ecogenicidad similar al tejido circundante, lo que puede dificultar su diferenciación[17].
Durante la colocación del CVC, la vena yugular interna se visualiza como una estructura anecoica, ovalada y compresible, mientras que la arteria carótida es hipoecoica, redonda y no compresible. La aguja se visualiza como una línea hiperecoica en plano o como un punto brillante fuera de plano[18].
Los artefactos ecográficos pueden ser útiles o nocivos. La sombra acústica ocurre cuando el haz choca con una interfase muy ecogénica (litiasis, hueso), impidiendo la visualización posterior. El refuerzo posterior se produce al atravesar medios anecoicos como vasos o quistes, generando un halo hiperecogénico detrás. La reverberación aparece como múltiples líneas hiperecoicas paralelas, típicas en interfases aire-tejido, y puede minimizarse ajustando la ganancia o utilizando armónicos. La imagen en espejo simula estructuras duplicadas por reflexión en interfases curvas muy ecogénicas. La anisotropía, por su parte, describe la variación de la ecogenicidad según el ángulo de incidencia del haz sobre ciertos tejidos, como tendones o nervios[12].
-
Atenuación y procesamiento de imagen
A medida que el haz ultrasónico se propaga por tejidos más profundos, su energía disminuye por absorción (transformación en calor) y dispersión (desviación de trayectoria), fenómeno conocido como atenuación. El hueso y el aire son los principales atenuadores, mientras que los líquidos permiten una transmisión eficiente[12].
El transductor convierte los ecos reflejados en señales eléctricas que son amplificadas y procesadas para formar imágenes. El uso de gel entre el transductor y la piel elimina el aire superficial y mejora la transmisión del haz[12].
-
Técnicas de colocación de accesos venosos guiados por ecografía
La ecografía ha revolucionado la práctica clínica en la colocación de accesos venosos, especialmente en pacientes pediátricos y en aquellos con anatomía vascular compleja. Su uso permite una visualización directa de las estructuras vasculares, mejora la precisión del procedimiento y reduce significativamente las complicaciones asociadas a la punción ciegas[19].
-
Principios técnicos fundamentales
Una colocación segura y eficaz del catéter venoso central (CVC) requiere el cumplimiento riguroso de principios técnicos de orientación ecográfica. La alineación espacial debe ser precisa: el lado izquierdo y derecho del paciente debe coincidir con la orientación del transductor y con la visualización en pantalla. Asimismo, el vaso objetivo, el transductor y el operador deben estar alineados en un mismo eje visual, lo que optimiza la identificación anatómica y la trayectoria de la aguja[20].
La orientación anatómica del transductor debe mantenerse uniforme durante el procedimiento. En visión longitudinal, se recomienda posicionar la muesca del transductor hacia craneal, lo que permite una lectura anatómica coherente y facilita la correlación con estructuras vasculares profundas[21].
-
Relación del plano ecográfico con el vaso
La visualización ecográfica puede realizarse en tres planos principales, cada uno con ventajas específicas según el contexto anatómico y clínico:
• Plano transversal (corte corto): El transductor se coloca perpendicular al eje del vaso, generando una imagen circular. Esta vista permite identificar estructuras adyacentes como arterias, nervios o músculos, siendo útil en la evaluación inicial del sitio de punción[21].
• Plano longitudinal (corte largo): El transductor se alinea paralelamente al vaso, produciendo una imagen cilíndrica. Esta modalidad permite visualizar la trayectoria completa de la aguja durante la punción, aunque limita la visión de estructuras vecinas[21].
• Plano oblicuo: Combina las ventajas de los planos transversal y longitudinal, permitiendo la visualización simultánea de la vena y la arteria. Es especialmente útil en accesos complejos o en pacientes con anatomía vascular alterada[22].
-
Principio de triangulación en el acceso vascular ecoguiado en Pediatría
El acceso vascular guiado por ultrasonido ha transformado la práctica clínica en pediatría al permitir una visualización directa del vaso y de la trayectoria de la aguja, reduciendo complicaciones y aumentando la tasa de éxito en la primera punción. Dentro de las estrategias técnicas que optimizan este procedimiento, el principio de triangulación representa una herramienta clave para mejorar la precisión en abordajes fuera de plano, especialmente en pacientes pediátricos, donde la anatomía vascular es más superficial, de menor calibre y con mayor variabilidad. La triangulación se basa en una relación geométrica entre tres elementos: la profundidad del vaso, la distancia desde el transductor al punto de punción y el ángulo de entrada de la aguja. Cuando la profundidad del vaso es igual a la distancia lateral desde el transductor al punto de inserción, y se utiliza un ángulo de entrada de 45°, la aguja debería alcanzar el vaso justo en el plano ecográfico. Esta configuración genera un triángulo rectángulo con lados iguales, y permite calcular la longitud del trayecto de la aguja mediante el teorema de Pitágoras. Por ejemplo, si el vaso se encuentra a 1 cm de profundidad y el punto de punción está a 1 cm del borde del transductor, el trayecto ideal de la aguja será de aproximadamente 1,4 cm[23] (Figura 3).
Este principio permite al operador anticipar el momento en que la aguja debe aparecer en el plano ecográfico, facilitando su visualización como un punto hiperecogénico en abordajes fuera de plano. En pediatría, esta estrategia es particularmente útil, ya que permite minimizar movimientos innecesarios, reducir el número de intentos y evitar lesiones vasculares o extravasaciones. Además, favorece el aprendizaje estructurado en entornos de simulación, al ofrecer una base geométrica reproducible y fácilmente comprensible[23].
La aplicación sistemática del principio de triangulación, junto con el dominio de los planos ecográficos y el reconocimiento anatómico dinámico, constituye una competencia esencial en el acceso vascular pediátrico guiado por ultrasonido. Su incorporación en protocolos clínicos y programas de formación contribuye a estandarizar la práctica y mejorar los resultados clínicos en unidades de cuidados intensivos pediátricos.
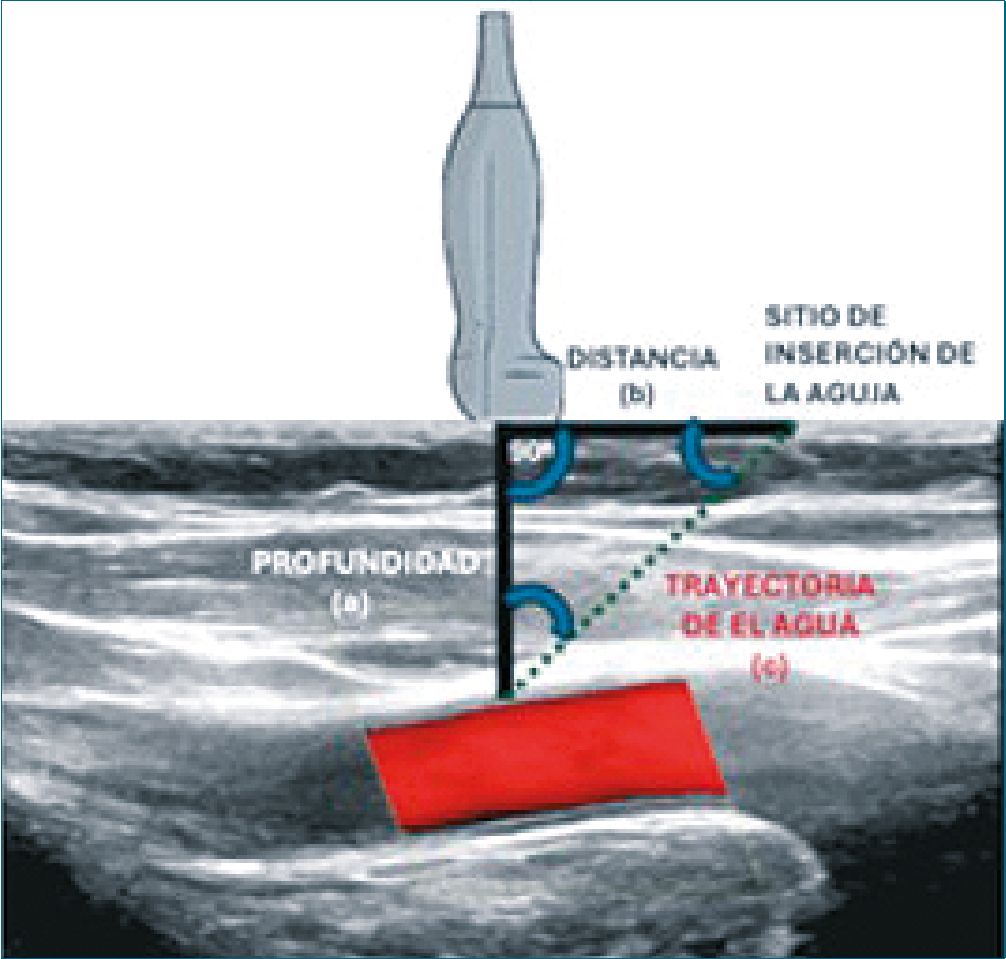
Figura 3. Triangulación ecográfica para optimizar la trayectoria de punción. Se representa la relación geométrica entre la profundidad del vaso, la distancia lateral desde el traductor al punto de inserción y el ángulo de entrada de la aguja (45°). Cuando los lados del triángulo rectángulo son iguales (1 cm de profundidad y 1 cm de distancia lateral), la aguja alcanza el vaso en eI plano ecográfico, con una trayectoria calculada mediante al teorema de Pitágoras (< 1,4 cm]. Este principio permite planificar abordajes precisos en procedimientos ecoguiados.
-
Técnica para la punción ecoguiada
Para obtener la imagen adecuada del vaso a canalizar, es fundamental que estemos bien orientados en la imagen. Hay dos principios que siempre debemos observar en la canalización vascular ecoguiada: a) debemos obtener una imagen anatómica en la pantalla y b) nuestro transductor, el vaso del paciente y la pantalla de ultrasonido deben estar en el mismo eje de visión (es decir, mirando de frente hay que verlo todo), para lo cual es ideal colocar el ecógrafo en el lado opuesto al paciente en el que nos encontramos.
Protocolo en la colocación de Acceso Venoso Central Integración del modelo GAVeCeLT con prácticas clínicas avanzadas para la colocación de accesos venosos centrales en población pediátrica
La colocación de catéteres venosos centrales (CVC) en pacientes pediátricos exige una técnica rigurosa, estandarizada y adaptada a las particularidades anatómicas y fisiológicas de esta población. El protocolo GAVeCeLT, desarrollado por Pit- tiruti et al.[24], propone un conjunto estructurado de medidas que incluye: evaluación ecográfica preprocedimiento, punción guiada en tiempo real, localización no radiológica de la punta, fijación sin suturas y protección del sitio de salida. Este enfoque ha demostrado reducir significativamente las complicaciones inmediatas y tardías, con una tasa global de eventos adversos de solo 3,7% en una cohorte de 729 pacientes pediátricos.
En nuestra práctica clínica, este protocolo se complementa con medidas adicionales que refuerzan la seguridad y precisión del procedimiento (Figura 4). Antes de la intervención, el paciente debe contar con monitoreo no invasivo completo y un equipo de soporte vital avanzado, dado que el procedimiento requiere sedación o anestesia, dependiendo de las condiciones del paciente.
La exploración ecográfica bilateral de las venas centrales (yugulares internas, subclavias y femorales) es indispensable para seleccionar el vaso óptimo, identificar su profundidad y descartar variantes anatómicas. Para confirmar la permeabilidad vascular, se recomienda aplicar presión suave con el transductor, lo que permite identificar trombosis mural o intraluminal antes de la punción.
La técnica se realiza bajo condiciones de esterilidad quirúrgica, idealmente en el quirófano, y con una disposición ergonómica que mantenga al paciente, al operador y al ultrasonido en el mismo plano visual. Durante la canalización, el transductor debe ser sostenido con la mano no dominante, mientras que la aguja y la jeringa con solución salina se manejan con la mano dominante. El vaso se identifica en eje transversal o longitudinal, centrando la imagen en pantalla. La aguja se avanza bajo visión directa continua, aspirando suavemente hasta obtener reflujo sanguíneo y visualizar el signo del “ojo de buey” (bull’s eye)[25].
Es importante considerar el signo de la “tienda de campa- ña”[26], frecuente en pediatría, donde la deformación de la pared vascular puede simular una punción exitosa sin que la aguja esté realmente intravascular, lo que representa un riesgo potencial.
Una vez canalizado el vaso, se introduce la guía bajo visualización ecográfica longitudinal, evitando retirar el transductor
del campo. Posteriormente, se retira la aguja, se realiza la dilatación y se introduce el catéter. La posición de la punta se verifica idealmente mediante ecografía cardíaca o técnica ECG intracavitaria[27], evitando el uso rutinario de radiografía en pacientes pediátricos.
Confirmada la correcta posición, se procede a la fijación y recubrimiento del acceso vascular, etapa crítica para garantizar la estabilidad del dispositivo y prevenir complicaciones. De acuerdo con las recomendaciones del grupo GAVeCeLT, se sugiere emplear sistemas de anclaje subcutáneo en lugar de suturas tradicionales. Estos dispositivos permiten una fijación segura del catéter mediante una estructura plástica que se inserta en el tejido subcutáneo, reduciendo significativamente el riesgo de desplazamiento accidental, infección en el sitio de inserción, trombosis y flebitis, además de facilitar el manejo clínico y disminuir la carga de trabajo del personal de enfermería.
El sistema de anclaje requiere aproximadamente 2 a 3 cm de catéter extracutáneo para su correcta colocación. En caso de no contar con dicho sistema, se optará por fijación mediante suturas no absorbibles (seda, nylon o prolene), con puntos simples o en U, generalmente en las alas o base del dispositivo. Aunque esta técnica proporciona una fijación inmediata y de bajo costo, se asocia con mayor riesgo de infección local, bacteriemia y desplazamiento accidental del catéter.
Finalmente, se debe aplicar un apósito transparente estéril sobre el sitio de inserción, complementado con una malla de sujeción no compresiva que proporcione protección adicional sin interferir con la visibilidad ni el acceso al punto de inserción.
Este enfoque combinado, que integra el protocolo GAVe- CeLT con prácticas clínicas optimizadas, permite una colocación segura, precisa y reproducible de CVC en neonatos y niños y minimizando complicaciones.
Técnicas ecográficas por sitio anatómico: yugular interna, subclavia y femoral
-
Vena yugular interna
La vena yugular interna se localiza en posición anterolateral o anterior respecto a la arteria carótida interna, siendo visible mediante ecografía cuando se coloca el transductor a nivel del cartílago cricoides. En pacientes pediátricos mayores, la vena yugular interna derecha suele presentar mayor longitud, trayecto más recto y mejor accesibilidad en comparación con la izquierda, lo que la convierte en el vaso preferido para canalización.
Para optimizar la visualización y reducir el riesgo de superposición vascular, se recomienda mantener la cabeza en posición neutra o con una rotación contralateral menor a 40°. Rotaciones superiores a este ángulo incrementan la probabilidad de que la arteria carótida se superponga sobre la vena yugular, dificultando una punción segura.
El abordaje longitudinal en plano es ideal en niños mayores, ya que permite una visualización continua de la aguja durante la canalización (Figura 5). Sin embargo, en lactantes, la limitación del espacio anatómico dificulta esta técnica, por lo que se sugiere emplear un abordaje transversal fuera de plano o transversal en plano, especialmente en casos donde exista superposición de la arteria carótida sobre la vena yugular interna.
La complicación más frecuente durante la canalización de la vena yugular interna es la punción accidental de la arteria carótida. Para minimizar este riesgo, se recomienda realizar un pre-escaneo en vista de eje corto, lo cual permite confirmar la relación anatómica entre la vena yugular interna y la arteria carótida común. Es fundamental evaluar la posición relativa de ambos vasos a lo largo de su trayecto, ya que esta puede variar y modificarse fácilmente con el movimiento de la cabeza. Por ello, no basta con observar una imagen redonda de la vena:
se debe analizar su relación con la carótida antes de elegir el punto de punción.
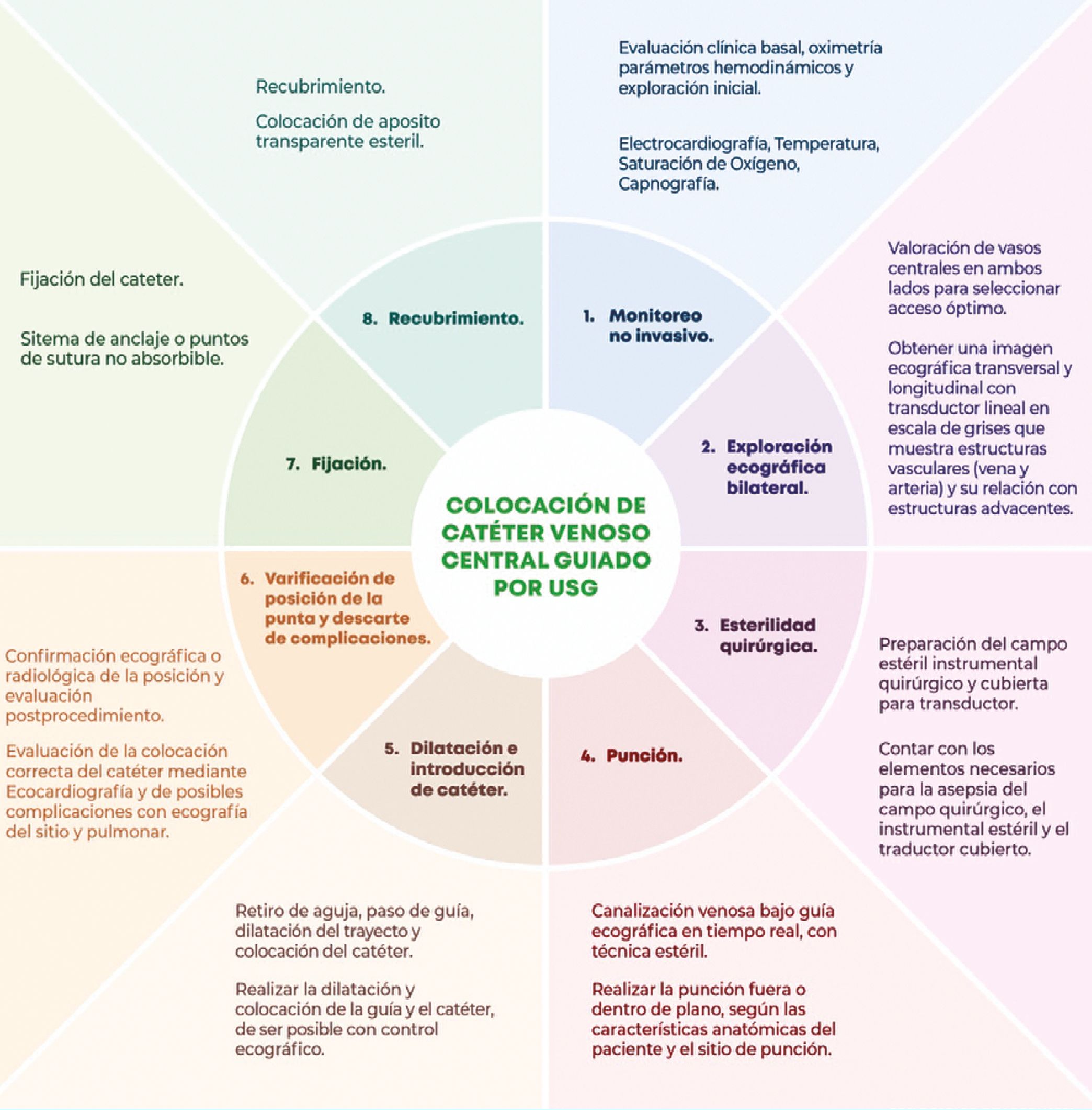
Figura 4. Integración del modelo GAVeCeLT con prácticas clínicas avanzadas para la colocación de accesos venosos centrales en población pedíatrica.
Para identificar el sitio óptimo de inserción, se utilizan dos técnicas complementarias. La técnica de barrido (“sweep”) consiste en deslizar el transductor a lo largo del trayecto de la vena yugular interna, asegurando que permanezca centrada en la imagen. Esto permite evaluar su tamaño y detectar posibles obstáculos. Una vez elegido el punto de punción, puede emplearse la técnica de oscilación (“swing”), que consiste en mantener el transductor fijo sobre el sitio seleccionado y realizar un movimiento de vaivén. Esta técnica permite seguir el avance de la aguja en tiempo real, especialmente en vista transversal[28].
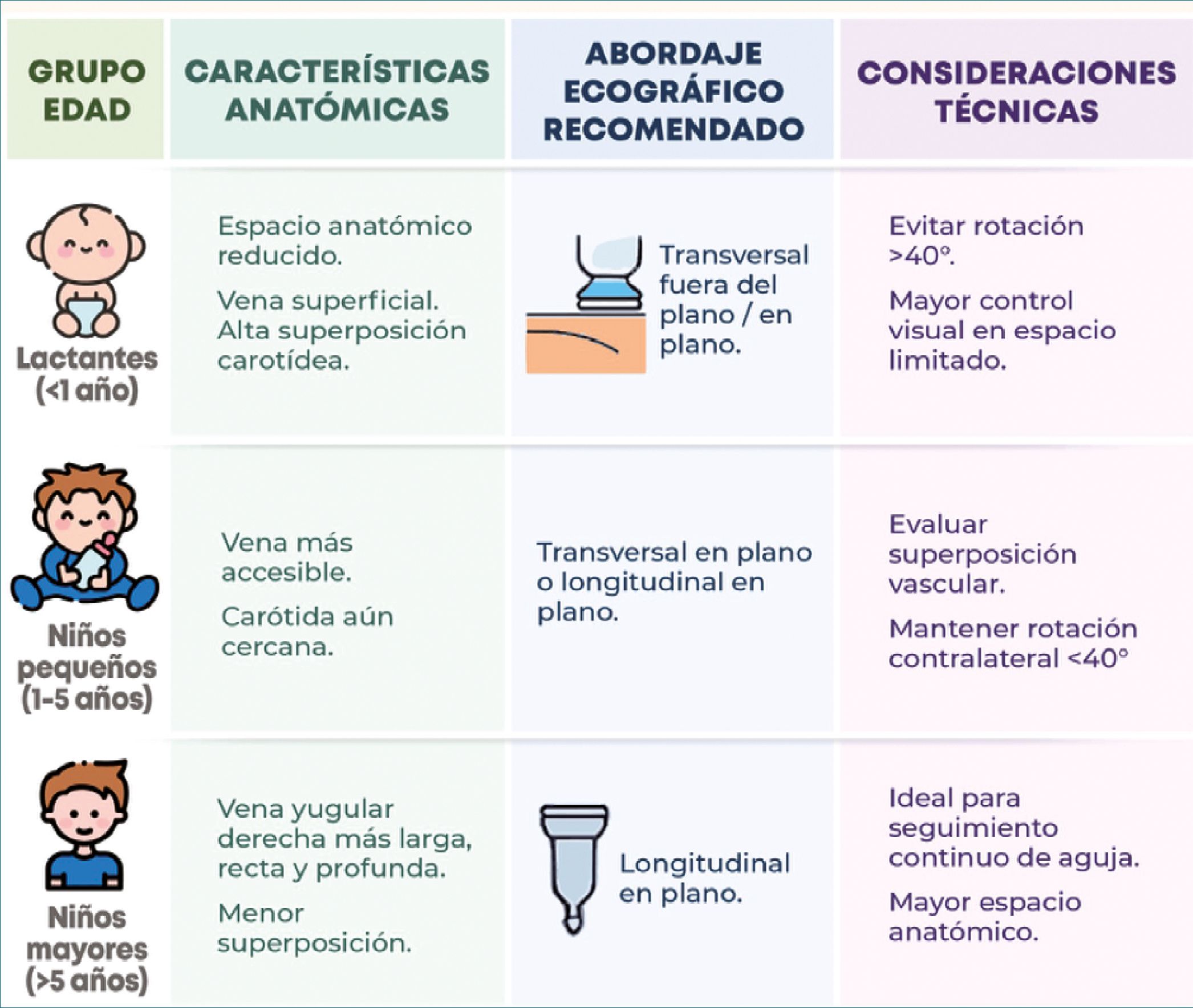
Figura 5. Abordaje ecográfico de la vena yugular interna por grupo etario.
-
Vena subclavia
La vena subclavia, ubicada anteromedial respecto a la arteria subclavia, puede ser visualizada mediante ecografía utilizando abordajes supraclaviculares e infraclaviculares. En pediatría, especialmente en menores de dos años, se observan variaciones anatómicas frecuentes que requieren una evaluación ecográfica detallada antes de intentar la canalización. El abordaje supraclavicular es el más utilizado en niños mayores, preferentemente con técnica longitudinal en plano, ya que permite una visualización continua de la aguja y del trayecto venoso. En lactantes, debido al espacio anatómico reducido, se recomienda el abordaje supraclavicular en vista transversal, que ofrece mayor control visual en zonas con menor margen de maniobra. El abordaje infraclavicular, aunque menos frecuente en pediatría, puede considerarse según la anatomía individual y la experiencia del operador.
El acceso ecoguiado a la vena subclavia presenta mayor complejidad que en otras venas centrales, principalmente porque la clavícula puede obstruir el haz ecográfico. Durante el pre-escaneo, es fundamental confirmar la distancia al vaso, la distancia al pulmón, la relación posicional con la arteria subclavia y el mejor punto de punción. Se debe evitar colocar la sonda en posición casi vertical sobre el sitio de punción, ya que esto dificulta la inserción de la guía. Se recomienda que el ángulo del transductor sea menor a 60 grados respecto a la piel, y que la punción se realice lo más cerca posible de la sonda para facilitar el avance de la aguja[29].
Una vez insertada correctamente la guía, se debe confirmar su presencia dentro del vaso mediante ecografía. En algunos casos, la guía introducida desde la vena axilar puede avanzar accidentalmente hacia la vena yugular interna o la vena braquiocefálica. No obstante, la canalización accidental de la vena braquiocefálica es poco frecuente, y una guía ubicada en la vena yugular interna puede identificarse fácilmente mediante ecografía[29].
-
Vena femoral
La vena femoral se localiza en posición posteromedial o medial respecto a la arteria femoral, y puede visualizarse mediante ecografía colocando el transductor justo por debajo del ligamento inguinal. Aunque la disposición anatómica clásica en la región femoral, de medial a lateral, es “vena, arteria y nervio”, tanto la posición como las ramas de la vena y la arteria femorales presentan variaciones significativas, especialmente en población pediátrica[30]. Por ello, el uso de técnica ecoguiada resulta fundamental para garantizar una canalización segura.
Es importante tener en cuenta el solapamiento vascular: la arteria femoral tiende a superponerse sobre la vena femoral, y este fenómeno se acentúa conforme el punto de punción se aleja del ligamento inguinal. En pacientes pediátricos, este solapamiento es aún más pronunciado, lo que aumenta el riesgo de punción arterial inadvertida[30].
Debido al tamaño reducido y a la limitación del área anatómica de trabajo en niños pequeños, se recomienda emplear un abordaje transversal fuera de plano, que permite una mejor visualización en espacios estrechos. Alternativamente, puede considerarse un abordaje transversal en plano, siempre que se logre una adecuada identificación de estructuras. En niños mayores, donde el espacio anatómico lo permite, es posible utilizar un abordaje longitudinal en plano, que ofrece mayor control visual durante la canalización.
Desde el punto de vista clínico, la vena femoral no es ideal para uso prolongado, debido al riesgo de infección y formación de trombos. Sin embargo, es relativamente más accesible que otras venas centrales y presenta una menor incidencia de complicaciones graves en el contexto de canalización aguda.
Durante el procedimiento, se recomienda colocar la sonda a menos de 60° respecto a la piel, lo que facilita el trayecto de la aguja y mejora la visualización ecográfica. Una vez insertada la guía correctamente, se debe confirmar su ubicación dentro de la vena femoral mediante ecografía, asegurando que no haya migración hacia estructuras adyacentes.
-
Complicaciones asociadas a la colocación de accesos vasculares centrales en pacientes pediátricos
Las complicaciones derivadas de la colocación de accesos venosos centrales en pacientes pediátricos pueden clasificarse en tempranas y tardías, según el momento de aparición y el mecanismo fisiopatológico involucrado. Las complicaciones tempranas incluyen neumotórax, hemotórax, malposición del catéter, arritmias, embolismo aéreo, lesión de estructuras adyacentes, perforación arterial y formación de hematomas. Estas suelen ser detectables mediante monitoreo básico estandarizado -según las recomendaciones de la American Society of Anesthesiologists (ASA)- y exploración ecográfica inmediata del sitio de punción, incluyendo evaluación pulmonar y cardíaca. Las complicaciones tardías comprenden eventos mecánicos como atrapamiento, fractura, desplazamiento o migración del catéter, extravasación de fluidos, infección local y flebitis; así como eventos trombóticos como trombosis venosa profunda, oclusión del lumen, embolismo pulmonar y síndrome de vena cava superior[31],[32].
Una revisión sistemática reciente que incluyó 11 estudios y 2.097 pacientes neonatos y lactantes menores de 12 meses evidenció que el uso de ultrasonido en tiempo real reduce significativamente la incidencia de punción arterial inadvertida, aco- damiento, malposición y dificultades en el avance del catéter, en comparación con técnicas convencionales. Aunque no se observaron diferencias significativas en la aparición de hematomas ni trombosis venosa, complicaciones graves como neumotórax, hemotórax, flebitis y taponamiento cardíaco fueron poco frecuentes. Estos hallazgos respaldan el uso sistemático de la guía ecográfica en la práctica clínica pediátrica para mejorar la seguridad del procedimiento[33].
Para optimizar la detección de complicaciones inmediatas, se ha desarrollado el protocolo estructurado ECHOTIP-Ped, el cual combina la evaluación ecográfica del vaso objetivo, guía dinámica durante la punción, seguimiento del trayecto del catéter y confirmación de la punta en vena cava superior o aurícula derecha. Este enfoque permite verificar en tiempo real la posición del catéter y descartar eventos adversos como malposición, perforación vascular o taponamiento cardíaco, contribuyendo a reducir significativamente las complicaciones mecánicas en neonatos y lactantes[34]. Además, se ha descrito el uso de ecocardiografía funcional con prueba de burbujeo (saline flush test) como método complementario para confirmar la ubicación intracardíaca de la punta del catéter venoso central. Esta técnica consiste en la inyección rápida de solución salina a través del catéter mientras se realiza ecocardiografía transtorácica en vista subcostal o apical de cuatro cámaras. La visualización inmediata de burbujeo en la aurícula derecha (< 2 segundos) indica una posición adecuada en la unión cavoauricular, mientras que una respuesta tardía o ausente sugiere malposición[35].
Entre las complicaciones mecánicas tempranas, el neumotórax destaca por su relevancia clínica, especialmente cuando se accede a venas subclavias o yugulares internas. La ecografía pulmonar, como extensión del protocolo FAST, ha demostrado alta especificidad (98,6%) para su detección, identificando signos como la ausencia de deslizamiento pleural, el punto pulmonar y el patrón de estratosfera en modo M. Sin embargo, su sensibilidad es limitada (45,5%), particularmente en neumotó- rax pequeños o apicales, lo que sugiere la necesidad de técnicas complementarias en casos de alta sospecha clínica[36].
De forma similar, el hemotórax puede ser identificado mediante ecografía torácica, observando líquido anecoico en el espacio pleural con desplazamiento pulmonar. En estudios comparativos con radiografía de tórax, la ecografía mostró una sensibilidad del 33% y una especificidad del 100%, lo que la posiciona como herramienta confirmatoria eficaz, especialmente en entornos pediátricos donde la exposición a radiación debe minimizarse. La incorporación sistemática de la ecografía torácica en el monitoreo postprocedimiento favorece la detección precoz y la toma de decisiones clínicas en tiempo real[37].
-
Conclusiones
La colocación de accesos venosos centrales guiada por ultrasonido en pediatría ha demostrado eficacia al ser una técnica
segura, eficaz y reproducible, especialmente en pacientes con anatomía compleja o alto riesgo vascular.
El uso de ultrasonido permite realizar una adecuada elección del catéter al permitir medir en tiempo real el calibre del vaso, tomar una adecuada orientación en el momento de la punción, lo que ha permitido disminuir el tiempo del procedimiento, el número de complicaciones e incrementar la tasa de éxito.
La aplicación de protocolos estructurados como GAVeCeLT y ECHOTIP-Ped, junto con herramientas como la triangulación y la ecocardiografía funcional, permite estandarizar la práctica clínica y optimizar los resultados.
La ecografía torácica postprocedimiento debe incorporarse sistemáticamente para la detección precoz de complicaciones pulmonares, minimizando la exposición a radiación.
La evidencia actual respalda el uso del ultrasonido como estándar internacional en la colocación de accesos venosos centrales en pediatría, por lo que los profesionales de la salud deberían de adquirir habilidades y destrezas para mejorar la seguridad en la atención de los pacientes.
-
Referencias
1. Demirdjian G, et al. Central venous catheter placement in pediatric patients: definitions and clinical indications. Pediatr Crit Care Med. 2023;24(1):45–52.
2. Montes R, et al. Ultrasonido en la canalización venosa central en neonatos de bajo peso: experiencia en una UCIN. Revista Mexicana de Pediatría. 2016;83(2):78–84.
3. Sociedad Española de Cuidados Intensivos Pediátricos (SECIP). Recomendaciones para el uso de ecografía en accesos vasculares pediátricos. Guía SECIP; 2020.
4. National Institute for Health and Care Excellence (NICE). (2002). Guidance on the use of ultrasound locating devices for placing central venous catheters (Technology Appraisal Guidance No. 49).
5. European Journal of Anaesthesiology (EJA). Ultrasound-guided central venous access in pediatric patients: a procedural framework. Eur J Anaesthesiol. 2020;37(4):312–8.
6. Association for Vascular Access (AVA). Pediatric vascular access: best practices and ultrasound guidance. AVA Clinical Guidelines; 2021.
7. World Congress on Vascular Access (WoCoVA). (2022). Global ultrasound use in pediatric vascular access: consensus statement. WoCoVA Proceedings.
8. Ruano JM. Gutierrez, jose, Accesos Vasculares en pediatria. Tipos de catéteres (III de V partes). Acta Pediatr Mex. 2002;23(3):150–3.
9. Terradillos I. Vías de acceso en nutrición parenteral pediátrica. Nutr Hosp. 2017;34(3 Supl.3):13. https://doi.org/10.20960/nh.1375.
10. Terradillos I. Vías de acceso en nutrición parenteral pediátrica. Nutr Hosp. 2017;34 Supl. 3:13. https://doi.org/10.20960/nh.1375.
11. Álvarez GF. Accesos venosos centrales guiados por ultrasonido: ¿existe evidencia suficiente para justificar su uso de rutina? Rev Med Clin Las Condes. 2011;22(3):361–8. https://doi.org/10.1016/S0716-8640(11)70436-9.
12. Aldrich JE. Basic physics of ultrasound imaging. Crit Care Med. 2007 May;35(5 Suppl):S131–7. https://doi.org/10.1097/01.CCM.0000260624.99430.22 PMID:17446771
13. Imadine. (2023). Tipos de transductor de ultrasonido para diagnóstico. https://imadine.com.mx/tipos-de-transductor-de-ultrasonido/
14. Salud P. (2022). Los tipos de transductores y cuándo se utilizan. https://pulsosaludyecografia.com/los-tipos-de-transductores/
15. Shriki J. Ultrasound physics. Crit Care Clin. 2014 Jan;30(1):1–24. https://doi.org/10.1016/j.ccc.2013.08.004 PMID:24295839
16. Troianos CA, Hartman GS, Glas KE, et al. Guidelines for performing ultrasoundguided vascular cannulation. J Am Soc Echocardiogr. 2012;25(11):1238–46.
17. Remerand F, et al. Ultrasound-guided catheterization of the internal jugular vein: anatomic considerations and practical implications. Anesth Analg. 2010;110:1756–63.
18. Rando K, Pratt JP, Castelli J. Cateterización venosa central guiada por ecografía: estudio randomizado controlado. Anest Analg Reanim. 2013;26(1):15–22.
19. Munshey F, Parra DA, McDonnell C, Matava C. Ultrasound-guided techniques for peripheral intravenous placement in children with difficult venous access. Paediatr Anaesth. 2020 Feb;30(2):108–15. https://doi.org/10.1111/pan.13780 PMID:31808244
20. Oulego I, Ferrer A, Gil J. Procedimientos ecoguiados. Sociedad Española de Cuidados Intensivos Pediátricos; 2019.
21. Takeshita J, Yamamoto T, Kinoshita Y. Ultrasound-guided central venous catheter placement in pediatric patients: technical considerations and anatomical correlations. Pediatr Crit Care Med. 2022;23(4):345–52. https://doi.org/10.1097/PCC.0000000000002891.
22. Liu Y, Chen J, Wang H. Optimizing ultrasound-guided vascular access: comparative analysis of imaging planes. J Vasc Access. 2018;19(6):567–73. https://doi.org/10.1177/1129729818784567.
23. López González J, López Prats JL, Murillo Pozo MÁ, Moyano Leiva O, Slöcker Barrio M, Gómez Luque JM, et al. Canalización vascular ecoguiada en Pediatría. Protoc diagn ter pediatr, 1, 379–392. Recuperado de Asociación Española de Pediatría; 2021.
24. Pittiruti M, et al. (2022). GAVeCeLT Clinical Recommendations on Central Venous Access in Pediatrics.
25. Thomas and Moore. The Vanishing Target Sign: Confirmation of Intraluminal Needle Position for Ultrasound Guided Vascular Access. Society for Academic Emergency Medicine; 2013.
26. Blaivas y cols. . D Ultrasound Line Placement, Acad Emerg Med D December 2003, Vol. 10, No. 12.
27. Sanches M, Coelho A, Oliveira E, Lopes A. Electrocardiograma en edad pediátrica. Semergen. 2014 Sep;40(6):334–40. https://doi.org/10.1016/j.semerg.2013.10.007 PMID:24907888
28. Escribà i Alepuz P. (2022). Canalización venosa central ecoguiada en neonatos y pacientes pediátricos. Campus Vygon. Recuperado de https://campusvygon.com/wp-content/uploads/2022/05/Apuntes-canalizacionvenosa-central-ecoguiada-en-pediatria.pdf
29. Giraldo Gutiérrez DS, Bautista Sánchez J, Reyes Patiño RD. Acceso central subclavio por vía supraclavicular en anestesia pediátrica: el renacer de una técnica antigua con la ayuda del ultrasonido. Rev Esp Anestesiol Reanim (Engl Ed). 2019 May;66(5):267–76. https://doi.org/10.1016/j.redar.2019.01.001 PMID:30718017
30. López González, J., López Prats, J. L., Murillo Pozo, M. Á., Moyano Leiva, O., Slöcker Barrio, M., Gómez Luque, J. M., et al. (2021). Canalización vascular ecoguiada en Pediatría. Protoc diagn ter pediatr, 1, 379–392.
31. Durán-Briones G. (2010). Angioaccesos guiados por ultrasonido de alta resolución en el paciente oncológico. Deleted Journal, 33, 150-155. https://www.medigraphic.com/pdfs/rma/cma-2010/cmas101al.pdf
32. Naik VM, Mantha SS, Rayani BK. Vascular access in children. Indian J Anaesth. 2019 Sep;63(9):737–45. https://doi.org/10.4103/ija.IJA_489_19 PMID:31571687
33. Cui Y, Wang Y, Gong T, Huang Q, Zhang QQ. Systematic review of ultrasound-guided central venous catheter placement-related complications in neonates and infants aged https://doi.org/10.1177/03000605241287168 PMID:39422062
34. Zito Marinosci G, Biasucci DG, Barone G, D’Andrea V, Elisei D, Iacobone E, et al. ECHOTIP-Ped: A structured protocol for ultrasound-based tip navigation and tip location during placement of central venous access devices in pediatric patients. J Vasc Access. 2023 Jan;24(1):5–13. https://doi.org/10.1177/11297298211031391 PMID:34256613
35. Ramos Casado A, Granados Ruiz R, Menéndez Suso MJ. (2018). Ecocardiografía funcional en el paciente pediátrico crítico. Sociedad Española de Cuidados Intensivos Pediátricos (SECIP). https://www.secip.com/images/uploads/2018/09/3-ECOCARDIOGRAFÍA-BÁSICA-Y-AVANZADA.pdf
36. Vasquez DG, Berg GM, Srour SG, Ali K. Lung ultrasound for detecting pneumothorax in injured children: preliminary experience at a community-based Level II pediatric trauma center. Pediatr Radiol. 2020 Mar;50(3):329–37. https://doi.org/10.1007/s00247-019-04509-y PMID:31473787
37. Oliveira L, Pilz L, Tognolo CM, Bischoff C, Becker KA, Oliveira GG, et al. Comparison between ultrasonography and X-ray as evaluation methods of central venous catheter positioning and their complications in pediatrics. Pediatr Surg Int. 2020 May;36(5):563–8. https://doi.org/10.1007/s00383-020-04642-y PMID:32232550

 ORCID
ORCID