Edgardo Banille1*, Alfredo Carlos Rodríguez-Portelles2, Ricardo Ledesma3, Javier Ponce4, Cecilia Traferri5, Carlos Maure6
Recibido: 30-05-2023
Aceptado: 10-06-2023
©2025 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 54 Núm. 5 pp. 756-762|https://doi.org/10.25237/revchilanestv54n5-39
PDF|ePub|RIS
Expanded VExUS score in hemodynamic monitoring of neonatal sepsis
Abstract
A 23-day-old patient is presented, admitted for severe respiratory distress caused by respiratory syncytial virus infection. Its evolution is unfavorable, it is complicated by pneumonia, pyopneumothorax and septic shock with biventricular cardiac dysfunction and moderate pulmonary hypertension and kidney failure. He requires high-frequency ventilation, pleural drainage, and inotropic infusion. Biomonitoring and pulsed Doppler of the abdominal venous vessels (inferior vena cava, portal vein, renal vessels) and the right common femoral vein are performed. Spectral Doppler profiles are analyzed at admission and after treatment. The objective was to describe the usefulness of a diagnostic tool (VExUS score) in the context of neonatal septic shock to evaluate the evolution and guide treatment.
Resumen
Se presenta un paciente de 23 días de nacido, que ingresa por dificultad respiratoria severa secundaria a infección por virus respiratorio sincitial. Su evolución es desfavorable, se complica con neumonía, pioneumotórax y shock séptico con disfunción cardíaca biventricular e hipertensión pulmonar moderada e insuficiencia renal. Requiere ventilación de alta frecuencia, drenaje pleural e infusión de inotrópicos. Se realiza biomonitorización y Doppler pulsado de los vasos venosos abdominales (vena cava inferior, vena porta, vasos renales) y vena femoral común derecha. Los perfiles de Doppler espectral se analizan al ingreso y después del tratamiento. El objetivo fue describir la utilidad de una herramienta diagnóstica (puntaje VExUS) en el contexto del shock séptico neonatal para evaluar la evolución y orientar el tratamiento.
Introducción
En los últimos años se ha popularizado la aplicación de la escala de puntuación de ultrasonido de exceso venoso (venous excess ultrasound = VexUS), por sus siglas en inglés en pacientes adultos para evaluar la sobrecarga de líquidos en estados de insuficiencia cardíaca de diferente etiología, preferentemente en escenarios post-cirugía cardiovascular[1]-[3].
El análisis Doppler de la vena porta, la vena hepática y la vena venosa intrarrenal se utiliza en el sistema de clasificación VExUS. En presencia de una vena cava inferior sin colapso, cada una de estas venas se evalúa y se asigna a congestión normal, leve o grave[2] (Figura 1).
Para entender la sobrecarga de líquidos, es necesario recordar el concepto de la llamada “presión media de llenado sistémico” (PMS), que representa la presión dentro del sistema circulatorio cuando se detiene la circulación, y su valor se estima en 8 mmHg. La “presión de perfusión”, (presión que impulsa la sangre hacia el corazón), depende del gradiente entre la PMS y la presión de la aurícula derecha (PAD) o presión venosa central (PVC). Si la presión venosa central está elevada, estos gradientes disminuyen y la presión de perfusión de los órganos abdominales se altera[1]-[3].
La congestión venosa central, generalmente causada por insuficiencia ventricular derecha, disminuye la distensibilidad de la pared venosa, aumenta la transmisión de presión y aumenta la pulsatilidad en las venas distales[1]-[4].
Presentamos un caso de un recién nacido séptico con compromiso hemodinámico en el que se utilizó el puntaje VExUS extendido con evaluación Doppler de la vena femoral común como expresión del impacto de la insuficiencia cardíaca retrógrada. Esta ventana se presenta como una opción atractiva para la evaluación cardiovascular en pacientes críticos[5].
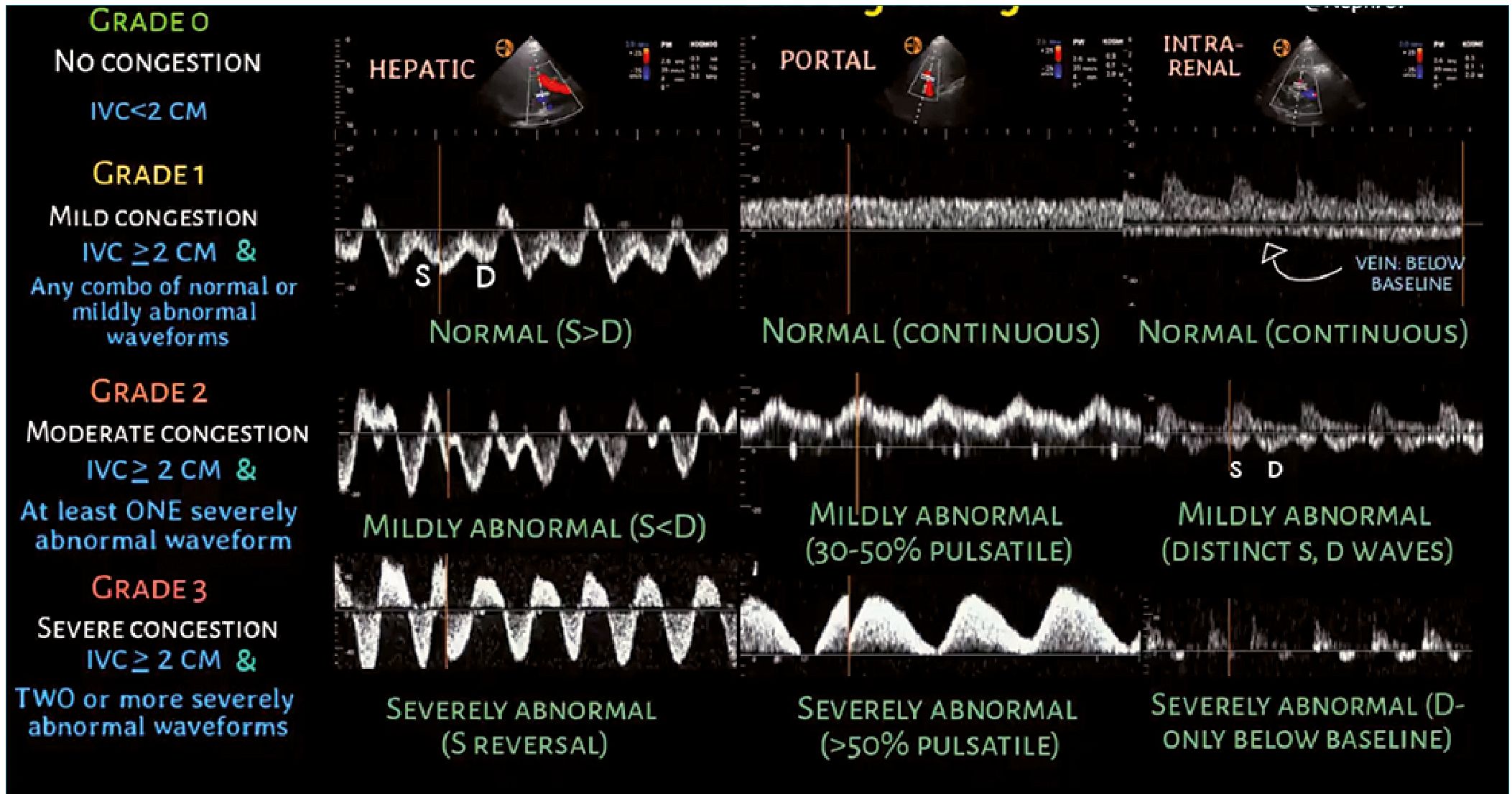
Figura 1. Sistema de puntuación VExUS para la determinación ecográfica de la congestión venosa. Tomado de Koratala A. VExUS flash cards [Internet]. NephroPOCUS. 2021 [citado 17 de febrero de 2023]. Disponible en: https://nephropocus.com/2021/10/05/vexus-flash-cards/. Con permiso del autor.
Caso clínico
Paciente de 23 días de edad, recién nacido a término (39 semanas), peso adecuado para la edad gestacional (3.370 gramos), que ingresa por dificultad respiratoria severa. Al ingreso se indicó policultivo, antibioticoterapia y radiografía de tórax. A las 12 h se decidió intubación electiva e infusión de dopamina por taquipnea y persistencia de mala dinámica respiratoria e inestabilidad hemodinámica.
La evolución clínica es desfavorable con neumonía y pioneu- motórax izquierdo que requiere drenaje quirúrgico y ventilación mecánica de alta frecuencia oscilatoria (VAFO). El biomonitoreo reveló hipoxemia e hipercapnia, lactatos séricos elevados y valores de urea y creatinina. A las 24 h, el resultado del cultivo de secreciones bronquiales fue positivo para virus sincitial respiratorio.
Al 4° día se observó radiografía de tórax y ecografía con opacidad del campo pulmonar izquierdo y presencia de neumotórax, por lo que se decidió cambio de estrategia ventilatoria. Se decidió rotar antibioterapia a vancomicina. y meropenem. El informe de cultivo de líquido pleural fue positivo para Staphilococcus aureus, se suspende meropenem.
Utilizando un ecógrafo Logic Q con transductor sectorial, se realiza un ecocardiograma que muestra dilatación global de las cavidades con disfunción sistólica del ventrículo izquierdo (VI): Fracción de acortamiento del ventrículo izquierdo (FAVI) 25% y disfunción del ventrículo derecho (VD): con desplazamiento sistólico del plano del anillo tricúspideo (TAPSE, por sus siglas en ingles) en 7 mm e insuficiencia tricúspidea, se estimó la presión sistólica arterial pulmonar (PASP ): 60 mmHg, con estos hallazgos, se indicó adrenalina: 0,1 mcg/kg/m (mcg/kg/m), milrino- na: 0,3 mcg/kg/m2 y sildenafil. Se suspende la dopamina. Con transductor lineal se evaluaron los vasos abdominales desde la vista subcostal, mostrando un diámetro del eje corto de la vena cava inferior (VCI): 8 mm (sin colapso) con relación a la aorta abdominal: 4 mm, en el análisis de las venas suprahepática, porta y renal. se calcula una puntuación VExUS: 2 (Figura 2 A- B-C). Se realizó evaluación doppler de la vena femoral común (VFC) izquierda, observándose alteración de su patrón normal (Figura 2D)
Al 7° día: el ecocardiograma muestra: dilatación de cavidades derechas con disfunción VD: TAPSE 7 mm, hipertensión pulmonar leve, PASP: 40 mmHg. El VI no está dilatado y con función sistólica normal. FAVI: 31%, se suspende soporte ino- trópico. Derrame pericárdico leve de 5 mm. Persiste, aunque en menor grado, la alteración del flujo de las venas abdominales y femorales secundaria a la disfunción del VD (Figura 3 A-B-C-D).
Al día 14 de hospitalización se realizó control con ecocardiograma y de vasos abdominales con resultado normal. Se retira tubo de drenaje pleural, continuando antibióticos hasta 21 días con alta hospitalaria.
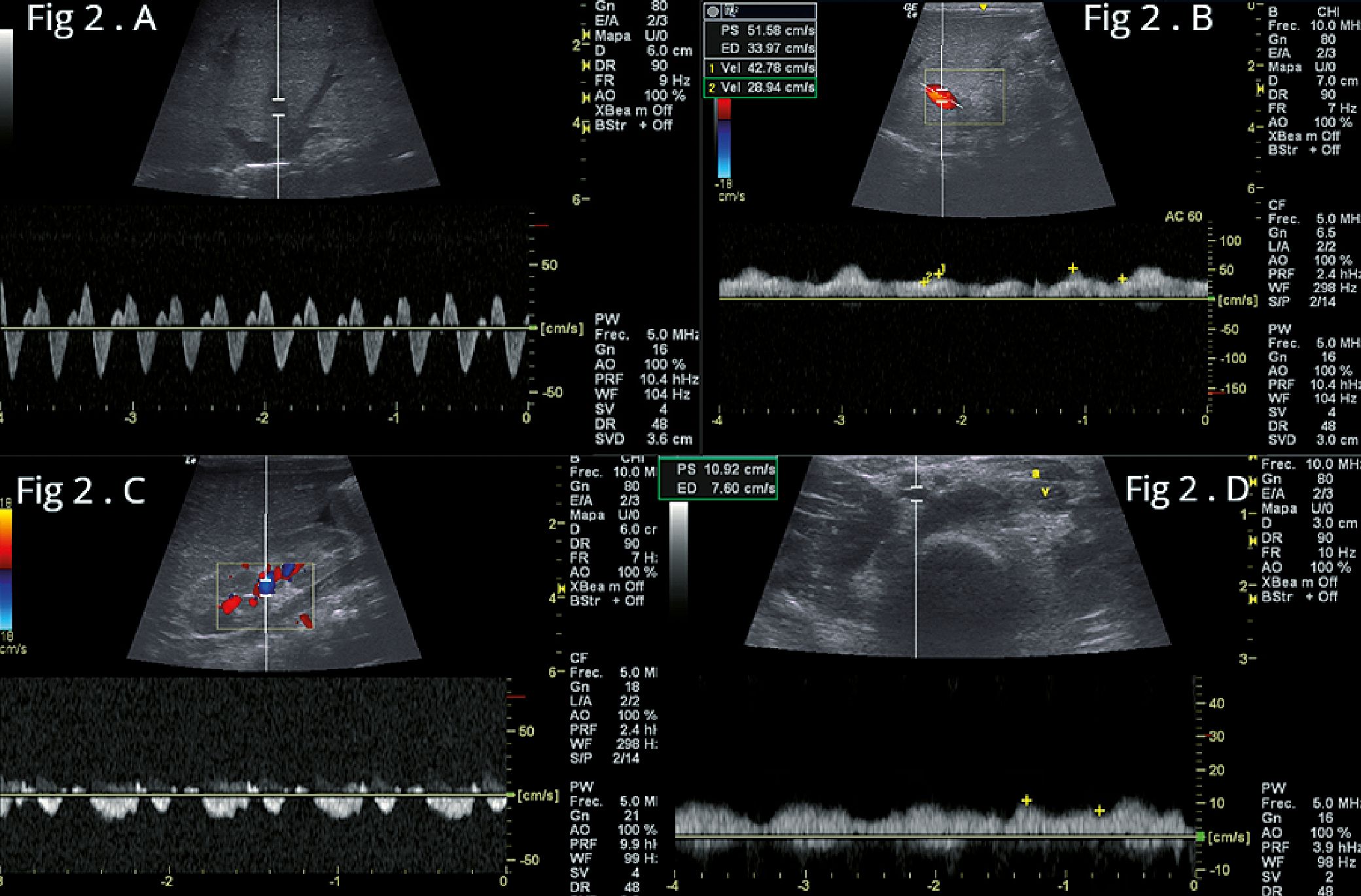
Figuras 2. Flujos venosos antes de iniciar el tratamiento. A: flujo de vena suprahepática, presencia de onda D mayor qué onda S y onda A retrógrada; B: flujo de la vena porta, flujo pulsátil con índice de pulsatilidad (IP) > 30%. (VExUS 2); C: Flujo de vena y arteria renal, flujo bifásico sistodiastólico (VExUS 2), índice de resistencia renal (IRR): 0,82; D: vena femoral común izquierda, onda pulsátil bifásica.
Discusión
Presentamos un paciente que, en el contexto clínico de shock séptico, presenta disfunción biventricular con hipertensión pulmonar e insuficiencia cardíaca retrógrada, evidenciada por nuevos métodos de monitorización (puntuación VExUS)
para evaluar principalmente sobrecarga hídrica e insuficiencia cardiaca derecha caracterizada por elevación de la presión venosa central (PVC)[1]-[4].
En pacientes pediátricos existen escasas publicaciones de la aplicación del score VexUS, Menéndez Suso et al.[6], analizó la factibilidad y utilidad de la puntuación VExUS para detectar y calificar la elevación de la presión venosa central (PVC) en pacientes pediátricos críticamente enfermos. Banille et al.[7],[8], muestran su utilidad en casos clínicos en una paciente adolescente con enfermedad de Ebstein e insuficiencia renal y en un paciente neonato con ductus permeable y shock cardiogénico.
En ecografía crítica, el tamaño y colapsibilidad de la vena cava inferior se considera un sustituto de la presión de la aurícula derecha debido a que se considera una prolongación anatómica de la misma, y la alteración en su flujo es mucho más temprana que la aparición de signos clínicos de líquido, sobrecarga como crepitantes o edema periférico[1].
En nuestra experiencia para realizar el score VExUS medimos el diámetro transversal y longitudinal de la vena cava inferior antes de la emergencia de las venas suprahepáticas, y son evaluados los pacientes que no presentan colapso de esta[9].
Hay que tener en cuenta que en pacientes pediátricos existe gran variabilidad del tamaño de la vena cava inferior, tanto etáreas como interindividuales y otros factores confundidores.
Di Nicolo et al., describen las influencias de la presión intratorácica (asistencia respiratoria mecánica, asma bronquial esfuerzo inspiratorios, derrame pleural, neumotórax), de la presión intraabdominal, (peritonitis, ascitis, síndrome compartimental, embarazo, masas), y cardíacas ya sea intracardíacas (disfunción crónica del ventrículo derecho, infarto de miocardio, hipervolemia, efecto de Bermheim inverso en caso de hipertensión pulmonar o malformación de Ebstein), o extracardíacas como derrame pericárdico de cualquier etiología[10].
Desde el plano subcostal se explora la vena cava inferior, que normalmente presenta un flujo bifásico (inspiratorio/espiratorio) con colapso inspiratorio durante la respiración normal[1]-[3].
El flujo de las venas suprahepáticas analizado desde el plano subcostal es de morfología trifásica: una primera onda sistólica (S) anterógrada (hacia el corazón, por debajo de la línea base), que refleja la caída de presión en la aurícula derecha provocada por la relajación auricular y el descenso del anillo tricúspideo hacia el ápex durante la sístole ventricular (corresponde a la onda V de la curva de PVC), la segunda onda diastólica (D) que también muestra una dirección anterógrada, con menor amplitud que la onda S y refleja la caída de presión en el lado derecho atrio causado por la apertura de la válvula tricúspide y por el llenado ventricular diastólico temprano (corresponde al colapso Y de la onda de PVC) y una tercera onda (A) que corresponde a la contracción auricular (onda A de PVC), que excede la presión de la vena cava inferior y muestra una dirección retrógrada hacia las venas hepáticas (por encima de la línea de base)[1]-[3].
El flujo normal de la vena porta es monofásico con una leve ondulación y un índice de pulsatilidad < 30%, y el flujo normal de la vena renal es monofásico continuo[1].
Cuando aumenta el volumen estresado o la presión en la aurícula derecha se produce insuficiencia tricúspidea, la transmisión retrógrada del flujo sistólico que proviene del ventrículo derecho modifica los patrones de flujo Doppler con inversión del flujo en venas suprahepáticas (predominio diastólico y exageración de la onda A), aumento de la pulsatilidad en la vena porta y aparición de una onda diastólica en las venas renales[1],[3],[4].
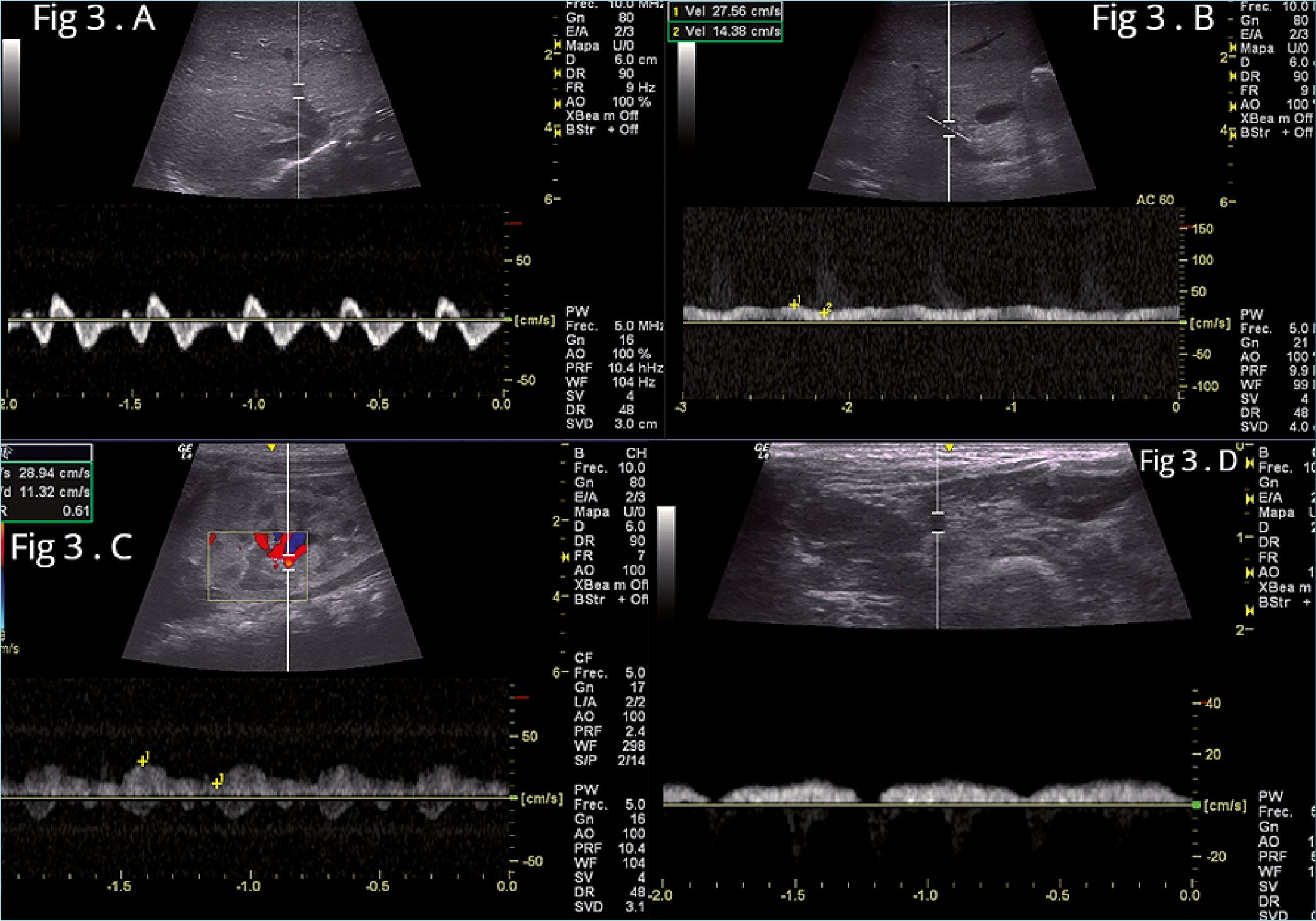
Figura 3. Flujos venosos después de 7 días de tratamiento. A: Flujo de la vena suprahepática, Trifásica con onda S > D y onda A persiste acentuada; B: Flujo de la vena porta, Pulsatilidad inferior: IP < 30%; C: Venas y arteria renal, vena renal pulsátil bifásica IRR: 0,61; D: Flujo de la vena femoral común, vena femoral con pulsatilidad disminuida.
En el análisis de los vasos abdominales de nuestro paciente se evidencia, En primer lugar, su Doppler de vena hepática mostró D onda S más larga (Figura 2A), su Doppler de vena porta mostró un índice de pulsatilidad superior al 30% (Figura 2B) y su Doppler venoso intrarrenal mostró un patrón de flujo bifásico (sistólico-diastólico) (Figura 2C). Los tres hallazgos de Doppler, en conjunto, argumentan fuertemente a favor de un estado congestivo venoso moderado (al menos de 2 de 3 sistemas venosos con congestión moderada producen una puntuación VExUS de 2).
La base de la insonación de la vena femoral común (VFC) radica en establecer si la insuficiencia del ventrículo derecho afecta también a los territorios venosos distales[5]. Nuestro paciente presentó disfunción biventricular con hipertensión pulmonar moderada y compromiso moderado del flujo venoso abdominal, (VExUS puntuación 2).
Para la detección de congestión venosa, el Doppler de la VFC tiene una alta sensibilidad y una concordancia moderada con la clasificación VExUS en adultos. Y podría ser un método sencillo y útil para determinar la congestión venosa en neonatos y pacientes pediátricos. Se recomienda la medición de Doppler de VFC mientras el paciente está en decúbito supino, lo que puede no ser posible en pacientes en ortopnea. El posible beneficio de la VFC es que puede no verse afectado por el debate sobre la visualización de la VCI (eje corto frente a largo), además de tener una accesibilidad anatómica más simple y una curva de aprendizaje más rápida[11].
El análisis de estos flujos permite obtener información inmediata sobre la severidad del compromiso hemodinámico, así como el compromiso de la perfusión de órganos, que, según la acepción actual, no depende sólo de la presión y el flujo anterógrado, sino también de una presión venosa central baja[1]-[3].
En la evolución notamos la mejoría de los patrones espectrales inicialmente en los territorios venosos más distales, pero la normalización de todos los flujos solo fue evidente a las 2 semanas.
Conclusiones
El puntaje VExUS, nos permite evaluar la sobrecarga hídrica de manera temprana, lo cual permite indicar restricción de líquidos, diuréticos o técnicas de reemplazo renal de manera precoz. El score VExUS debe incluirse en el manejo hemodinámico sistemático de los pacientes críticos, como una herramienta fundamental de su manejo hemodinámico. El score VExUS extendido con insonación de la vena femoral común es un método aplicable en la evaluación del shock cardiogénico de diferentes etiologías y nos permite evaluar la evolución del tratamiento indicado. El complemento de evaluación POCUS permite un abordaje holístico de este escenario clínico.
Cuestiones no resueltas
Todavía no hay suficientes publicaciones de series pediátricas, donde se pueda evaluar los efectos de la asistencia respiratoria mecánica. También deben unificarse los criterios de inclusión de pacientes para evaluar VExUs pediátrico porque existen múltiples factores confundidores.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
Referencias
1. Koratala A, Kazory A. Point of Care Ultrasonography for Objective Assessment of Heart Failure: Integration of Cardiac, Vascular, and Extravascular Determinants of Volume Status. Cardiorenal Medicine [Internet]. 21 de enero de 2021 [citado 2 de enero de 2023];11(1):5-17. Disponible en: https://doi.org/10.1159/000510732.
2. Rola P, Miralles-Aguiar F, Argaiz E, Beaubien-Souligny W, Haycock K, Karimov T, et al. Clinical applications of the venous excess ultrasound (VExUS) score: conceptual review and case series. The Ultrasound Journal [Internet]. 19 de junio de 2021 [citado 4 de enero de 2023];13(1):32. Disponible en: https://doi.org/10.1186/s13089-021-00232-8.
3. Beaubien-Souligny W, Rola P, Haycock K, Bouchard J, Lamarche Y, Spiegel R, et al. Quantifying systemic congestion with Point-Of-Care ultrasound: development of the venous excess ultrasound grading system. The Ultrasound Journal [Internet]. 9 de abril de 2020 [citado 2 de enero de 2023];12(1):16. Disponible en: https://doi.org/10.1186/s13089-020-00163-w.
4. Argaiz ER. VExUS Nexus: Bedside Assessment of Venous Congestion. Advances in Chronic Kidney Disease [Internet]. 1 de mayo de 2021 [citado 2 de enero de 2023];28(3):252-61. Disponible en: https://doi.org/10.1053/j.ackd.2021.03.004.
5. Denault AY, Aldred MP, Hammoud A, Zeng YH, Beaubien-Souligny W, Couture EJ, et al. Doppler Interrogation of the Femoral Vein in the Critically Ill Patient: The Fastest Potential Acoustic Window to Diagnose Right Ventricular Dysfunction? Critical Care Explorations [Internet]. octubre de 2020 [citado 2 de enero de 2023];2(10):e0209. Disponible en: https://doi.org/10.1097/CCE.0000000000000209.
6. Menéndez-Suso JJ, Rodríguez-Álvarez D, Sánchez-Martín M. Feasibility and Utility of the Venous Excess Ultrasound Score to Detect and Grade Central Venous Pressure Elevation in Critically Ill Children. Journal of Ultrasound in Medicine [Internet]. 2023 [citado 1 de enero de 2023];42(1):211-20. Disponible en: https://doi.org/10.1002/jum.16057.
7. Banille E, Haycock K, Iriarte M, Peirone A, Contreras A, Muñoz F, et al. Usefulness of VExUS in a pediatric patient with Ebstein’s anomaly. Rev chil anest [Internet]. 2022 [citado 1 de enero de 2023];51(2):221-4. Disponible en: https://doi.org/10.25237/revchilanestv5109021632.
8. Banille E, Ledesma R, Rosso C, Espósito M, Traferi C, Fernández C, et al. Ecografía Doppler de vasos abdominales. Nuevo paradigma de monitoreo en inestabilidad hemodinámica. Rev chil anest [Internet]. 2021 [citado 2 de enero de 2023];50(6):890-3. Disponible en: https://doi.org/10.25237/revchilanestv5007101025.
9. Kathuria N, Ng L, Saul T, Lewiss RE. The Baseline Diameter of the Inferior Vena Cava Measured by Sonography Increases With Age in Normovolemic Children. Journal of Ultrasound in Medicine [Internet]. 2015 [citado 27 de diciembre de 2022];34(6):1091-6. Disponible en: https://doi.org/10.7863/ultra.34.6.1091.
10. Di Nicolò P, Tavazzi G, Nannoni L, Corradi F. Inferior Vena Cava Ultrasonography for Volume Status Evaluation: An Intriguing Promise Never Fulfilled. Journal of Clinical Medicine [Internet]. enero de 2023 [citado 25 de abril de 2023];12(6):2217. Disponible en: https://doi.org/10.3390/jcm12062217.
11. Bhardwaj V, Rola P, Denault A, Vikneswaran G, Spiegel R. Femoral vein pulsatility: a simple tool for venous congestion assessment. The Ultrasound Journal [Internet]. 10 de mayo de 2023 [citado 17 de mayo de 2023];15(1):24. Disponible en: https://doi.org/10.1186/s13089-023-00321-w.
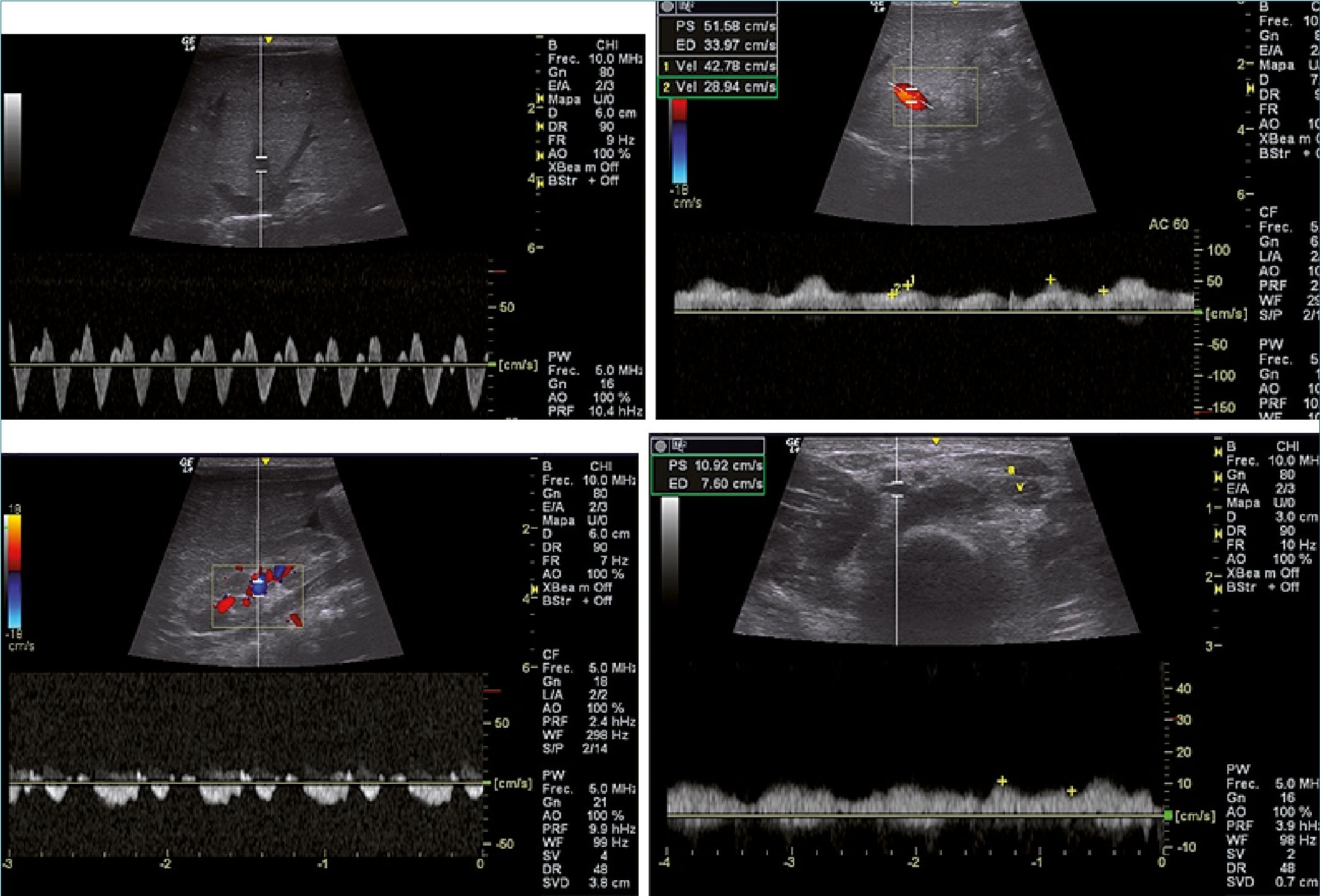
Figuras 2 y 3 descompuestas en imágenes.
Figura 2. 4 imágenes (en el siguiente orden).
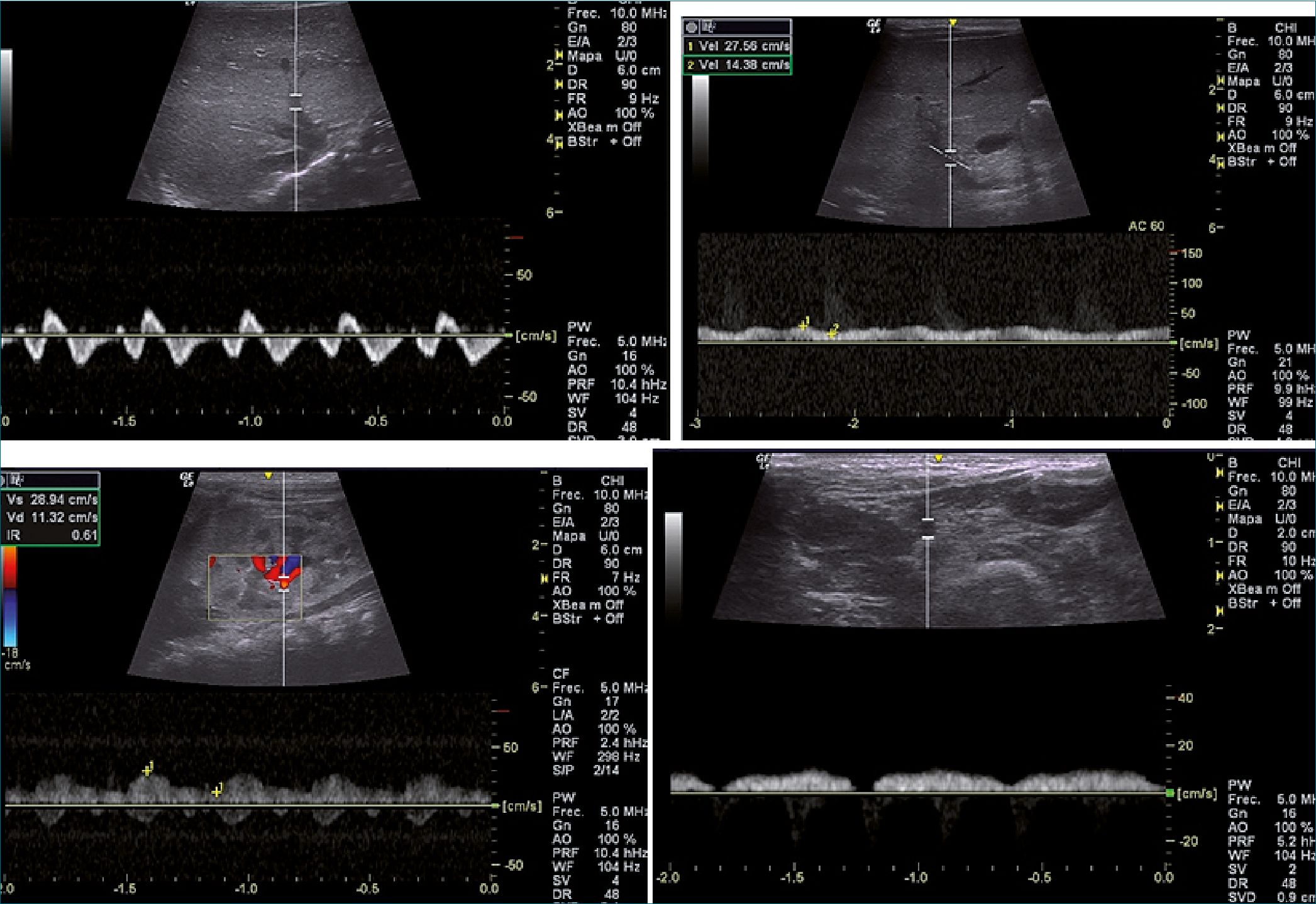
Figura 3. 4 imágenes (en el siguiente orden).

 ORCID
ORCID