Eliana Viroga1, Juan Martino2, Gonzalo Irizaga3*
Recibido: 03-10-2023
Aceptado: 05-01-2025
©2025 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 54 Núm. 6 pp. 948-951|https://doi.org/10.25237/revchilanestv54n6-23
PDF|ePub|RIS
Anesthetic management of a patient with hereditary angioedema
Abstract
Hereditary angioedema (HAE) is a rare group of autosomal dominant genetic disorders resulting from mutations in the C1 esterase inhibitor (C1-INH) gene. It is characterized by recurrent, transient episodes of angioedema in the subcutaneous and submucosal tissues. Knowledge of this pathology and its implications in the perioperative period is important, given the risk of a severe asphyxiating episode due to upper airway edema, which is unpredictable. Risk factors for angioedema episodes have been described, including trauma, surgical stress, psychological stress, acute illnesses, and cold exposure, among others. We present a clinical case of a 24-year-old patient with hereditary angioedema (HAE) scheduled for right inguinal hernioplasty. We analyzed the perioperative management, anesthetic technique, and intra- and postoperative care. It is concluded that the fundamental pillar in the management of these patients is early diagnosis, prevention, and effective treatment to minimize the risk of angioedema and reduce morbidity and mortality. A multidisciplinary team approach and careful perioperative preparation-including treatment of triggering factors, prophylactic therapy, and appropriate follow-up-are essential to reduce perioperative risks.
Resumen
El angioedema hereditario (AEH) es un grupo poco común de enfermedades genéticas autosómicas dominante que resulta de mutaciones en el gen inhibidor de la esterasa C1 (C1-INH). Se caracteriza por episodios recurrentes y transitorios de angioedemas de los tejidos subcutáneos y submucosos. Es importante el conocimiento de esta patología, y su implicancia en el perioperatorio, dado el riesgo de tener un episodio grave asfíctico por edema de la vía aérea superior, siendo esta impredecible. Se han descrito factores de riesgo para episodios de angioedema como: el trauma, el estrés quirúrgico, el estrés psicológico, enfermedades agudas, exposición al frío entre otros. Se presenta un caso clínico de un paciente de 24 años, coordinado para cirugía de hernioplastia inguinal derecha, portador de angioedema hereditario (AEH). Analizamos el manejo perioperatorio, técnica anestésica, cuidados para intra y posoperatorio. Se concluye que el pilar fundamental en el manejo de estos pacientes es el diagnóstico precoz, la prevención y tratamiento eficaz para minimizar el riesgo de angioedema y disminuir la morbilidad y mortalidad. Es fundamental el abordaje con equipo multidisciplinario, una preparación cuidadosa perioperatoria, que incluye tratamiento de los factores desencadenantes, tratamiento profiláctico y adecuado seguimiento, para disminuir los riesgos perioperatorios.
-
Introducción
El angioedema hereditario es una afección potencialmente mortal debido al riesgo de compromiso de las vías respiratorias durante el período perioperatorio. Es una enfermedad genética autosómica dominante que resulta de una anomalía bioquímica en los niveles o la funcionalidad de inhibidor plasmático de la esterasa del primer componente del complemento (C1 INH). Se clasifica en dos variantes fenotípicas: El tipo I por niveles plasmáticos reducidos de C1-INH funcionando normalmente; el tipo II se caracteriza por la presencia de valores plasmáticos normales o elevados de una proteína C1-INH que no funciona o funciona anormalmente[1],[10],[16].
C1-INH regula varias proteínas de los sistemas del complemento, de contacto, de coagulación y de la fibrinólisis. La activación del sistema de contacto lleva un aumento en la producción de bradicinina que va a generar aumento de la permeabilidad vascular de los capilares y las vénulas poscapilares, produciendo edema localizado[1]-[16].
Los síntomas se caracterizan por presentar episodios transitorios de edema que pueden durar varios días 3-5 días (al menos 12-24 h, nunca menos). Se caracterizan por edema episódico de la piel y la mucosa del tracto gastrointestinal y del sistema respiratorio como resultado del aumento de la permeabilidad vascular de los capilares y las vénulas poscapilares mediado por bradicinina. El edema laríngeo es poco frecuente pero es la complicación más temida, pudiendo causar una obstrucción completa de la vía respiratoria, que puede llevar a la muerte por asfixia. Estos pacientes tienen un riesgo estimado de mortalidad por edema laríngeo del 25% al 40%[1],[3],[8],[16].
Hay varios factores de riesgo descritos como desencadenantes: el trauma, el estrés quirúrgico, el estrés psicológico, enfermedades agudas, exposición al frío, entre otros, siendo el período perioperatorio un momento crítico en estos pacientes con mayor riesgo que pueda desencadenar una crisis de angioedema.
Resulta de gran relevancia un plan de manejo anestésico seguro y la colaboración de múltiples especialidades. Es importante tener en cuenta que este tipo de angioedema no responde al tratamiento habitual con epinefrina, antihistamínicos y corticosteroides[2],[3],[8],[16] y debemos considerar que cualquier paciente presenta este riesgo, aunque lleve varios meses asintomático (e incluso años)[2],[4],[16].
Actualmente, no existen directrices universales sobre el tratamiento perioperatorio, sin embargo, varios estudios han informado resultados exitosos para reducir el riesgo de angioedema, evitar la intubación si es posible, la manipulación de la vía aérea, evitar y tratar desencadenantes como el estrés psicológico, evitar la exposición al frío y realizar el tratamiento farmacológico basado en 3 pilares: tratamiento de los ataques de angioedema agudo (tratamiento a demanda), a corto plazo (pre procedimiento) y profilaxis a largo plazo[1],[7],[8],[16].
-
Descripción del caso
Se presenta un caso clínico de un paciente de sexo masculino de 24 años de edad, coordinado para hernioplastia inguinal derecha, portador de angioedema hereditario tipo 1 diagnosticado hace 4 años, en tratamiento con danazol 100 mg al día. Desde los 10 años presenta síntomas episódicos de edema en zonas acras y dolores abdominales cólicos inespecíficos. Presentó como complicación grave episodio de edema de laringe que requirió intubación orotraqueal e ingreso a cuidados intensivos, con remisión del mismo tras recibir tratamiento específico con plasma fresco congelado y danazol. Destacándose como probable desencadenante la suspensión del tratamiento. Previo a dicho evento evidenció angioedema a nivel mucosa oral (Figura 1).
Al momento de la consulta el paciente se encontraba asintomático. Sin evidencia en examen físico de edemas ni lesiones en piel.
En cuanto a la vía aérea no presenta predictores de ventilación ni intubación difícil.
Examen cardiovascular y pleuropulmonar normal.
Paraclínica preoperatorio hemograma, crasis, ionograma función renal y hepática normal.
Se valoró al paciente con equipo multidisciplinario anestesistas, cirujanos, hematología y dermatología, que de forma conjunta se definió previo al procedimiento:
– 5 días antes se aumentó dosis de danazol a 600 mg día.
– 24 h antes se administró ácido tranexámico 75 mg/kg.
– 12 h antes se administró 1 unidad de plasma fresco y otra en preoperatorio inmediato.
El objetivo fundamental en el perioperatorio fue evitar o atenuar los factores de riesgo para desencadenar angioedema. Se realizó premedicación con benzodiazepinas para disminuir la ansiedad. La temperatura de block quirúrgico se mantuvo a 23°C, se utilizaron sueros calientes y calefactor de aire forzado. Para el intraoperatorio se tuvo disponibilidad de plasma descongelado para administrar ante una eventual crisis. Dispusimos de materiales para el manejo de vía aérea difícil.
Se realizó monitorización estándar ASA, con electrocardiografía, presión arterial no invasiva, pulsioximetría y capnografía.
La técnica anestésica elegida fue una anestesia raquídea a nivel del interespacio L3-L4, aguja 25G punta de lápiz, con bupivacaína isobárica 12 mg y fentanil 0,02 mg. Se realizó sedación con propofol y se administró oxigenoterapia 6 L/min con máscara de flujo libre.
No presentó ninguna complicación en el intraoperatorio. Permaneció en toda la intervención con hemodinamia estable, sin necesidad de uso de vasopresores. No se evidenció ningún episodio de edema, ni se requirió instrumentación de la vía aérea.
Se optó por una analgesia multimodal balanceada, se realizó bloqueo TAP derecho ecoguiado con bupivacaína 0,125% 20 ml, y por vía sistémica se administró paracetamol, dipirona.
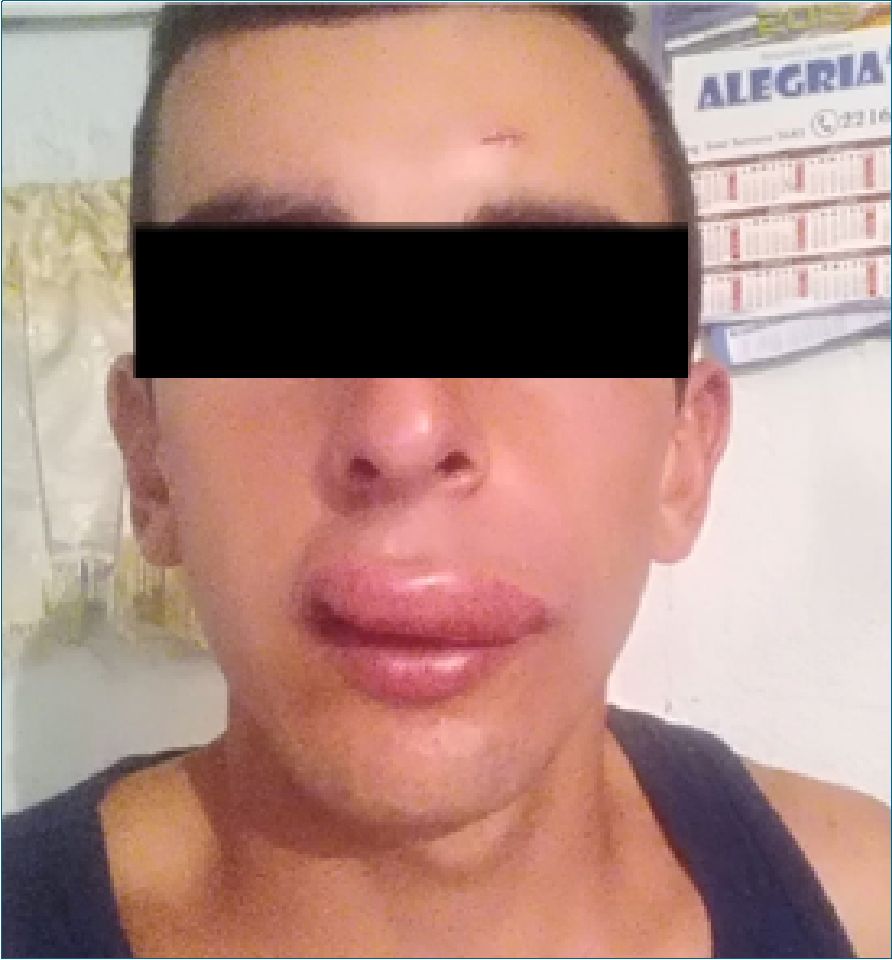
Figura 1.
El paciente cursó las primeras 6 h del posoperatorio inmediato en sala de recuperación postanestésica, monitorizado, con buen control del dolor, sin evidencia de episodios de edema. Se otorgó alta a cuidados intermedios ventilando espontáneamente al aire con una saturación de O2 de 98%, hemodinámicamente estable, sin bloqueo motor, sin náuseas, sin vómitos posoperatorios. Las siguientes 48 h en cuidados intermedios cursó sin complicaciones. Se continuó con ácido tranexámico a dosis de 50 mg/kg por 48 h y se mantuvo las dosis triplicada de danazol por 3 días con buena evolución.
-
Discusión
En el angioedema hereditario se produce por un defecto en el gen que codifica las proteínas del sistema del complemento, en este caso, C1-inhibidor (C1-inh). La disfunción del inhibidor de la esterasa C1 (C1-INH) modula la activación por contacto, la coagulación y las cascadas del complemento. Si no se inhiben, estas vías conducen a una sobreproducción de bradicinina, lo que aumenta la permeabilidad vascular y produce edema[1],[5],[6].
Estos pacientes tienen riesgo de tener un episodio grave asfíctico por edema de la vía aérea superior, siendo esta imprevisible a pesar de estar recibiendo tratamiento[1],[5],[6].
Estos pacientes previo al desarrollo del angioedema pueden tener pródromos, como erupción reticulada, también llamada eritema marginatum, malestar general, decaimiento, alteración del estado de ánimo, tirantez u hormigueo en la zona que se hinchará[2],[3],[8],[16]. Otro síntoma importante observado es la crisis de dolor abdominal intenso tipo cólico, causadas por el edema de la mucosa de cualquier parte del tubo digestivo. La intensidad del dolor puede acercarse a la de un abdomen agudo y, a menudo, da lugar a una intervención quirúrgica innecesaria[4],[8],[16]. El diagnóstico se basa en la asociación de criterio clínico y criterio de laboratorio. Los estudios de laboratorio miden la cuantificación de C4 y cualitativamente y cuantitativamente C1-INH. Los pacientes con angioedema hereditario tipo 1 como en el caso de este paciente, tienen una disminución funcionalidad y los niveles de C1 inhibidor y C4 disminuido[1]-[16].
En el período perioperatorio existen factores que pueden desencadenar una agudización de angioedema. Aunque habitualmente no se conoce un factor desencadenante claro, sí se ha demostrado que una agresión tisular local, estrés emocional, dolor, infecciones, embarazo, alcohol algunos alimentos o el uso de antiinflamatorios no esteroideos (AINES) e inhibidores de la enzima convertidora de angiotensina (IECA), exposición al frío, períodos prolongados en posición supina o sentado entre otros, pueden precipitar un brote[5],[8],[9],[16].
En este paciente se planificó el período perioperatorio en conjunto con equipo multidisciplinario integrado por anestesistas, cirujanos, hematología y dermatología. Se identificaron los posibles factores que podrían llegar a desencadenar episodio angioedema y se realizó una prevención enérgica de los mismo, disminuyendo el estado de ansiedad del paciente, brindándole información de la cirugía y técnica anestesia, evitamos ayunos prolongados y además se realizó premedicación con benzodiazepinas y se realizó sedación en intraoperatorio. La temperatura de block quirúrgico se mantuvo a 23°C, se utilizaron sueros calientes y calefactor de aire forzado, evitando la hipotermia.
Se optó por una técnica anestesia neuroaxial dado que cumplía con requerimientos quirúrgicos, el paciente estaba de acuerdo y no presentaba contraindicaciones. Algunos estudios plantean que la técnica anestésica locorregional tiene ventajas frente a la anestesia general, ya que evita manipulación activa de la vía aérea, por lo que se piensa que de esta manera disminuiría el riesgo de edema de las vías respiratorias superiores evitando el estrés directo de la mucosa[4],[5],[13],[14],[15],[17]. No existen fármacos utilizados en anestesia formalmente contraindicados para el manejo de estos pacientes a excepción de los dextranos[17].
En cuanto al tratamiento farmacológico, el paciente venía recibiendo tratamiento profiláctico a largo plazo o profilaxis de rutina, que es un tratamiento continuo o de mantenimiento destinado a disminuir la frecuencia, gravedad y duración de los ataques de angioedema. Se indicó danazol que son andrógenos y mejoran la síntesis hepática del inhibidor de C1. Otras alternativas son antifibrinolíticos (ácido epsilonaminocaproico y ácido tranexámico) y el Lanadelumab que es un anticuerpo monoclonal contra la calicreína plasmática, siendo este último el tratamiento de elección pero de muy alto costo[2],[7],[8],[9],[12],[16].
En caso de someterse a procedimientos quirúrgicos, manipulaciones orofaríngeas o situaciones que puedan desencadenar un ataque agudo, se recomienda la profilaxis a corto plazo. Es necesaria una preparación de 4 a 5 días antes, con 600 mg/día de danazol, que puede asociarse a un antifibrinolítico. Cuando no es posible la preparación con danazol o en caso de urgencia, la infusión de concentrado de C1-INH debe realizarse de 1 a 6 h previas a la operación y posiblemente en el posoperatorio dependiendo de las consecuencias, tiene una eficacia terapéutica de 2 a 5 días, como alternativa en caso de no contar con el producto se debe administrar al menos 2 U de PFC (plasma fresco congelado) que restablece el nivel de C1-INH y ATX (ácido tranexámico 75 mg/kg/d) durante un período de 2 a 5 días[2],[4],[7],[8],[12],[16].
A pesar de la profilaxis previa al procedimiento, algunos pacientes aún experimentaron episodios y por este motivo es esencial tener medicación de rescate[4]. Las exacerbaciones agudas del edema se pueden tratar con INH-C1, el inhibidor de la calicreína ecallantida o el antagonista del receptor de bradicinina icatibant[4],[7],[16].
El concentrado de C1-INH, ya sea derivado de plasma o recombinante, reemplaza a la proteína C1-INH deficiente o disfuncional y, por lo tanto, regula la producción de bradicinina mediante la inhibición del sistema de contacto[1],[7],[8],[16].
En caso de no contar con C1-INH se puede administrar plasma tratado con detergente y solvente (SDP), el mismo contiene C1 INH, pero su uso es controvertido ya que también contiene C2 y C4 que al actuar como sustrato podrían empeorar el angioedema. Si tampoco se cuenta con SDP la tercer alternativa menos segura sería el plasma fresco congelado convencional[1],[2],[17].
En este paciente se administró 12 h antes 1 unidad de plasma fresco y otra en preoperatorio inmediato y además se dispuso para el intraoperatorio ante un eventual ataque angioedema.
Se obtuvo una buena respuesta sin ninguna complicación con la estrategia planificada y el tratamiento disponible en nuestro medio.
Dado potencial riesgo de tener una complicación grave que puede poner en peligro la vida del paciente, se debe de tener siempre la capacidad de proteger las vías respiratorias durante el período perioperatorio. Y asegúrese de que el paciente tenga cuidados posoperatorios en una área vigilada como cuidados intermedios fundamentalmente las primeras 48 h posoperatorias[6],[7],[14].
-
Conclusión
El AEH es una patología rara, poco frecuente, y en el contexto perioperatorio pueden haber factores desencadenantes, con potencial riesgo de complicación grave como el edema de la vía aérea, con riesgo de mortalidad si no se realiza un tratamiento oportuno. No existe ningún marcador que permita predecir la aparición de un episodio.
Es fundamental una preparación preoperatoria cuidadosa, con la participación de equipos multidisciplinarios (hemoterapeutas, cirujanos, intensivistas, alergólogos, anestesiólogos), para la adopción de una adecuada profilaxis, la planificación anestésica y tratamiento oportuno en caso de aparecer una crisis que asegure el bienestar del paciente.
-
Referencias
1. Ferrari AM, Amoroso CL. Evaluación perioperatoria de una paciente con un angioedema grave para una cirugía de coordinación. Anest Analg Reanim [Internet]. 2013 [citado 2021 Jul 17]; 26 (1): 8-8. Disponible en: http://www.scielo.edu.uy/scielo.php?script=sci_arttext&pid=S1688-12732013000100008&lng=es
2. Serpa FS, Mansour E, Aun MV, Giavina-Bianchi P, Chong Neto HJ, Arruda LK, et al. Hereditary angioedema: how to approach it at the emergency department? Einstein (Sao Paulo). 2021 Apr;19:eRW5498. https://doi.org/10.31744/einstein_journal/2021RW5498 PMID:33852678
3. Bouillet L. Angioedemas bradicinérgicos hereditarios y adquiridos. EMC – Dermatología [Internet]. 2021 Jun 1 [cited 2021 Jul 26];55(1):1–7. Available from: http://search.ebscohost.com.proxy.timbo.org.uy:2048/login.aspx?direct=true&db=eds elp&AN=S1761289621447084&lang=es&site=eds-live https://doi.org/10.1016/S1761-2896(21)44708-4.
4. Rodrigues C, Adrego T, Vieira H. Perioperative Approach to Patients with Hereditary Angioedema. 2018 Mar 30; Available from: http://search.ebscohost.com.proxy.timbo.org.uy:2048/login.aspx?direct=true&db=edsrca&AN=rcaap.article.14816&lang=es&site=eds-live
5. MacBeth LS, Volcheck GW, Sprung J, Weingarten TN. Perioperative course in patients with hereditary or acquired angioedema. J Clin Anesth. 2016 Nov;34:385–91. https://doi.org/10.1016/j.jclinane.2016.05.010 PMID:27687418
6. Zeerleder S, Levi M. Hereditary and acquired C1-inhibitor-dependent angioedema: from pathophysiology to treatment. Ann Med. 2016;48(4):256–67. https://doi.org/10.3109/07853890.2016.1162909 PMID:27018196
7. Caballero T. Treatment of Hereditary Angioedema. J Investig Allergol Clin Immunol. 2021 Feb;31(1):1–16. https://doi.org/10.18176/jiaci.0653 PMID:33602658
8. Longhurst HJ, Bork K. Hereditary angioedema: an update on causes, manifestations and treatment. Br J Hosp Med (Lond). 2019 Jul;80(7):391–8. https://doi.org/10.12968/hmed.2019.80.7.391 PMID:31283393
9. Melo MC, Boas WW, Faria MD, Lima AA, Souza RS. Anaesthetic Approach for Patient with Hereditary Angioedema. Turk J Anaesthesiol Reanim. 2020 Feb;48(1):68–70. https://doi.org/10.5152/TJAR.2019.90522 PMID:32076683
10. L. Vilaça MJ, M. Coelho F, Faísco A, Carmona C. Considerações anestésicas perante um doente com angioedema hereditário – Caso clínico. Brazilian Journal of Anesthesiology [Internet]. 2017 Sep;67(5):541–3. Available from: http://dx.doi.org/10.1016/j.bjan.2015.03.005
11. Jindal AK, Singh A, Anjani G, Kaur A, Jaiswal M, Chopra S, et al. Successful perioperative management of three patients with hereditary angioedema without C1 esterase inhibitor therapy: A developing country perspective. Immunobiology. 2020 Nov;225(6):152022. https://doi.org/10.1016/j.imbio.2020.152022 PMID:33197705
12. Maynard AA, Burger CF, Schlesinger JJ. Angioedema: Perioperative management. SAGE Open Medical Case Reports [Internet]. 2017 Jan 1;5. Available from: http://dx.doi.org/10.1177/2050313×17713912
13. Teranishi R, Makino Y, Amano E, Shibuya H, Okada T. [Perioperative Management of a Patient with Hereditary Angioedema: A Case Report]. Masui. 2015 Apr;64(4):441–3. PMID:26419114
14. Williams AH, Craig TJ. Perioperative management for patients with hereditary angioedema. Allergy Rhinol (Providence). 2015 Jan;6(1):50–5. https://doi.org/10.2500/ar.2015.6.0112 PMID:25860171
15. Fujii M, Higashiguchi T, Shime N, Kawabata Y. Successful anesthetic management during abdominal wall-lifting laparoscopic cholecystectomy in a patient with hereditary angioedema. JA Clin Rep. 2018 May;4(1):38. https://doi.org/10.1186/s40981-018-0174-1 PMID:32026009
16. Bouillet L. Angioedemas bradicinérgicos hereditarios y adquiridos. EMC – Dermatología [Internet]. 2021 Jun;55(1):1–7. Available from: http://dx.doi.org/10.1016/s1761-2896(21)44708-4
17. Fernández MC, Redondo GZ, Dayné GG. Anestesia en una paciente con angioedema hereditario. Rev cuba anestesiol reanim [Internet]. 2022 Dic [citado 2024 Mar 12]; 21 (3) : e828. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1726-67182022000300002&lng=es

 ORCID
ORCID