Felipe Marihuén1, Magdalena Estefó2, Dagoberto Ojeda2, Claudio George3, Francisco Sepúlveda3
Recibido:
Aceptado: 2025-08-25
©2026 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 55 Núm. 2 |https://doi.org/10.25237/revchilanestv55n2-06
PDF
Transdermal buprenorphine in cardiac surgery: Results of a randomized doubleblind clinical trial
Abstract
Introduction: Moderate to severe pain has been reported in about 75% of patients after cardiac surgery and predisposes to complications. We evaluated whether a 5 pg/h transdermal buprenorphine patch applied immediately before surgery improves analgesia within a standardized multimodal protocol. Materials and Methods: Singlecenter, randomized, doubleblind, placebocontrolled trial. Adults 18-75 years, BMI 21-35 kg/m2 and LVEF > 35% undergoing coronary revascularization, singlevalve surgery or cardiac tumor resection were allocated 1:1 to buprenorphine 5 pg/h or placebo patch; all received multimodal analgesia. Primary outcome: pain (static and dynamic NRS > 3) at 12, 24, 48, 72 h and day 7, analyzed with multilevel logistic regression. Secondary outcomes: rescue opioid use and adverse events (nausea/vomiting, constipation, urinary retention). Results: No differences were observed in static NRS (OR 1.2, 95% CI 0.7-2.2) or dynamic NRS (OR 1.7, 95% CI 0.9-3.3) between groups. Secondary outcomes were also comparable. No serious patchrelated adverse events occurred. Conclusions: Immediate application of a 5 pg/h buprenorphine patch did not improve analgesia or reduce rescue opioid use; routine use in this setting is not supported by these data. Discussion: Lack of effect may relate to the low dose, absence of a preoperative (12-24 h) uptake window to achieve steady levels, and the high analgesic ceiling of the multimodal protocol. The rigorous design supports internal validity; future trials should assess higher doses and earlier application.
Resumen
Introducción: Se ha reportado un dolor moderadosevero en cerca 75% de los pacientes tras cirugía cardíaca y favorece complicaciones. Evaluamos si un parche transdérmico de buprenorfina 5 pg/h aplicado inmediatamente antes de la cirugía mejora la analgesia sobre un protocolo multimodal. Materiales y Métodos: Ensayo aleatorizado, doble ciego, controlado con placebo, unicéntrico. Adultos 18-75 años con IMC 21-35 y FEVI > 35% sometidos a revascularización, cirugía valvular o resección tumoral fueron asignados 1:1 a buprenorfina 5 pg/h o apósito placebo; ambos recibieron analgesia multimodal. Desenlace primario: dolor (EVN estática y dinámica > 3) a 12, 24, 48, 72 h y día 7 analizado con regresión logística multinivel. Secundarios: opioides de rescate y eventos adversos (náuseas/vómitos, constipación, retención urinaria). Resultados: No hubo diferencias en la EVN estática (OR 1,2; IC95% 0,7-2,2) ni en la EVN dinámica (OR 1,7; IC95% 0,9-3,3) entre los grupos. Tampoco se evidenciaron diferencias en los resultados secundarios. No se registraron eventos adversos graves atribuibles a buprenorfina.Conclusiones: El parche de buprenorfina 5 pg/h aplicado inmediatamente no mejoró la analgesia ni redujo el uso de opioides de rescate; su empleo rutinario en este contexto no se respalda con estos datos. Discusión: La falta de efecto puede deberse a la dosis baja, la aplicación sin ventana preoperatoria (12-24 h) para alcanzar niveles estables y el techo analgésico elevado del protocolo. El diseño riguroso aporta validez; futuros ensayos deberían explorar dosis mayores y colocación anticipada.
Introducción
El dolor posoperatorio en pacientes sometidos a cirugía cardíaca representa un problema relevante por su impacto en la morbimortalidad, los costos asociados y la prolongación de la estadía hospitalaria. Se ha descrito que hasta 75% de estos pacientes experimentan dolor moderado a severo en las primeras horas del posoperatorio[1]. Su origen es multifactorial, con componentes somáticos, viscerales y neuropáticos[1],[2], derivados de la incisión cutánea, retracción esternal, disección de tejidos profundos, colocación de drenajes torácicos, lesión muscular por la posición quirúrgica y la inmovilidad prolongada[1],[2]. Estas agresiones desencadenan una cascada inflamatoria que activa las vías nociceptivas aferentes.
El dolor es habitualmente más intenso en las primeras 24 h, localizándose en zonas relacionadas con la esternotomía y la posición en decúbito supino[3],[4]. Se ha documentado que el dolor severo durante ese período inicial constituye un factor de riesgo para desarrollar dolor posoperatorio persistente[3]. Su incidencia alcanza hasta 43% a los tres meses, 37% a los seis meses y persiste en el 17% de los pacientes a los dos años[5],[6].
Un manejo analgésico deficiente afecta múltiples sistemas, como respiratorio, cardiovascular y musculoesquelético, pudiendo comprometer tanto la recuperación como la funcionalidad del paciente. En este contexto, la analgesia multimodal se plantea como una estrategia que permite optimizar el control del dolor y reducir el uso de opioides en dosis altas, disminuyendo así sus efectos adversos[7]. Esta estrategia busca combinar fármacos con mecanismos de acción complementarios para lograr un efecto sinérgico, más eficaz y seguro.
El uso de opioides de acción corta o ultracorta, como el fentanilo o el remifentanilo, se ha asociado a fenómenos de tolerancia aguda, hiperalgesia y mayor riesgo de dolor persistente, por lo que su empleo en el período posoperatorio ha sido cuestionado[7],[8],[9]. Diversos estudios han reportado una incidencia de uso persistente de opioides tras cirugía cardíaca que oscila entre 5% y 15%, cifras superiores a las observadas en otros tipos de cirugía mayor o menor. Este fenómeno se asocia a un mayor riesgo de dependencia, abuso y sobredosis, lo que representa un desafío importante en salud pública, como ha ocurrido en Estados Unidos[10].
La buprenorfina es un agonista parcial de los receptores p-opioides, con una elevada afinidad y una prolongada duración de acción. Su formulación transdérmica permite una liberación sostenida del fármaco, generando niveles plasmáticos estables, mejor tolerancia y un perfil de efectos adversos más favorable. Su potencia es comparable a la del fentanilo transdérmico[11],[12]. En cirugía abdominal mayor, el uso de buprenorfina transdérmica ha mostrado resultados alentadores: el estudio de Kumar et al., demostró que su administración (10 mcg/h) redujo significativamente los puntajes EVA y la necesidad de analgesia de rescate en pacientes sometidos a cirugía abdominal abierta, sin aumentar los eventos adversos[13]. Estos hallazgos fueron respaldados por un metaanálisis reciente de Albaqami et al., que incluyó 911 pacientes de 11 estudios y evidenció una disminución del dolor posoperatorio en las primeras 48 h, menor consumo de opioides y menor incidencia de náuseas y vómitos, en comparación con terapias estándar[14].
Adicionalmente, se ha reconocido que el dolor mal manejado en el posoperatorio inmediato incrementa el riesgo de desarrollar dolor persistente, deterioro funcional y uso crónico de opioides, lo cual perpetúa un círculo vicioso de mala calidad de vida, mayor carga asistencial y riesgo de dependencia[7].
En respuesta a esta problemática, la Asociación Americana de Cirugía Torácica (AATS) publicó en 2023, recomendaciones para el manejo analgésico en cirugía cardíaca. En ellas se enfatiza el uso de estrategias multimodales no opioides (recomendación fuerte, nivel de evidencia C) y se desaconseja el uso rutinario de opioides en altas dosis tanto en el intra como en el posoperatorio, abogando por una prescripción juiciosa basada en la evaluación individual de riesgos y beneficios[15].
Hasta la fecha, ningún estudio previo ha comparado los efectos de la buprenorfina transdérmica en cardiocirugía, pero si en otras cirugías que cursan con alta incidencia de dolor posoperatorio moderado a severo como la cirugía abdominal mayor, con resultados favorables, por lo que el objetivo de este estudio fue evaluar la eficacia del parche transdérmico de buprenorfina como coadyuvante analgésico en pacientes sometidos a cirugía cardíaca con circulación extracorpórea, comparado con un grupo placebo con manejo analgésico estándar, en términos de control del dolor posoperatorio y necesidad de opioides de rescate.
Materiales y Métodos
Diseño del estudio
Se realizó un ensayo clínico aleatorizado, doble ciego y unicéntrico entre junio de 2024 y enero de 2025, en la Clínica Dávila, Santiago de Chile. El objetivo principal fue comparar la evolución del dolor posoperatorio en pacientes sometidos a cirugía cardíaca que cumplían criterios de extubación precoz, entre aquellos que recibieron el esquema analgésico institucional estándar y un grupo que, además, recibió un parche transdérmico de buprenorfina 5 mcg/h (Norspan®). Como desenlaces secundarios se evaluaron la necesidad de opioides de rescate y la aparición de efectos adversos asociados al uso del parche, incluyendo náuseas y/o vómitos posoperatorios (NVPO) y constipación.
Participantes
Se incluyeron pacientes que cumplían con los criterios del protocolo institucional de extubación precoz en cirugía cardíaca, los cuales consideraban: edad entre 18 y 75 años, índice de masa corporal (IMC) entre 21 y 35 kg/m2, y fracción de eyección ventricular izquierda (FEVI) mayor a 35%. Los procedimientos quirúrgicos permitidos incluyeron revascularización miocárdica, cirugía univalvular, reparación de defectos septales únicos o resección de tumores cardíacos, todos realizados con circulación extracorpórea (CEC).
Fueron excluidos los pacientes con antecedentes de dolor crónico (mayor a 6 meses), alergia o contraindicación a los fármacos del protocolo, procedimientos que requirieran paro circulatorio, cirugías no aisladas (bivalvulares o combinadas valvular y coronaria), trasplante cardíaco, cirugía de urgencia, reoperaciones por esternotomía previa y casos de endocarditis infecciosa.
Al momento de la inclusión, se registraron las características clínicas y demográficas de los participantes: sexo, edad, IMC, tipo de cirugía realizada, EuroSCORE II, capacidad funcional (CF) según clasificación NYHA, tabaquismo, comorbilidades relevantes (hipertensión arterial, Diabetes Mellitus tipo 2 insulinorrequirente, enfermedad pulmonar obstructiva crónica [EPOC] o limitación crónica al flujo aéreo [LCFA]), variables ecocardiográficas (FEVI (%) y presencia de presión sistólica de arteria pulmonar (PSAP) > 30 mmHg), y si la extubación se realizó en pabellón.
Randomización y cegamiento
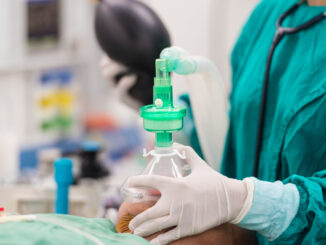
La asignación de los participantes se realizó mediante una secuencia aleatoria generada por computador (aleatorización simple), preparada un investigador externo. El estudio adoptó un diseño doble ciego: pacientes, profesionales asistenciales y evaluadores desconocieron en todo momento el grupo asignado. Para preservar el cegamiento, un único investigador, que sí conocía la secuencia, aplicó el dispositivo correspondiente según el grupo: en el brazo de intervención colocó el parche transdérmico de buprenorfina (Norspan® 5 mcg/hr) y lo cubrió con un apósito con parche (Tegapad®); en el brazo placebo aplicó el mismo apósito sobre piel intacta. El parche o el apósito se mantuvieron in situ hasta completar el seguimiento al séptimo día.
Intervenciones
El manejo de ambos grupos fue guiado por el protocolo institucional de extubación precoz. Ambos recibieron el mismo esquema terapéutico, con la única diferencia del uso del parche transdérmico de buprenorfina 5 mcg/h en el grupo intervención.
En el preoperatorio, todos los pacientes recibieron analgesia multimodal por vía oral la noche anterior a la cirugía, con paracetamol 1 g y pregabalina 75 mg. Las indicaciones de ayuno siguieron las recomendaciones estándar: suspensión de sólidos entre 6 y 8 h antes de la inducción anestésica, y autorización para líquidos claros hasta cuatro horas antes.
Durante el intraoperatorio, la inducción anestésica quedó a criterio del anestesiólogo tratante, en función del estado clínico del paciente. La mantención se realizó con sevoflurano a 1-1,5 MAC. Se administró profilaxis antibiótica conforme al protocolo institucional. El manejo analgésico intraoperatorio incluyó fentanilo, con una dosis acumulada máxima de 10 pg/kg, y metadona 0,05 mg/kg al momento de la inducción. Se inició infusión de dexmedetomidina a 0,6 pg/kg/h, reducida a 0,3 pg/ kg/h durante la CEC, y mantenida hasta la llegada a la Unidad Coronaria (UCO). Tras el weaning de la CEC, se administraron por vía intravenosa: paracetamol 1 g, metamizol 2 g, un antiinflamatorio no esteroideo (ketoprofeno 100 mg), y sulfato de magnesio 1,25 g. Para analgesia regional, el cirujano realizó un bloqueo paraesternal con bupivacaína (máximo 2 mg/kg) y lidocaína (máximo 3 mg/kg) en un volumen total 40 mL, junto con infiltración de los sitios de inserción de los drenajes torácicos. La profilaxis de náuseas y vómitos intraoperatoria incluyó dexametasona 4 mg y ondansetrón 4 mg.
En los casos en que el paciente fue extubado en pabellón, se trasladó a UCO con infusión continua de dexmedetomidina a 0,3 pg/kg/h. Si la extubación precoz se realizaba en UCO, se administraban 5 mg de metadona intravenosa y se iniciaba una infusión de propofol (1-2 mg/kg/h) en combinación con dexmedetomidina a 0,3 pg/kg/h, la cual se titulaba progresivamente hasta la extubación.
En el posoperatorio inmediato, los pacientes reiniciaban la ingesta de líquidos a las cuatro horas post-extubación, según el nivel de conciencia, y recibían oxigenoterapia de acuerdo con la necesidad clínica. El manejo analgésico incluía paracetamol 1 g intravenoso cada 8 h y metamizol 4 g en 250 mL de suero fisiológico a 10 mL/h. La infusión de dexmedetomidina se mantenía a 0,3 pg/kg/h, ajustándose según el nivel de agitación o sobre-sedación. Si el paciente refería dolor (definido como un valor > 3 en la Escala Visual Numérica [EVN]), se administraba ketorolaco 30 mg EV; en caso de persistencia del dolor, se indicaba metadona 3 mg EV.
El protocolo para la prevención y manejo de NVPO contemplaba ondansetrón 4 mg EV cada 8 h como primera línea; en caso de falla, se utilizaba granisetrón 1 mg, y como tercera línea, droperidol 0,625 mg EV.
Determinación de resultados
El desenlace primario fue la intensidad del dolor posoperatorio, evaluada mediante la EVN, donde 0 indica ausencia de dolor y 10 el peor dolor imaginable. Las mediciones se realizaron a las 12, 24, 48 y 72 h, y al séptimo día posterior a la cirugía. La evaluación fue aplicada por investigadores cegados a la asignación de grupos. En los casos en que el alta se produjo antes del séptimo día, la medición correspondiente se efectuó mediante entrevista telefónica utilizando el mismo formato estructurado.
Los desenlaces secundarios se evaluaron en los mismos puntos temporales (12, 24, 48, 72 h y día 7 posoperatorio) e incluyeron:
buprenorfina, entre ellos: constipación, NVPO y retención urinaria. Estos eventos fueron pesquisados mediante entrevistas presenciales estandarizadas.
Análisis estadístico
El tamaño muestral fue calculado considerando una reducción en la proporción de pacientes con dolor moderado (EVN > 4), desde 39,5% a 15,7%. Se utilizó una prueba unilateral para la comparación de dos medias, con un error tipo I de 2,5% y una potencia estadística del 90%, lo que determinó un tamaño de muestra de 20 pacientes por grupo.
El análisis descriptivo de la muestra se realizó mediante frecuencias y porcentajes para variables categóricas, y medias con desviación estándar para variables continuas. Para el análisis del desenlace principal, la escala EVA se categorizó en dos niveles: ausencia de dolor o dolor leve (EVN < 3) y dolor significativo (EVN > 3). Dado que se trata de un estudio prospectivo longitudinal con cinco mediciones repetidas (a las 12, 24, 48 y 72 h, y al séptimo día posoperatorio), se aplicó un modelo de regresión logística multinivel para estimar unOdds Ratio (OR) resumen a lo largo del seguimiento.
Implicancias éticas
El estudio fue aprobado por el Comité de Ética de la Clínica Dávila. Todos los participantes firmaron consentimiento informado. Ambos grupos recibieron analgesia multimodal eficaz y acceso a analgesia de rescate. La confidencialidad de los datos fue resguardada según normativa vigente.
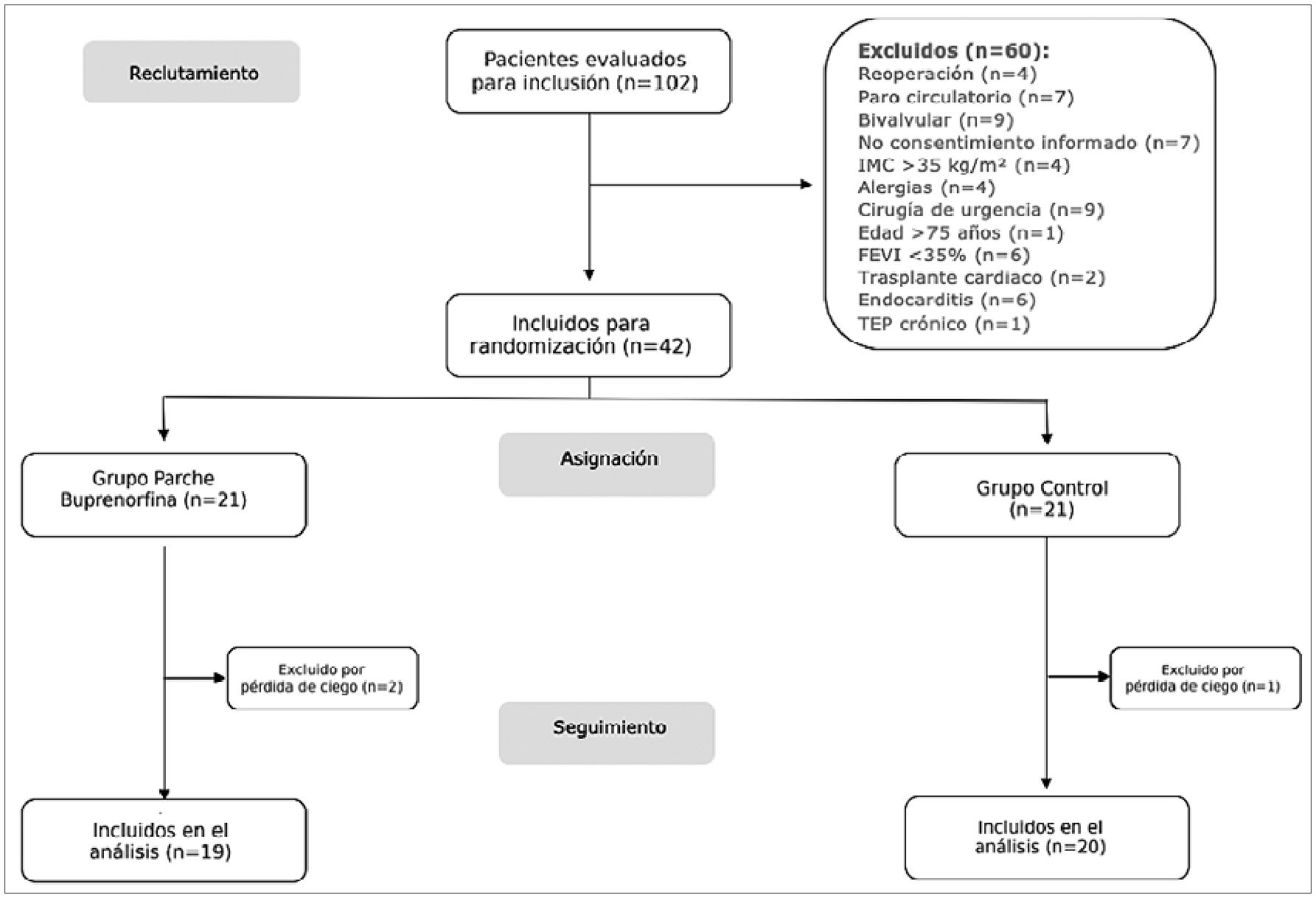
Figura 1. Diagrama de flujo de pacientes.
Resultados
Durante el período comprendido entre marzo y octubre de 2024 se reclutaron un total de 102 pacientes, de los cuales 60 fueron excluidos por criterios predefinidos (reoperación, cirugía con paro circulatorio, cirugía bivalvular, cirugía de urgencia, trasplante cardíaco, endocarditis activa, tromboendarterectomía pulmonar, ausencia de consentimiento informado, IMC > 35 kg/m2, edad > 75 años, FEVI < 35% y alergias a fármacos del protocolo). Finalmente, 42 pacientes cumplieron los criterios de inclusión y fueron aleatorizados: 21 al grupo parche de buprenorfina y 21 al grupo control (placebo).
Durante el seguimiento, se registraron 3 exclusiones (dos del grupo parche y uno del grupo placebo), todas ellas asociadas a pérdida del cegamiento producto de la remoción del apósito. De este modo, el análisis final se realizó sobre 39 pacientes: 19 en el grupo buprenorfina y 20 en el grupo control (Figura 1).
Ambos grupos fueron comparables en edad, sexo, índice de masa corporal y perfil clínico general. Se observó una diferencia porcentual en la variable tabaquismo (57,1% en grupo parche y 33,3% en grupo control). La media de edad fue de 64,5 ± 6,4 años en el grupo parche y 60,7 ± 7,8 años en el grupo control. La distribución del tipo de cirugía fue similar en ambos brazos, predominando las revascularizaciones miocárdicas (CRM), con 76,2% en el grupo parche y 85,7% en el grupo control. Así mismo, la extubación en pabellón fue similar en ambos grupos (66,6% vs. 76,2%).
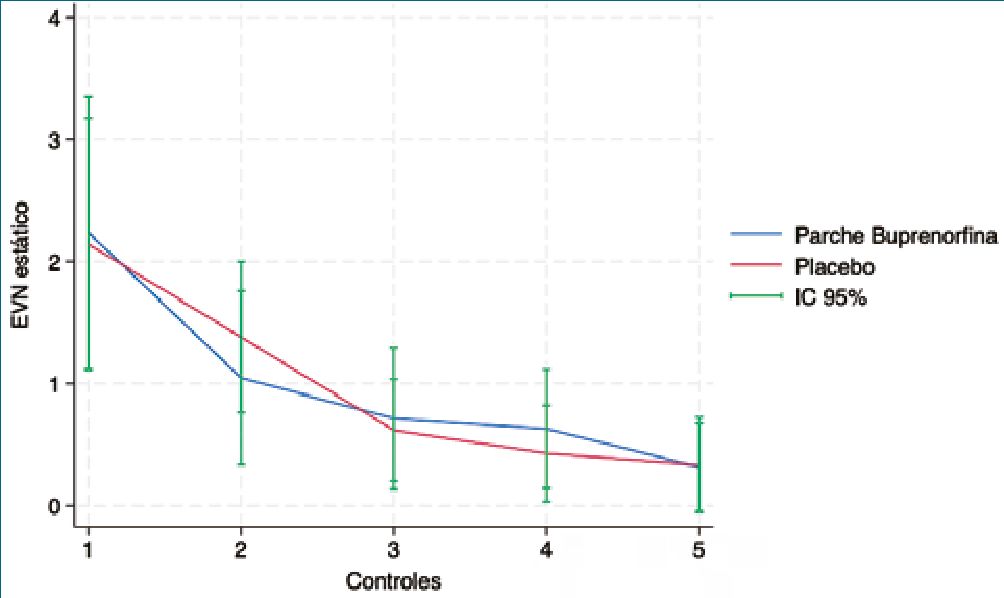
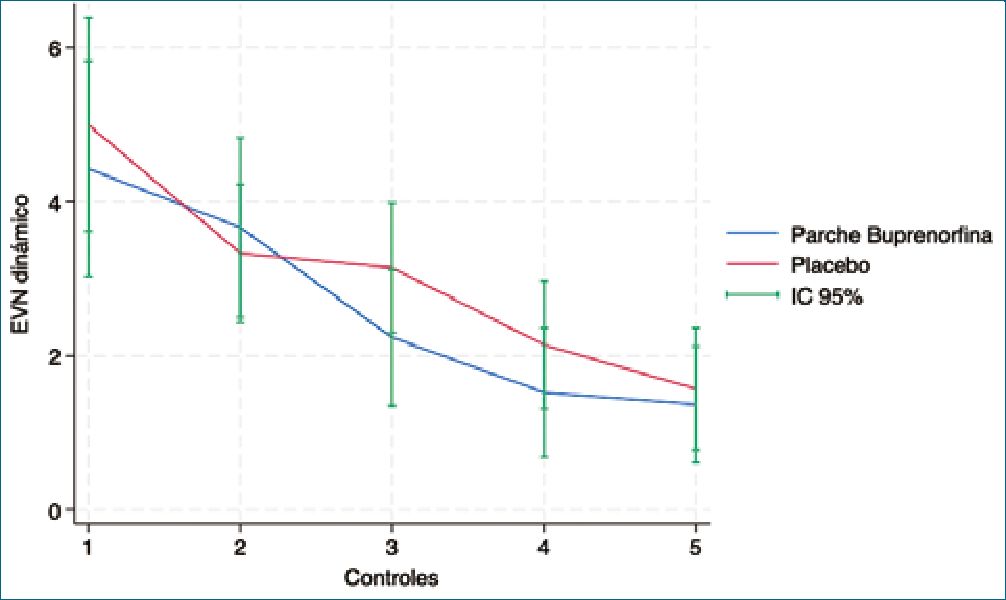
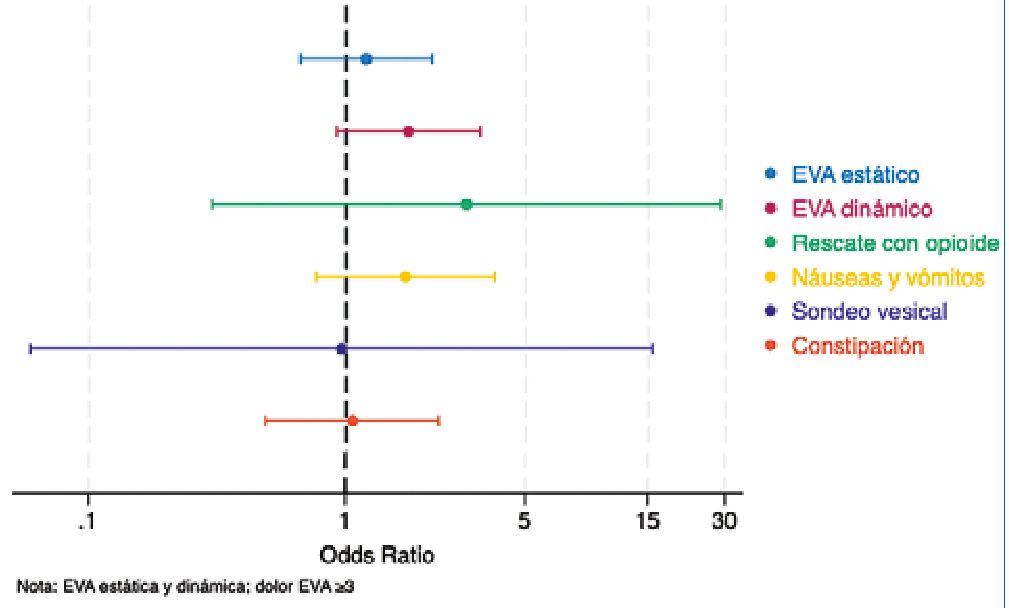
En relación con el desenlace primario, no se observaron diferencias estadísticamente significativas en las puntuaciones de dolor posoperatorio entre los grupos de parche de buprenorfina y placebo, tanto en EVA estático como dinámico a lo largo de los distintos puntos de control (Figuras 2 y 3). El análisis de OR tampoco evidenció diferencias relevantes entre ambos grupos: EVA estático OR 1,2 (IC 95%: 0,7-2,2) y EVA dinámico OR 1,7 (IC 95%: 0,9-3,3) (Figura 4).
Figura 2. Evolución del EVA estático (12 horas, 24 horas, 48 horas, 72 horas y séptimo día posoperatorio).
Figura 3. Evolución del EVA dinámico (12 horas, 24 horas, 48 horas, 72 horas y séptimo día posoperatorio).
Figura 4. Odds ratio (OR) con intervalos de confianza del 95% para desenlace primario y secundarios.
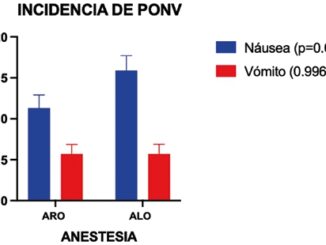
Respecto a los desenlaces secundarios, no se encontraron diferencias significativas en la incidencia de NVPO (OR 1,7; IC 95%: 0,8-3,8), requerimiento de opioides de rescate (OR 2,9; IC 95%: 0,3-28,7), necesidad de sondeo vesical (OR 0,96; IC 95%: 0,06-15,6), ni en la aparición de constipación (OR 1,1; IC 95%: 0,5-2,3). Los resultados se muestran en la Figura 4.
Discusión
En este ensayo randomizado doble ciego, evalúa el parche transdérmico de buprenorfina en cirugía cardíaca, no se observaron diferencias clínicamente ni estadísticamente significativas en la intensidad del dolor posoperatorio entre el grupo parche (5 pg/h) y el grupo control, tanto para EVA estático como dinámico a lo largo de los cinco controles programados. Asimismo, la incidencia de eventos adversos (NVPO, constipación, retención urinaria) y el uso de opioides de rescate fueron similares, con intervalos de confianza anchos que descartan beneficios clínicamente relevantes de la intervención.
Estos hallazgos contrastan con la evidencia derivada de procedimientos abdominales, donde el uso de buprenorfina transdérmica ha mostrado beneficios consistentes. Kumar et al., reportaron que la administración de un parche de 10 pg/h, aplicado 12 h antes de cirugía abdominal abierta, se asoció a una reducción significativa del dolor en las primeras 48 h y una menor necesidad de analgesia de rescate, sin incremento en los efectos adversos[13]. De forma concordante, un metaanálisis reciente de Albaqami et al., que incluyó 11 ensayos clínicos controlados y más de 900 pacientes, concluyó que la buprenorfina transdérmica se asocia a menor intensidad de dolor posoperatorio, menor consumo acumulado de opioides y una reducción en la incidencia de náuseas y vómitos, en comparación con placebo o AINEs[14]. Asimismo, una revisión sistemática brasileña de nueve ensayos clínicos aleatorizados encontró que el uso de parches de 10 a 20 pg/h aplicados entre 6 y 48 h antes del acto quirúrgico se asoció a una modesta pero consistente disminución del dolor y del uso de analgésicos en el posoperatorio[16]. Estos resultados fueron respaldados por un metaanálisis posterior que sugirió un beneficio clínico relevante de buprenorfina transdérmica frente a placebo o AINEs, especialmente en el contexto de analgesia multimodal[17].
La ausencia de efecto en nuestra cohorte puede explicarse por múltiples motivos. En primer lugar, la dosis utilizada. Optamos por un parche de 5 pg/h, inferior al rango de 10-20 pg/h empleado en la mayoría de estudios previos, debido a que nuestros pacientes presentaban patología cardiovascular significativa, mayor vulnerabilidad hemodinámica y no eran usuarios crónicos de opioides, según lo recomendado por el fabricante[18]. En segundo lugar, el momento de aplicación difiere de la evidencia publicada. En la literatura, el parche se aplicó varias horas previo a la cirugía para asegurar niveles plasmáticos estables desde el inicio del posoperatorio. En cambio, en nuestro estudio se colocó al momento de la inducción anestésica, lo que podría haber resultado en niveles subóptimos durante las primeras 48 h, período clave para el control del dolor.
Además, cabe destacar que todos los pacientes recibieron un esquema multimodal intensivo (paracetamol, AINEs, metamizol, dexmedetomidina y metadona), conforme al protocolo ERAS para cirugía cardíaca, que promueve un enfoque analgésico sin depender excesivamente de opioides. Este elevado “techo analgésico” pudo haber enmascarado cualquier beneficio incremental derivado del parche. Por último, la fisiopatología propia de la circulación extracorpórea, como inflamación sistémica, hipotermia y alteraciones hemodinámicas, podría haber afectado la absorción transdérmica y distribución tisular de la buprenorfina, limitando su eficacia analgésica en nuestro contexto.
A pesar de no confirmar la hipótesis de beneficio, este estudio presenta varias fortalezas, primero su diseño aleatorizado, doble ciego y controlado con placebo, un cegamiento cuidadoso y pérdidas mínimas y simétricas. Además, se utilizó protocolo analgésico multimodal estandarizado y acorde a las prácticas actuales de uso racional de opioides. La realización de mediciones seriadas de EVN realizadas por evaluadores cegados que describen la evolución del dolor e inclusión de desenlaces secundarios pertinentes (rescate de opioides y eventos adversos) en el mismo período le dan un enfoque pragmático en una cohorte real de cirugía cardíaca con estrategias de recuperación acelerada, aumentando su aplicabilidad. Estos elementos refuerzan la validez interna y externa y orientan futuras investigaciones sobre dosis mayores y colocación preoperatoria anticipada del parche.
Este estudio también presenta limitaciones. Primero, el carácter unicéntrico reduce la generalización de los resultados. En segundo lugar, la potencia se calculó para detectar una reducción de aproximadamente 40% de dolor moderado, por lo que pudo no captar diferencias más pequeñas, pero clínicamente relevantes. Además, se usó deliberadamente la dosis más baja (5 pg/h) en una cohorte con pacientes cardiópatas y lábiles, por lo que el uso de dosis mayores, y eventualmente la instalación del parche en horas previas a la cirugía, podrían producir otro efecto. Por otro lado, no se documentó de forma sistemática la adherencia cutánea o niveles plasmáticos, impidiendo confirmar exposición farmacológica óptima. Finalmente, la analgesia multimodal intensa en ambos grupos eleva el techo terapéutico y puede haber atenuado un beneficio incremental del parche.
En conjunto, nuestros resultados sugieren que añadir un parche transdérmico de buprenorfina 5 pg/h inmediatamente antes de la cirugía cardíaca, dentro de un programa de analgesia multimodal intensiva, no mejora el control del dolor posoperatorio. Futuras investigaciones deberían probar dosis más altas aplicadas con antelación suficiente y evaluar desenlaces a largo plazo, además de comparar costos y complicaciones respiratorias. Hasta entonces, la adopción rutinaria del parche en cardiocirugía debe considerarse experimental.
Declaración de aspectos éticos: Este estudio se condujo de acuerdo con los Principios Éticos para las Publicaciones Médicas del ICMJE y con los principios de la Declaración de Helsinki de la Asociación Médica Mundial. El protocolo fue revisado y aprobado por el Comité Ético Científico de Clínica Dávila. Todos los participantes firmaron consentimiento informado escrito. Se garantizó la privacidad y anonimato de los pacientes.
Referencias
1. Choiniere M, WattWatson J, Victor JC. Prevalence of and risk factors for persistent postoperative nonanginal pain after cardiac surgery: a 2year prospective multicentre study. CMAJ. 2014;186(7):E213E223. https://doi.org/10.1503/cmaj.131012
2. Jayakumar S, Borrelli M, Milan Z, Kunst G, Whitaker D. Optimising pain management protocols following cardiac surgery: A protocol for a national quality improvement study. Int J Surg Protoc. 2019 Jan;14:1-8. https://doi.org/10.1016/j.isjp.2018.12.002 PMID:31851755
3. Zubrzycki M, Liebold A, Skrabal C, Reinelt H, Ziegler M, Perdas E, et al. Assessment and pathophysiology of pain in cardiac surgery. J Pain Res. 2018 Aug;11:1599-611. https://doi.org/10.2147/JPR.S162067 PMID:30197534
4. Lahtinen P, Kokki H, Hynynen M. Pain after cardiac surgery: a prospective cohort study of 1-year incidence and intensity. Anesthesiology. 2006 Oct;105(4):794-800. https://doi.org/10.1097/00000542-200610000-00026 PMID:17006079
5. Guimaraes-Pereira L, Farinha F, Azevedo L, Abelha F, Castro- Lopes J; Persistent postoperative pain after cardiac surgery: incidence, characterization, associated factors and its impact on quality of life. Eur J Pain. 2016;20(9):14331442. https://doi.org/10.1002/ejp.866
6. GuimaraesPereira L. Reis P, Abelha F, Azevedo LF, CastroLopes JM. Persistent postoperative pain after cardiac surgery: a systematic review with metaanalysis regarding incidence and pain intensity. Pain. 2017;158(10):18691885. https://doi.org/10.1097/j.pain.0000000000000997
7. Krakowski JC, Hallman MJ, Smeltz AM. Persistent pain after cardiac surgery: prevention and management. Semin Cardiothorac Vasc Anesth. 2021 Dec;25(4):289-300. https://doi.org/10.1177/10892532211041320 PMID:34416847
8. Murphy GS, Avram MJ, Greenberg SB, Shear TD, Deshur MA, Dickerson D, et al. Postoperative pain and analgesic requirements in the first year after intraoperative methadone for complex spine and cardiac surgery. Anesthesiology. 2020 Feb;132(2):330- 42. https://doi.org/10.1097/ALN.0000000000003025 PMID:31939849
9. Lobova VA, Roll JM, Roll ML. Intraoperative methadone use in cardiac surgery: a systematic review. Pain Med. 2021 Dec;22(12):2827-34. https://doi.org/10.1093/pm/pnab269 PMID:34487175
10. Brummett CM, Waljee JF, Goesling J, Moser S, Lin P, Englesbe MJ, et al. New persistent opioid use after minor and major surgical procedures in US adults. JAMA Surg. 2017 Jun;152(6):e170504. PMID:28403427
11. Sittl R, Likar R, Nautrup BP. Equipotent doses of transdermal fentanyl and transdermal buprenorphine in patients with cancer and noncancer pain: results of a retrospective cohort study. Clin Ther. 2005 Feb;27(2):225-37. https://doi.org/10.1016/j.clinthera.2005.02.012 PMID:15811486
12. Vadivelu N, Anwar M. Buprenorphine in postoperative pain management. Anesthesiol Clin. 2010 Dec;28(4):601-9. https://doi.org/10.1016/j.anclin.2010.08.015 PMID:21074740
13. Kumar S, Chaudhary AK, Singh PK, Verma R, Chandra G, Bhatia VK, et al. Transdermal buprenorphine patches for postoperative pain control in abdominal surgery. J Clin Diagn Res. 2016;10(6):UC05UC08. https://doi.org/10.7860/JCDR/2016/18152.7982
14. Albaqami MS, Alqarni AA, Alabeesy MS, Alotaibi AN, Alharbi HA, Alshammari MM, et al. Buprenorphine for acute post-surgical pain: A systematic review and meta-analysis. Saudi J Anaesth. 2023;17(1):65—71. https://doi.org/10.4103/sja.sja_822_22 PMID:37032687
15. Grant MC, Chappell D, Gan TJ, Manning MW, Miller TE, Brodt JL, et al.; PeriOperative Quality Initiative (POQI) and the Enhanced Recovery After Surgery (ERAS) Cardiac Society Workgroup. Pain management and opioid stewardship in adult cardiac surgery: Joint consensus report of the PeriOperative Quality Initiative and the Enhanced Recovery After Surgery Cardiac Society. J Thorac Cardiovasc Surg. 2023 Dec;166(6):1695-1706.e2. https://doi.org/10.1016/j.jtcvs.2023.01.020 PMID:36868931
16. Machado FC, Neto GC, Paiva LO, Soares TC, Nakamura RK, Nascimento LF, et al. [Transdermal buprenorphine for acute postoperative pain: a systematic review]. Braz J Anesthesiol. 2020;70(4):419-28. https://doi.org/10.1016/j.bjan.2020.04.004 PMID:32819729
17. Aguilar B, Penm J, Liu S, Patanwala AE. Efficacy and safety of transdermal buprenorphine for acute postoperative pain: a systematic review and metaanalysis. J Pain. 2023 Nov;24(11):1905- 14. https://doi.org/10.1016/j.jpain.2023.07.001 PMID:37442403
18. Mundipharma (NZ) Ltd. NORSPAN transdermal patch (buprenorphine) data sheet. 2023. Available from: https://www.wps.ac.nz/Portals/9/Documents/Buprenorphine-Norspanpatch

 ORCID
ORCID