Bernardita Valenzuela M. 1 , Constanza Yen L. 2 y David Torres P. 3
Rev. chil. anest. Vol. 43 Número 4 pp. 322-326|doi:
PDF|ePub|RIS
• Los beneficios potenciales (Reducciones de Riesgos Absolutas) son mayores en pacientes con alto riesgo de eventos adversos que en los que tienen un riesgo menor.
• En la toma de decisiones, también se debe incorporar la posibilidad de incurrir en daño al paciente.
• Los médicos clínicos pueden conocer y aplicar los resultados de los estudios a pacientes individuales calculando las diferencias de riesgo si se conocen o se pueden estimar los riesgos individuales de los eventos relevantes (con y sin tratamiento).
• Presentar los resultados como diferencia de riesgos hace que los beneficios y efectos adversos del tratamiento o intervención sean más fáciles de comparar.
• El número a tratar es una forma de medir riesgos versus beneficios que considera las consecuencias de tratar o no tratar: corresponde a número de pacientes al que se debiera administrar una terapia o intervención, para evitar que un paciente tenga un evento adverso en un período definido de tiempo.
• El número necesario para hacer daño es otra forma de medir riesgos versus beneficios que corresponde al número de pacientes que es necesario tratar para que experimenten un evento adverso.
La estadística no sólo es un tema árido para los médicos clínicos, sino para todos aquellos involucrados en la salud, incluyendo las autoridades. En 1967, D.L. Mahler presentó un artículo en Anesthesiology 1 , en que navegaba por las escabrosas aguas del Chi cuadrado, test de Fisher y la campana de Gauss, por nombrar lo más sencillo. Actualmente, la probabilidad que el análisis estadístico esté equivocado o no corresponda a lo medido es menor, ya que existen numerosos programas de acceso libre de análisis estadístico 2 , guías acerca de qué test estadístico a usar en determinada situación 3 , o simplemente una mayor interacción entre los estadísticos y los investigadores. Donde sí persisten problemas es en el análisis de los resultados, ya que si bien los resultados pueden ser los mismos, nuestra interpretación de estos depende de la manera en que nos son presentados 4 , 5 . Existe una serie de términos y conceptos que aparecen con frecuencia en la literatura y que no siempre son bien conocidos o comprendidos. Este artículo revisa varios de ellos para así facilitar su comprensión y contar con mejores herramientas para tomar decisiones que nos permitan dar a los pacientes un mejor cuidado.
No debe obviarse, sin embargo, que para saber interpretar los resultados, debemos asegurarnos antes que estos son correctos, que los estudios están bien realizados desde el punto de vista metodológico, tratar de deducir de la información presentada que están bien diseñados para contestar la pregunta que deben contestar y que tienen una baja probabilidad de presentar sesgos. Para contestar estas preguntas, que escapan a los objetivos de esta presentación, sugiero revisar otros artículos de este número o del anterior, o bien recurrir a los recursos disponibles en la red para evaluación de lectura crítica 6 , 7 . Buena parte de este artículo resume conceptos de Series de Medicina Basada en la Evidencia que han sido publicadas en British Medical Journal 8 , JAMA 9 y Canadian Medical Association Journal 10 .
Los objetivos específicos son:
-
Aprender a determinar las tasas de evento de los grupos tratados y los grupos control.
-
Aprender a determinar reducciones de riesgo relativas y absolutas.
-
Entender cómo las reducciones de riesgo se aplican a distintas poblaciones.
-
Aprender a utilizar la reducción de riesgo relativo para estimar el riesgo de un paciente individual.
-
Aprender a usar las diferencias de riesgo para evaluar si los beneficios del tratamiento superan al eventual daño.
-
Comprender el concepto de número necesario para tratar (NNT) y saber cómo se calcula a partir de la diferencia de riesgos.
-
Familiarizarse con el concepto de NNT, comparando el NNT de distintas intervenciones.
-
Interpretar el NNT y comprender cómo se modifica en función de las preferencias de los pacientes.
RIESGO Y REDUCCIÓN DE RIESGO
Algunas definiciones:
Tasa de evento : (o incidencia) el número de pacientes que presentan un evento como proporción del número de pacientes en la población estudiada. (x/población estudiada).
Riesgo Relativo (RR): Relación entre las tasas de eventos entre 2 grupos, con el grupo no tratado como denominador (tasas de eventos en grupo intervención/ tasa de eventos en grupo control).
Reducción de riesgo relativo (RRR): La diferencia en las tasas de eventos entre 2 grupos, expresado como proporción de la tasa de evento en el grupo no tratado. (1-RR).
Reducción de riesgo absoluto (RRA): Diferencia aritmética entre 2 tasas de eventos (tasa de evento en grupo intervención-tasa de eventos en grupo control).
Imagine que un vendedor de productos médicos le presenta una nueva droga que reduce la incidencia de náuseas y vómitos postoperatorios (NVPO), y para entusiasmarlo le muestra el gráfico de la Figura 1, que muestra una RRR de 25% (diferencia de tasas de NVPO 40%-30%). Sin embargo, el vendedor tuvo la precaución de no mostrarle otro estudio, que evaluaba la RRR en pacientes de bajo riesgo, donde la RRR es de sólo 2,5% (10%-7,5%). Entre los pacientes de alto riesgo en el estudio 1, la tasa de eventos en el grupo control es de 40% y en el tratamiento de 30%. La RRA (o diferencia de riesgo absoluto) es la diferencia entre las tasas de NVPO (40%-30% = 10%). RRR (o reducción de riesgo relativo) es la disminución proporcional en la tasa de evento que recibe el tratamiento (Figura 1).
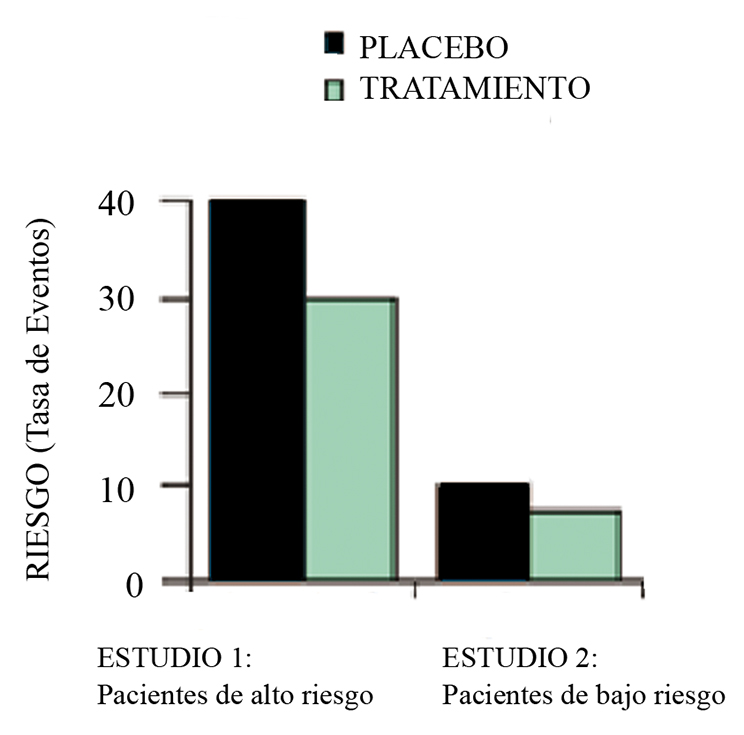
Figura 1 Resultados de un estudio hipotético de NVPO. Izquierda (Estudio 1): pacientes de alto riesgo de NVPO: Tasa de evento de 40% que se reduce a 30% con el tratamiento, dando una RRR de 25% (10% desde 40%). Derecha (Estudio 2): pacientes de bajo riesgo de NVPO: Tasa de eventos de sólo 10% que se reduce a 7,5% con tratamiento, dando una RRR también de 25%, pero con una diferencia de riesgo absoluto de 2,5%.
En el ejemplo, la tasa de NVPO en el grupo tratamiento es 25% menos que en el grupo control (la RRA de 10% como proporción de la tasa de evento del grupo control es de 10/40 ó 25% menos). En los pacientes de bajo riesgo del estudio 2, la tasa de NVPO en el grupo control es de sólo 10%. La tasa de NVPO en el grupo tratado, es de 7,5%, que es una RRR de 25%, pero con una diferencia de riesgo absoluto de 2,5%. Ambos grupos tienen la misma RRR, pero en términos absolutos, el beneficio en los pacientes de bajo riesgo es mucho menor.
Se puede observar que la RRA se hace más pequeña cuando la tasa de evento es menor, mientras la RRR, o la “eficacia” del tratamiento a menudo permanece constante. Esto puede influir en el diseño de los ensayos clínicos. El medicamento se estudia en pacientes de muy alto riesgo, en los que la RRA es más impresionante, pero finalmente es comercializado para pacientes con menor riesgo, en los cuales su beneficio es significativamente menor. Esto subraya la importancia de considerar ambas cifras en el momento de decidir la administración de un medicamento.
BENEFICIOS Y EFECTOS ADVERSOS
Cuando se indica un medicamento, se debe conocer los potenciales beneficios y el eventual daño que puedan causar. Quedó claro que los beneficios potenciales (Reducciones de Riesgo Absolutas) serán mayores en pacientes con alto riesgo de eventos adversos que en los que tienen un riesgo menor. Sin embargo, en la toma de decisiones, también debemos incorporar la posibilidad de incurrir en daño al paciente.
Imagine que trabaja en una maternidad y que debe administrar anestesia para cesárea en dos pacientes. Laura es una mujer de 22 años, sana, con un embarazo de término y una cesárea anterior hace 2 años, sin incidentes. Usted estima en 2% su riesgo de presentar una cefalea post punción dural (CPPD) 11 . En ella, usted quiere probar un nuevo trocar de anestesia espinal que tiene una reducción del riesgo relativo de CPPD de 30%, de acuerdo a ensayos clínicos aleatorizados publicados recientemente. Más tarde, llega Julieta, mujer de 24 años, embarazada de término, con una escoliosis moderada, que en su embarazo anterior recibió anestesia espinal e hizo un cuadro de CPPD; usted estima que la probabilidad que sufra una nueva CPPD, es de 20% 12 .
De este modo, se debe decidir si se ocupa el trocar nuevo en ambas pacientes o si el beneficio es mayor en una de ellas. Una manera de determinar el potencial beneficio del nuevo tratamiento es completar una tabla de beneficios, como la Tabla 1. Del análisis de la Tabla, queda claro que el beneficio para los pacientes de alto riesgo es mucho mayor, diez veces, que en los de bajo riesgo.
Tabla 1 Tabla de beneficios
|
Tasa de evento de CPPD (%) |
|||
|
Grupo de pacientes |
Sin tratamiento (Trocar tradicional) |
Con tratamiento (trocar “nuevo”) |
RRA (Trocar tradicional-trocar nuevo) |
|
Bajo riesgo (Ej. Laura) |
2% |
1,4% |
0,6% |
|
Alto riesgo (Ej. Julieta) |
20% |
14% |
6% |
A continuación es necesario estimar el daño del nuevo trocar, pues de los ensayos clínicos se desprende que su uso aumenta la probabilidad de punción no exitosa 5 veces (riesgo relativo de 5). Un estudio previo mostró que el riesgo de punción no exitosa con el trocar tradicional era de 0,1%. Ahora, se agrega esta información a una nueva tabla de daños y beneficios (Tabla 2).
Tabla 2 Tabla de efectos adversos y beneficios
|
Tasa de evento de CPPD |
Tasa de evento de punción No exitosa |
|||||
| Grupo de pacientes |
Sin tratamiento (Trocar tradicional) |
Con tratamiento (Trocar “nuevo”) |
RRA (Trocar tradicional-trocar nuevo) |
Sin tratamiento (Trocar tradicional) |
Con tratamiento (Trocar “nuevo”) |
Aumento de riesgo absoluto (Trocar nuevo-trocar tradicional) |
| Bajo riesgo (Ej. Laura) |
2% |
1,3% |
0,7% |
0,1% |
0,5% |
0,4% |
| Alto riesgo (Ej. Julieta) |
20% |
13% |
7% |
0,1% |
0,5% |
0,4% |
¿Se debe ocupar el nuevo trocar? Al tomar la decisión, debe tenerse presente que no existe una sola respuesta y esta puede estar influenciada por factores que no se están discutiendo en esta presentación, que serán omitidos para no hacer más complejo el ejercicio. Para responder esta pregunta, se debe hacer un análisis similar a este: Laura tiene un pequeño beneficio (RRA 0,7%) al usar el nuevo trocar, pero se expone a un aumento de riesgo de punción fallida de 0,4%, lo que prácticamente equipara los riesgos y los beneficios. Julieta, por otro lado tiene un beneficio potencial mucho mayor (RRA de 7%) que el eventual riesgo de punción fallida (0,4%). Por lo tanto, es probable que el nuevo trocar beneficie más a Julieta (que tiene mayor riesgo basal) que a Laura (que tiene menor riesgo basal). La decisión final depende, en último término, del valor que los pacientes le den a reducir su tasa de CPPD o a sufrir una punción fallida. Muchos pacientes están más preocupados de lo primero, aunque algunas embarazadas no quieren recibir anestesia general por ningún motivo.
En resumen:
-
Los médicos clínicos pueden conocer y aplicar los resultados de los estudios a pacientes individuales calculando las diferencias de riesgo si se conocen o se pueden estimar los riesgos individuales de los eventos relevantes (con y sin tratamiento).
-
Presentar los resultados como diferencia de riesgos hace que los beneficios y efectos adversos del tratamiento o intervención sean más fáciles de comparar.
NÚMERO NECESARIO A TRATAR (NNT)
Otra manera de medir riesgos y beneficios es el NNT, que considera las consecuencias de tratar o no tratar. El NNT es el número de pacientes al que se debiera administrar una terapia o intervención, para evitar que un paciente tenga un evento adverso en un período definido de tiempo.
Por ejemplo, si el NNT para el droperidol en profilaxis de NVPO es de 8, significa que debemos administrar la dosis de droperidol a 8 pacientes, para que 1 se beneficie. Dicho de otro modo, la probabilidad de beneficiarse del uso de droperidol como profilaxis es de 1/8.
El NNT se calcula como el inverso del riesgo relativo absoluto, cuando está expresado como proporción (1/RRA). Si el riesgo está expresado como porcentaje, la fórmula es 100/RRA.
Si la reducción de riesgo absoluto es grande, se necesita tratar un pequeño número de pacientes para que varios se beneficien; por el contrario, si es pequeña, se deben tratar muchos pacientes para observar un beneficio en unos pocos. De la misma forma, se puede determinar el número de pacientes que es necesario tratar para que experimenten un evento adverso. Este es el número necesario para hacer daño (NNH, por sus siglas en inglés), que es el inverso del aumento de riesgo absoluto (1/aumento riesgo absoluto). Como se podrá deducir de los ejemplos anteriores, el NNT depende de la reducción de riesgo absoluto, el que a su vez depende del riesgo basal y de la reducción de riesgo relativo.
En la Tabla 3 se puede apreciar algunos ejemplos de situaciones comunes para el anestesiólogo, extraídos de la literatura.
Tabla 3 Tabla de beneficios para pacientes en anestesia
|
Tasa de eventos |
||||
| Pregunta clínica |
Grupo control |
Grupo tratamiento |
RRA (%) |
NNT |
| ¿Cuál es la reducción de riesgo de vómitos postoperatorios con ondansetrón en paciente con alto riesgo? 13 |
44,9% |
30,8% |
14,1% |
7 |
| ¿Cuál es la reducción de riesgo de awareness con el uso de BIS en pacientes de alto riesgo? 14 |
0,62% |
0,19% |
0,43% |
233 |
| ¿Cuál es la reducción de CPPD cuando utilizo un trocar punta lápiz 25 en vez de un biselado 25 en embarazadas? 15 |
8,7% |
3,1% |
5,1% |
18 |
Generalmente, los médicos tenemos dificultades para determinar el riesgo basal de poblaciones específicas, lo que puede subestimar o sobreestimar el efecto del tratamiento 16 . Por ejemplo, si en determinada población de pacientes de cirugía no cardiaca estimamos equivocadamente el riesgo de infarto en un 40%, se sobreestimará el beneficio del tratamiento con beta bloqueadores que produce una reducción de riesgo relativo de infarto de 26%, ya que el riesgo basal real de infarto es de 5,7% (Tabla 4) 17 .
Tabla 4 Estimaciones de riesgo basal de infarto en cirugía vascular
| Riesgo |
Riesgo basal estimado |
RRA, % |
NNT estimado |
Riesgo basal real |
RRA, % |
NNT real |
| Riesgo de infarto en cirugía no cardiaca en riesgo de enfermedad ateroesclerótico 17 |
40% |
10,4% |
10 |
5,7% |
1,5% |
67 |
En este momento, se debe determinar cuál NNT es razonable o NNT Umbral 18 , o en otras palabras, cuál es el NNT mínimo que usted o su paciente aceptarán para justificar los beneficios y los riesgos del tratamiento o intervención. Si el NNT calculado está sobre el umbral, los beneficios no son lo suficientemente grandes (o los riesgos son muy altos) para justificar iniciar el tratamiento o intervención. El NNT Umbral está determinado por varios factores, que incluyen las preferencias individuales de los pacientes, la severidad del evento adverso que quiere ser evitado y los costos y los efectos adversos de la intervención. Es casi seguro que este NNT umbral será distinto para los distintos pacientes y que no existe una sola respuesta a la pregunta de cuando el NNT es lo suficientemente bajo como para justificar el tratamiento.
En resumen:
-
El NNT es una manera sencilla y clínicamente útil de presentar el efecto o resultado de la intervención.
-
El NNT se puede calcular fácilmente a partir de la diferencia de riesgo.
-
Debemos tener cuidado en no sobreestimar el efecto de los tratamientos, y por lo tanto, subestimar el NNT.
CONCLUSIONES
La capacidad de interpretar y calcular la reducción de riesgo relativo, las diferencias de riesgo y el NNT a partir de los datos publicados en ensayos clínicos o revisiones sistemáticas es una habilidad esencial para aplicar la evidencia clínica al cuidado de pacientes individuales. Estos conceptos han sido descritos, definidos y presentados con ecuaciones y Tablas para ayudar a superar los problemas más comunes en su aprendizaje.
REFERENCIAS
- Mahler DL. Elementary statistics for the anesthesiologist. Anesthesiology 1967; 28: 749-759.
- Epi Info Versión 3.5.1. 2008 [updated 2008]. Disponible en www.cdc.gov/epiinfo/.
- Choosing the Correct Statistical Test. Disponible en http://bama.ua.edu/~jleeper/627/choosestat.html.
- Forrow L, Taylor WC, Arnold RM. Absolutely relative: how research results are summarized can affect treatment decisions. Am J Med. 1992; 92: 121-124.
- Naylor CD, Chen E, Strauss B. Measured enthusiasm: does the method of reporting trial results alter perceptions of therapeutic effectiveness? Ann Intern Med. 1992; 117: 916-921.
- Critical Appraisal Skills Programme. Disponible en www.phru.nhs.uk/pages/phd/casp.htm.
- Centre for Evidence Based Medicine. Disponible en www.cebm.net.
- Guyatt GH, Juniper EF, Walter SD, et al. Interpreting treatment effects in randomized trials. BMJ 1998; 316: 690-693.
- Oxman AD, Sackett DL, Guyatt GH. The Evidence-Based Medicine Working Group. Users’ Guides to the Medical Literature: I. How to Get Started. JAMA.1993; 270: 2093-2095.
- Barratt A, Wyer PC, Hatala R, et al. Tips for learners of evidence-based medicine: 1. Relative risk reduction, absolute risk reduction and number needed to treat. CMAJ. 2004; 171: 353-358.
- Turnbull DK, Shepherd DB. Post-dural puncture headache: pathogenesis, prevention and treatment. Br J Anaesth. 2003; 91: 718-729.
- Amorim JA, Valenca MM. Postdural puncture headache is a risk factor for new postdural puncture headache. Cephalalgia. 2008; 28: 5-8.
- Carlisle JB, Stevenson CA. Drugs for preventing postoperative nausea and vomiting. Cochrane Database Syst Rev. 2006; 3: CD004125.
- Punjasawadwong Y, Boonjeungmonkol N, Phongchiewboon A. Bispectral index for improving anaesthetic delivery and postoperative recovery. Cochrane Database Syst Rev. 2007 (4): CD003843.
- Vallejo MC, Mandell GL, Sabo DP, Ramanathan S. Postdural puncture headache: a randomized comparison of five spinal needles in obstetric patients. Anesth Analg. 2000; 91: 916-920.
- Chatellier G, Zaplet al E, Lemaitre D, et al. The number needed to treat: a clinically useful nomogram in its proper context. BMJ. 1996; 312: 426-429.
- Devereaux PJ, Yang H, Yusuf S, et al. Effects of extended-release metoprolol succinate in patients undergoing non-cardiac surgery (POISE trial): a randomised controlled trial. Lancet. 2008; 371: 1839-1847.
- Sinclair JC, Cook RJ, Guyatt GH, et al. When should an effective treatment be used? Derivation of the threshold number needed to treat and the minimum event rate for treatment. J Clin Epidemiol. 2001; 54: 253-262.
