Fernando Aranda G.*
Reve Chil Anest Vol. 42 Número 1 pp. 26-32|doi:
PDF|ePub|RIS
INTRODUCCIÓN
Hay muchos estudios que han demostrado que la optimización del paciente y los apropiados cuidados perioperatorios disminuyen sustancialmente la mortalidad quirúrgica. Dentro de las estrategias a seguir se consideran:
-
La estratificación de riesgos del paciente, identificando los grupos de alto riesgo.
-
Realizar alguna intervención específica, tal como, la administración de beta-bloqueadores o de estatinas en el preoperatorio.
-
La optimización de la entrega de oxígeno en el perioperatorio, objetivo de todo nuestro monitoreo perioperatorio.
-
Una anestesia que limite la respuesta al stress, la respuesta inflamatoria y la activación de la coagulación.
-
Cuidados postoperatorios adecuados a la situación, que mantengan la guardia y el manejo propuesto.
-
Un enfoque multimodal, considerando el entrenamiento, la seguridad, la experiencia, las evaluaciones continuas y un volumen adecuado de procedimientos, son factores también a considerar para mejorar el rendimiento de los resultados quirúrgicos.
Si bien la mortalidad quirúrgica es de alrededor de un 0,8% en todo tipo de cirugías, aquélla atribuible al proceso anestésico es probablemente de 1 por cada 250.000 anestesias1. Sin embargo, esto no considera los pacientes que fallecen en el postoperatorio, que son muchos más, de los cuales un 20% son ASA I o II y cerca de un 40% son ASA III 1 .
-
¿Cómo identificar los pacientes de alto riesgo?
Algunos pacientes pueden ser identificados en el preoperatorio, combinando factores como la edad, comorbilidades, su patología principal, el tipo de cirugía y los estudios realizados. A pesar de todo, un grupo tendrá complicaciones en el intraoperatorio. En un estudio hecho en pacientes geriátricos se logró determinar que la mayoría de los pacientes que tenían mayor mortalidad en el postoperatorio a los 30 días, eran aquéllos que sufrieron eventos adversos que se identificaron en las primeras 24 horas después de la cirugía 2 , indicando la importancia de la continuidad en los cuidados perioperatorios.
-
¿Cuáles son los eventos que podríamos evitar?
Esencialmente los eventos cardíacos mayores como la muerte cardíaca, el infarto miocárdico agudo (IAM) no fatal, el paro cardíaco no fatal, los accidentes vasculares cerebrales (AVC) y la confusión del postoperatorio. Una amplia revisión hecha por Deveraux muestra que aproximadamente 4% de pacientes con factores de riesgo cardiovasculares bajo cirugía no cardíaca experimentan un evento cardíaco mayor 3 .
OPTIMIZACIÓN DEL PERIOPERATORIO POR MEDIO DE BETA-BLOQUEADORES Y ESTATINAS
-
1. La Importancia del uso de beta-bloqueadores (BB) en el control de la frecuencia cardíaca
Una frecuencia cardíaca (FC) elevada es un factor independiente de morbi-mortalidad en pacientes sanos con o sin hipertensión arterial (HTA), en pacientes con enfermedad coronaria, infarto al miocardio e insuficiencia cardíaca congestiva (ICC). Incluso ha sido un factor predictor de mortalidad más fuerte que una mala función ventricular 4 (Figura 1). Este concepto implica que un aumento en la FC no sólo es reflejo de una depresión de la función ventricular en un paciente con ICC, sino que también puede contribuir al aumento de la falla cardíaca.
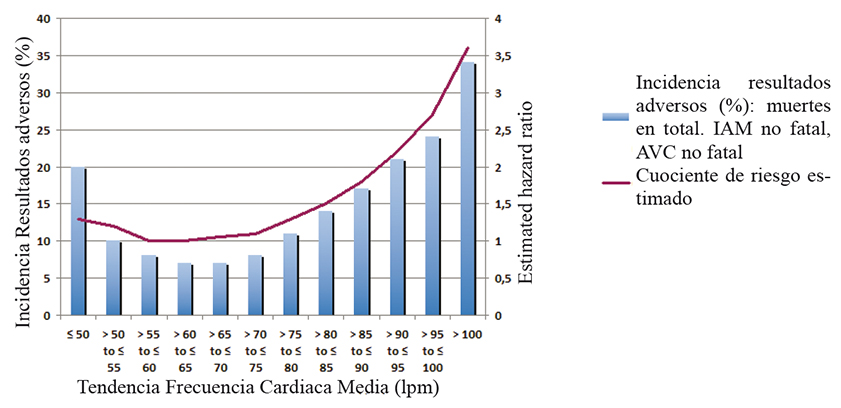
Figura 1 Impacto de la frecuencia cardíaca (FC) en paciente hipertensos y con cardiopatía coronaria (Modificado de: Kolloch R, Legler UF, Champion A, et al. Impact of resting heart rate on outcome in hypertensive patients with coronary artery disease: International Verapamil–SR/trandolapil STudy (INVEST). Eur Heart J 2008; 29: 1327-34).
Varios reportes han mostrado la utilidad del uso de BB en disminuir la morbi-mortalidad en pacientes con IAM o ICC. Entonces, el aumento de la FC debe ser visto al igual que otros factores de riesgo cardiovascular, tales como: HTA, dislipidemia, tabaquismo, disfunción miocárdica y diabetes. Se ha notado que este efecto protector es más marcado en pacientes con FC elevada en reposo antes del tratamiento, y se ha demostrado una disminución efectiva de la FC, demostrando que este es el efecto principal del BB, lo cual también ha sido observado con antagonistas del calcio 5 .
El grupo más beneficiado del control de la FC en el perioperatorio son los pacientes coronarios programados para cirugía no cardíaca, particularmente aquéllos que son sintomáticos y aquéllos programados para cirugía vascular 6 .
Se deben tomar precauciones en relación al momento en que se inicia el beta-bloqueo, especialmente en los pacientes de alto riesgo (quiénes son los que más se pueden beneficiar del control de la FC). En efecto, la iniciación del BB en el preoperatorio inmediato ha resultado en un aumento de la morbi-mortalidad como lo demostró el estudio POISE. Esto ha mostrado la principal dificultad del BB, la cual es, encontrar la dosis adecuada para evitar la bradicardia e hipotensión aguda cuando se asocia a los anestésicos y los efectos de la cirugía 7 .
-
1.1. Importancia de la Frecuencia Cardíaca
Es comúnmente conocido que los mamíferos pequeños tienen FC más elevadas y una expectativa de vida más corta que los mamíferos más grandes. Esto se explica porque la relación entre la pérdida de calor (como función de la superficie corporal) y la producción de calor (como función de la masa corporal) aumenta al disminuir el tamaño corporal 8 . Esto se ha visto que condiciona en los mamíferos su expectativa de vida.
Extrapolando lo anterior al ser humano, se ha demostrado que la frecuencia cardíaca en reposo (FCR) se correlaciona con la morbilidad cardiovascular y con la expectativa de vida 9 , 10 . El tono vagal dado por el sistema nervioso parasimpático, juega un rol importante en la recuperación de la FC y en la variabilidad de la FC tras el ejercicio 11 . Un aumento de la FCR refleja una disminución del tono parasimpático o un aumento del tono simpático, o de ambos 12 .
En el corazón normal, el ejercicio induce activación del tono simpático y un aumento de la FC, lo que lleva a una aumento de la presión arterial (PA) y aumento de la resistencia vascular periférica, con un aumento del consumo miocárdico de oxígeno. Así, el sistema nervioso autónomo regula la FC y el gasto cardíaco en función de las demandas del organismo.
Tanto la relajación miocárdica como la contracción se asocian a una alta utilización de ATP. Esto en conjunto a altos niveles de estrés oxidativo, acarreará un envejecimiento celular y otros mecanismos de enfermedad cardiovascular, como la aterosclerosis y la falla cardíaca. Tan solo la reducción de 10 latidos por minuto en la FC, lleva a un ahorro de un 15% en el ATP al día para el corazón, asociándose a una disminución en el estrés oxidativo 13 .
Una FCR elevada ha sido considerada como un factor pronóstico de importancia en morbi-mortalidad de pacientes coronarios 14 , tal como se ha demostrado en el estudio CASS publicado en el año 2005, y corroborado en otras poblaciones como pacientes con ICC, diabetes e HTA 15 . Sin embargo, en la población general, el factor de tener una alta FCR también es de relevancia en la morbi-mortalidad como se demostró en el estudio Framingham del año 1987 16 .
-
1.2. Fisiopatología del daño cardíaco frente a la taquicardia
Al aumentar la FC se produce un desbalance entre la entrega y la demanda de oxígeno, lo que a nivel cardíaco puede desarrollar isquemia y remodelamiento crónico. Frente a esto, una FC baja puede elevar el umbral de isquemia y mejorar la performance miocárdica (Figura 2).
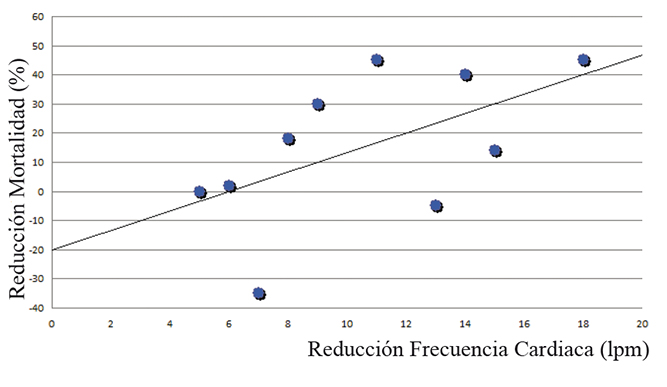
Figura 2 Importancia del control frecuencia cardíaca en la Mortalidad por Infarto Agudo al Miocardio. (Modificado de: Kjekshus JK. Importance of heart rate in determining beta-blocker efficacy in acute and long-term acute myocardial infarction intervention trial. Am J Cardiol 1986, 57: 43F-49F).
Al aumentar el tono del sistema nervioso simpático (SNS) aumenta la FC y la PA. Este aumento en la resistencia vascular periférica (RVP) aumentará el trabajo miocárdico (Figura 3). El aumento de la FC disminuirá la duración del diástole afectando la perfusión miocárdica, siendo el factor precipitante de una isquemia miocárdica en un paciente con coronariopatía, y a la larga, alterando la función contráctil. Este aumento de la FC en un corazón normal sólo resulta en un aumento del flujo sanguíneo coronario (dada la preservación de la función vasodilatadora del endotelio) 17 .
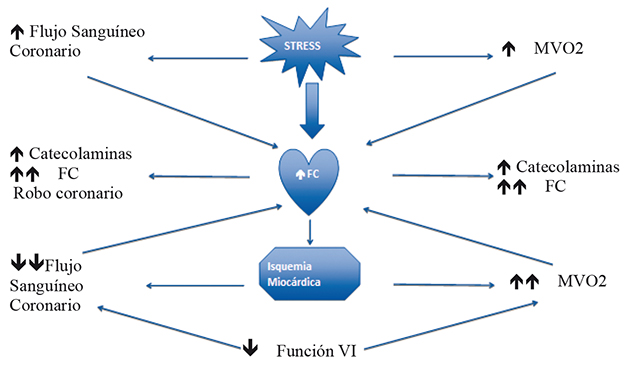
Figura 3 Fisiopatología del aumento de la Frecuencia Cardíaca y la Isquemia Miocárdica. FC: Frecuencia Cardíaca. MVO2: Consumo Miocárdico de Oxígeno. VI: Ventrículo Izquierdo.
Otro factor a considerar es que, el aumento de la FC está relacionado con el “shear stress” o estrés tangencial de las coronarias. Una alta FCR se ha asociado a un alto estrés de aceleración y desaceleración en los vasos induciendo el estrés oxidativo, disfunción endotelial y aceleración de la aterogénesis. El mecanismo envuelto está parcialmente comprendido, incluyendo una reducción en la compliance vascular y aumento de la inflamación, facilitando la disrupción de una placa de ateroma en un paciente coronario y acelerando la enfermedad.
Al aumentar la FC en el vaso, se prolonga el tiempo de distención, aumentando la exposición del endotelio a partículas aterogénicas; así, más áreas de la íntima estarán expuestas a fluctuaciones de estrés quedando más proclive a la formación de placas de ateromas 18 , 19 .
Bajo condiciones normales, la perfusión miocárdica durante la fase de relajación isovolumétrica es más alta en el lado coronario izquierdo (Figura 4), sin embargo, la arteria coronaria derecha muestra una dominancia de flujo en sístole 20 . Por esta razón, una disminución del diástole por un aumento en la FC causará una disminución en la perfusión del lado izquierdo. Así también, una hipotensión causará una reducción en el flujo de ambas coronarias. Este mecanismo es ciertamente el principal involucrado en la reducción de la perfusión miocárdica.
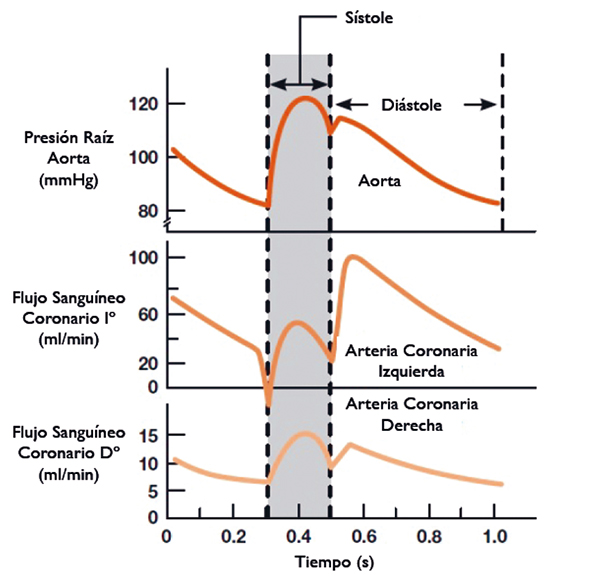
Figura 4 Flujo Sanguíneo Coronario.
Se suma al factor anterior la disfunción diastólica que será otro evento que redundará en una disminución de la perfusión miocárdica. Así, en pacientes coronarios, la disminución de la presión intraventricular después del cierre de la válvula aórtica será más lenta, aumentando las presiones telediastólicas del ventrículo izquierdo, causando una hipoperfusión del subendocardio y una eventual isquemia 20 .
Algunas enfermedades que resulten en una alteración de la relajación ventricular como la diabetes, HTA y estenosis aórtica pueden facilitar que ocurra esta hipoperfusión subendocárdica.
-
1.3. Aplicación Clínica
La isquemia perioperatoria ocurre principalmente al final de la cirugía y en las horas posteriores hasta el tercer o cuarto día del postoperatorio, y muy rara vez en el intraoperatorio. Al ocurrir la isquemia, esta puede ser por dos mecanismos 21 :
-
En presencia de una estenosis crítica de las coronarias.
-
En ausencia de estenosis.
Estas dos condiciones causan dos tipos de IAM en el período perioperatorio: IAM Tipo 1 y Tipo 2, de acuerdo a la clasificación actual 22 . Ellos ocurren casi con la misma frecuencia, con la diferencia que los IAM Tipo 2 ocurren más frecuentemente cerca del segundo día del postoperatorio. La influencia de la taquicardia en la génesis del IAM puede ser fácilmente comprendida según la explicación precedente.
Hay muchas situaciones del perioperatorio que pueden causar taquicardia: dolor, hipotensión, sangrado, ayuno, anemia, el estrés inducido por la cirugía, alergias, etc. La activación del SNS produce una elevación de los niveles de catecolaminas y del cortisol plasmáticos, que pueden causar la fisura de una placa de ateroma y una trombosis posterior ocasionando isquemia. En el caso de no existir una trombosis, la taquicardia juega un rol fundamental en el desbalance energético miocárdico 22 .
La mayor razón de la subutilización de los BB en el escenario perioperatorio radica esencialmente en los temores relacionados con el riesgo y el beneficio: alteraciones de la conducción, empeoramiento de la función ventricular izquierda y aumento de la broncoconstricción en asmáticos. Sin embargo, el uso crónico de BB ha mejorado sustancialmente el pronóstico de pacientes con antecedentes de ICC y post IAM. Es por esto que su efecto terapéutico debe ser cuidadosamente vigilado, caso a caso, sobre todo en el contexto de pacientes de alto riesgo sometidos a intervenciones electivas. En el caso de pacientes de urgencia el uso de BB de vida media corta (como esmolol) puede ayudar a testear su tolerancia.
-
1.4. Betabloqueadores y la evidencia clínica.
A pesar del “factor Poldermans”, donde se desvirtuó parte de la evidencia disponible en relación a la utilidad de los BB en el contexto perioperatorio, hay situaciones en las cuales los BB han demostrado tener su lugar 23 – 26 :
-
La administración de BB en el perioperatorio pueden disminuir la incidencia de complicaciones cardiovasculares mayores en pacientes de alto riesgo en cirugía no cardíaca. La identificación de estos pacientes debe ser acuciosa.
-
Pacientes con terapia crónica con BB deberían mantener su tratamiento.
-
El uso de BB en pacientes de riesgo debe iniciarse lo más precozmente posible en el preoperatorio, dando la posibilidad para una titulación adecuada, manteniendo una frecuencia cardíaca entre 60 y 80 latidos por minuto. No se recomienda el inicio del beta bloqueo muy cercano a la fecha de la intervención quirúrgica.
-
Dada la evidencia actual, se deben preferir en el preoperatorio BB de vida media larga.
-
Los BB deben ser administrados con precaución en el postoperatorio, teniendo presente que pueden enmascarar otros fenómenos como dolor, déficits de volemia, fiebre, etc.
-
Los BB pueden ser usados en situaciones de hiperdinamia (taquicardia, taquiarritmia, hipertensión arterial) siempre y cuando, este no sea un mecanismo adaptativo a una situación subyacente (ICC aguda, sepsis, superficialidad anestésica, etc.).
-
2. Las Estatinas como ayuda al control de la reacción inflamatoria del perioperatorio
-
2.1. Importancia
El uso de estatinas es muy amplio y forma parte del tratamiento de muchos pacientes que se intervendrán quirúrgicamente. Hay suficiente evidencia de su efecto benéfico en la disminución de los lípidos, incluyendo el riesgo perioperatorio de complicaciones cardíacas, y en la sepsis 32 .
-
2.2. Mecanismo de acción
Las estatinas que se utilizan ampliamente para disminuir el colesterol LDL, han demostrado disminuir un número importante de accidentes cardiovasculares. El mecanismo por el cual estas drogas pueden ser cardio o neuro-protectoras es variado 27 , 28 :
-
Actúan como scavengers o “basureros” de radicales superóxidos.
-
Efectos antitrombóticos: tienen efectos pleiotrópicos muy valorados en los pacientes vasculares. Tendrían acción en el aumento del óxido nítrico endotelial 32 .
-
Efectos antiinflamatorios: producen una reducción de la concentración plasmática de las citoquinas inflamatorias como el TNFα y la interleukina 6 36 .
-
Producen una disminución de la apoptosis endotelial 36 .
-
2.3. Aplicaciones clínicas
Existen numerosas publicaciones estos últimos años buscando los eventuales beneficios de las estatinas en cirugía no cardíaca, sin embargo, la evidencia actual más fuerte apoya solamente el hecho que los pacientes que están tomando estatinas previamente, deben continuar su tratamiento.
El efecto antiinflamatorio se ha demostrado en el contexto de:
-
Sepsis: disminuyendo la mortalidad en Cuidados Intensivos.
-
Nefropatía en diabéticos: disminuyendo el daño renal.
-
Enfermedad de Alzheimer y demencia: disminuyendo la incidencia y progresión 32 .
-
Artritis reumatoide y enfermedades autoinmunes: produciendo efectos clínicos beneficiosos,
-
Enfermedades gastrointestinales, disminuyendo la incidencia del cáncer de colon y enfermedades inflamatorias del intestino.
-
Trasplantes: disminuyendo la incidencia de rechazos.
Un estudio realizado en pacientes sometidos a cirugía endovascular de la aorta no demostró que el uso de estatinas en el preoperatorio tuviera un efecto protector frente a una insuficiencia renal aguda 31 .
-
2.4. Efectos colaterales
Como toda droga, las estatinas pueden producir efectos colaterales que no pueden ser ignorados; la mayoría de los efectos adversos incluyen mialgias y rabdomiolisis con serios problemas hepáticos.
Las estatinas pueden acrecentar el daño muscular inducido por succinilcolina, evidenciado por un aumento de las concentraciones de mioglobina plasmática. Sin embargo, no se ha demostrado una relevancia clínica 35 .
Incluso, se ha reportado que las estatinas pueden causar un aumento del riesgo de sufrir un accidente vascular cerebral hemorrágico 32 , 34 .
-
2.5. Estatinas y la evidencia clínica
Está actualmente demostrado que la suspensión de la estatinas por más de 4 días es un predictor independiente de eventos miocárdicos en el postoperatorio 33 .
Un meta-análisis del Cochrane Summaries demuestra que en cirugía cardíaca el uso previo de estatinas producen una disminución de la incidencia de fibrilación auricular postoperatoria y una menor estadía en la UCI 29 , 37 . Si bien los pacientes pretratados con Estatinas presentaron menor tasa de IAM y falla renal, estos resultados no alcanzaron significancia estadística. Más aún, la terapia con estatinas no tienen impacto en la mortalidad a corto plazo o la incidencia de accidente vascular cerebral postoperatorio. No se han reportado efectos adversos importantes por estatinas previo a cirugía cardíaca. Sin embargo, estos resultados no pueden generalizarse a la cirugía no cardíaca.
A pesar todo, el uso de estatinas y BB está incluido en las recomendaciones para disminuir el riesgo de accidente vascular cerebral perioperatorio tanto en cirugía cardíaca como no cardíaca: 23 , 30 , 32 , 34 .
-
Recomendación Clase I:
-
En aquellos pacientes que usan estatinas en forma habitual y se presentan par una cirugía no cardíaca, las estatinas deben ser continuadas. (Nivel de Evidencia B).
-
-
Recomendación Clase IIa:
-
En pacientes programados para cirugía vascular con o sin factores de riesgo, el uso de estatinas es razonable. (Nivel de Evidencia B).
-
-
Recomendación IIb:
-
En pacientes con al menos 1 factor de riesgo y programados para un procedimiento de riesgo intermedio, debe considerarse el uso de estatinas. (Nivel de Evidencia C).
-
En relación al tiempo de inicio previo a la cirugía, no existe aún consenso, existiendo reportes que inician la terapia entre 14 días a un mes previo a la intervención. En relación a la dosis recomendada, no hay estudios que demuestren una curva de dosis-respuesta para evaluar riesgos versus beneficios 32 .
CONCLUSIÓN
El perioperatorio de un paciente de riesgo puede ser optimizado considerando técnicas y drogas que nos ayuden a controlar la respuesta al estrés y la respuesta inflamatoria. Dentro de este marco los bloqueadores beta adrenérgicos y las estatinas tienen un rol destacado, ayudando a disminuir las complicaciones incluso a largo plazo.
REFERENCIAS
- Goldhill D. Preventing surgical deaths: critical care and intensive care outreach services in the post-operative period. Br J Anesth 2005; 95: 88-94.
- Khuri SF, Henderson WG, De Palma RG, et al. Determinants of long-term survival after mayor surgery and the adverse effect of postoperative complications. Ann Surg 2005; 242: 326-341.
- Devereaux PJ, Goldman L, Cook DJ, et al. Perioperative cardiac events in patients undergoing noncardiac surgery: a review of the magnitude of the problema, the pathophysiology of the events and the methods to estimate and communicate risk. Can Med Assoc J 2005; 173: 627-634.
- Dyer AR, Persky V, Stamler J, et al. Heart rate is a prognostic factor for coronary heart disease and motality: findings of three Chicago epidemiologic studies. Am J Epidemiol 1980; 112: 736-749.
- López-Sendón J, Swedbelg K, Mc Murray J, et al. Expert consensus document on B-adrenergic receptor blockers. Eur Heart J 2004; 25: 1341-1362.
- Task Force for Preoperative Cardiac Risk Assesment and Perioperative Cardiac Mangement in Non-cardiac Surgery; European Society of Cardiology (ESC): Poldermans D, Bax JJ, Boersma E, et al. Guidelines for pre-operative cardiac risk assessment and perioperative cardiac management in non-cardiac surgery. Eur Heart J 2009; 30: 2769-2812.
- POISE Study Group, Devereaux P J, Yang H, Yusuf S, et al. Effects of extended-release metoprolol succinate in patients undergoing non-cardiac surgery (POISE trial): a randomized controlled trial. Lancet 2008; 371: 1839-1847.
- Levine HJ. Rest heart rate and life expectancy. J Am Coll Cardiol 1997; 30:1104-1106.
- Singh BN. Increased heart rate as a risk factor for cardiovascular disease. Eur Heart J Suppl 2003; 5(suppl G): G3-G9.
- Kristal-Boneh E, Silber H, Harari G, Froom P. The association of resting heart rate with cardiovascular, cancer and all-cause mortality. Eight year follow-up of 3527 male Israeli employees (the CORDIS Study). Eur Heart J 2009; 21: 116-124.
- London M. Cardiovascular Aging and Anesthetic Implications. J Cardiothorac Vasc Anesth 2003: 17: 512-523.
- Choate JK, Danson EJ, Morris JF, Paterson DJ. Peripheral vagal control of heart rate is impaired in neuronal NOS knockout mice. Am J Physiol Heart Circ Physiol 2003; 281: H676-H682.
- Ferrari R, Censi S, Mastrorilli F, Boraso A. Prognostic of heart rate reduction in cardiovascular disease. Eur Heart J Suppl 2003; 5(Suppl G): G10-G14.
- Okrainec K, Platt R, Pilote L, Eisenberg MJ. Cardiac medical therapy in patients after undergoing coronary artery bypass graft surgery: a review of randomized controlled trials. J Am Coll Cardiol 2005; 45: 177-184.
- Perk G, Stessman J, Ginsberg G, Bursztyn M. Sex differences in the effects of heart rate on mortality in the elderly. J Am Geriatr Soc 2003; 51: 1260-1264.
- Kannel WB, Kannel C, Paffenbarger RS Jr, Cupples LA. Heart rate and cardiovascular mortality: the Framingham Study. Am Heart J 1987; 113: 1489-1494.
- Zaugg M, Schaub MC. Cellular mechanisms in sympathomodulation of the heart. Br J Anaesth 2004; 93: 34-52.
- Cutodis F, Schirmer SH, Baumhäkel M, et al. Vascular pathophysiology in response to increased heart rate. J Am Coll Cardiol 2010; 56: 1973-1983.
- Hjalmarson A. Significance of reduction in heart rate in cardiovascular disease. Clin Cardiol 1998; 21(12 Suppl 2): 113-117.
- Feigi EO. Coronary physiology: Physiol Rev 1983; 63: 1-205.
- Ellenberger C, Tait G, Beattie WS. Chronic B Blockade is associated with a better outcome after elective noncardiac surgery than acute B Blockade: a single-center propensity-matched cohort study. Anesthesiology 2011; 114: 817-823.
- Landersberg G. The pathophysiology of perioperative myocardial infarction: facts and perspectives. J Cardiothorac Vasc Anesth 2003; 17: 90-100.
- Fleisher LA, Beckman JA, Brown KA, et al. ACC/AHA 2007 guidelines on perioperative cardiovascular evaluation and care for noncardiac surgery: a report of American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2007; 50:e 242. J Am Coll Cardiol 2007; 50: e 159-241.
- American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines; American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Ritme Society; Society of Cardiovascular Anesthesiologists; Society of Cardiovascular Angiography and Interventions; Society of Vascular Medicine; Society for Vascular Surgery; Fleisher LA, Beckman JA, Brown KA, et al. 2009 ACCF/AHA focused update on perioperative beta blockade incorporated into the ACC/AHA 2007 guidelines on perioperative cardiovascular evaluation and care for noncardiac surgery. J Am Coll Cardiol 2009; 54: e13-e118.
- Wiesbauer F, Schlager O, Domanovits H, et al. Perioperative B-Blockers for preventing surgery-related mortality and morbidity: a systematic review and meta-analysis. Anesth Analg 2007; 104: 27-41.
- Poldermans D, Schouten O, Bax J, Winkel TA. Reducing Cardiac Risk in non-cardiac surgery: evidence from the DECREASE studies. Eur Heart J Suppl 2009; 11(Suppl A): A9-A14.
- Kersten J, Fleisher LA. Statins: the next in cardioprotection?. Anesthesiology 2006; 105: 1079-1080.
- Hindler K, Eltzschig HK, Fox AA, et al. Influence of statins on perioperative outcomes. J Cardiothorac Vasc Anesth 2006; 20: 251-258.
- Liakopoulos OJ, Kuhn EW, Slottosch I, et al. Preoperative statin therapy for patients undergoing cardiac surgery. Cochrane Summaries Beta. April 18, 2012.
- Papangelou A, Mirski M. What are the risk factors for perioperative stroke?. Evidence-Based Practice of Anesthesiology. Second Edition. Saunders 2009. pp 33-43.
- Argalious MY, Dalton JE, Cywinski JB, et al. Association between preoperative statin therapy and postoperative change in glomerular filtration rate in endovascular aortic surgery. BJA 2012; 109: 161-167.
- Brookes ZLS, McGown C, Reilly S. Statins for all: the new premed?. BJA 2009; 103: 99-107.
- Le Manach Y, Godet G, Coriat P, et al. The impact of postoperative discontinuation or continuation of chronic statin therapy on cardiac outcome after mayor vascular surgery. Anesth Analg 2007; 104: 1326-1333.
- Prinz V, Endres M. The Acute (Cerebro) Vascular Effects of Statins. Anesth Analg 2009; 109: 572-584.
- Turan A, Mendoza M, Gupta S, et al. Consequences of Succinylcholine administration in patients using statins. Anesthesiology 2011; 115: 28-35.
- Homburger J, Steffen E. Anesthesia drugs, immunity, and long-term outcome. Curr Opin Anaesthesiol 2006; 19: 423-428.
- Blanchard L, Collard C. Non-antiarrhythmic agents for prevention atrial fibrillation: Role of Statins. Curr Opin Anaesthesiol 2007; 20: 53-56.


 Creative Commons Attribution
Creative Commons Attribution