Laura Monteagudo Moreno 1 ,Olatz Alduntzin Etxetxikia 2 , Irene Ortiz Martin 1 , Mikel Batllori Gastón 1 ,3
Recibido: 20-10-2020
Aceptado: 12-12-2020
©2021 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 50 Núm. en avance pp. -|https://doi.org/10.25237/revchilanestv5027071109
PDF|ePub|RIS
Prune-Belly syndrome and intestinal occlusion in an adult patient: anesthetic considerations
Abstract
Prune Belly syndrome is a rare congenital disease, which is characterized by abdominal wall muscular deficiency, cryptorchidism and urinary tract abnormalities. Its incidence is estimated at 3.8/100.000 live births. The prognosis is determined by the degree of pulmonary and renal affectation, which in turn depend on abdominal wall and urinary tract deficiencies, respectively. Although early mortality in the first months of life can be as high as 25%, many of these patients survive until later stages of the paediatric and adult ages, when they can require a great variety of surgical procedures. We present the case of an adult patient diagnosed with Prune Belly syndrome who required two surgical interventions in a month, in relation to two episodes of intestinal occlusion.
Resumen
El síndrome de Prune Belly es una enfermedad congénita rara caracterizada por hipoplasia de la musculatura abdominal, crip- torquidia y anomalías del tracto urinario. Su incidencia se estima en 3,8 de cada 100.000 recién nacidos vivos. El pronóstico está determinado por el grado de afectación pulmonar y renal secundarias a las alteraciones de la musculatura abdominal y del tracto urinario, respectivamente. Si bien la mortalidad precoz en los primeros meses de vida llega a ser hasta del 25%, muchos de estos pacientes sobreviven hasta etapas posteriores de las edades pediátrica y adulta, períodos en los que pueden requerir someterse a una gran variedad de procedimientos quirúrgicos. Presentamos el caso de un paciente adulto con síndrome de Prune Belly que precisó dos intervenciones quirúrgicas urgentes en el plazo de un mes en relación con sendos episodios de oclusión intestinal.
-
Introducción
El síndrome de Prune Belly es una enfermedad congénita rara caracterizada por hipoplasia y laxitud de la musculatura de la pared abdominal, criptorquidia bilateral y anomalías del tracto urinario (displasia renal)[1],[2]. Hasta 75% de los pacientes pueden asociar además otras anomalías a nivel cardiopulmonar
(hipoplasia pulmonar), gastrointestinal (malrotación intestinal) y musculoesquelético (escoliosis)[3].
La incidencia del síndrome se estima en 3,8 de cada 100.000 recién nacidos vivos[4],[5]. El pronóstico está determinado por el grado de afectación pulmonar y renal secundarias a las alteraciones de la musculatura abdominal y del tracto urinario, respectivamente. Si bien la mortalidad precoz en los primeros meses de vida llega a ser hasta del 25%[5], muchos de estos pacientes sobreviven hasta etapas posteriores de las edades pediátrica y adulta, períodos en los que pueden requerir someterse a una gran variedad de procedimientos quirúrgicos. En dicho contexto, como se ejemplifica en el caso clínico que a continuación presentamos, pueden presentarse problemas en el manejo anestésico-quirúrgico principalmente debidos a alteraciones anatómicas.
-
Caso clínico
Paciente varón de 34 años de edad, diagnosticado al nacimiento de síndrome de Prune Belly y atrofia renal derecha. Posteriormente, desarrolló escoliosis, que fue tratada quirúrgicamente en la infancia. Asimismo, desde la infancia y hasta el momento de consultar en nuestro centro, había presentado de manera habitual cuadros de infecciones urinarias de repetición y suboclusión intestinal (unos 2 episodios anuales) tratados de manera conservadora. Acudió al Servicio de Urgencias por cuadro clínico de 10 días de evolución consistente en distensión abdominal progresiva y vómitos, compatible con oclusión intestinal. Inicialmente se manejó de forma conservadora mediante la colocación de una sonda nasogástrica, pero ante la persistencia del cuadro se decidió realizar un TC abdominal (Figura 1). En este estudio se identificó el “signo del remolino”, una rotación de asas de intestino delgado que envuelve a los vasos mesentéricos (que actúan como eje de la rotación) y es sugestiva de un vólvulo. Además, el ciego y colon ascendente se encontraban en la fosa ilíaca y flanco izquierdos, medializándose el colon ascendente por detrás de los vasos mesentéricos superiores. Ante los hallazgos descritos se indicó una laparotomía urgente por el riesgo de isquemia intestinal y perforación consecuente.
A su llegada a quirófano el paciente se encontraba estable (presión arterial 118/68 mmHg, frecuencia cardiaca 123 lpm, SpO2 94%), llamando la atención una marcada distensión abdominal pese a haberse colocado previamente una sonda nasogás- trica, así como una hipoplasia de la región torácica sugestiva de patología pulmonar restrictiva (Figura 2). A la exploración de la vía aérea, no se detectaron predictores de dificultad aparentes (Mallampati II, distancia tiromentoniana mayor de 6 cm, distancia interincisiva mayor de 3 cm y ausencia de limitación para la flexoextensión cervical). El paciente presentaba antecedentes de manejo de la vía aérea con una máscara laríngea para una intervención quirúrgica previa (herniorrafia inguinal) hacía 1 año, pero no se había realizado una laringoscopia directa desde la cirugía ortopédica espinal que tuvo lugar en la infancia.
Dado lo anterior, se planificó realizar anestesia general con inducción de secuencia rápida empleando un videolaringoscopio para la intubación (McGrath® MAC; Aircraft Medical, Edimburgo, Reino Unido). Se realizó preoxigenación con mascarilla facial hasta verificar una fracción espirada de oxígeno por encima del 90%. A continuación se administraron 100 mcg de fentanilo, 150 mg de propofol y 100 mg de succinilcolina. Se empleó la maniobra de Sellick durante la inducción y hasta conseguir la intubación orotraqueal, que se realizó al primer intento sin incidencias. Para el mantenimiento se utilizaron sevoflurano y rocuronio. Tras la inducción se canalizó un acceso venoso central yugular interno derecho, previendo la necesidad de nutrición parenteral posoperatoria. Se empleó una estrategia de ventilación pulmonar protectora con volumen corriente bajo (350 ml), frecuencia respiratoria alta (16 rpm) y presión positiva telespiratoria de 6 cm H2O. La distensibilidad pulmonar observada con estos parámetros fue de 17 ml/cm H2O. Las presiones en vía aérea no superaron los 40 cm H2O. Utilizando una fracción inspirada de oxígeno del 60%, la SpO2 se mantuvo en 98% durante toda la intervención. Asimismo, persistió la estabilidad hemodinámica durante la misma sin necesidad de soporte vasopresor ni bolos de fluidoterapia.
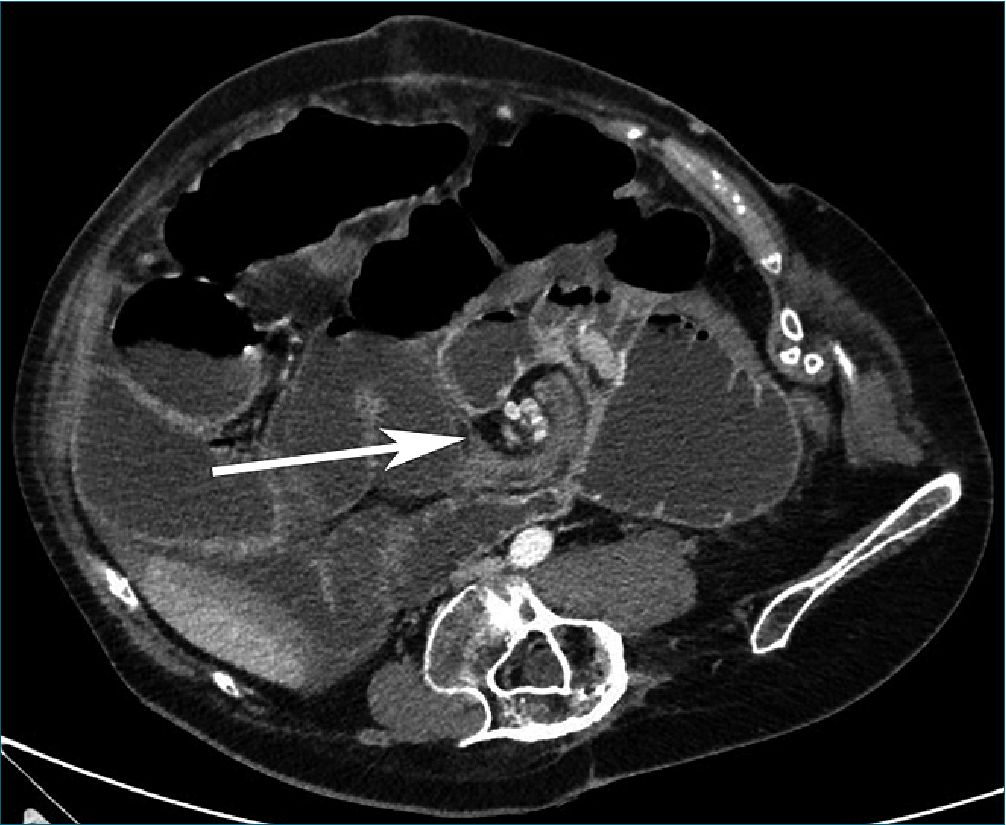
Figura 1. Corte de TC abdominal en el que puede apreciarse el signo del remolino (flecha), secundario a torsión del propio mesenterio alrededor de los vasos mesentéricos superiores.

Figura 2. Se observaba una muy marcada distensión abdominal, mayor aún que la que presentaba el paciente de forma habitual, a consecuencia del cuadro oclusivo. Llamaba la atención también la hipoplasia de la región torácica. Marcado cutáneo de la incisión de laparotomía prevista, realizado justo antes de la preparación quirúrgica abdominal.
Tras realizar la laparotomía, se identificó una brida que se extendía desde el epiplón hacia la raíz del mesenterio, confor
mando un orificio herniario interno por donde se encontraba herniado gran parte del intestino delgado, así como el ciego, colon ascendente y parte de colon transverso. Se procedió a seccionar la brida y reducir el contenido herniario, que se encontraba dilatado y sin signos de isquemia (mínimos signos de congestión venosa). Se exploró el resto del paquete intestinal sin que se objetivaran otras lesiones.
Antes de la extubación se realizó un bloqueo analgésico bilateral del plano del transverso del abdomen, bajo guía ecográ- fica, utilizando 40 ml de una mezcla de levobupivacaína 0,25% y lidocaína 1%. También se administraron 6 mg de morfina intravenosa. Tras revertir el bloqueo neuromuscular residual con sugammadex, el paciente fue extubado en quirófano sin incidencias, y tras 2 h en la unidad de recuperación posanestésica fue trasladado a planta de hospitalización con un buen control analgésico y en situación de estabilidad hemodinámica y respiratoria. La evolución posoperatoria fue favorable, y el paciente recibió el alta hospitalaria a los 10 días de la intervención, habiendo recuperado la tolerancia oral y el tránsito intestinal.
Una semana después del alta, el paciente volvió a ingresar por un nuevo cuadro de oclusión intestinal. Después de realizar un nuevo TC, donde se observaban de nuevo hallazgos compatibles con vólvulo intestinal (signo del remolino) y malrotación intestinal con el ciego cruzando por detrás de los vasos mesen- téricos superiores, se indicó una nueva laparotomía urgente. El manejo anestésico fue equiparable al previo. A nivel de la raíz del mesenterio se halló una rotación de 360°, la cual se devolvuló. Manteniendo el intestino delgado con la raíz del mesenterio normoposicionada, el ciego y el colon ascendente se localizaban en el lado izquierdo, cruzando el colon ascendente posterior a los vasos mesentéricos superiores; se procedió a colocarlos en su localización anatómica. Tras esta segunda cirugía no volvieron a producirse episodios de oclusión intestinal.
-
Discusión
Los casos de pacientes adultos de edad media diagnosticados de síndrome de Prune Belly son raros en la literatura. La malrota- ción intestinal es una anomalía congénita de la rotación y fijación intestinal que ocurre aproximadamente en 1/500 nacimientos. Entre el 30%-62% de los casos de malrotación están asociados a numerosos síndromes entre los que se encuentra el síndrome de Prune Belly. La sintomatología aparece predominantemente en el período neonatal y la infancia con el desarrollo de episodios de oclusión intestinal causados por la presencia de bandas fibróticas (de Ladd) o volvulación del intestino con o sin isquemia asociada. Sin embargo, la incidencia de casos sintomáticos disminuye con la edad. En este contexto, en los pacientes adultos puede llegarse al diagnóstico de forma incidental al realizarse exploraciones radiológicas (TC o ecografía abdominal) por otras causas, o bien al presentarse episodios suboclusivos u oclusivos como en el caso que nos ocupa[6].
El manejo anestésico en pacientes con síndrome de Prune Belly y malrotación intestinal debe comenzar con una cuidadosa evaluación preoperatoria. Algunos pacientes con síndrome de Prune Belly presentan malformaciones craneofaciales asociadas. No es infrecuente la presencia de retrognatia, que puede dificultar tanto la ventilación con bolsa y mascarilla facial como la intubación orotraqueal[7]. En estas circunstancias, debe re
cordarse la importancia de una adecuada preoxigenación y de la disponibilidad de material para el manejo de una posible vía aérea difícil, que debe estar preparado y disponible en quirófano antes de comenzar la inducción anestésica. Es importante tener en cuenta la habitual presencia de deformidad torácica que asocie hipoplasia pulmonar y un escaso desarrollo de la musculatura accesoria de la ventilación. Estas alteraciones conllevan patología pulmonar restrictiva que puede dificultar la ventilación mecánica. En nuestro caso decidimos emplear una estrategia de ventilación protectora con volumen corriente bajo y frecuencia respiratoria alta. Durante procedimientos que requieran bloqueo neuromuscular, se debe tener en cuenta que estos pacientes pueden presentar una mayor susceptibilidad al efecto farmacológico de los relajantes neuromusculares[8]. En nuestro caso empleamos monitorización objetiva del bloqueo neuromuscular mediante cinemiografía (Módulo E-NMT y Me- canosensor; Datex-Ohmeda, Helsinki, Finlandia) para titular las dosis de succinilcolina y rocuronio, cuyos requerimientos fueron aparentemente similares a los habituales en pacientes sanos. En cirugía torácica y abdominal, es importante considerar que un control analgésico óptimo minimiza el riesgo de complicaciones respiratorias posoperatorias. A este respecto, se ha sugerido la utilización de técnicas de analgesia locorregional evitando a la vez una analgesia posoperatoria basada en opioides que pueda favorecer alteraciones ventilatorias en el posoperatorio[9].
Como conclusión, nos gustaría resaltar la importancia de tener presente la posibilidad de una malrotación intestinal congénita ante episodios de suboclusión u oclusión intestinal recidivantes en un paciente adulto diagnosticado de síndrome de Prune Belly. Al tratarse de casos poco frecuentes es posible que el diagnóstico de malrotación pase desapercibido y predisponga a la aparición de nuevos episodios si no se detecta y soluciona a tiempo.
La presente comunicación no ha recibido financiación alguna, y los autores declaran que no existe conflicto de intereses.
Referencias
1. Diao B, Diallo Y, Fall PA, et al. Prune Belly syndrome: Epidemio- logic, clinic and therapeutic aspects. Prog Urol. 2008;18:470474. https://doi.org/10.1016/j.purol.2008.04.003.
2. Woods AG, Brandon DH. Prune belly syndrome. A focused physical assessment. Adv Neonatal Care. 2007 Jun;7(3):132–43. https://doi.org/10.1097/01.ANC.0000278211.95767.05 PMID:17844777
3. Dénes FT, Arap MA, Giron AM, Silva FA, Arap S. Comprehensive surgical treatment of prune belly syndrome: 17 years’ experience with 32 patients. Urology. 2004 Oct;64(4):789–93. https://doi.org/10.1016/j.urology.2004.05.053 PMID:15491721
4. Hassett S, Smith GH, Holland AJ. Prune belly syndrome. Pediatr Surg Int. 2012 Mar;28(3):219–28. https://doi.org/10.1007/s00383-011-3046-6 PMID:22198807
5. Seidel NE, Arlen AM, Smith EA, Kirsch AJ. Clinical manifestations and management of prune-belly syndrome in a large contemporary pediatric population. Urology. 2015 Jan;85(1):211–5. https://doi.org/10.1016/j.urology.2014.09.029 PMID:25444629
6. Ballesteros Gómiz E, Torremadé Ayats A, Durán Feliubadaló C, Martín Martínez C, Caro Tarragó A. Malrotación-vólvu- lo intestinal: hallazgos radiológicos. Radiologia (Madr). 2015;57(1):9–21. https://doi.org/10.1016/j.rx.2014.07.007.
7. Grimsby GM, Harrison SM, Granberg CF, Bernstein IH, Baker LA. Impact and frequency of extra-genitourinary manifestations of prune belly syndrome. J Pediatr Urol. 2015 Oct;11(5):280.e1–6. https://doi.org/10.1016/j.jpurol.2015.06.005 PMID:26231776
8. Yoon J, Ryu J, Kim J, Jeong CY, Park SG. Anesthetic experience of a patient with Prune-belly syndrome. Korean J Anesthesiol. 2014 Dec;67 Suppl:S94–5. https://doi.org/10.4097/kjae.2014.67.S.S94 PMID:25598927
9. Goyal S, Gupta SK, Kothari N, Bhatia P, Kumar M. Prune-belly syndrome: Anesthetic implications and management. Indian Anaesth Forum 2019;20:47-9.

 ORCID
ORCID