Felipe Maldonado C.1,* Roberto González C.2, Mónica Cáceres Ll.2,3
Recibido: 26-07-2024
Aceptado: 01-09-2024
©2025 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 54 Núm. 1 pp. 51-56|https://doi.org/10.25237/revchilanestv54n1-06
PDF|ePub|RIS
Abstract
The endothelium is the inner layer of blood vessels, serving as a physical barrier and playing a metabolic role in the organism>s homeostasis. Considering that cardiovascular diseases remain among the leading causes of global morbidity and mortality, identifying conditions like endothelial dysfunction, which span various pathologies, is significant. This dysfunction has been extensively described in cardiovascular pathologies, recognized as a risk factor for the development of long-term complications, and playing a crucial role in the atherosclerotic process, even preceding it during thickening, plaque formation, and subsequently in the pathophysiology of inflammation, plaque vulnerability, and eventual rupture. Various animal studies have demonstrated impaired endothelial function is associated with poorer cardiovascular performance. Despite this, evaluating this organ is not routine in clinical practice, and even less so in the perioperative context, as many techniques require sampling of endothelial tissue, consequently causing injury to the vascular tree. Several non-invasive techniques have been developed to evaluate endothelial function, which have been associated with the presence of atherosclerosis or as predictors of cardiovascular events. One such technique used in functional studies is the Flow-Mediated Dilation (FMD) test. This test is based on the normal vasodilation reactive to ischemia caused by the release of endothelial nitric oxide due to increased turbulence over the endothelium. Initially used in endothelial function research laboratories, it has gradually been adopted in clinical practice with an increasing number of publications. This article describes the theoretical foundations supporting the phenomenon and provides a guide to adapting its use in daily surgical settings.
Resumen
El endotelio es la capa interna de los vasos sanguíneos que no solo actúa como barrera física, sino que también tiene función metabólica ya que participa en la homeostasis el organismo. Considerando que las enfermedades cardiovasculares se mantienen dentro de las primeras causas de morbilidad y mortalidad mundial, entidades transversales a distintas patologías como es la disfunción endotelial son relevantes de identificar^]. Esta disfunción ha sido ampliamente descrita en patologías cardiovasculares, identificada como parte de los factores de riesgo para el desarrollo de complicaciones a largo plazo y jugando una parte esencial del proceso aterosclerótico, incluso precediéndola durante el engrasamiento, formación de la placa y luego en la fisiopatología de la inflamación, vulnerabilidad de placa y subsecuente ruptura[],[]. Diversos estudios en animales han demostrado que una función endotelial deteriorada se asocia a peor rendimiento cardiovascular[]. A pesar de esto, la evaluación de este órgano no es rutinaria en clínica, y mucho menos en el contexto perioperatorio, pues muchas técnicas requieren tomar muestras de tejido endotelial y consecuentemente, una lesión del árbol vascular. Se han desarrollado diversas técnicas no invasivas para enfrentar la evaluación de la función endotelial las que se han logrado asociar con la presencia de ateroesclerosis o como predictores de eventos cardiovasculares. Una de ellas, utilizada en estudios funcionales, es la prueba de Flow-Mediated-Dilation (FMD; dilatación mediada, o dependiente, de flujo)[]. Esta prueba tiene su base en la vasodilatación normal reactiva a una isquemia, dada por la liberación de óxido nítrico endotelial consecuente al aumento de turbulencia sobre el endotelio. Su uso nace en laboratorios de estudio de función endotelial pero paulatinamente se ha utilizado en clínica con un número creciente de publicaciones. En este artículo describimos las bases teóricas que respaldan el fenómeno y una guía para adaptar su uso al ambiente quirúrgico diario.
-
Introducción
El endotelio es la capa interna de los vasos sanguíneos que no solo actúa como barrera física, sino que también tiene función metabólica ya que participa en la homeostasis del organismo. Considerando que las enfermedades cardiovasculares se mantienen dentro de las primeras causas de morbilidad y mortalidad mundial, entidades transversales a distintas patologías como es la disfunción endotelial son relevantes de identificar[1]. Esta disfunción ha sido ampliamente descrita en patologías cardiovasculares, identificada como parte de los factores de riesgo para el desarrollo de complicaciones a largo plazo y jugando una parte esencial del proceso aterosclerótico, incluso precediéndola durante el engrosamiento, formación de la placa y luego en la fisiopatología de la inflamación, vulnerabilidad de placa y subsecuente ruptura[2],[3]. Diversos estudios en animales han demostrado que una función endotelial deteriorada se asocia a peor rendimiento cardiovascular[4].
A pesar de esto, la evaluación de este órgano no es rutinaria en clínica, y mucho menos en el contexto perioperatorio, pues muchas técnicas requieren tomar muestras de tejido endotelial y consecuentemente, una lesión del árbol vascular. Se han desarrollado diversas técnicas no invasivas para enfrentar la evaluación de la función endotelial las que se han logrado asociar con la presencia de ateroesclerosis o como predictores de eventos cardiovasculares. Una de ellas, utilizada en estudios funcionales, es la prueba de Flow-Mediated-Dilation (FMD; dilatación mediada, o dependiente, de flujo)[5]. Esta prueba tiene su base en la vasodilatación normal reactiva a una isquemia, dada por la liberación de óxido nítrico endotelial consecuente al aumento de turbulencia sobre el endotelio. Su uso nace en laboratorios de estudio de función endotelial pero paulatinamente se ha utilizado en clínica con un número creciente de publicaciones.
En este artículo describimos las bases teóricas que respaldan el fenómeno y una guía para adaptar su uso al ambiente quirúrgico diario.
Disfunción endotelial en contexto de complicaciones cardiovasculares: FMD, una alternativa factible de estratificación perioperatoria
La prueba FMD, es una prueba no invasiva realizada mediante ultrasonografía introducida en 1992. Consiste en la medición del diámetro de la arteria braquial y/o su velocidad antes y después de un período de suspensión de flujo sanguíneo. Básicamente, se realiza compresión de la arteria braquial
(proximal a la fosa cubital) o distal (en antebrazo) con un manguito de isquemia durante 3-5 minutos y se mide la variación del diámetro de la arteria braquial respecto al basal luego de que se recupere el flujo sanguíneo[3],[6]. Se define un endotelio funcional como el capaz de producir suficiente óxido nítrico para conseguir una vasodilatación en al menos 10% de su diámetro basal. Este procedimiento ultrasonográfico es posible de instaurar en el ámbito perioperatorio dado el aumento en la disponibilidad de equipos de ecografía a nivel de quirófanos en todo el mundo.
Específicamente en el ámbito quirúrgico, el uso de FMD ha demostrado ser predictor de eventos cardiovasculares[21],[22]. Así aplicar la evaluación endotelial, mediante FMD, nos puede dar luces para la prevención y tratamiento de complicaciones cardiovasculares en pacientes sometidos a intervenciones quirúrgicas. Pacientes mayores de 65 años con una buena respuesta vasodilatadora en FMD presentan menos eventos cardiovasculares a largo plazo, considerándose un factor protector en riesgo cardiovascular[7].
En consideración de lo previamente mencionado, dado el bajo costo de FMD y la importancia epidemiológica de identificar pacientes con riesgo cardiovascular en el perioperatorio, el estudio de FMD como valor pronóstico surge como una propuesta para optimizar la estratificación de riesgo perioperatorio y el seguimiento de pacientes con riesgo cardiovascular en el contexto hospitalario.
En el presente artículo exponemos un protocolo técnico basado en guías internacionales adaptado a nuestros protocolos de investigación, como base para la realización de FMD en el contexto perioperatorio.
-
Protocolo para Flow Mediated Dilatation (FMD)
La realización de FMD en el ámbito perioperatorio puede ser hecha en policlínico, sala de hospital, en unidades preoperatorias o en el quirófano.
Equipo necesario:
• Ecógrafo con sonda lineal de alta frecuencia.
• Manguito de isquemia.
• Cronómetro.
-
Procedimiento
Con el paciente en decúbito supino, se realiza la medición de signos vitales basales (importante es considerar la presión arterial basal del paciente). Luego se descubre el brazo a examinar. Se instala un manguito de isquemia traumatológico a nivel de brazo dejando libre la fosa cubital.
Se realiza la inspección ecográfica de la arteria braquial inmediatamente distal al manguito. Recomendamos la visualización en un eje transversal a la arteria de forma inicial usando la menor profundidad del ecógrafo, optimizar la ganancia y foco del objetivo ecográfico (arteria), para mejorar la resolución espacial. La confirmación del objetivo se puede realizar observando la pulsatilidad de la arteria, mediante Doppler color o pulsado según la preferencia del usuario. Luego centrar el objetivo, se busca la imagen en el eje longitudinal, en esta imagen se aprecia la presencia de varias capas vasculares, siendo la más interna la que corresponde al endotelio. Con esta imagen en pantalla, recomendamos adquirir videos o fotografías usando el software del equipo ecográfico para su análisis fuera de línea al finalizar el procedimiento. Se puede realizar una marca en la piel de la ubicación del transductor ecográfico para referencias de las siguientes mediciones.
Luego de adquirida las imágenes de la arteria en estado basal, se presuriza el manguito de isquemia traumatológico con al menos 100 mmHg sobre la presión sistólica para abolir el flujo a nivel del brazo. Se sugiere mantener un tiempo de isquemia de 4 a 5 minutos. Los pacientes deben ser instruidos de la sensación de entumecimiento y frialdad que sentirán al iniciar el inflado. La presión sobre la extremidad que ejercen los manguitos de isquemia traumatológicos es bien tolerada por los pacientes (a diferencia de lo que ocurre muchas veces con el uso de un mango de presión clínico para la evaluación de la presión arterial). Si el paciente presenta dolor o intolerancia al procedimiento, sugerimos suspender la evaluación.
Luego de transcurrido el tiempo, se debe estar preparado para realizar la adquisición de imágenes y buscar el objetivo ecográfico rápidamente. Sugerimos que el operador del ecógrafo localice el transductor en el brazo (a la misma altura que la medición basal) buscando el eje transversal de la arteria y se prepare para reiniciar la evaluación. Con el objetivo ecográfico en pantalla, un segundo operador desactiva el manguito de isquemia. El operador ecográfico observará la reanudación de la pulsatilidad arterial. Rápidamente se busca la imagen arterial longitudinal asegurando la visión de las capas arteriales. Al recobrar pulsatilidad se inicia el cronómetro para obtener imágenes a los 15, 30, 60, 90 y 120 segundos de recuperado el flujo sanguíneo. Las imágenes adquiridas son luego analizadas mediante el software del ecógrafo y archivadas en el disco duro u otra unidad.
El análisis de imágenes busca comparar el diámetro de la arteria en imágenes longitudinales, con los diámetros arteriales en los 120 segundos posteriores a la isquemia braquial. Utilizando las herramientas de Zoom y de medición de imágenes, se medirá la distancia entre los endotelios vasculares de ambas capas de la arteria braquial (Figura 1).
El valor de FMD es el porcentaje de cambio del diámetro arterial respecto a los valores basales. Este análisis se puede realizar en una hoja de cálculo estándar. Consideramos como resultado el valor de dilatación máximo obtenido en comparación a la respuesta basal. Como mencionamos, se describe que un endotelio funcional debe generar un aumento en su diámetro de al menos 10% del valor basal.
Es importante realizar la medición en el mismo segmento de la arteria braquial en todas las imágenes (Figura 2).
Sugerimos un entrenamiento antes de realizar esta prueba en pacientes. La práctica entre pares es una buena herramienta tanto para la adquisición de la competencia en la evaluación de FMD como para evaluar los efectos adversos o molestias que se generan con el uso de un manguito de isquemia, así adelantar los síntomas que pueden presentarse al evaluar a los pacientes. Consideramos que la dificultad para realizar el examen es baja para un anestesiólogo usuario de ecografía promedio, y que el procedimiento, una vez implementado es rápido, no requiriendo más de 10 minutos en total.
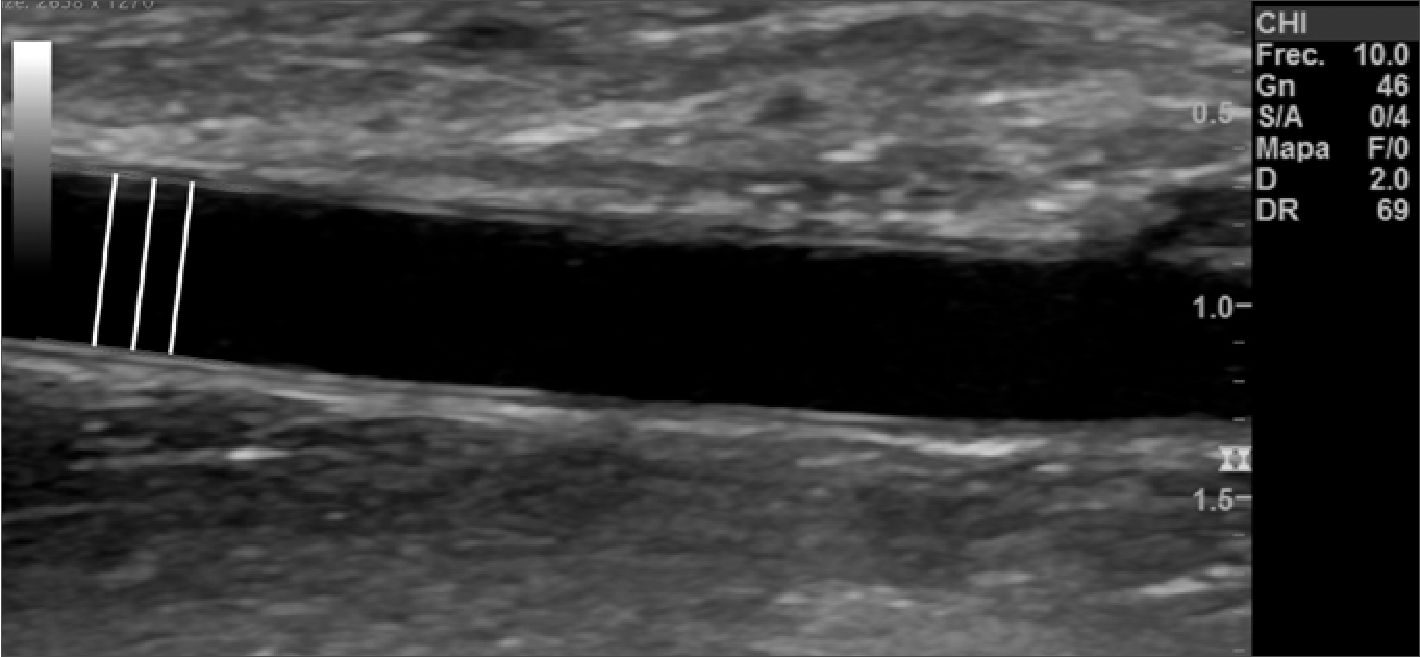
Figura 1. Imagen representativa de medición braquial. Se observa la imagen ecográfica de la arteria braquial. Con una profundidad de 2 cm y el foco ajustado a la profundidad de la arteria. Marcado con línea roja endotelio vascular y con líneas blancas perpendiculares al eje mayor de la arteria, la medición del diámetro arterial.
-
Discusión
Las células endoteliales, junto con los pericitos, mantienen la integridad estructural del endotelio, formando una unidad mecano-protectora vascular que se extiende desde las arteriolas hasta los capilares y venulas[8]. Además, la producción de prostaglandinas como factores de relajación endotelial contrasta con la producción de endotelina, tromboxano A2, especies reactivas de oxígeno y angiotensina-2, las cuales inducen vasoconstricción, completando así la regulación del tono y la permeabilidad vascular[9].
La monocapa endotelial no es uniforme en todo el territorio vascular, presentando variaciones fenotípicas que permiten respuestas diferentes a un mismo estímulo según la expresión de antígenos y receptores de superficie[10]. Incluso en un mismo territorio, las células pueden responder de manera distinta a estímulos, algo que se hace aún más evidente in vitro, especialmente en cultivos celulares y líneas endoteliales inmortalizadas. En estos casos, la pérdida del contexto tisular puede resultar en la desaparición de algunos elementos no constitutivos del tejido[11]. En el cáncer, el ambiente tumoral induce propiedades anormales en los vasos y el epitelio vascular, tanto morfológicas como funcionales. Esta heterogeneidad de funciones caracteriza al endotelio, siendo más notable en estudios in vitro[12],[13], lo que resalta la importancia de evaluar la función endotelial in vivo.
Aunque en pacientes con enfermedades crónicas como hipertensión, diabetes o aterosclerosis se suele asumir la existencia de una alteración en la función endotelial, en la práctica clínica habitual rara vez se evalúa esta función o se utiliza este antecedente para modificar el manejo o tratamiento del paciente[14]. En este contexto, la introducción del análisis de la función endotelial mediante FMD puede ser un avance en la categorización de pacientes y eventualmente en el manejo de ellos.
En este artículo, proponemos una adaptación simplificada de las guías internacionales para la realización de la prueba FMD, con el objetivo de facilitar su aplicación en la práctica anestésica. Desde su introducción en 1992, la evaluación no invasiva de la dilatación mediada por flujo del endotelio en arterias periféricas ha ganado adeptos y generado información valiosa para la clínica[3],[6],[15]. Alteraciones en la función endotelial detectadas con FMD se han asociado a progresión del daño tisular como engrosamiento de capa intima carotidea, cambios en la velocidad de la onda de pulso, albuminuria e hipertrofia ventricular izquierda[3]. Metaanálisis concluyen en una disminución entre 8% y 13% en el riesgo de eventos cardiovasculares con cada punto en el aumento en el porcentaje de dilatación de arteria braquial. A pesar de estos resultados, que otorgan valor predictivo al uso de FMD, hasta ahora, la técnica no ha mostrado agregar valor a los clásicos factores de riesgo en términos de discriminación o reclasificación de pa- cientes[3],[16].
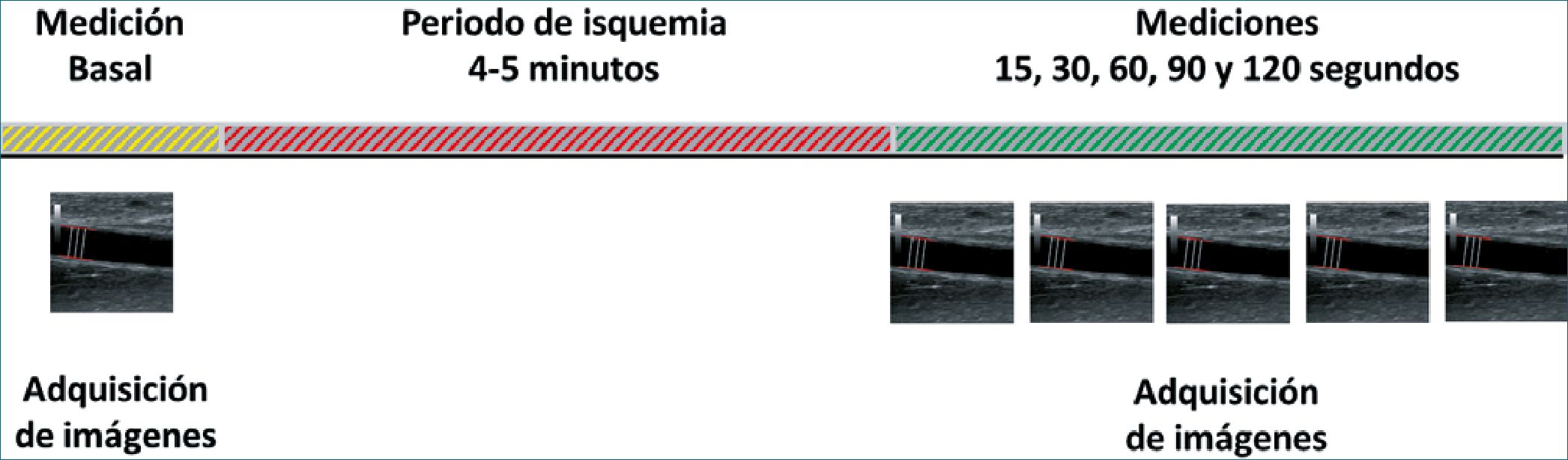
Figura 2. Esquema temporal del proceso de adquisición de imágenes para FMD. Se realiza una medición basal del diámetro basal de la arteria braquial. Luego de realizada la adquisición de la imagen con diámetro basal, se procede a comprimir el flujo sanguíneo con un manguito de isquemia. Finalizado 4 a 5 minutos de interrupción del flujo arterial, se realiza la adquisición de la arteria al menor por dos minutos. Sugerimos un mínimo de 5 imágenes para observar los cambios en el diámetro arterial.
La baja adherencia a guías internacionales se esgrime como causa de resultados dispares en la literatura. FMD podría reflejar simplemente la carga de riesgo compuesta que afecta la función vascular, sin ofrecer una predicción de riesgo adicional. Actualmente, un grupo de trabajo sobre circulación periférica de la Sociedad Europea de Cardiología concluyó que la FMD es principalmente una herramienta valiosa para la investigación y que debido a la escasa estandarización entre laboratorios y la falta de adherencia a las guías, la FMD no se recomienda actualmente para la evaluación del riesgo cardiovascular[17]-[19].
Diferencias en la aplicación de las guías a la práctica anestésica. Ventajas y desventajas del uso de quirófano en el preoperatorio
Las guías internacionales realizan recomendaciones derivadas de los estudios en laboratorios en sujetos voluntarios. En el contexto preanestésico, la realización de FMD en pabellón antes de realizar la inducción de un procedimiento anestésico cumple con varias de las recomendaciones de preparación para la prueba. Los pacientes se encuentran en reposo, acostados por 10 a 15 minutos mínimo antes de la medición. Se encuentran en posición supina y generalmente cirugías de alto riesgo se realizan a primera hora, lo que controla los efectos que podría tener la variación circadiana en el sistema cardiovascular. Los pacientes se encuentran en ayuno y sin fumar por más de 6 horas, concordante con la recomendación, y generalmente no han realizado actividad física durante el día anterior[3].
Con relación al protocolo, la medición del diámetro arterial se puede realizar fácilmente y sin interrupciones previo al período de isquemia braquial así obtener los diámetros basales de la arteria y definir el sitio de medición. Sugerimos en este protocolo poner el mango proximal al sitio de punción para maximizar la dilatación. Nuestro grupo de trabajo utiliza una presión de 100 mmHg sobre la presión arterial (concordante a la práctica quirúrgica habitual) que es 50 mmHg sobre lo sugerido por las guías, lo que asegura una disminución del flujo arterial. Post isquemia realizamos una medición por 120 segundos del diámetro[6]. Esto puede extenderse a 180 segundos según las últimas recomendaciones[3]. En el contexto quirúrgico, no creemos necesario realizar la prueba luego de administración de nitroglicerina que sirve como control positivo de la prueba. En este contexto, más estudios podrían dilucidar la diferencia entre esto y el uso de fármacos anestésicos y la medición en el intraoperatorio.
La técnica de medición con uso de traductores continuos en modo B de 7.5 MHz es accesible a la mayoría de los quirófanos en la actualidad. En este contexto el uso de la mayor frecuencia disponible en el equipo puede ayudar a visualizar mejor la imagen endotelial. Nuestro grupo utiliza la dilatación de la arteria como parámetro, de todas maneras en caso de analizar velocidad de la sangre, el ángulo de insonación debe ser menor a 60° o 70° para no interferir en el efecto Doppler y debe ser el mismo para comparar en el mismo o entre distintos pacientes[3].
En el laboratorio, el uso de software de detección de bordes de forma continua y seguimiento del diámetro de la pared con algoritmos matemáticos automatizados para calcular el diámetro máximo es esencial para mejorar la precisión y reproducibilidad de las mediciones. La falta de estas herramientas puede introducir variabilidad y disminuir la exactitud de los resultados obtenidos. Por ello, los evaluadores deben estar entrenados en el uso de la ecografía, recomendándose más de 100 mediciones previas a la realización del estudio para reducir el coeficiente de variación intra y entre exámenes. En el contexto anestésico, consideramos que el anestesiólogo es el operador ideal para realizar esta técnica, dado su uso habitual de la ecografía para la visualización vascular y las punciones venosas en plano. La necesidad de análisis automatizado puede convertirse en un requisito futuro para el software de los equipos ecográficos.
Finalmente, sugerimos que el análisis de las imágenes obtenidas, para definir la respuesta endotelial a FMD, se realice utilizando los diámetros basales, la respuesta al FMD como cambios absolutos en milímetros y como porcentaje del cambio basal y que sea realizada por un sujeto ciego a los datos clínicos del paciente.
-
Conclusión
En este artículo, sugerimos un protocolo para el uso de FMD en el período perioperatorio. Su introducción a la práctica, la caracterización de los pacientes acorde a su respuesta y la asociación de este a resultados clínicos a corto y largo plazo puede abrir nuevas formas de trabajo y manejo de los pacientes en el futuro.
Financiamiento: Este artículo cuenta con el apoyo de la Agencia Nacional de Investigación y Desarrollo (ANID) a través de la Subdirección de Investigación Aplicada con fondos adjudicados en el XIX Concurso de Investigación y Desarrollo en Salud 2022 – FONIS SAI22I0146
-
Referencias
1. Grover-Páez F, Zavalza-Gómez AB. Endothelial dysfunction and cardiovascular risk factors. Diabetes Res Clin Pract. 2009 Apr;84(1):1–10. https://doi.org/10.1016/j.diabres.2008.12.013 PMID:19185380
2. Poredos P, Poredos AV, Gregoric I. Endothelial Dysfunction and Its Clinical Implications. Angiology. 2021 Aug;72(7):604–15. https://doi.org/10.1177/0003319720987752 PMID:33504167
3. Thijssen DH, Bruno RM, van Mil AC, Holder SM, Faita F, Greyling A, et al. Expert consensus and evidence-based recommendations for the assessment of flow-mediated dilation in humans. Eur Heart J. 2019 Aug;40(30):2534–47. https://doi.org/10.1093/eurheartj/ehz350 PMID:31211361
4. Riedel B, Rafat N, Browne K, Burbury K, Schier R. Perioperative Implications of Vascular Endothelial Dysfunction: Current Understanding of this Critical Sensor-Effector Organ. Curr Anesthesiol Rep. 2013;3(3):151–61. https://doi.org/10.1007/s40140-013-0024-7.
5. Smilowitz NR, Redel-Traub G, Hausvater A, Armanious A, Nicholson J, Puelacher C, et al. Myocardial Injury After Noncardiac Surgery: A Systematic Review and Meta-Analysis. Cardiol Rev. 2019;27(6):267–73. https://doi.org/10.1097/CRD.0000000000000254 PMID:30985328
6. Thijssen DH, Black MA, Pyke KE, Padilla J, Atkinson G, Harris RA, et al. Assessment of flow-mediated dilation in humans: a methodological and physiological guideline. Am J Physiol Heart Circ Physiol. 2011 Jan;300(1):H2–12. https://doi.org/10.1152/ajpheart.00471.2010 PMID:20952670
7. Yeboah J, Crouse JR, Hsu FC, Burke GL, Herrington DM. Brachial flow-mediated dilation predicts incident cardiovascular events in older adults: the Cardiovascular Health Study. Circulation. 2007 May;115(18):2390–7. https://doi.org/10.1161/CIRCULATIONAHA.106.678276 PMID:17452608
8. Jin Y, Ji W, Yang H, Chen S, Zhang W, Duan G. Endothelial activation and dysfunction in COVID-19: from basic mechanisms to potential therapeutic approaches. Signal Transduct Target Ther. 2020 Dec;5(1):293. https://doi.org/10.1038/s41392-020-00454-7 PMID:33361764
9. Godo S, Shimokawa H. Endothelial Functions. Arterioscler Thromb Vasc Biol. 2017 Sep;37(9):e108–14. https://doi.org/10.1161/ATVBAHA.117.309813 PMID:28835487
10. Galley HF, Webster NR. Physiology of the endothelium. Br J Anaesth. 2004 Jul;93(1):105–13. https://doi.org/10.1093/bja/aeh163 PMID:15121728
11. Nagy JA, Chang SH, Shih SC, Dvorak AM, Dvorak HF. Heterogeneity of the tumor vasculature. Semin Thromb Hemost. 2010 Apr;36(3):321–31. https://doi.org/10.1055/s-0030-1253454 PMID:20490982
12. Aird WC. Phenotypic heterogeneity of the endothelium: I. Structure, function, and mechanisms. Circ Res. 2007 Feb;100(2):158–73. https://doi.org/10.1161/01.RES.0000255691.76142.4a PMID:17272818
13. Burridge KA, Friedman MH. Environment and vascular bed origin influence differences in endothelial transcriptional profiles of coronary and iliac arteries. Am J Physiol Heart Circ Physiol. 2010 Sep;299(3):H837–46. https://doi.org/10.1152/ajpheart.00002.2010 PMID:20543076
14. C FM. A CV, P CD, J NV, P CR, A ÓC, Ll MC. Disfunción endotelial. Mecanismos e implicancias en Covid-19. Rev Hosp Clinico Univ Chil. 2021;32:•••. [cited 2024 Jul 20] Available from: https://revistahospitalclinico.uchile.cl/index.php/RHCUC/article/view/69442
15. Celermajer DS, Sorensen KE, Gooch VM, Spiegelhalter DJ, Miller OI, Sullivan ID, et al. Non-invasive detection of endothelial dysfunction in children and adults at risk of atherosclerosis. Lancet. 1992 Nov;340(8828):1111–5. https://doi.org/10.1016/0140-6736(92)93147-F PMID:1359209
16. Peters SA, den Ruijter HM, Bots ML, Moons KG. Improvements in risk stratification for the occurrence of cardiovascular disease by imaging subclinical atherosclerosis: a systematic review. Heart. 2012 Feb;98(3):177–84. https://doi.org/10.1136/heartjnl-2011-300747 PMID:22095617
17. Vlachopoulos C, Xaplanteris P, Aboyans V, Brodmann M, Cífková R, Cosentino F, et al. The role of vascular biomarkers for primary and secondary prevention. A position paper from the European Society of Cardiology Working Group on peripheral circulation: Endorsed by the Association for Research into Arterial Structure and Physiology (ARTERY) Society. Atherosclerosis. 2015 Aug;241(2):507–32. https://doi.org/10.1016/j.atherosclerosis.2015.05.007 PMID:26117398
18. Goff DC Jr, Lloyd-Jones DM, Bennett G, Coady S, D’Agostino RB, Gibbons R, et al.; American College of Cardiology/American Heart Association Task Force on Practice Guidelines. 2013 ACC/AHA guideline on the assessment of cardiovascular risk: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation. 2014 Jun;129(25 Suppl 2):S49–73. https://doi.org/10.1161/01.cir.0000437741.48606.98 PMID:24222018
19. Piepoli MF, Hoes AW, Agewall S, Albus C, Brotons C, Catapano AL, et al.; ESC Scientific Document Group. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J. 2016 Aug;37(29):2315–81. https://doi.org/10.1093/eurheartj/ehw106 PMID:27222591

 ORCID
ORCID