Gonzalo Henríquez 1 , Sebastian Inostroza 1 , Patricia Mogrovejo 2 , Christian Guentelican 1 , Sebastián Herrero 1 , Robin Estrada 2 , Isabel Quispe PhD, MSc. 3 , Waldo Merino MSc. 4 ,*, Francisco Rubilar 4 , Claudio Carcamo 4
Recibido: 22-04-2021
Aceptado: 08-07-2021
©2022 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 51 Núm. 3 pp. 273-280|https://doi.org/10.25237/revchilanestv5115031730
PDF|ePub|RIS
Abstract
Human health has been negatively impacted by the difficult environmental conditions produced by climate change. The health industry, paradoxically, generates a carbon footprint (CF) that drives climate change and represents 9.8% of the greenhouse gas (GHG) emissions in the United States (2013) and 6.3% of CF in England (2017). A considerable portion of these emissions comes from the clinical practice of anesthesia. Anesthetic gases present global warming potentials (GWPs) of up to 3,714 times higher than CO2 throughout their life cycles, from their manufacture and use to their disposal. In this context, this review compiled and assessed the environmental impacts of the anesthetic strategy in clinical practice, making use of the life cycle analysis tool. This review describes how the anesthetic technique has a major impact on CF, through the emission of GHG expressed through tools such as the GWP. As an example, at the manufacturing stage, the GWP of halogenated gases is up to 2,540 kg COeq versus 21 kg COeq for Propofol. This and other variables determine the contribution of the anesthetic technique in the emission of GHG. Finally, this review aims to help health care providers make informed decisions when considering the CH and sustainability of each anesthetic technique.
Resumen
La salud de las personas se ha visto afectada negativamente debido a las difíciles condiciones ambientales producidas por el cambio climático. La industria sanitaria, paradójicamente, genera una huella de carbono (HC) que impulsa el cambio climático y representa el 9,8% de las emisiones de gases de efecto invernadero (GEI) en Estados Unidos (2013) y el 6,3% de la HC en Inglaterra (2017). Una parte considerable de estas emisiones proviene de la práctica clínica de la anestesia. Los gases anestésicos presentan potenciales de calentamiento global (GWP) de hasta 3.714 veces superiores al CO2 a lo largo de su ciclo de vida, desde su fabricación y uso, hasta su eliminación. En este contexto, esta revisión compiló y evaluó los impactos ambientales de la estrategia anestésica en la práctica clínica, haciendo uso de la herramienta de análisis del ciclo de vida. Esta revisión describe como la técnica anestésica presenta un impacto de magnitud en la HC, a través de la emisión de GEI expresado a través de herramientas como es el GWP. Como ejemplo, en el caso de los gases halogenados estos pueden generar hasta 2.540 kg COeq en su etapa de fabricación frente a 21 kg COeq para el Propofol. Esta y otras variables determinan el aporte de la técnica anestésica en la emisión de GEI. Finalmente, esta revisión tiene como objetivo ayudar al cuerpo médico a tomar decisiones informadas al considerar la HC y la sustentabilidad de cada técnica de anestesia.
-
Introducción
La Organización Mundial de la Salud (OMS), en el año 2015 se refirió al cambio climático como el problema más importante para los sistemas de salud en el siglo XXI[1]. Gracias al cambio climático se han dado condiciones favorables para la transmisión de enfermedades como Dengue, Malaria, V. cho- lerae y otros. Los incendios forestales y condiciones extremas en precipitación, que han resultado en inundaciones y sequías, han impactado en la salud y el bienestar humano[2].
Toda actividad humana genera una HC, paradójicamente, la propia industria sanitaria es un contribuyente importante. En promedio los hospitales de países desarrollados producen un 2,1% de las emisiones de gases de efecto invernadero (GEI)[3]. En Estados Unidos, durante el año 2013, el sistema de salud fue responsable del 9,8% de los GEI, 30% más que el 2003[4], mientras que en Inglaterra el 2017, el departamento de salud y asistencia social produjo el 6,3% de la HC del país[5].
¿Cómo la actividad clínica impacta en la emisión de GEI? ¿Cuál es el aporte del sector y de la anestesia en particular? ¿De qué manera se emite CO2 en nuestra práctica clínica? Son preguntas que hoy están en alguna medida contestadas, aunque no completamente. Gracias a la información actualizada es posible comprender de mejor manera este tema y tomar decisiones para reducir la HC en técnicas de anestesia y mitigar su aporte al cambio climático.
El propósito de esta revisión es identificar las emisiones de GEI derivadas de la actividad anestésica junto a sus implicancias económicas y su impacto ambiental a través de la HC, aportando con información relevante para tomar medidas que permitan disminuir su contribución al cambio climático.
-
Material y Método
En esta revisión se realizó una síntesis de la literatura disponible acerca del impacto medioambiental, la HC, el impacto económico que tiene en el ámbito hospitalario y el impacto en la salud de la población que tienen las emisiones de GEI o equivalentes en la práctica profesional de la anestesiología. De tal manera que se ha realizado una búsqueda amplia. Se utilizó la base de datos PubMed. La estrategia de búsqueda utilizó términos Mesh: ((((anesthesia [MeSH Terms]) OR (“Anesthesiologists”[Mesh])) OR (“Anesthesiology”[Mesh])) OR (“Anesthetics”[Mesh])) AND (((((((“Greenhouse Effect”[Mesh]) OR (“Environmental Medicine”[Mesh])) OR (“Air Pollution”[Mesh])) OR (“Environmental Indicators”[Mesh])) OR (“Biological Monitoring”[Mesh])) OR (“Global Warming”[Mesh])) OR (“Car- bon Footprint”[Mesh])).
Se obtuvo como resultado un total de 483 artículos, a los cuales se les aplicó los siguientes filtros: publicados en los últimos 10 años, idioma inglés y español. Esto redujo los resultados a 79 publicaciones. Luego, se realizó un cribado por título y abstract. Posteriormente, se realizó una lectura completa de aquellos artículos seleccionados y fueron excluidos aquellos que no describieron información relevante. Finalmente, se agregaron un total de 7 artículos de conocimiento de los autores y encontrados a través de las referencias de los artículos obtenidos en la búsqueda sistemática. De esta manera, se obtuvo un total de 21 publicaciones.
Además, este estudio utilizó como referencia la metodología Análisis de Ciclo de Vida (ACV). El ACV es una técnica que ayuda a evaluar los posibles impactos ambientales de un determinado producto o servicio en todo su ciclo de vida, a través de la cuantificación de sus entradas y salidas. El ACV incluye la adquisición de la materia prima, producción, uso, tratamiento final, reciclado y disposición final, denominado de la cuna a la tumba. El proceso del ACV presenta un enfoque sistémico que consta de cuatro fases que interactúan entre sí: definición de objetivos y alcance, análisis de inventario, evaluación del impacto ambiental e interpretación de resultados, mostrados en la Figura 1. Esta herramienta contribuye en la identificación de oportunidades de mejora ambientales y en la toma de decisiones con respecto a las distintas etapas del ciclo de vida[6].
En el ACV, el concepto clave es la unidad funcional, el cual indica la función principal del sistema y sirve como unidad base de comparación entre las mediciones de los impactos ambientales de varios productos. En la presente revisión bibliográfica se utilizará estos conceptos para comparar diferentes técnicas anestésicas y sus impactos ambientales.
-
Desarrollo
En el ambiente hospitalario se emiten GEI, especialmente gases anestésicos, utilizados ampliamente en anestesia general, entre ellos sevoflurano, desflurano, isoflurano y N2O. Dentro de los cuales, el desflurano y N2O presentan los potenciales de calentamiento global más altos (de sus siglas en inglés GWP). Este indicador fue desarrollado para establecer una comparación entre distintos gases sobre el impacto y rol que juegan en el calentamiento global. Específicamente, es una medida de cuánta energía absorberán las emisiones de una tonelada de gas, en un período determinado (habitualmente 100 años) en relación a 1 tonelada de CO2. Cuanto más grande es el GWP, más calienta la tierra ese determinado gas, en un período, en comparación al CO2. Así, la medida para estimar los efectos invernaderos de diferentes elementos o fármacos es el GWP.
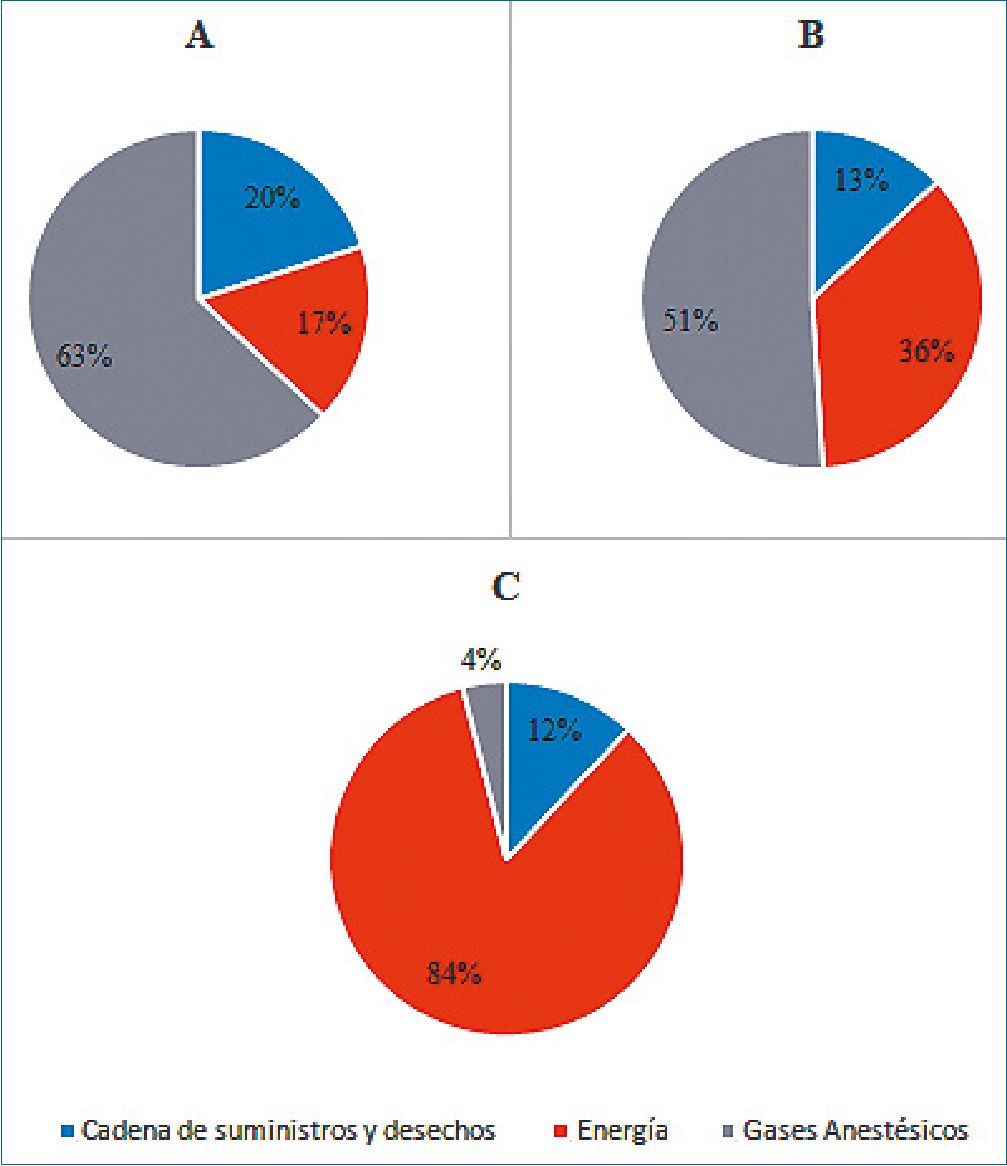
Figura 1. Fases de un ACV de acuerdo con la normativa ISO 14040.
Los fármacos anestésicos en general liberan GEI (CO2, metano, óxido nitroso, entre otros), son producidos por distintas actividades o procesos y liberados a la atmósfera donde absorben y re-emiten hacia la corteza la radiación infrarroja liberada por el sol impidiendo que parte del calor sea reflejado, permaneciendo en la tierra. Para comparar el GWP se usa como medida la unidad de CO2 equivalente (CO2eq) que es definida como la cantidad de CO2eq emitida que provocaría la misma intensidad radiante que una determinada cantidad de CO2[7],[8].
Hoy, los anestesiólogos tienen distintas alternativas para una práctica clínica sustentable, con la evidencia publicada de las emisiones de GEI de los diferentes fármacos utilizados, se puede estimar la cantidad de CO2eq que se emite a diario. Una descripción acerca del impacto de las diferentes técnicas anestésicas y estrategias para reducir los GEI es lo que se describe a continuación, a través de un enfoque ACV.
Anestesia general con halogenados
La práctica anestésica contribuye al calentamiento global mediante la liberación de gases al ambiente. Entre estos gases podemos mencionar los halogenados, como el halotano, isoflurano, sevoflurano y desflurano, los que tienen un GWP considerablemente más alto que el del CO2[8] (Tabla 1). De la misma forma el N2O, ampliamente usado en anestesia, juega un rol como GEI y aún más, hay evidencia que participa en la degradación del ozono atmosférico[9], como lo muestra la Figura 2.
La emisión de GEI por parte del desflurano es 15 veces las producidas por el isoflurano y 20 veces las del sevoflurano durante una anestesia general cuando se usa O2/aire, y cuando estos gases se suministran con N2O/O2, las emisiones aumentan en un 65% para el isoflurano y en casi 900% para el sevoflura- no[1] (Figura 3).
Las altas emisiones de desflurano se deben principalmente al proceso de fabricación del fármaco (su liberación al medio ambiente permite su permanencia en la atmósfera hasta 21,6 años) y la electricidad utilizada para su administración[8]. El iso- flurano y sevoflurano poseen perfiles de emisión de GEI similares, dados por residuos de gas anestésico. Sin embargo, cuando se usa O2/aire, el isoflurano tiene mayores emisiones asociadas
que el sevoflurano, en gran parte porque su factor GWP100 (potencial de calentamiento global en 100 años) es casi 4 veces mayor[1].
En este escenario en general, la relativa preferencia de los usuarios por sevoflurano hoy podría invertir las mayores emisiones por parte del sevoflurano que son cercanas al doble a las asociadas con isoflurano. Las emisiones del gas anestésico residual siguen el mismo patrón: Cuando se usa N2O/O2, la manufactura del N2O es la mayor fuente de impacto, donde la emisión de gases anestésicos residuales se incrementa en aproximadamente 200% en comparación a cuando se usa O2/aire[1].
En la Figura 3, para realizar la comparación de emisiones de las diferentes técnicas anestésicas (halogenados e intravenosa), los autores consideraron un alcance de cuna a tumba y como unidad funcional la concentración alveolar mínima (MAC) y, para propofol un MAC equivalente, que es mantener bajo anestesia a un paciente adulto de 70 kg promedio durante 1 hora (1 MAC-h).
En relación a la realidad chilena, Balkenhol et al, señalan que los gases anestésicos fueron la tercera fuente de emisión de GEI en el Hospital Base de Puerto Montt (HBPM) el 2016, alcanzando 10% del total de las emisiones de CO2eq. Dentro de los gases anestésicos, destacó el sevoflurano, que por sí solo alcanzó el 4° lugar de todos los agentes emisores. El amplio uso que se le da al sevoflurano contrasta con el escaso uso de desflurano, que a pesar de tener un mayor factor de emisión, su impacto al ambiente es menor. El isoflurano no estuvo presente en el arsenal farmacológico del hospital. Así, la emisión de CO2eq. a propósito de la práctica anestésica en el HBPM está principalmente compuesto por el uso de sevoflurano[7].
MacNeill AJ et al, en esta investigación, describieron la HC en tres hospitales de alta complejidad, uno en el Reino Unido, otro en Canadá y un tercero en Estados Unidos, complejizando el análisis con respecto al estudio de Puerto Montt, detallando aún más la información obtenida como es su fuente energética, entre otros, y comparándola entre ellos (Figura 4). Los resultados de este estudio muestran claramente que la fuente de energía, la técnica anestésica utilizada (halogenados) y la cadena de suministros y desechos, fueron los factores determinantes en la generación de CO2 equivalente de cada centro[10].
Algunos autores se han abstenido de recomendar directamente la TIVA como la alternativa más medioambientalmente sustentable a los gases halogenados, debido a la falta de información respecto a las emisiones producidas por el proceso de manufactura de anestésicos intravenosos y el manejo de sus residuos[1],[11]. Sin embargo, hoy se tiene acceso a esta información lo que permite comparar las emisiones del ciclo de vida de anestésicos inhalatorios e intravenosos directamente.
Tabla 1. Vida troposférica y Potencial de Calentamiento Global a 20 años de agentes anestésicos
| Compuesto | Vida (años) | GWP20 |
| Dióxido de carbono | 1 | |
| Sevoflurano | 1,2 | 349 |
| Isoflurano | 3,6 | 1.401 |
| Desflurano | 10 | 3.714 |
| Óxido nitroso | 114 | 289 |
Adaptado de: Ryan S, Nielsen C. Global Warming Potential of Inhaled Anesthetics, Application to Clinical Use. Anesthesia & Analgesia. 2010;111(1):92- 8.
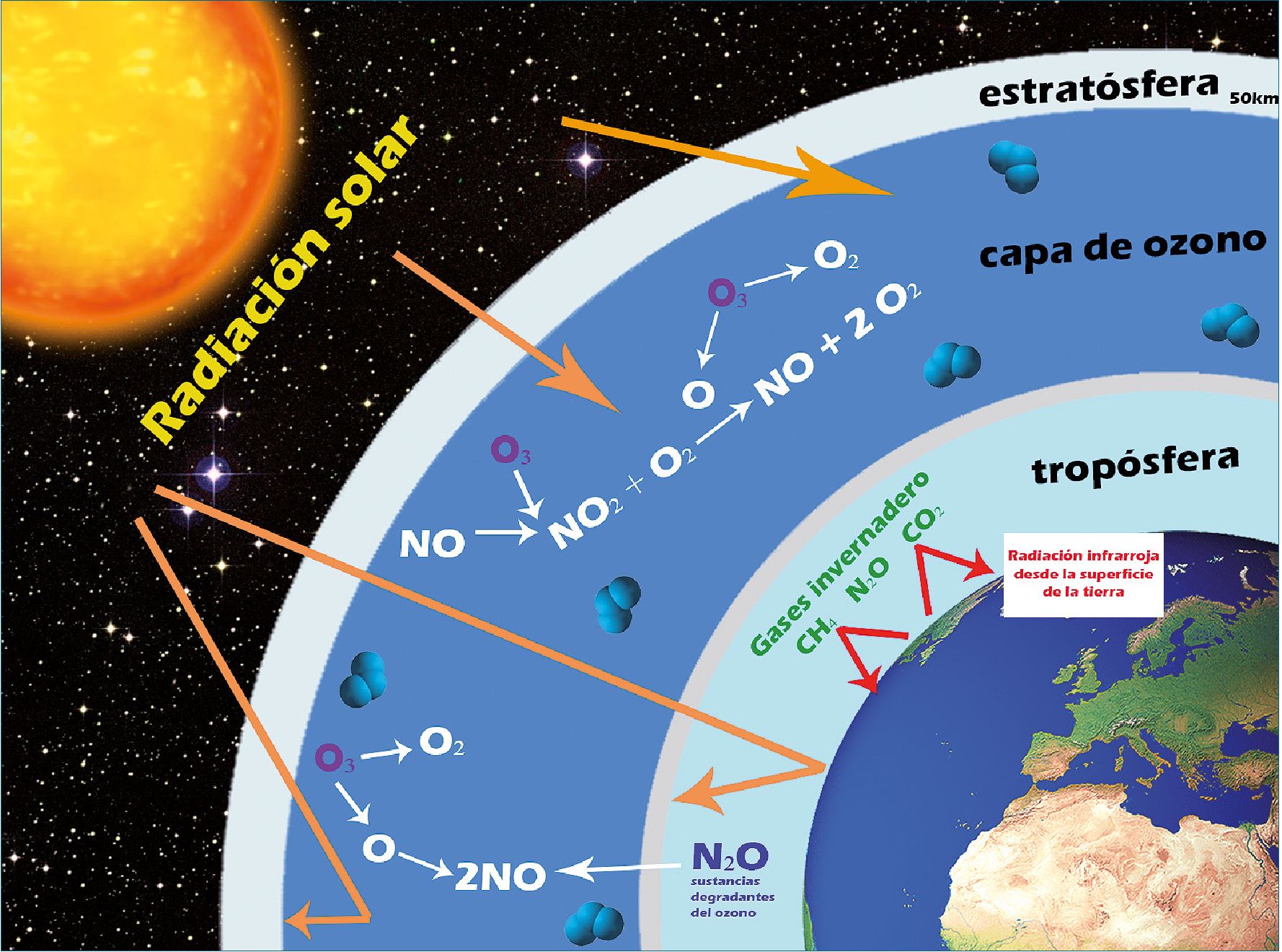
Figura 2. GEI, su interacción con la radiación solar y sus consecuencias sobre el planeta tierra. Adaptado de: Ichizawa Y. General Anesthetic Gases and the global Environment. Anesthesia-Analgesia 2011; 112 (1): 213-7.
Así, pensando en una práctica clínica sustentable, se plantean diferentes estrategias en la administración de la anestesia, como es evitar el uso de desflurano y N2O, administrar bajos flujos de gases frescos, sustituir la anestesia general inhalatoria por anestesia total intravenosa (por sus siglas en inglés TIVA)[1] o mejor aún, por anestesia regional cuando es posible.
Anestesia intravenosa y anestesia regional o local
En las últimas décadas ha habido un significativo aumento en el uso de agentes anestésicos intravenosos, tanto para sedación como anestesia general[12]. En comparación con los halo- genados, la administración de anestesia intravenosa no genera directamente emisiones de CO2eq.[11]. El impacto medioambiental de los fármacos intravenosos varían sustancialmente entre ellos por las grandes diferencias en las emisiones de CO2eq que aportan los procesos de manufactura de cada uno.
Hasta la publicación de Parvatker et al, el 2019, detalles sobre el proceso de manufactura del propofol no eran de dominio público y se desconocía su impacto medioambiental[11],[13]. A través del análisis y “scale up” de datos sobre la síntesis en laboratorios, se conoce que el GWP100 del proceso de manufactura del propofol es 22 kg CO2eq. Llama la atención la recientemente publicada lista de otros anestésicos, como la dex- medetomidina cuyo GWP100 es 3.006 kg CO2eq, midazolam 444 kg CO2eq, ketamina 140 kg CO2eq y remifentanilo 103 kg CO2eq. Por otro, lado el GWP100 de la lidocaína y la bupivacaína, fármacos utilizados extensamente en anestesia regional y local son 29 y 23 kg CO2eq, respectivamente[14].
Gracias a estos datos obtenidos por Parvatker, es posible comparar las emisiones de CO2eq entre gases y propofol, teniendo en cuenta las emisiones de la manufactura del último (Tabla 2). Este primer acercamiento a los aportes al calentamiento global de los diferentes fármacos aún no está completo, hace falta esclarecer del todo los métodos utilizados por la industria para la manufactura de estos fármacos y si las materias primas utilizadas para su producción provienen o no de fuentes sustentables. Aún más, hay otro aspecto a considerar antes de recomendar su uso en base al GWP100, esto es el manejo de residuos del propio fármaco y de los insumos para su uso.
En el caso del propofol su impacto de GEI es muy pequeño comparado con los anestésicos inhalatorios, en alrededor de 4 órdenes de magnitud, o sea entre 1.000 y 10.000 veces menores que el desflurano y el N2O. A diferencia de estas drogas el principal impacto de GEI que produce el propofol proviene de la energía necesaria para operar la bomba eléctrica para la jerin- ga[1] y de su proceso de manufactura. Al contrario de los gases halogenados, el propofol es rápido, extensamente metaboliza- do y es excretado a niveles de traza[1]. Sin embargo, rutinariamente se encuentra propofol en los basureros de pabellones, el 51% del propofol retirado de farmacia es desperdiciado[15]. El propofol no metabolizado entra en contacto con el medioam- biente de manera directa, como no se degrada, al ser ingerido por organismos acuáticos se acumula en el tejido adiposo y es tóxico. Requiere de incineración para ser eliminado apropiadamente[16]. Este hecho no está disponible en el análisis de su HC.
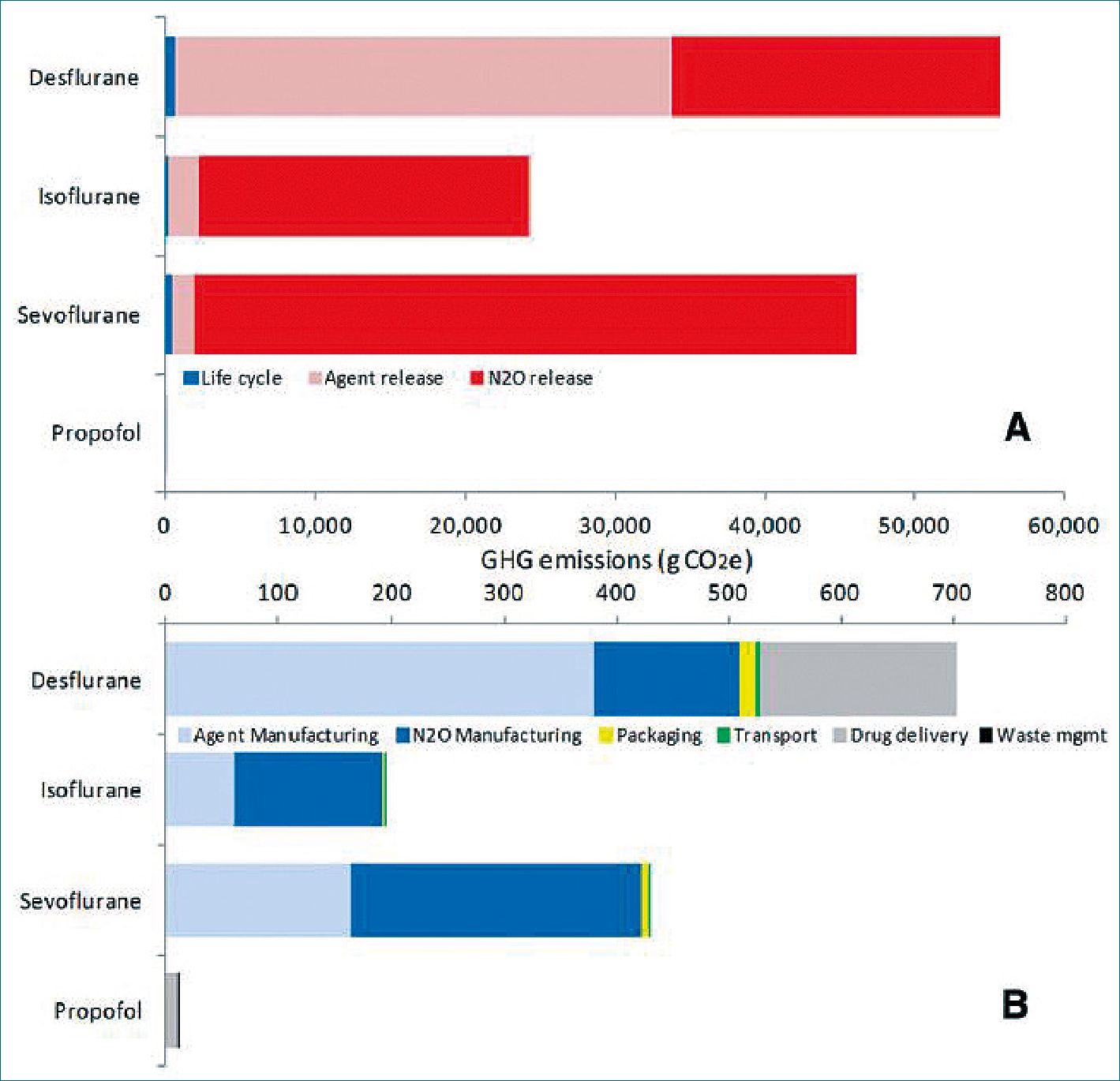
Figura 3. Emisiones de anestésicos de los GEI del ciclo de vida expresado en gramos de CO2 emitidos por la unidad funcional 1 MAC-h de un paciente adulto de 70 kg de peso. (A) Incluyendo las emisiones de gases anestésicos de desecho de fármacos halogenados y óxido nitroso (N2O). (B) excluyendo las emisiones de gases anestésicos de desecho. Extraído de: Sherman J, Le C, Lamers V, Eckelman M. Life Cycle Greenhouse Gas Emissions of Anesthetic Drugs. Anesthesia & Analgesia. 2012;114(5):1086-1090.
Tabla 2. Comparación del impacto al calentamiento global de anestésicos inhalatorios y propofol
| Fármaco | MAC% o Equivalente | Agente utilizado por MAC-h (g) | GWP
100 | CDE100 (g/h) |
| Desflurano* | 6,7% | 10,2 | 2.540 | 25.908 |
| Isoflurano* | 1,2% | 2,0 | 510 | 1.020 |
| Sevoflurano* | 2,2% | 8,0 | 130 | 1.040 |
| Propofol** | 100-140 mcg/kg/min | 0,42 – 0,558 | 21 | 8,82 – 11.718 |
*Datos obtenidos de Sherman J, Le C, Lamers V, Eckelman M. Life Cycle Greenhouse Gas Emissions of Anesthetic Drugs. Anesthesia & Analgesia. 2012;114(5):1086-1090. a excepción de CDE100.
**Datos calculados en base a dosis recomendadas. GWP100 obtenido de: Parvatker A, Tunceroglu H. Cradle-to-Gate Greenhouse Gas Emissions for Twenty Anesthetic Active Pharmaceutical Ingredients Based on Process Scale-Up and Process Design Calculations ACS Sustainable Chem. Eng. 2019, 7, 7, 6580-6591.
Con respecto a la manufactura del propofol, las farmacéuticas utilizan aceite de soya como materia prima para la elaboración del fármaco y en algunos no se revela si sus fuentes son sustentables o no[13]. Esto, sin duda, limita gravemente las comparaciones entre halogenados y TIVA en su impacto en el medio ambiente, pues falta información para estimar el ciclo de vida completo (ACV, detallado más adelante) y cómo afecta las diferentes categorías de impacto ambiental (consumo de agua, eutrofización, entre otros), aspecto que se desconoce.
Finalmente, se podría interpretar, de acuerdo con lo publicado por Parvatker y Macneill, que la anestesia regional tendría una menor emisión de GEI, con un mejor perfil ambiental, que la anestesia general con TIVA o halogenados, aunque está pendiente estimar el impacto ambiental de los residuos generados por las diferentes técnicas.
-
Medidas de mitigación
Sopesar el impacto que la práctica del cuidado sanitario genera sobre el medioambiente es solo el primer paso hacia un mejor futuro en términos de sustentabilidad, para generar un
balance ecológico, en donde se puedan preservar los recursos naturales y no dañar los distintos ecosistemas. El siguiente paso es realizar cambios, y esta transición a la sustentabilidad puede ser guiada por estudios de análisis de ciclo de vida (de las siglas en inglés LCA). Los ACV proveen información fundamental para tomar decisiones correctas a la hora de elegir entre distintos productos o procedimientos, teniendo en cuenta los costos que esto conlleva.
Es por esta razón que es importante generar conciencia entre el personal de salud, como ya se ha señalado, debido a que toda actividad humana tiene o genera una HC, desde la fabricación y uso de artículos o productos hasta cada uno de los procedimientos o actividades que se realizan, en este caso, todas las acciones hospitalarias.
Un ejemplo de lo anterior es el estudio realizado por Mc- Gain et al, en relación con el ACV de las bandejas de fármacos anestésicos, comparando las reutilizables (lavables) vs las de un solo uso. Los resultados mostraron que el uso de bandejas re- utilizables se asoció a emisiones de CO2eq similares, pero con un menor consumo de agua y menor costo que las bandejas de un solo uso. Además, el proceso de embalaje de bandejas con dos gasas de algodón y una toalla de papel fueron asociadas a un aumento dramático de las emisiones de CO2eq, consumo de agua y de los costos, motivo por el que esta práctica fue modificada[17].
En el mismo ejemplo, la evidencia permitió al Western Hospital (Melbourne, Australia) que posee 6 pabellones, cambiar de las bandejas de un solo uso con embalaje de gasa de algodón, a las bandejas reutilizables con gasa solo si era necesario. Se estima que esta nueva implementación generaría un ahorro de $6.500 dólares, 600 kg de emisiones de Kg CO2eq y 170.000 litros de agua cada año[17].
Ejemplos de medidas que se pueden adoptar: En relación con los agentes anestésicos se ha demostrado que la anestesia de bajo flujo reduce el costo y las emisiones (Tabla 3). Weinberg et al, estimaron el volumen y costo asociado de agente líquido utilizado para mantener una concentración alveolar de 1 MAC a varias tasas de entrada, y demostraron la ventaja farmacoeco- nómica de reducir el flujo de gas. Para un agente dado, el costo era lineal en relación con el flujo de gas, un flujo de 2 l/min tuvo un costo cuatro veces mayor que un flujo de 0,5 l/min[18].
Un aspecto importante es la exploración de actividades o formas de disminuir el desperdicio y mitigar el impacto ambiental de los anestésicos intravenosos. En un estudio publicado en el 2012 por Mankes RF, se demostró que al reemplazar botellas de propofol de 50 y 100 ml por botellas de 20 ml se logró disminuir el desperdicio de propofol de 29,2 mL/dia/contenedor a 2,8 ml/día/contenedor[16]. Asi se obtuvo una disminución en el impacto ambiental de su centro hospitalario, así como los costos asociados a este fármaco. Considerar el uso de TIVA como alternativa para disminuir las emisiones y/o disminuir la administración de N2O y desflurano, es una importante medida de mitigación que se fundamenta en los estudios realizados por Ryan et al[8].
Entre otras medidas de mitigación que se pueden realizar, respecto a los dispositivos médicos, el apagar las máquinas anestésicas y monitores cuando no se usan y evaluar modo “stand by” entre los casos de pacientes, generan posibles ahorros en cuanto a costos y energía[19]. El uso de gorro y zapatos lavables, individuales, y de uso exclusivo en pabellones evita el uso de plástico, ahorra dinero y costos medioambientales[11]. En cuanto al uso de jeringas, se obtienen beneficios tanto financieros como medioambientales, si se ajusta al mínimo el número de jeringas utilizadas en un mismo paciente[11]. En procedimientos de menos de una hora de duración es poco probable que los pacientes se beneficien de aparatos de calentamiento activos. De esta manera, evitando el calentamiento activo de todos los pacientes, se puede reducir el uso de plástico y de energía.
Por último, en relación con la frecuencia en la que los circuitos anestésicos deben ser lavados. Hartman et al, estudiaron el riesgo microbiológico que conlleva el uso extendido de los circuitos anestésicos respiratorios, y demostraron que, desde el punto de vista del riesgo de infección, el cambio de los circuitos es igualmente satisfactorio realizarlo cada 24, 48 o 72 h[20]. Es importante, nuevamente, señalar la importancia de efectuar estudios de ACV para tomar decisiones correctas como por ejemplo para elegir los circuitos anestésicos respiratorios, tanto en su opción reutilizable como la de un solo uso[11].
Otras medidas relevantes para mitigar las emisiones producidas por anestésicos incluyen la educación del personal sobre el impacto relativo en la HC que poseen distintos fármacos, así
Tabla 3. Comparación del impacto al calentamiento global de anestésicos inhalatorios de uso frecuente, por MAC-horas de uso a varios flujos de gas
| FGF (L/min) | Gramos/hora | GWP20 | CDE20 (g/h) | CDE20 ratio |
| 2% Sevoflurano | ||||
| 2 | 20,0 | 349 | 6.980 | 1 |
| 1,2% Isoflurano | ||||
| 0,5 | 2,8 | 1.401 | 3.881 | 0,6 |
| 1 | 5,5 | 1.401 | 7.762 | 1,1 |
| 2 | 11,1 | 1.401 | 15.551 | 2,2 |
| 6% Desflurano | ||||
| 0,5 | 12,6 | 3.714 | 46.796 | 6,7 |
| 1 | 25,2 | 3.714 | 93.593 | 13,4 |
| 2 | 50,4 | 3.714 | 187.186 | 26,8 |
Adaptado de: Ryan S, Nielsen C. Global Warming Potential of Inhaled Anesthetics, Application to Clinical Use. Anesthesia & Analgesia. 2010;111(1):92- 8; MAC = concentración alveolar mínima; GWP20 = Potencial de Calentamiento Global a 20 años; CDE20 = Dióxido de Carbono equivalente a 20 años.
| Tabla 4. Recomendaciones para disminuir la huella de carbono en pabellón | |
| Agentes anestésicos | Anestesia de bajo flujo
Considerar anestesia intravenosa siempre que sea posible Disminuir o evitar el uso de N2O y desfluorano |
| Dispositivos médicos | Apagar máquinas y monitores de anestesia cuando no se usen
Utilizar zapatos y gorros individuales, lavables y exclusivos para pabellón Considerar elementos reusables en pabellón (laringoscopios, herramientas quirúrgicas, máscaras laríngeas, etc.) Mínimo número de jeringas posible por paciente No calentar los fluidos de los pacientes, ni aportar calor al paciente si no es estrictamente necesario Considerar la frecuencia con que los circuitos anestésicos necesitan lavado |
| Iniciativas de sustentabilidad | Promover el reciclaje en pabellón Alentar prácticas sustentables |
| Reducir | Formar un comité o equipo multidisciplinario encargado del medioambiente en pabellón
Explorar las posibilidades de disminuir el desperdicio (reducir empaques, utilizar menos plástico, etc.) |
| Reusar | Considerar reutilizar dispositivos pertinentes tras limpieza y esterilización |
| Reciclar | Averiguar acerca de recicladores o plantas de reciclaje locales |
| Investigar | Averiguar con los fabricantes de los equipos el ciclo de vida de sus productos (fármacos y dispositivos mecánicos o eléctricos) |
Adaptado de: Balkenhol M, Castillo A, Soto M, Feijoo M, Merino W. Huella de Carbono en el Hospital Base de Puerto Montt. Revista Médica de Chile. 2018;146: 1384-1389.
como la educación sobre el uso óptimo de máquinas anestésicas (Tabla 4).
En 2018 Burrell R, señaló que a través de medidas que apelan a la competitividad y el trabajo en equipo como el cálculo mensual de emisiones de carbono provenientes de anestésicos en el departamento de anestesia y publicación mensual de dichos datos en formato gráfico a todos los miembros del departamento, entre otras, lograron en 3 años reducir las emisiones provenientes de gases anestésicos a aproximadamente en un tercio[21].
-
Discusión
La reciente información publicada en revistas científicas permite alcanzar una aproximación general acerca del impacto de la HC producida por la práctica anestésica y cómo mitigar el calentamiento global todos los días. Al mismo tiempo se obtuvo información relevante de las distintas formas en que este daño puede ser mitigado.
En estudios previos con ACV de gases anestésicos se ha recomendado la utilización TIVA para disminuir nuestros aportes con GEI, por su menor impacto ambiental. Sin embargo, la mayoría de estos estudios señalan que hace falta más información acerca del impacto global que genera la manufactura de los anestésicos intravenosos utilizados. Hoy, publicaciones como la de Parvatker: “Cradle-to-Gate Greenhouse Gas Emissions for Twenty Anesthe- tic Active Pharmaceutical Ingredients Based on Process Scale-Up and Process Design Calculations ACS Sustainable Chem”, entregan información sobre la HC producida por estos procesos de manufactura, calculados en base a datos de laboratorio, que nos acercan a poder decidir si la TIVA es efectivamente la alternativa medioambientalmente más sustentable en lo que a HC se refiere.
Al comparar tanto el GWP100 como el CDE100 entre anestésicos inhalatorios e intravenosos nos damos cuenta que el impacto medioambiental de los fármacos utilizados en TIVA es mucho menor a los gases, esto incluso teniendo en cuenta el hecho de que los fármacos intravenosos son normalmente utilizados en distintas combinaciones y además teniendo en cuenta las emisiones producidas por el transporte de estos anestésicos y el manejo de residuos como lo señalaba Sherman J. et al,[1]. Aún teniendo en cuenta un modelo donde se capture todo el gas halogenado y éste pueda ser desechado de manera segura, las emisiones producidas por la manufactura de los gases, su empaquetado y su transporte superan las emisiones producidas por el ciclo de vida de los fármacos utilizados en TIVA. Según los cálculos de Sherman et al, aún no es claro el lugar que ocupan los desechos como el plástico y el propofol sobrante que se elimina al medio ambiente donde no se degrada, tampoco conocemos acabadamente sus efectos en el agua y otros procesos medioambientales. Al respecto, autores como McGain, señalan que a través de simples cambios en la sala de operaciones tales como: uso de anestesia a bajo flujo, considerar uso de TIVA, evitar el uso N2O y desflurano, usar bandejas de anestésicos reutilizable, apagar las máquinas anestésicas y monitores cuando no se encuentra en uso, entre otros, permiten disminuir el desperdicio de fármacos de manera significativa[7].
Es importante mencionar que no siempre es posible realizar un ACV completo, esto debido a que los detalles de los procesos de manufactura de ciertos agentes anestésicos no se encuentran disponibles y las empresas no parecen dispuestas a facilitar esta información siempre. Este último punto nos parece de la mayor importancia, ya que el transparentar esta información, eventualmente, nos permitirá diseñar procesos clínicos y anestésicos sustentables. En términos de atención en salud es fundamental respetar el principio ético “primero no dañar”, aspecto que hoy no siempre cuidamos en la medida que el uso de gases y fármacos anestésicos resultan en la producción de GEI que aportan al cambio climático y este afecta la salud de las personas.
El análisis de las 3R; reciclar, reutilizar y reducir; sumado a los ACV, entregan una vasta información en relación a las medidas que se pueden adoptar en la práctica anestésica, innovar e investigar y mejorar la sustentabilidad medioambiental es un campo abierto a la investigación y la gestión.
Por lo tanto, hay un gran desafío por delante como profesionales clínicos e investigadores, obtener información para tomar medidas para entregar a los pacientes una técnica anestésica sustentable que permitan mitigar la contribución al cambio climático no pensando en el futuro sino en el presente. Hoy, la declaración oficial de universidades y sociedades científicas en el mundo señala “Estamos en Emergencia Climática”.
Agradecimientos: Se agradece a Fondecyt (Perú) por el soporte brindado.
Financiamiento: Proyecto CF-HEALTHSUD (código 21-CLIMAT-03; Climat Amsud).
Declaramos que ninguno de los autores de este trabajo presenta conflicto de intereses.
Referencias
1. Sherman J, Le C, Lamers V, Eckelman M. Life cycle greenhouse gas emissions of anesthetic drugs. Anesth Analg. 2012 May;114(5):1086–90. https://doi.org/10.1213/ANE.0b013e31824f6940 PMID:22492186
2. Watts N, Amann M, Arnell N, Ayeb-Karlsson S, Belesova K, Boykoff M, et al. The 2019 report of The Lancet Countdown on health and climate change: ensuring that the health of a child born today is not defined by a changing climate. Lancet. 2019 Nov;394(10211):1836–78. https://doi.org/10.1016/S0140-6736(19)32596-6 PMID:31733928
3. Wyssusek KH, Keys MT, van Zundert AA. Operating room greening initiatives – the old, the new, and the way forward: A narrative review. Waste Manag Res. 2019 Jan;37(1):3–19. https://doi.org/10.1177/0734242X18793937 PMID:30132405
4. Eckelman MJ, Sherman J. Environmental impacts of the U.S. healthcare system and effects on public health. PLoS One. 2016 Jun;11(6):e0157014. https://doi.org/10.1371/journal.pone.0157014 PMID:27280706
5. NHS Sustainable Development Unit. (2018). Reducing the use of natural resources in health and social care 2018 report. Recuperado de: https://www.sduhealth.org.uk/documents/Policy%20and%20strategy/20180912_Health_and_Social_Care_NRF_web.pdf (consultado el 10 de mayo, 2020).
6. International Organization for Standardization. Environmental Management: Life Cycle Assessment. Volume 14044. Principles and Framework; 2006.
7. Balkenhol M, Castillo A, Soto M, Feijoo M, Merino W. Huella de carbono en el Hospital Base de Puerto Montt. Rev Med Chil. 2018 Dec;146(12):1384–9. https://doi.org/10.4067/s0034-98872018001201384 PMID:30848740
8. Ryan SM, Nielsen CJ. Global warming potential of inhaled anesthetics: application to clinical use. Anesth Analg. 2010 Jul;111(1):92–8. https://doi.org/10.1213/ANE.0b013e3181e058d7 PMID:20519425
9. Ishizawa Y. Special article: general anesthetic gases and the global environment. Anesth Analg. 2011 Jan;112(1):213–7. https://doi.org/10.1213/ANE.0b013e3181fe02c2 PMID:21048097
10. MacNeill AJ, Lillywhite R, Brown CJ. The impact of surgery on global climate: a carbon footprinting study of operating theatres in three health systems. Lancet Planet Health. 2017 Dec;1(9):e381–8. https://doi.org/10.1016/S2542-5196(17)30162-6 PMID:29851650
11. McGain F, Story D, Kayak E, Kashima Y, McAlister S. Workplace sustainability: the “cradle to grave” view of what we do. Anesth Analg. 2012 May;114(5):1134–9. https://doi.org/10.1213/ANE.0b013e31824ddfef PMID:22523411
12. Yasny JS, White J. Environmental implications of anesthetic gases. Anesth Prog. 2012;59(4):154–8. https://doi.org/10.2344/0003-3006-59.4.154 PMID:23241038
13. Lane SF. The environmental sustainability of propofol use in daily practice. Br J Anaesth. 2020 Jun;124(6):e221–2. https://doi.org/10.1016/j.bja.2020.03.009 PMID:32252981
14. Parvatker A, Tunceroglu H, Sherman JD, Coish P, Anastas P, Zimmerman JB, et al. Cradle-to-Gate Greenhouse Gas Emissions for Twenty Anesthetic Active Pharmaceutical Ingredients Based on Process Scale-Up and Process Design Calculations ACS Sustainable. ACS Sustain Chem& Eng. 2019;7(7):6580–91. https://doi.org/10.1021/acssuschemeng.8b05473.
15. Gillerman RG, Browning RA. Drug use inefficiency: a hidden source of wasted health care dollars. Anesth Analg. 2000 Oct;91(4):921–4. https://doi.org/10.1097/00000539-200010000-00028 PMID:11004049
16. Mankes RF. Propofol wastage in anesthesia. Anesth Analg. 2012 May;114(5):1091–2. https://doi.org/10.1213/ANE.0b013e31824ea491 PMID:22415537
17. McGain F, McAlister S, McGavin A, Story D. The financial and environmental costs of reusable and single-use plastic anaesthetic drug trays. Anaesth Intensive Care. 2010 May;38(3):538–44. https://doi.org/10.1177/0310057X1003800320 PMID:20514965
18. Weinberg L, Story D, Nam J, McNicol L. Pharmacoeconomics of volatile inhalational anaesthetic agents: an 11-year retrospective analysis. Anaesth Intensive Care. 2010 Sep;38(5):849–54. https://doi.org/10.1177/0310057X1003800507 PMID:20865868
19. Chakladar A, White SM. Unnecessary electricity consumption by anaesthetic room monitors. Anaesthesia. 2010 Jul;65(7):754–5. https://doi.org/10.1111/j.1365-2044.2010.06398.x PMID:20642531
20. Hartmann D, Jung M, Neubert TR, Susin C, Nonnenmacher C, Mutters R. Microbiological risk of anaesthetic breathing circuits after extended use. Acta Anaesthesiol Scand. 2008 Mar;52(3):432–6. https://doi.org/10.1111/j.1399-6576.2007.01529.x PMID:18269394
21. Burrell RH. Primum non nocere: greening anaesthesia. Anaesth Intensive Care. 2018 Nov;46(6):630–1. PMID:30447678

 ORCID
ORCID