Rodrigo Fuentes G.1,*, Francesca Astele G.2
Recibido: 30-06-2022
Aceptado: 22-07-2022
©2023 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 52 Núm. 2 pp. 208-216|https://doi.org/10.25237/revchilanestv5228121402
PDF|ePub|RIS
EXITE-like procedure to treat gastroschisis, is anesthesia an issue? A retrospective cohort study
Abstract
Objectives: To describe the anesthetic techinque used during EXIT-like procedures and assess its effects in the overall success rate of the inter- vention. Methodology: Retrospective cohort study of 32 mother-newborn pairs with an antenatal diagnosis of gastroschisis in whom a primary closure was planned using the EXIT-like procedure. Results: In 26 (81.3%, 95%CI 63.5-92.8%) cases a successful closure of the abdominal de- fect was achieved. A slightly reduced success rate was found amongst patients receiving spinal anesthesia (71.4%) when compared with general (80.0%) and mixed techniques (86.7%), which did not reach statistical significance. Conclusions: No association was found between anesthesia technique and EXIT-like procedure success rates. Futher randomised studies are needed to confirm these findings.
Resumen
Objetivos: Describir la técnica anestésica actual utilizada para el cierre primario de la gastrosquisis mediante técnica Simil-EXIT y evaluar si esta condiciona a la tasa de éxito del procedimiento. Metodología: Análisis de una cohorte de 32 binomios madre-recién nacidos con diagnóstico antenatal de gastrosquisis en los que se planificó cierre primario mediante técnica Simil-EXIT entre los años 2010 y 2021 en el Hospital Carlos Van Buren. Resultados: Se reportó una tasa de éxito del procedimiento quirúrgico en 26 participantes (81,3%, IC 63,5%-92,8%), sin encontrar una diferencia estadística en relación con la técnica anestésica utilizada (espinal, general o general-espinal), aunque se encontró una menor tasa de éxito con la técnica espinal (71,4%, 80%, 86,7% respectivamente). Conclusiones: No se observó diferencia en la tasa de éxito de del procedimiento Simil-EXIT y su relación con la técnica anestésica utilizada. Sin embargo, no se puede descartar la superioridad de la técnica general o general-espinal con los datos obtenidos siendo necesario realizar un estudio clínico aleatorizado con un mayor número de participantes.
-
Introducción
La gastrosquisis corresponde a un defecto de la pared abdominal, generalmente menor a 4 cm, que conduce a la ubicación extra abdominal parcial y/o total de las vísceras a través de este defecto[1],[2]. Es la forma más frecuente de defectos congénitos de la pared abdominal, cuya incidencia ha ido en aumento durante las últimas décadas[1],[3], estimándose una incidencia de 5 a 10 casos por cada 10.000 recién nacidos vivos, con una mortalidad del 5%[4],[5].
El diagnóstico se hace usualmente de forma antenatal, mediante ecografía. El 5%-15% de los pacientes pueden presentar malformaciones extraintestinales asociadas. Estos elementos son importantes para planificar el manejo posterior de los recién nacidos con gastrosquisis, el que requerirá de equipos multidisciplinarios[1],[3].
Actualmente, el único tratamiento corresponde a la resolución quirúrgica[6]. Las metas de dicho tratamiento consisten en la reducción de las vísceras herniadas dentro de la cavidad peritoneal y su cierre, evitando generar trauma directo a las mismas o incrementos excesivos de la presión intraabdominal. Las alternativas quirúrgicas incluyen la instalación protésica de un silo, que permite una reducción visceral gradual seguida por un cierre parietal diferido, o bien a la reducción primaria seguida de un cierre precoz de la pared abdominal, ambas realizadas bajo anestesia general horas posterior al nacimiento[4],[6],[7].
Recientemente, se ha descrito el procedimiento denominado Símil-EXIT, desarrollado por Svetliza, que consiste en la reducción de las vísceras herniadas en el minuto cero, previo al pinzamiento del cordón umbilical, mientras se mantiene la oxigenación fetal por medio de la circulación útero placentaria sin requerir anestesia general para el recién nacido[8],[9],[10]. Si bien los estudios en torno a esta técnica son escasos, algunas de sus ventajas sobre las técnicas clásicas son: un menor tiempo de soporte ventilatorio invasivo y de nutrición paren- teral posopertorio con un inicio precoz de aporte enteral a diferencia de los métodos clásicos de cierre[11],[12]. El Hospital Carlos van Buren ha realizado este procedimiento a contar del año 2008, y al igual que la técnica original la selección de los recién nacidos se basa en criterios ecográficos prenatales de la gastrosquisis y la ausencia de otras patologías incompatibles con la vida.
Existe una importante controversia en relación a la técnica anestésica para permitir la realización de este procedimiento de manera segura y evitar la aparición de efectos secundarios y/o aumento del requerimiento de apoyo neonatal. Dentro de las técnicas descritas esta la anestesia neuroaxial materna, la anestesia neuroaxial materna con sedoanalgesia fetal y la anestesia general materno-fetal, en estas dos últimas el soporte se- doanalgésico y anestésico fetal se realiza a través del traspaso placentario de los fármacos o la administración directa fetal, facilitando la inmovilidad del neonato y evitando la deglución de aire hacia el intestino lo que podría aumentar la tasa de éxito del procedimiento[8],[11],[12],[13].
El objetivo primario de este trabajo es describir la técnica anestésica empleada en el Hospital Carlos van Buren y evaluar si esta condiciona la tasa de éxito en la reducción visceral mediante la técnica Símil-EXIT. Como objetivos secundarios se ha establecido evaluar la relación entre la técnica anestésica y el puntaje Apgar bajo 7 puntos en el primer y quinto minuto, la necesidad y tiempo de soporte respiratorio invasivo y tiempo de estadía en UCI de los recién nacidos.
-
Metodología
Previo a su ejecución, el presente estudio contó con la aprobación del Comité de Ética Científica del Servicio de Salud Valparaíso San Antonio, acreditado por el Ministerio de Salud en conformidad al Decreto 114 y la Ley 20.120 de la República de Chile.
Se realizó un estudio observacional de cohorte retrospectiva única que incluyo a mujeres embarazadas con diagnóstico eco- gráfico antenatal de gastrosquisis fetal, cuyo parto se produjo entre los años 2010 y 2021 en el Hospital Carlos Van Buren de Valparaíso, mediante una cesárea programada con indicación preoperatoria de eventual reducción visceral en el recién nacido mediante técnica Símil-EXIT. Se excluyeron de este estudio aquellas embarazadas con diagnóstico fetal de otra malformación congénita mayor asociada o incompatible con la vida, presencia de hallazgos ecográficos sugerentes de atresia intestinal y/o complicación de la gastrosquisis como son la dilatación severa de asas intestinales fetales intraabdominales o evisceración sobre las 32 semanas de gestación y aquellas sin diagnóstico antenatal de gastrosquisis fetal y que éste, se haya realizado posterior al trabajo de parto (estos neonatos se resolvieron mediante cierre primario deferido o mediante la instalación de un silo, de acuerdo a las condiciones de cada paciente).
De acuerdo con el protocolo de manejo obstétrico local de esta patología, a todas las pacientes se les indicó la interrupción del embarazo a la semana 34 de gestación mediante cesárea electiva, realizando previamente una doble maduración pulmonar fetal.
La técnica quirúrgica Símil-EXIT se puede dividir en dos procedimientos quirúrgicos: la cesárea propiamente tal y la cirugía del recién nacido. En la cesárea destaca la realización de una incisión amplia para permitir la salida del feto lo menos traumática posible. Una vez extraído el feto, éste es colocado en una cuña de paños clínicos sobre los muslos maternos. Uno de los objetivos primordiales es procurar mantener la circulación fetoplacentaria, evitando cualquier maniobra que pudiera desencadenar el desprendimiento placentario, de esta forma se asegura la oxigenación fetal y el paso de los agentes anestésicos manteniendo condiciones adecuadas para la reducción visceral. Posteriormente, comienza la reducción de ésta, la que se realiza según el orden de la herniación, preferentemente se reduce primero el colon y luego el intestino delgado. Durante la intervención, el equipo de cirujanos obstetras monitorea continuamente el latido del cordón, realizándose el pinzamiento de éste una vez finalizada la reducción o al cese de los latidos. En forma paralela, un neonatólogo monitoriza los latidos fetales con un fonendoscopio estéril y la aparición de material entérico en la boca, que es frecuente durante el proceso de reducción de la hernia.
Una vez realizado el pinzamiento del cordón, el recién nacido es trasladado a la servocuna; el neonatólogo inicia la asistencia del recién nacido con apoyo ventilatorio, usualmente mediante bolsa autoinflable, aun cuando no se haya conseguido completar la reducción de las asas. Una vez lograda la reanimación neonatal, el cirujano pediatra procede a realizar el cierre del defecto. De no lograrse este último paso, se lleva a cabo el manejo tradicional de la gastrosquisis, cubriendo las asas con polietileno estéril que se fija a la piel mediante un apósito adhesivo, para posteriormente realizar el cierre primario o reducción a gravedad (silo), según cada caso, en pabellón bajo anestesia general.
Posterior al nacimiento, a todos los recién nacidos son trasladados a UCI neonatal para monitorización, soporte ventila- torio del eventual distrés respiratorio y manejo específico del postoperatorio.
El manejo anestésico local para esta intervención ha variado a lo largo de los años, utilizándose diferentes técnicas anestésicas. En la actualidad, el objetivo anestésico fundamental es lograr una anestesia materno-fetal. Para ello, la técnica anestésica se inicia con la administración remifentanilo en infusión controlada por objetivo (TCI) aproximadamente 15 minutos antes del inicio de la cirugía; esto asociado o no, a la administración de morfina intratecal como parte del manejo analgésico posoperatorio de la embarazada (técnica general-espinal). Posteriormente, se realiza la inducción de la anestesia general con propofol como agente inductor, sumado a la administración de halogenados (sevofluorano), para alcanzar una concentración alveolar mínima (CAM) 0,8-1 durante la fase de mantención. Se administra succinilcolina y/o rocuronio como agente bloqueador neuromuscular, el cual se revierte o no previo a la emergencia de la anestesia. Se realiza monitorización no invasiva estándar (PANI; ECG, SPO2, ETCO2), monitorización de CAM, profundidad anestésica (SEDline®, SEDline Incorporated, Irvine, California, Estados Unidos) y medición del bloqueo neu- romuscular. Como analgesia intraoperatoria se utiliza metami- zol y ketoprofeno. Como retractores uterinos se utiliza como primera línea oxitocina y carbetocina, según preferencia de anestesiólogo.
De todas las fichas clínicas revisadas se obtuvo el perfil demográfico y clínico básico de todas las gestantes. Este perfil incluyó la información sobre la edad, paridad previa, patologías maternas previas (hipertensión esencial, síndromes hipertensi- vos del embarazo, diabetes mellitus pregestacional o gestacio- nal, obesidad, tabaquismo, consumo de alcohol o drogas). Asimismo, se obtuvo información respecto a la técnica anestésica utilizada espinal, general o general-espinal, el uso de opioides (incluyendo las dosis más altas y bajas de remifentanil según TCI), la CAM de sevofluorano empleada, el uso de fármacos concomitantes, incluyendo propofol, bloqueadores neuromus- culares, vasopresores (efedrina, atropina, fenilferina) y las medidas utilizadas para optimizar la retracción uterina, así como si éstas fueron exitosas o no. Estas medidas incluyeron fármacos como oxitocina, carbetocina, metilergonovina o procedimientos como la estimulación manual, sutura tipo B-Lynch. Se registraron los tiempos quirúrgicos, la necesidad de transfusión de hemoderivados durante la intervención y su cantidad.
Se tomó registro de los signos vitales maternos, considerando las cifras medias de presión arterial, así como sus valores mínimos y máximos durante la cirugía. El mismo procedimiento se empleó para la frecuencia cardíaca, dióxido de carbono espirado (ETCO2). La profundidad anestésica se cuantificó mediante algoritmos de electroencefalografía continua durante el pabellón (SEDline®).
También se recopiló información del protocolo quirúrgico fetal y de atención del parto. Dentro de los datos a considerar se incluyó el tiempo de reducción intestinal, el tiempo total de reducción y el tiempo al pinzamiento del cordón. Se evaluó las cifras del puntaje APGAR al minuto y los 5 minutos de los recién nacidos, así como su peso de nacimiento, talla y perímetro craneano. Se registró la necesidad de asistencia con instrumentos de ventilación positiva, su tipo en específico (bolsa autoinflable, C-PAP, intubación orotraqueal), y el tiempo de permanencia de ventilación mecánica invasiva (VMI) y tiempo de estadía en UCI.
Se llevó a cabo un análisis estadístico descriptivo en base a medias, desviaciones estándar, medianas, rangos intercuartíli- cos, frecuencias absolutas y relativas. Para el análisis inferencial se utilizó las pruebas t de Student o de Mann Whitney para la comparación de medias según las características de distribución y varianzas de los datos obtenidos, y la Prueba Exacta de Fisher para la evaluación de variables cualitativas. Se cuantificó la magnitud de eventuales asociaciones mediante el estadístico Odds ratio (OR), el que se acompañó de las correspondientes estimaciones de intervalo de confianza del 95%. Asimismo, se empleó dicha herramienta para obtener estimadores poblacio- nales de datos descriptivos relevantes, como la frecuencia de cierre exitoso de la pared abdominal.
Los desenlaces que contemplaron un tiempo a un evento, como el tiempo requerido en soporte ventilatorio invasivo o en UCI, se estudiaron mediante curvas de supervivencia de Ka- plan-Meier. Eventuales contrastes entre grupos se compararon mediante el estadístico logrank. Todos los datos se analizaron por un estadístico independiente utilizando el software STATA v.16.1® (StataCorp LP, 1996-2020).
-
Resultados
-
Características de las participantes
La base de datos está compuesta por 32 binomios materno- recién nacido. En 26 recién nacidos (81,3%, IC95% 63,5%- 92,8%) se logró el cierre primario del defecto de la pared abdominal.
La edad mediana de las gestantes fue de 23 años, con una edad gestacional de 34 semanas. Veintiún mujeres (65,6%) era primigestas. No hubo casos de hipertensión pregestacional, eclampsia, diabetes gestacional o pregestacional en la muestra.
Al comparar las características de las participantes según el resultado del cierre primario del defecto de pared abdominal, no se encontraron diferencias en ninguna de las características de la madre. Se muestra un resumen de estas en la Tabla 1.
-
Características del recién nacido
Los recién nacidos de la presente cohorte tuvieron un peso mediana de nacimiento de 2.010 g. El puntaje Apgar al minuto fue de 5 puntos (RIC 4-8 puntos), mientras que el de 5 minutos fue de 8 puntos (RIC 6-9 puntos), como se muestra en la Tabla 1. Al comparar los puntajes Apgar según las técnicas anestésicas empleadas, se observó un menor puntaje en el primer minuto en el grupo de recién nacidos con madres sometidas a anestesia general o general-espinal (p = 0,032), esta diferencia desaparece al quinto minuto. Se describen estos resultados en la Tabla 2.
Tabla 1. Características clínicas de las participantes
| Característica | Cierre fallido (n = 6) | Cierre exitoso (n = 26) | Total (n = 32) | Valor p |
| Características de la madre | ||||
| Edad | 22,5 (21-27) | 23 (19-25) | 23 (20-26) | 0,761 |
| Edad gestacional (sem) | 33 (33-34) | 33 (33-34) | 34 (33-34) | 0,511 |
| Paridad n, (%) Primigesta | 3 (50) | 18 (69,2) | 21 (65,6) | |
| Multípara | 2 (33,3) | 5 (19,2) | 7 (21,9) | 0,522 |
| Gran Multípara | 1 (16,7) | 3 (11,5) | 4 (12,5) | |
| Estado nutricional n, (%) Eutrófica | 1 (16,7) | 11 (42,3) | 12 (37,5) | |
| Sobrepeso | 2 (33,3) | 6 (23,1) | 8 (25,0) | 0,612 |
| Obesidad | 3 (50) | 9 (34,6) | 12 (37,5) | |
| Hipertensión pregestacional n, (%) | 0 | 0 | 0 | – |
| Preeclampsia n, (%) | 0 | 0 | 0 | – |
| Diabetes gestacional o pregestacional n, (%) | 0 | 0 | 0 | – |
| Infección por virus de la inmunodeficiencia humana n, (%) | 0 | 0 | 0 | – |
| Tabaquismo n, (%) | 1 (16,7) | 2 (7,7) | 3 (9,4) | 0,482 |
| Alcoholismo n, (%) | 1 (16,7) | 2 (7,7) | 3 (9,4) | 0,482 |
| Abuso de sustancias n, (%) | 0 | 1 (3,9) | 1 (3,1) | > 0,992 |
| Características del Recién Nacido | ||||
| Peso de nacimiento (g) | 1.930 | 2.100 | 2.010 | 0,401 |
| (1.870-1.965) | (1.920-2.290) | (1.895-2.265) | ||
| Talla de nacimiento (g) | 42 | 44 | 43,0 | 0,151 |
| (42) | (42-46) | (42,0-45,5) | ||
| Circunferencia craneana | 30,5 | 31 | 31,0 | 0,351 |
| (30-32) | (30-32) | (30,0-32,0) | ||
| Puntaje Apgar 1 min | 5 (4-8) | 5 (3-8) | 5 (4-8) | 0,891 |
| Puntaje Apgar 5 min | 9(7-9) | 8 (6-9) | 8 (6-9) | 0,241 |
| 1Prueba de Mann-Whitney. Valores corresponden a mediana y (RIC); 2Prueba Exacta de Fisher; RIC: Rango Intercuartil. | ||||
Tabla 2. Resultados Puntaje Apgar al primer, quinto minuto y máximo soporte ventilatorio recibido según técnica anestésica
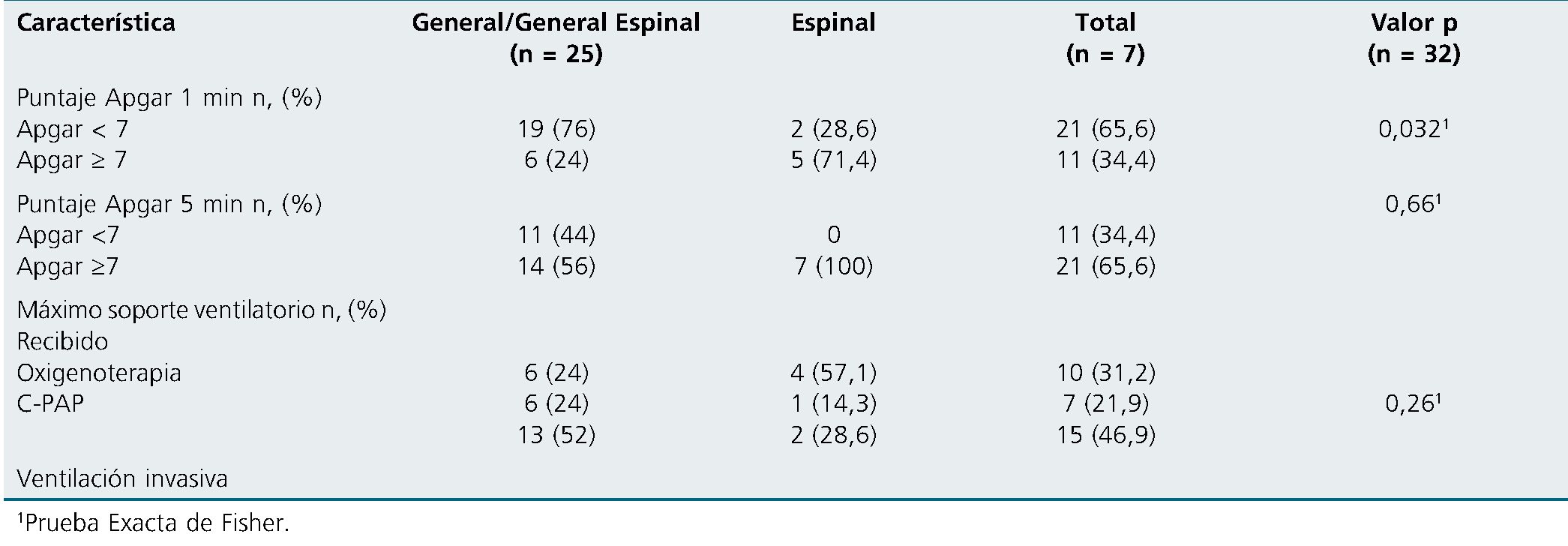
Tabla 3. Características de la anestesia y cirugía
| Característica | Cierre fallido (n = 6) | Cierre exitoso (n = 26) | Total (n = 32) | Valor p |
| Tiempo anestésico total minutos
Técnica anestésica utilizada n, (%) |
60
(60) |
67,5 (60 – 75) | 60 (60-75) | 0,331 |
| Espinal | 2 (33,3) | 5 (19,2) | 7 (21,9) | 0,842 |
| General | 2 (33,3) | 13 (50,0) | 15 (46,9) | |
| General-Espinal | 2 (33,3) | 8 (30,8) | 10 (31,2) | |
| Mínima de remifentanilo empleada | 3,9 | 4,0 | 4 | |
| (2,5-5,9) | (3,0-4,0) | (3,0-4,5) | 0,821 | |
| Máxima de remifentanilo empleada | 4,9 | 7.0 | 6 | |
| (3,7-6,0) | (4,5-8,0) | (4,5-8,0) | 0,291 | |
| Dosis total de opioides empleada | 5,0 | 6.5 | 6 | |
| (3,0 – 10,0) | (5,0 – 8,0) | (5,0 – 8,0) | 0,821 | |
| MAC de sevofluorano | 1,0 | 1,0 | 1,0 | |
| (0,8-1,4) | (0,8-1,0) | (0,8-1,2) | > 0,991 | |
| Uso de propofol n,(%) | 4 (66,7) | 21 (80,8) | 25 (78,1) | 0,59 |
| Uso de bloqueantes neuromusculares n, (%) | 4 (66,7) | 19 (73,1) | 23 (71,9) | > 0,992 |
| Uso de efedrina o fenilefrina n, (%) | 5 (83,3) | 26 (100) | 31 (96,9) | 0,192 |
| Uso de atropina n,(%) | 2 (33,3) | 8 (30,8) | 10 (31,3) | > 0,992 |
| PAM durante la cirugía (mmHg) | 78,5 (73-80) | 80 (77-87) | 80 (75-87) | 0,581 |
| PAM mínima durante la cirugía (mmHg) | 63 (57-70) | 63 (60-67) | 63 (60-67) | 0,971 |
| PAM máxima durante la cirugía (mmHg) | 95 (83-97) | 91,5 (87-97) | 93 (85-97) | 0,821 |
| Frecuencia cardiaca durante la cirugía (lpm) | 90 (80-100) | 80 (80-90) | 85 (80-90) | 0,511 |
| ETCO2 durante la cirugía (mmHg) | 34,5 (33,5-36,0) | 35,0 (32,0-37,0) | 35,0 (33-0-37,0) | 0,821 |
| Uso de oxitocina n, (%) | 6 (100) | 26 (100) | 32 (100) | > 0,992 |
| Uso de carbetocina n, (%) | 0 | 2 (7,7) | 2 (6,25) | > 0,992 |
| Uso de metilergonovina n, (%) | 2 (33,3) | 9 (34,6) | 11 (34,3) | > 0,992 |
| Tiempo quirúrgico total minutos | 42,5 (38 – 70) | 40,0
(31 – 50) |
40 (35-50) | 0,341 |
| Tiempo de reducción intestinal minutos | – | 9 (3-12) | 9 (3-12) | – |
| Tiempo total de reducción minutos | – | 8 (3-17) | 8 (3-17) | – |
| Tiempo de clamp del cordón segundos | 65
(65) |
113,5 (90-150) | 110 (65-150) | 0,531 |
| Estimulación manual uterina n,(%) | 0 | 0 | 0 | – |
| Instalación de sutura (B-Lynch o equivalente n, (%) | 0 | 0 | 0 | – |
| 1Prueba de Mann-Whitney. Valores corresponden a mediana y (RIC); 2Prueba Exacta de Fisher; RIC: Rango Intercuartil. | ||||
-
Características de la anestesia
La técnica anestésica más frecuentemente empleada fue la anestesia general con 15 pacientes (46,9%), seguida por la anestesia general-espinal (10 pacientes, 31,2%) y la anestesia espinal (7 pacientes, 21,95%). Al dividir la cohorte en dos periodos (2010-2015 y 2016 a 2021), se apreció una disminución en la preferencia de la técnica espinal (46,2% vs 5,3%) y un aumento en el empleo de la técnica general-espinal (0% a 52,6%), lo que alcanzó significancia estadística (p = 0,001). El tiempo anestésico total correspondió a una mediana de 60 minutos, siendo discretamente mayor entre pacientes que fueron sometidas a técnica general-espinal, con una mediana de 72,5 minutos (Kruskall & Wallis p = 0,07). En la Tabla 3 se describen las características de la anestesia y monitorización hemodinámi- ca de los procedimientos.
Al comparar las cifras de éxito en el cierre primario según técnica anestésica, se apreció que las menores tasas se obtuvieron con la anestesia espinal (71,4%, IC95% 29,0%-96,0%), seguidas por la técnica general-espinal (80,0%, IC95% 44,4%- 97,4%) y la técnica general (86,7%, IC95% 59,5%-98,3%). No obstante, al contrastar las técnicas utilizadas entre pacientes con cierre primario exitoso y fallido, no se apreciaron evidencias de una diferencia estadísticamente significativa (p = 0,84). Se muestra un resumen de las tasas de éxito del cierre primario del defecto en el Gráfico 1.
-
Características de la cirugía
La mediana de tiempo quirúrgico total fue de 40 minutos. Los tiempos mediana de reducción intestinal y de reducción total fueron de 9 (3-12 minutos) y 8 (3-17 minutos), respectivamente. La mediana del tiempo del pinzamiento del cordón en segundos fue de 110 segundos. Se logró una retracción uterina exitosa en todos los casos, sin necesidad de transfusión de glóbulos rojos ni estimulación manual uterina o la instalación de una sutura (tipo B-Lynch o equivalente) en ninguna de las pacientes. Se muestra un resumen de las características de la cirugía en la Tabla 3.
-
Desenlaces clínicos
La mediana de tiempo de estadía en UCI fue de 22 días (RIC 17-27 días). Esta última fue significativamente mayor entre los recién nacidos en los que no se logró el cierre primario del defecto (45 RIC 31-84 días vs 21,5 RIC 17-24 días, p < 0,001). Todos los recién nacidos sobrevivieron hasta el alta de la UCI. Se muestra el perfil temporal del tiempo al egreso de la UCI en el Gráfico 2.
Se evidenció que 15 recién nacidos (46,9%) requirieron soporte ventilatorio con VMI. Al comparar los requerimientos de VMI según la técnica anestésica empleada o el resultado del cierre primario, no se observaron diferencia significativa (p = 0,26 y p = 0,21 respectivamente). Aunque el soporte de VMI en horas, fue significativamente mayor en el grupo de cierre fallido (504 horas RIC 264-672 vs 0,33 RIC 0,33-24, p < 0,002). Se detallan los resultados de soporte ventilatorio y horas en VMI en las Tablas 2 – 4 y perfil temporal de tiempo en VMI en el Gráfico 3.
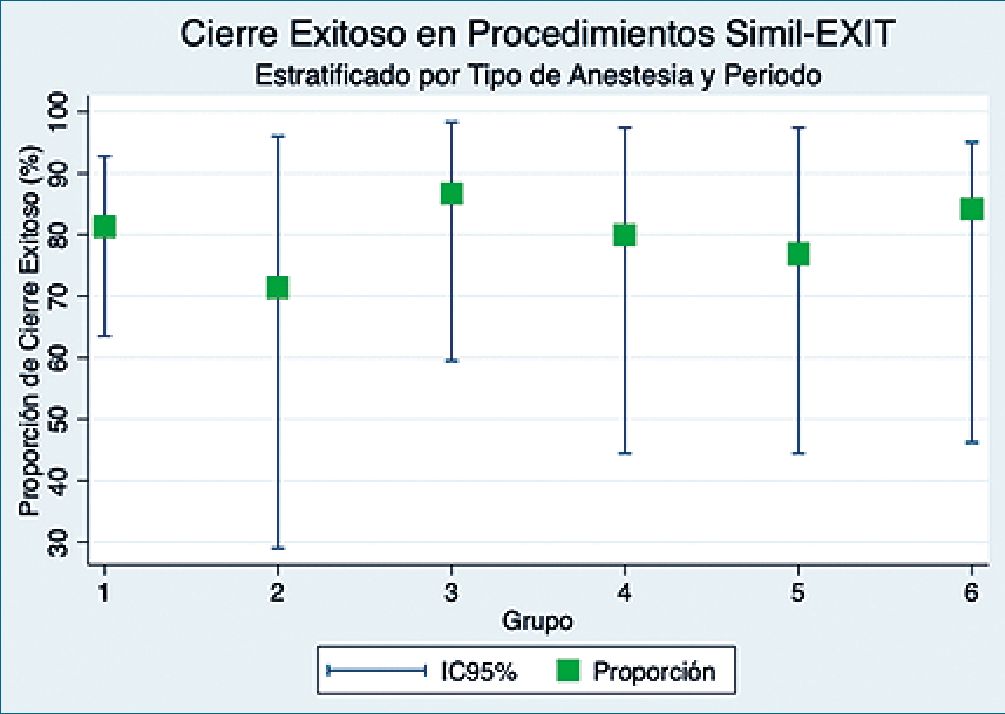
Gráfico 1. 1 Proporción Global de cierre exitoso; 2 Anestesia espinal; 3 Anestesia general; 4 Anestesia general-espinal; 5 Período 2010-2015; 6 Período 2016-2021.
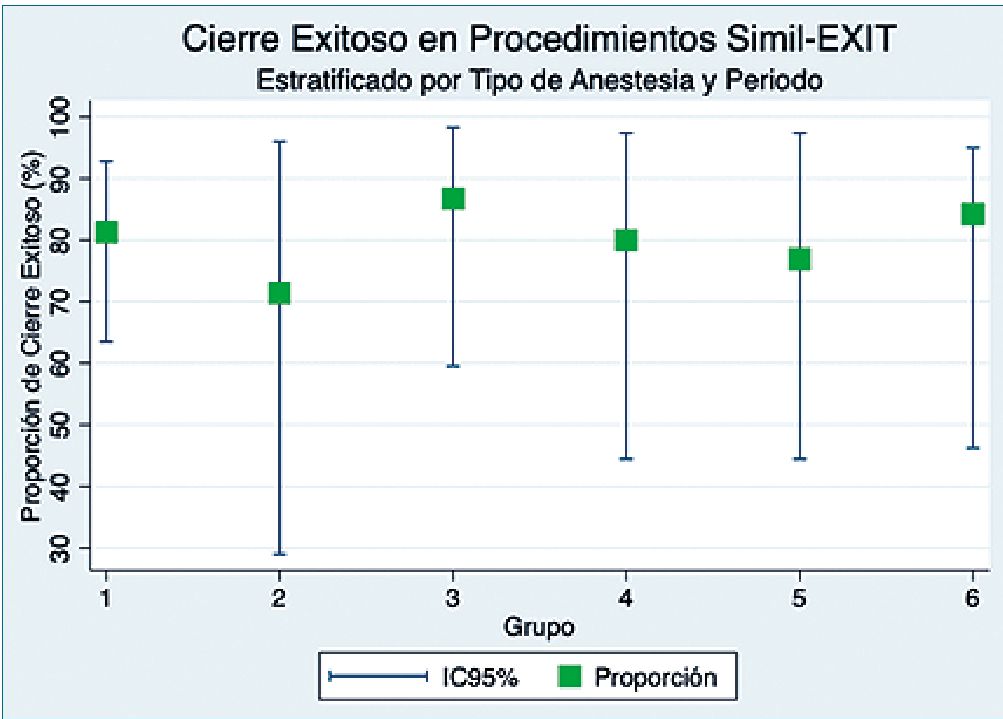
Gráfico 2. Estadía en UCI.
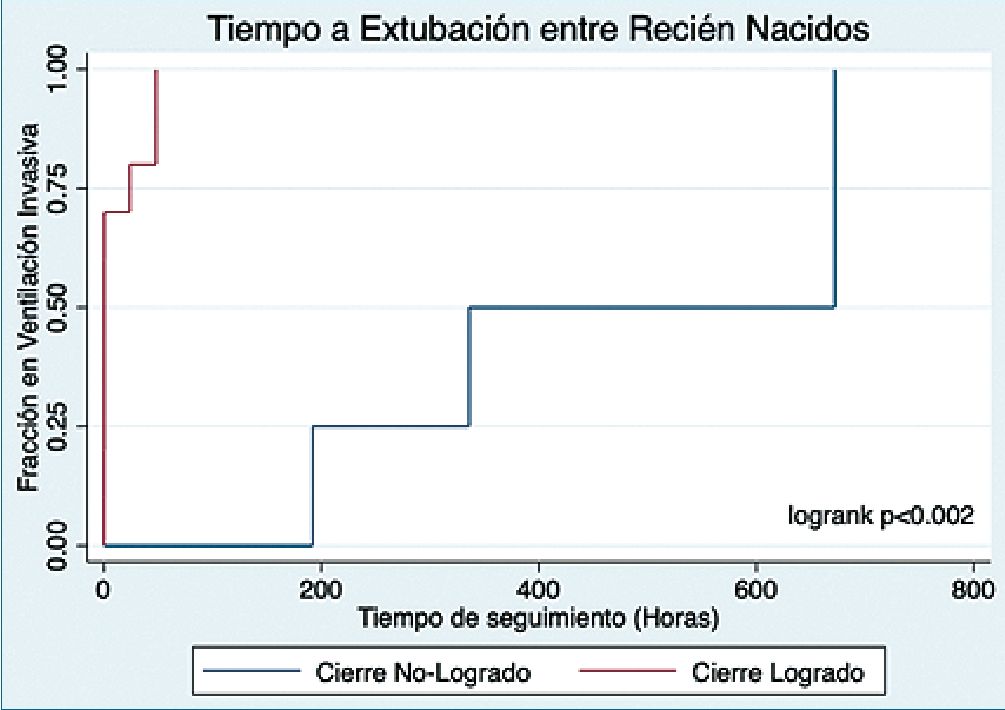
Gráfico 3. Tiempo a extubación entre recién nacidos.
-
Discusión
El Símil-EXIT corresponde a una técnica descrita por Svetliza el año 2007, la cual deriva del procedimiento EXIT (Ex Utero Intrapartum Treatment) descrito por Norris et al. en 1980[14], en que se establece una vía aérea segura sin interrupción de la circulación materno fetal; fue recomendado inicialmente para el manejo de la oclusión traqueal en recién nacidos con hernias diafragmáticas congénitas, ampliándose su indicación para diferentes patologías (EXIT-to-airway, EXIT-to-ECMO, EXIT-to- resection), siendo fundamental para ello establecer un plano anestésico materno-fetal mediante el paso transplacentario de agentes anestésicos[15].
En esta cohorte estudiada durante los años 2010 a 2021, se observó al igual que en otros estudios un predominio de madres menores de 25 años[1],[4], sin encontrar diferencias estadísticas entre los grupos estudiados. La interrupción del embarazo se realizó a las 34 semanas, del mismo modo que en centros internacionales en donde se realiza una cesárea programada como parte de la planificación del manejo de la gastros- quisis[12],[16],[17].
La técnica anestésica para la resolución quirúrgica de la gastrosquisis mediante procedimiento Simil-EXIT sigue siendo materia de debate, sin existir aún un protocolo unificado que evidencie ser el mejor soporte materno-fetal para condicionar el éxito de este. El Hospital Carlos van Buren ha sido muestra de esto, evolucionado desde la anestesia espinal para la madre a una anestesia materno-fetal con una técnica general o general- espinal la cual ha predominado en los últimos 5 años. Si bien, la técnica anestésica empleada en los primeros casos realizados corresponde a lo descrito por el procedimiento de Svetliza[8], es decir, una anestesia espinal materna sin elementos de sedación o anestesia fetal, nuestro manejo actual se ha modificado para lograr una anestesia general para la gestante mediante halogenados, asociado al uso de remifentanilo en infusión para obtener fundamentalmente un plano de sedación o anestesia del recién nacido que permita la reducción visceral sin presentar movimientos, llanto ni deglución de aire que puedan condicionar el fracaso del procedimiento, como también abarcar el manejo del dolor durante el procedimiento quirúrgico.
Esto se fundamenta en los estudios que demuestran el rápido traspaso de remifentanilo al feto (F/M 0,8-0,7), y una rápida metabolización por esterasas plasmáticas (AU/VU 0,26-0,33) [18],[19], lo que limitaría su efecto clínico al suspender su infusión. Según el estudio de Noskova[20], en neonatos que nacen por cesárea con anestesia general con uso de remifentanilo al momento de la inducción, se observó un puntaje Apgar menor al minuto (0-7) y una mayor necesidad de estimulación táctil para el inicio de la respiración, sin encontrar diferencias en el puntaje a los 5 minutos ni en la necesidad de soporte ventilatorio con CPAP o invasivo.
En cuanto a los halogenados, el bajo coeficiente de partición sangre:gas para el sevofluorano (0,69), permite un incremento rápido en la sangre materna, un fácil traspaso a través de la barrera placentaria y una rápida eliminación al suspender su administración[21]. Este fármaco cumple dos importantes objetivos. El primero consiste en su efecto tocolítico[22], el cual disminuiría el riesgo de separación de la placenta al útero durante la reducción visceral, manteniendo así la circulación feto- placentaria a expensas de un mayor riesgo de sangrado opera- torio[21],[25],[26]. El segundo objetivo, corresponde al efecto anestésico en el recién nacido, el cual se consigue mediante el traspaso transplacentario del halogenado. Distintos estudios han comparado la anestesia general versus la anestesia regional con relación al puntaje Apgar al primer y quinto minuto como marcador de bienestar del recién nacido, encontrando resultados dispares[21],[25],[26]. Una revisión de la base de datos Co- chrane confirma la ausencia de diferencias significativas en los puntajes y en otros desenlaces como la necesidad de oxígeno para reanimación y valores de gasometría vena umbilical[27].
Al igual que lo descrito previamente, en esta cohorte de estudio se encontraron resultados dispares, destacando en el primer minuto puntajes Apgar bajos (< 7), con diferencia significativa en aquellos neonatos de madres sometidas a técnica anestésica general o general-espinal. Esta diferencia desaparece al quinto minuto, lo que puede ser explicado por la rápida metabolización y eliminación de los agentes anestésicos una vez realizado el pinzamiento del cordón.
En esta revisión se evidenció que, a pesar de no existir una diferencia significativa en relación a la técnica anestésica utilizada y la tasa de éxito procedimiento Simil-EXIT, este último es 8,6 y 15,3 puntos superior al utilizar una anestesia general- espinal o general respectivamente versus una técnica espinal (71,4%), lo que podría sugerir mejores condiciones anestésicas para la reducción del defecto con las primeres técnicas señaladas. Esta ausencia de significancia estadística se debe principalmente al escaso número de participantes incluidas en esta revisión, lo cual no descarta la posibilidad de superioridad de la técnica mixta o general sobre la anestesia espinal.
En los recién nacidos en que no se logró el cierre primario, se observó el doble de tiempo estadía en UCI (45 versus 21,5 días), lo que se correlaciona con el mayor tiempo de soporte de VMI y la planificación para resolver el defecto mediante cierre diferido mediante instalación de Silo o el cierre primario diferido. La asistencia de soporte VMI fue necesaria en el 46,9% de los recién nacidos independiente del resultado del cierre primario, sin embargo, hay una diferencia significativa en el tiempo total de soporte invasivo el cual va desde una mediana de 0,33 h para el grupo de cierre exitoso hasta 504 h para el grupo de cierre fallido. Esto nos parece importante destacar debido a que el éxito del cierre del defecto condicionaría menores tiempos de VMI y por tanto, menor estadía en UCI, lo que podría conseguirse con las mejores tasas de reducción con las técnicas general-espinal y/o general. En un reciente estudio retrospectivo multicéntrico que comparó resultados clínicos entre un cierre primario y el cierre gradual con silo en distintos tiempos (menos de 5, 6-10 y más de 10 días), evidenció que la demora en lograr el cierre con la técnica del silo fue un factor significativo en el tiempo en soporte ventilatorio[28].
Tabla 4. Desenlaces clínicos según resultado de la cirugía
| Característica | Cierre fallido (n = 6) | Cierre exitoso (n = 26) | Total | Valor p (n = 32) |
| Tiempo de estadía en UCI días | 45 (31-84) | 21.5 (17-24) | 22 (17-27) | < 0,0011 |
| Máximo soporte ventilatorio recibido (n, %) | 1 (16,7) | 9 (34,6) | 10 (31,3) | 0,212 |
| Oxigenoterapia | 0 | 7 (26,9) | 7 (21,9) | |
| C-PAP | 5 (83,3) | 10 (38,5) | 15 (46,9) | |
| Ventilación mecánica invasiva | ||||
| Tiempo en ventilación mecánica horas | 504 (264-672) | 0,33 (0,33-24) | 12,2 (0,33-192) | < 0,0021 |
| 1Estadístico logrank. Valores corresponden a mediana y (RIC); 2Prueba Exacta de Fisher; RIC: Rango Intercuartil. | ||||
Nuestro estudio, al ser de carácter retrospectivo, tiene algunas limitaciones. Primero, la recolección de los datos se restringe a lo que se registró en las fichas clínicas y por lo mismo, no se encontraron de manera regular los tiempos de reducción intestinal, concentraciones mínimas o máximas de remifentanilo, CAM de sevofluorano, entre otras variables de menor importancia clínica en las primeras cirugías. Segundo, en cuanto a las técnicas anestésicas realizadas, al no existir un protocolo quirúrgico-anestésico unificado, fueron dependientes de la experiencia y confort del anestesiólogo a cargo de la cirugía, por lo que existe una variabilidad de técnicas, fármacos y dosis empleadas.
En esta cohorte retrospectiva desde el año 2010 hasta el año 2021, no se observó una diferencia en relación con la técnica anestésica empleada y la tasa de éxito del cierre primario de la gastrosquisis, sin embargo, no se puede descartar la superioridad de la técnica general-espinal o general con los datos obtenidos. Para lograr evidenciar esta superioridad se requeriría realizar un estudio clínico aleatorizado con un número mayor de participantes.
Agradecimientos: Queremos agradecer al equipo de Concentra Investigación, por la ayuda brindada en el diseño y análisis estadístico de los datos recopilados.
Fuente de Financiamiento: No se contó con fuentes de financiamiento.
Declaración Conflicto de interés: ambos autores declaran no tener conflicto de interés.
Referencias
1. Ledbetter DJ. Gastroschisis and omphalocele [vii.]. Surg Clin North Am. 2006 Apr;86(2):249–60. https://doi.org/10.1016/j.suc.2005.12.003 PMID:16580922
2. Wilson RD, Johnson MP. Congenital abdominal wall defects: an update. Fetal Diagn Ther. 2004;19(5):385–98. https://doi.org/10.1159/000078990 PMID:15305094
3. Abdullah F, Arnold MA, Nabaweesi R, Fischer AC, Colombani PM, Anderson KD, et al. Gastroschisis in the United States 1988-2003: analysis and risk categorization of 4344 patients. J Perinatol. 2007 Jan;27(1):50–5. https://doi.org/10.1038/sj.jp.7211616 PMID:17036030
4. Bhat V, Moront M, Bhandari V. Gastroschisis: A State-of-the-Art Review. Children (Basel). 2020 Dec;7(12):302. https://doi.org/10.3390/children7120302 PMID:33348575
5. Raitio A, Lahtinen A, Syvänen J, Kemppainen T, Löyttyniemi E, Gissler M, et al. Gastroschisis in Finland 1993 to 2014-Increasing Prevalence, High Rates of Abortion, and Survival: A Population-Based Study. Eur J Pediatr Surg. 2020 Dec;30(6):536–40. https://doi.org/10.1055/s-0039-3401797 PMID:31891948
6. Skarsgard ED. Management of gastroschisis. Curr Opin Pediatr. 2016 Jun;28(3):363–9. https://doi.org/10.1097/MOP.0000000000000336 PMID:26974976
7. Petrosyan M, Sandler AD. Closure methods in gastroschisis. Semin Pediatr Surg. 2018 Oct;27(5):304–8. https://doi.org/10.1053/j.sempedsurg.2018.08.009 PMID:30413261
8. Svetliza J, Palermo M, Espinosa A, Gallo M, Calahorra M, Guzmán E. Procedimiento Simil-Exit para el manejo de Gastrosquisis. Rev Ibero de Med Fetal y Perin. 2007;1(1):7–12.
9. Svetliza J, Espinoza A, Gallo M, Palermo M, Deguer C, Moreno Abad A, et al. Experiencia conjunta en Argentina y Chile con la técnica Símil-EXIT para el tratamiento quirúrgico de la gastrosquisis. Rev Ped Elec 2009. Vol 6, N°3. Disponible en: https://www.revistapediatria.cl/volumenes/2009/vol6num3/pdf/congreso_cirugia/cirugia80.pdf
10. Moreno A, Márquez R, Quijada P, Peralta M. Tratamiento mínimamente invasivo de la gastrosquisis: 2 años de experiencia con el procedimiento Símil-EXIT. Rev Ped Elec 2010. Vol 7, N°3. Disponible en: https://www.revistapediatria.cl/volumenes/2010/vol7num3/pdf/CONGRESO_CIRUGIA25.pdf
11. Svetliza J, Espinoza A, Gallo M, Adelaida Velez M. Gastrosquisis: nuevo manejo perinatal mediante el procedimiento Símil-EXIT. Rev Colomb Salud Libre. 2011;10:11–22.
12. Oliveira GH, Svetliza J, Vaz-Oliani DC, Liedtke Junior H, Oliani AH, Pedreira DA. Novel multidisciplinary approach to monitor and treat fetuses with gastroschisis using the Svetliza Reducibility Index and the EXIT-like procedure. Einstein (Sao Paulo). 2017;15(4):395–402. https://doi.org/10.1590/s1679-45082017ao3979 PMID:29364360
13. Luo D, Wu L, Wu H, Huang W, Huang H. Anesthetic management of a neonate receiving prenatal repair of gastroschisis. Int J Clin Exp Med. 2015 May;8(5):8234–7. PMID:26221401
14. Norris MC, Joseph J, Leighton BL. Anesthesia for perinatal surgery. Am J Perinatol. 1989 Jan;6(1):39–40. https://doi.org/10.1055/s-2007-999541 PMID:2910316
15. Mychaliska GB, Bealer JF, Graf JL, Rosen MA, Adzick NS, Harrison MR. Operating on placental support: the ex utero intrapartum treatment procedure. J Pediatr Surg. 1997 Feb;32(2):227–30. https://doi.org/10.1016/S0022-3468(97)90184-6 PMID:9044127
16. Reigstad I, Reigstad H, Kiserud T, Berstad T. Preterm elective caesarean section and early enteral feeding in gastroschisis. Acta Paediatr. 2011 Jan;100(1):71–4. https://doi.org/10.1111/j.1651-2227.2010.01944.x PMID:21143293
17. Cisneros-Gasca LC, Pérez-Lorenzana H, Jiménez- García G, et al. Simil-exit en el manejo de gastrosquisis, estudio comparativo. Rev Mex Cir Pediatr. 2014;18(4):169–82.
18. Kan RE, Hughes SC, Rosen MA, Kessin C, Preston PG, Lobo EP. Intravenous remifentanil: placental transfer, maternal and neonatal effects. Anesthesiology. 1998 Jun;88(6):1467–74. https://doi.org/10.1097/00000542-199806000-00008 PMID:9637638
19. Shen MK, Wu ZF, Zhu AB, He LL, Shen XF, Yang JJ, et al. Remifentanil for labour analgesia: a double-blinded, randomised controlled trial of maternal and neonatal effects of patient-controlled analgesia versus continuous infusion. Anaesthesia. 2013 Mar;68(3):236–44. https://doi.org/10.1111/anae.12098 PMID:23294132
20. Noskova P, Blaha J, Bakhouche H, Kubatova J, Ulrichova J, Marusicova P, et al. Neonatal effect of remifentanil in general anaesthesia for caesarean section: a randomized trial. BMC Anesthesiol. 2015 Mar;15(1):38. https://doi.org/10.1186/s12871-015-0020-1 PMID:25821405
21. Karaman S, Akercan F, Aldemir O, Terek MC, Yalaz M, Firat V. The maternal and neonatal effects of the volatile anaesthetic agents desflurane and sevoflurane in caesarean section: a prospective, randomized clinical study. J Int Med Res. 2006;34(2):183–92. https://doi.org/10.1177/147323000603400208 PMID:16749414
22. Turner RJ, Lambros M, Kenway L, Gatt SP. The in-vitro effects of sevoflurane and desflurane on the contractility of pregnant human uterine muscle. Int J Obstet Anesth. 2002 Oct;11(4):246–51. https://doi.org/10.1054/ijoa.2002.0963 PMID:15321529
23. Heesen M, Hofmann T, Klöhr S, Rossaint R, van de Velde M, Deprest J, et al. Is general anaesthesia for caesarean section associated with postpartum haemorrhage? Systematic review and meta-analysis. Acta Anaesthesiol Scand. 2013 Oct;57(9):1092–102. https://doi.org/10.1111/aas.12178 PMID:24003971
24. Abboud TK, Swart F, Zhu J, Donovan MM, Peres Da Silva E, Yakal K. Desflurane analgesia for vaginal delivery. Acta Anaesthesiol Scand. 1995 Feb;39(2):259–61. https://doi.org/10.1111/j.1399-6576.1995.tb04053.x PMID:7793195
25. Kavak ZN, Başgül A, Ceyhan N. Short-term outcome of newborn infants: spinal versus general anesthesia for elective cesarean section. A prospective randomized study. Eur J Obstet Gynecol Reprod Biol. 2001 Dec;100(1):50–4. https://doi.org/10.1016/S0301-2115(01)00417-1 PMID:11728657
26. Sung TY, Jee YS, You HJ, Cho CK. Comparison of the effect of general and spinal anesthesia for elective cesarean section on maternal and fetal outcomes: a retrospective cohort study. Anesth Pain Med. 2021 Jan;16(1):49–55. https://doi.org/10.17085/apm.20072 PMID:33389986
27. Afolabi BB, Lesi FE. Regional versus general anaesthesia for caesarean section. Cochrane Database Syst Rev. 2012 Oct;10:CD004350. https://doi.org/10.1002/14651858.CD004350.pub3 PMID:23076903
28. Kunz SN, Tieder JS, Whitlock K, Jackson JC, Avansino JR. Primary fascial closure versus staged closure with silo in patients with gastroschisis: a meta-analysis. J Pediatr Surg. 2013 Apr;48(4):845–57. https://doi.org/10.1016/j.jpedsurg.2013.01.020 PMID:23583145

 ORCID
ORCID