Daniel Perez-Ajami1, Elisa Viscasillas Navarro1, Esteban Estupiñan Valido2
Recibido:
Aceptado: 2025-08-28
©2026 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 55 Núm. 2 |https://doi.org/10.25237/revchilanestv55n2-04
PDF
Recent updates in the anesthetic management of patients with obesity
Abstract
Obesity imposes significant physiological challenges in anesthesiology, including reduced functional residual capacity, increased pharyngeal collapsibility, and a higher incidence of obstructive sleep apnea. In recent years, strategies have been developed to optimize perioperative oxygenation, along with novel therapeutic modalities that have reshaped the clinical profile of obese patients. This review addresses recent advances in perioperative oxygen therapy (including CPAP and high-flow nasal oxygen), the perioperative management of GLP-1 receptor agonists (semaglutide, tirzepatide) and their impact on gastric emptying, and updated criteria for ambulatory surgery in patients with obesity. The aim of this analysis is to provide practical, up-to-date, and evidence-based recommendations for the individualized management of these patients, based on recent studies and international guidelines.
Resumen
La obesidad impone desafíos fisiológicos significativos en anestesiología, asociando menor capacidad residual funcional, colapsabilidad faríngea y mayor incidencia de SAH. En los últimos años se han desarrollado estrategias para optimizar la oxigenación perioperatoria y nuevas modalidades terapéuticas que modifican el perfil clínico del paciente obeso. Se revisan en este documento los avances recientes en: oxigenoterapia perioperatoria (incluyendo CPAP y ONAF), manejo perioperatorio de los agonistas GLP-1 (semaglutida, tirzepatida) y su impacto en el vaciamiento gástrico, y los criterios actualizados para cirugía ambulatoria en obesos. El siguiente análisis, cuyo objetivo es ofrecer recomendaciones prácticas, actualizadas y basadas en evidencia sólida para el manejo individualizado de estos pacientes, está basado en evidencia de estudios recientes y guías internacionales.
Introducción
La obesidad (IMC > 30 kg/m2) ha alcanzado una prevalencia global del 13%-15% en adultos[1] y se asocia con aumento de morbimortalidad perioperatoria[2],[3]. Desde el punto de vista anestésico, el exceso de adiposidad en vía aérea superior reduce el diámetro faríngeo y aumenta la colapsabilidad, empeorando la ventilación espontánea durante la inducción anestésica[4]. La reducción de la capacidad residual funcional (CRF) y la elevada demanda de oxígeno incrementan la desaturación tan rápida tras la apnea postinducción[2]. El Síndrome de Apnea-Hipoapnea (SAH), cuya prevalencia en obesos puede llegar al 70%[5], es un factor de riesgo independiente de complicaciones cardiovasculares y respiratorias perianestésicas[6].
Para enfrentar estos retos, se han propuesto diversas estrategias perioperatorias. Primero, optimizar la preoxigenación y la oxigenación apneica utilizando técnicas como ventilación con presión positiva continua (CPAP), ventilación no invasiva (NIV) o cánula nasal de alto flujo (ONAF)[7]. Segundo, reconocer el impacto de los nuevos fármacos antiobesidad (agonistas GLP-1) que, además de mejorar el metabolismo y reducir drásticamente el peso, tienen el inconveniente de retrasar el vaciamiento gástrico. Tercero, definir criterios claros para seleccionar candidatos obesos a cirugía mayor ambulatoria (CMA) bajo anestesia general. Este artículo, revisa la evidencia reciente en estas áreas, con el fin de proporcionar un marco científico sólido que guíe el manejo anestésico integral de pacientes con obesidad.
Métodos
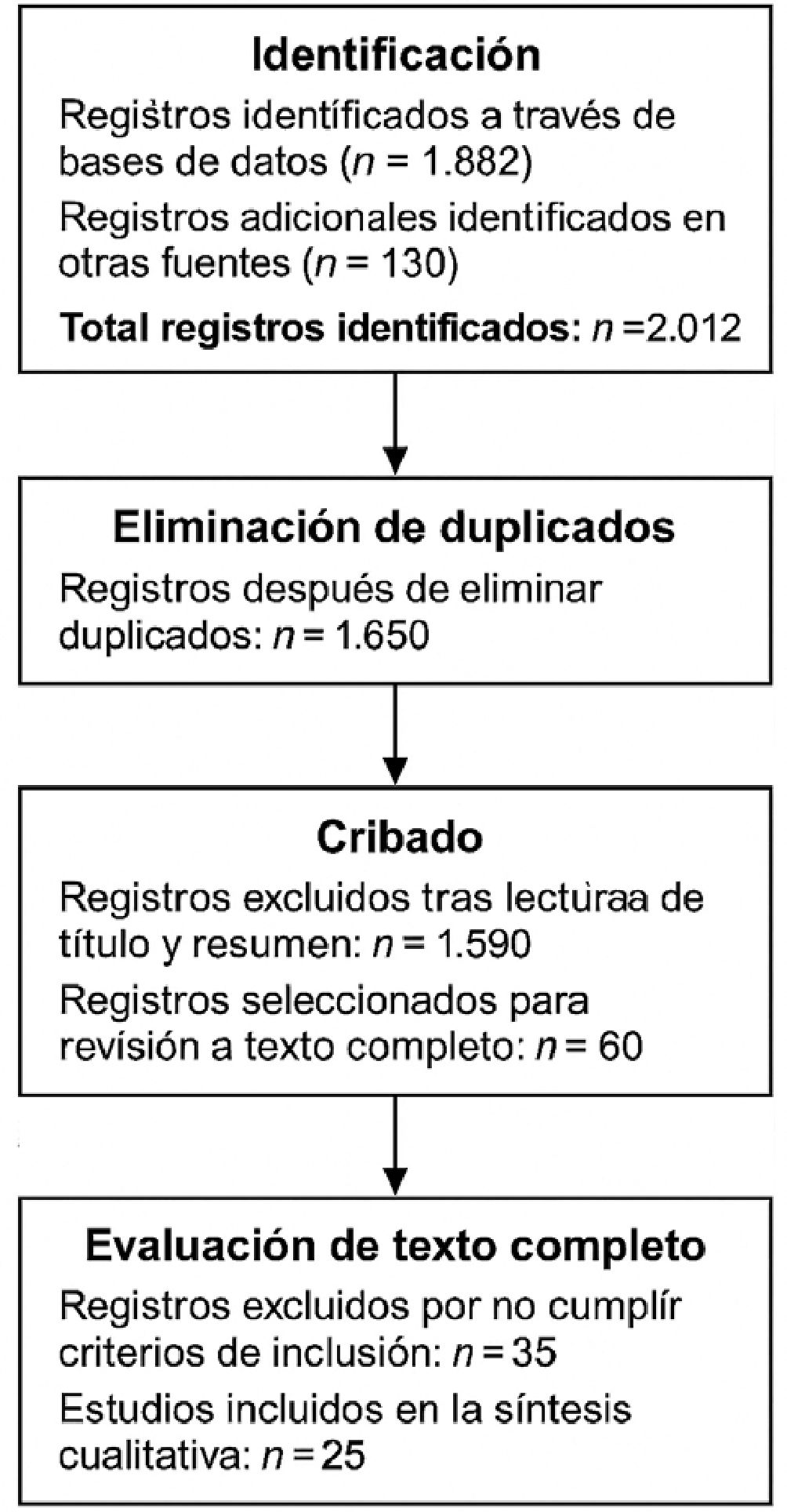
Se realizó una búsqueda sistemática de la literatura en bases de datos electrónicas (Medline, Embase, Cochrane, Web of Science) y literatura gris hasta abril de 2025. Los términos incluían combinaciones como “obesity anesthesia”, “high-flow nasal cannula obese”, “GLP-1 agonists anesthesia”, “ambulatory surgery obesity criteria” y sinónimos en inglés y español. Se aplicaron criterios de inclusión: revisiones sistemáticas, metaanálisis, ensayos clínicos y guías publicadas desde 2020, con énfasis en evidencias de alta calidad (niveles A/B). Se excluyeron comunicaciones sin revisión por pares, estudios de casos aislados y artículos previos a 2015, excepto cuando ilustran conceptos básicos. La estrategia de selección siguió las recomendaciones PRISMA (Figura 1) y se documenta en el material suplementario.
Figura 1. Diagrama de flujo PRISMA de la búsqueda bibliográfica.
| Tabla 1. Estrategias de oxigenación perioperatoria en pacientes con obesidad[7],[8] | |
|---|---|
| Técnica | Beneficio (evidencia) |
| Posición sentada o incorporada | T FRC y tiempo de apnea seguro |
| ONAF (50-60 L/min) | T Tiempo de apnea |
| j Hipoxemia perioperatoria | |
Estrategias de oxigenación perioperatoria
Dada la disminución de CRF y el riesgo de atelectasias, la optimización de la oxigenación es crucial en pacientes obesos. Tradicionalmente se ha utilizado CPAP (o NIV) durante la preoxigenación para aumentar el CRF. Aunque no hay ensayos RCT recientes exclusivos de CPAP en obesos, las revisiones recomiendan su uso para reclutar alveolos y prolongar la apnea tolerada[6]. La ONAF ha ganado popularidad por su mayor facilidad de uso y tolerancia (Tabla 1). Estudios controlados han mostrado que administrar flujos de 50-60 L/min con FiO2 cercana al 100% prolonga significativamente el tiempo de apnea segura. En un ensayo aleatorizado con obesos mórbidos, el tiempo medio hasta SpO2 < 95% fue mayor con ONAF (261 segundos) que con máscara facial convencional (185 segundos)[3]. Un metaanálisis de 2022 confirmó que la ONAF mejora la saturación mínima y reduce la incidencia de hipoxemia perioperatoria (RR » 0,60) comparada con oxigenoterapia convencional[8]. En cuidados postextubación tempranos, la ONAF también demostró beneficios: un RCT en cirugía bariátrica encontró que 3 h de ONAF tras extubación redujeron la hipoxemia posoperatoria (28,6% vs. 80,0%) y las atelectasias en TAC[9]. Estos resultados apoyan la utilización de ONAF tanto en inducción como en el posoperatorio inmediato en este tipo de pacientes tanto para incrementar el tiempo de apnea segura como para mejorar la oxigenación postextubación[10].
Otras maniobras han mostrado ventajas. La elevación de la cabeza y del tronco superior (posición “en rampa”) mejora la preoxigenación al disminuir la presión diafragmática permi
tiendo una mayor incursión torácica y una disminución de las atelectasias. Ya en el 2005, Altermatt et al., hallaron que sentar a pacientes obesos al tiempo de inducción prolongó el tiempo hasta SpO2 < 90% vs. supino[11]. Del mismo modo, estudios previos señalan que inclinar la camilla 25-30° aumenta la CRF y la reserva de oxígeno. En conjunto, una combinación de aumento de CRF (p. ej. CPAP, posición) y ONAF optimiza la seguridad durante apnea[12].
Agonistas de GLP-1: implicancias anestésicas
Los agonistas de GLP-1 (p. ej. semaglutida semanal, dulaglutida semanal, liraglutida diaria) y los duales GLP-1/GIP (tirzepatida) han revolucionado el tratamiento de la obesidad y diabetes tipo 2. No obstante, además de mejorar la glucemia y disminuir el apetito, provocan un efecto destacado en el retraso del vaciamiento gástrico. Estudios recientes cuantifican este efecto, hallando episodios de atragantamiento y regurgitación en pacientes tratados con semaglutida y observando un enlentecimiento en su vaciamiento gástrico. Un metaanálisis reciente concluye que los pacientes en terapia con GLP-1 tienen mayores volúmenes gástricos residuales tras ayuno estándar[13]. En efecto, Wolla et al., encontraron por ecografía gástrica que los diabéticos en GLP-1 tenían más contenido residual (mediana 0,61 vs 0,16 mL/kg; p < 0,001) y mayor riesgo de estómago “lleno” y broncoaspiración[14]. Además, aquellos con dosis en los últimos 7 días mostraron volúmenes significativamente mayores que si el último dosis fue > 7 días antes. Estos hallazgos respaldan las recomendaciones recientes: la American Society of Anesthesiologists aconseja suspender agonistas GLP-1 de dosis diaria el día del procedimiento y los semanales al menos 1 semana antes[15].
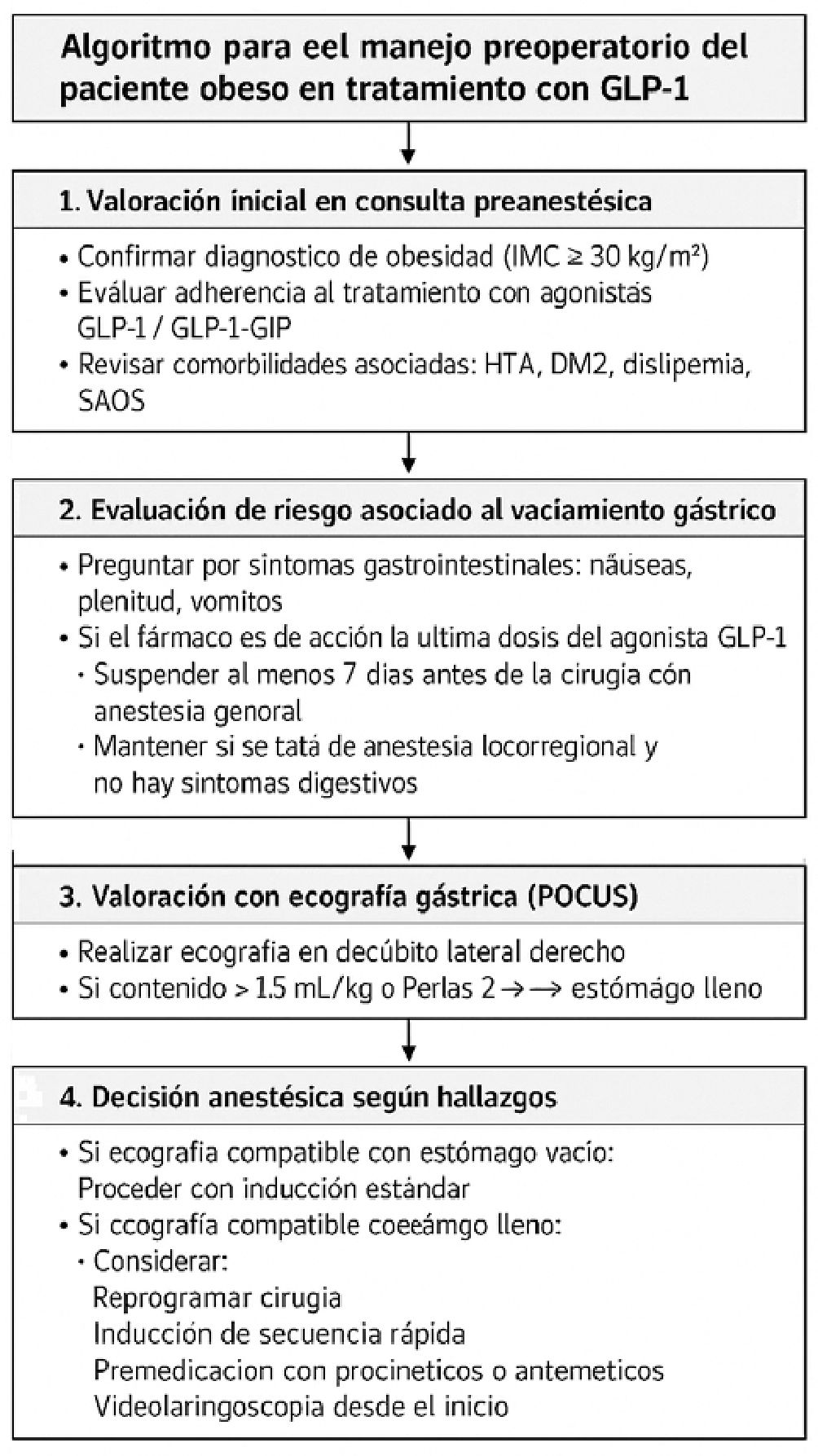
En la práctica perioperatoria se debe evaluar meticulosamente. Si el paciente refiere síntomas gastrointestinales (náuseas, vómitos, distensión abdominal), debe considerarse posponer el procedimiento[15]. Si no hay síntomas y el fármaco fue suspendido según guía (1-7 días antes), puede procederse sin cambios especiales[15]. En caso de no haberlo suspendido a tiempo, se recomienda tratar al paciente comoestómago lleno, resultando muy útil la ecografía gástrica perioperatoria. El ultrasonido gástrico (POCUS) es una herramienta validada de alta sensibilidad para estimar volumen gástrico en tiempo real. Si tras POCUS el estómago está «vacío» (Perlas 0-1 o contenido < 1,5 mL/kg), se avanza; si se detecta contenido alto o ecografía dudosa, hay que demorar cirugía o asumir precauciones de estómago lleno[14]. En todo caso, deben discutirse los riesgos de broncoaspiración con el equipo quirúrgico y también deben de valorarse lo perjudicial que puede resultar los cambios glucémicos perioperatorios según la fragilidad y el estado basal del paciente. En resumen, los pacientes en agonistas GLP-1 requieren especial vigilancia de aspiración: las guías actuales sugieren 7 días sin dosis semanales, y la ecografía gástrica juega un papel crucial en la evaluación perioperatoria[15]. En la Figura 2 se describe un algoritmo de actuación para estos pacientes basado en las recomendaciones anteriormente expuestas.
Cirugía ambulatoria en pacientes obesos
El auge de la CMA plantea la pregunta sobre criterios de selección en pacientes obesos[16]. Tradicionalmente, la obesidadper se no contraindica la cirugía ambulatoria: estudios recientes muestran que pacientes con IMC elevado, seleccionados adecuadamente, no tienen peores desenlaces tras CMA comparados con no obesos[2],[3]. Por ejemplo, Hajmohamed et al., analizaron > 30.000 casos y encontraron que los pacientes superobesos (BMI > 50) no tuvieron mayor tasa de complicaciones perioperatorias tempranas que los mórbidos (BMI 40-50) después de CMA[17]. Sin embargo, la selección rigurosa es esencial debido a las importantes comorbilidades que presentan estos pacientes.
Figura 2. Algoritmo para el manejo del paciente obeso en tratamiento con agonistas GLP-1.
| Tabla 2. Criterios sugeridos para cirugía mayor ambulatoria en pacientes obesos[2],[6],[16],[18],[20] | |
|---|---|
| Categoría | Criterios |
| IMC | Preferible < 40 kg/m. Con IMC 40-50 valorar individualmente según riesgo/beneficio |
| AHI (AH de sueño) | Ideal < 5 (no OSA). En todo caso < 15 (OSA leve). AHI > 15 sugiere OSA moderado-grave: optimizar con CPAP antes de CMA |
| Comorbilidades | Hipertensión o diabetes con buen control. Sin insuficiencia cardíaca/pulmonar descompensada |
| Vía aérea | Evaluación preanestésica favorable. Disponer de videolaringoscopio (siempre, pero especialmente si IMC > 35) |
| Función respiratoria | SatO2 basal > 95% en aire ambiente. PaCO2 < 45 mmHg (descartar síndrome de hipoventilación) |
Lee JH. Anesthesia for ambulatory surgery. Korean J Anesthesiol. 2017 Aug;70(4):398-406.https://doi.org/10.4097/kjae.2017.70.4.398 PMID:28794834
Las recomendaciones actuales enfatizan la capacidad funcional y el control de comorbilidades sobre el IMC aislado[2],[18]. Por ello, muchos centros proponen criterios (Tabla 2) que permiten discriminar a los pacientes que más se van a beneficiar de la cirugía sin ingreso hospitalario sin repercutir en su seguridad. Los criterios varían entre centros, pero algunos de ellos incluyen: 1) IMC idealmente < 40 (aunque un IMC 40-50 puede ser aceptable con valoración riesgo/beneficio individual); 2) Índice de Apneas-Hipoapneas (AHÍ) bajo: ideal < 5, y < 15 en todo caso. Pacientes con AHI > 15 (stop-bang > 5) tienen SAH moderado-grave y deben optimizarse con CPAP antes de CMA[18]; 3) Comorbilidades controladas: hipertensión o diabetes bien ajustadas, sin insuficiencia cardíaca o pulmonar descompensada; 4) Vía aérea despejada: evaluación preoperatoria que no sugiera vía aérea difícil grave (si IMC > 35, disponer de videolaringoscopio); 5)Función respiratoria normal: SaO2 basal > 95% y PaCO2 < 45 mmHg, descartando el síndrome de hipoventilación asociada a obesidad (BMI > 30 + PaCO2 > 45)[19]. En suma, la selección ambulatoria debe basarse en la estabilidad clínica y funcional más que simplemente en el peso.
Por otro lado, un adecuado protocolo posoperatorio es esencial para minimizar complicaciones y reingresos en pacientes con obesidad. La monitorización prolongada en la unidad de recuperación permite la detección temprana de hipoxemia o hipoventilación. Asimismo, la valoración del control del dolor y de la función hemodinámica, junto con pautas de movilización y fisioterapia respiratoria, contribuye a una recuperación más segura[21]. Por tanto, en pacientes obesos con comorbilidades crónicas debidamente estabilizadas (p. ej., hipertensión, diabetes, apnea obstructiva del sueño con adherencia a CPAP) y con buena reserva funcional, la cirugía mayor ambulatoria resulta factible siempre que se garantice este seguimiento posalta estructurado[21].
Discusión y Conclusiones
La creciente prevalencia de la obesidad en la población quirúrgica plantea desafíos anestésicos únicos, derivados de alteraciones fisiológicas y de la introducción de nuevas modalidades terapéuticas. En primer lugar, la combinación de disminución de la capacidad residual funcional y mayor colapsabilidad faríngea, junto con la alta incidencia de apnea obstructiva del sueño, caracteriza un perfil de alto riesgo de hipoxemia durante la inducción y el despertar anestésico. Los datos de ensayos controlados confirman que la ONAF prolonga de forma significativa el tiempo de apnea segura y minimiza eventos de desaturación, tanto en la fase de inducción como en la postextubación de pacientes bariátricos. Complementar ONAF con maniobras de posicionamiento en rampa o uso mesurado de CPAP optimiza la reserva pulmonar y facilita una ventilación más estable, reduciendo la morbilidad respiratoria inmediata.
En segundo lugar, el uso extensivo de agonistas del receptor de GLP-1 y GLP-1/GIP ha transformado el manejo metabólico de la obesidad, pero introduce un nuevo factor de riesgo: el retraso del vaciamiento gástrico. La evidencia ecográfica demuestra volúmenes residuales elevados en pacientes que mantienen dosis recientes de estos fármacos, aun tras ayuno convencional. Esta realidad obliga a replantear las pautas preoperatorias: suspensión preventiva de la medicación al menos siete días antes de la intervención, y empleo sistemático de ecografía gástrica como herramienta de cribado para descartar estómago “lleno” antes de la inducción. De este modo, se minimiza el riesgo de broncoaspiración y se adapta el protocolo anestésico a la situación clínica individual.
Por último, la CMA en pacientes obesos ya no debe descartarse de forma automática. Estudios recientes demuestran que, siempre que exista un control estricto de comorbilidades (HTA, diabetes, AOS con CPAP), valoración funcional adecuada (SaO2 > 95%, PaCO2 < 45 mmHg) y un plan de monitorización posoperatoria prolongada, los resultados quirúrgicos y anestésicos son comparables a los de la población no obesa. De este modo, la obesidad, más que un criterio de exclusión, se convierte en un elemento más de la evaluación de riesgos, enfatizando la capacidad funcional y la estabilidad clínica.
En conjunto, el manejo anestésico del paciente obeso exige un enfoque multidimensional: integración de tecnologías avanzadas (ONAF, ecografía gástrica), criterios de selección funcionales para CMA y adaptación de las pautas preoperatorias a la farmacología antiobesidad moderna. La implementación de protocolos basados en esta evidencia fortalecerá la seguridad perioperatoria y permitirá ofrecer una atención personalizada, eficiente y ajustada a los retos fisiopatológicos de esta creciente población quirúrgica.
Referencias
1. Ng M, Fleming T, Robinson M, Thomson B, Graetz N, Margono C, et al. Global, regional, and national prevalence of overweight and obesity in children and adults during 1980-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet. 2014 Aug;384(9945):766-81. https://doi.org/10.1016/S0140-6736(14)60460-8 PMID:24880830
2. Nathan N. Super Morbid Obesity: Implications of BMI for Ambulatory Surgery. Anesth Analg. 2021 Dec;133(6):1365- 1365. https://doi.org/10.1213/ANE.0000000000005793 PMID:34784320
3. Hartfield PJ, Janczy J, Sharma A, Newsome HA, Sparapani RA, Rhee JS, et al. Anatomical determinants of upper airway co- llapsibility in obstructive sleep apnea: A systematic review and meta-analysis. Sleep Med Rev. 2023 Apr;68:101741. https://doi.org/10.1016/j.smrv.2022.101741 PMID:36634409
4. Esmaeili N, Gell L, Imler T, Hajipour M, Taranto-Montemurro L, Messineo L, et al. The relationship between obesity and obstructive sleep apnea in four community-based cohorts: an individual participant data meta-analysis of 12,860 adults. EClinicalMedicine. 2025 Apr;83:103221. https://doi.org/10.1016/j.eclinm.2025.103221 PMID:40330547
5. Di Giacinto I, Guarnera M, Esposito C, Falcetta S, Cortese G, Pascarella G, et al. Emergencies in obese patients: a narrative review. J Anesth Analg Crit Care. 2021 Nov;1(1):13. https://doi.org/10.1186/s44158-021-00019-2 PMID:37386567
6. Gaszynski T, McKechnie A. Pre-oxygenation and apneic oxygenation in patients living with obesity – A review of novel techniques. Saudi J Anaesth. 2022;16(3):322-6. https://doi.org/10.4103/sja.sja_351_22 PMID:35898525
7. Zhou R, Wang HT, Gu W. Efficacy of High-Flow Nasal Cannula versus Conventional Oxygen Therapy in Obese Patients during the Perioperative Period: A Systematic Review and MetaAnalysis. Can Respir J. 2022 Sep;2022:4415313. https://doi.org/10.1155/2022/4415313 PMID:36247078
8. Ferrando C, Puig J, Serralta F, Carrizo J, Pozo N, Arocas B, et al. High-flow nasal cannula oxygenation reduces postoperative hypoxemia in morbidly obese patients: a randomized controlled trial. Minerva Anestesiol. 2019 Oct;85(10):1062-70. https://doi.org/10.23736/S0375-9393.19.13364-0 PMID:30994312
9. Ricottilli F, Ickx B, Van Obbergh L. High-flow nasal cannula preoxygenation in obese patients undergoing general anaesthesia: a randomised controlled trial. Br J Anaesth. 2019;123(3):e443-4. https://doi.org/10.1016/j.bja.2019.05.006
10. Altermatt FR, Muñoz HR, Delfino AE, Cortínez LI. Pre-oxygenation in the obese patient: effects of position on tolerance to apnoea. Br J Anaesth. 2005 Nov;95(5):706-9. https://doi.org/10.1093/bja/aei231 PMID:16143575
11. Couture EJ, Provencher S, Somma J, Lellouche F, Marceau S, Bussières JS. Effect of position and positive pressure ventilation on functional residual capacity in morbidly obese patients: a randomized trial. Canadian Journal of Anesthesia/Journal canadien d’anesthésie. 2018;65(5):522-528. https://doi.org/10.1007/s12630-018-1050-1
12. Hiramoto B, McCarty TR, Lodhia NA, Jenkins A, Elnaiem A, Muftah M, et al. Quantified Metrics of Gastric Emptying Delay by Glucagon-Like Peptide-1 Agonists: A Systematic Review and Meta-Analysis With Insights for Periprocedural Management. Am J Gastroenterol. 2024 Jun;119(6):1126-40. https://doi.org/10.14309/ajg.0000000000002820 PMID:38634551
13. Wolla CD, Pecha TJ, Sirianni JM, Schorg LM, Wolf BJ, Wilson SH. Ultrasound assessment of preoperative gastric volume in fasted diabetic surgical patients: A prospective observational cohort study on the effects of glucagon-like peptide-1 agonists on gastric emptying. J Clin Anesth. 2025 Jun;104:111853. https://doi.org/10.1016/j.jclinane.2025.111853 PMID:40324318
14. Girish P. Joshi MBBS, MD, Basem B. Abdelmalak MD, Wade A. Weigel MD. Consensusbased guidance on preoperative management of patients (adults and children) on glucagonlike peptide1 (GLP1) receptor agonists [News release]. American Society of Anesthesiologists. American Society of Anesthesiologists.
15. Arance García M, Docobo Durántez F, Conde Guzmán C, Pérez Torres MC, Martín-Gil Parra R, Fernández Jiménez PE. ¿Es la obesidad un factor de riesgo de complicaciones, ingresos y suspensiones quirúrgicas en cirugía mayor ambulatoria? Rev Esp Anes- tesiol Reanim. 2015 Mar;62(3):125-32. https://doi.org/10.1016/j.redar.2014.03.016 PMID:25048995
16. Hajmohamed S, Patel D, Apruzzese P, Kendall MC, De Oliveira G. Early Postoperative Outcomes of Super Morbid Obese Compared to Morbid Obese Patients After Ambulatory Surgery Under General Anesthesia: A Propensity-Matched Analysis of a National Database. Anesth Analg. 2021 Dec;133(6):1366-73. https://doi.org/10.1213/ANE.0000000000005770 PMID:34784321
17. Joshi GP, Ankichetty SP, Gan TJ, Chung F. Society for Ambulatory Anesthesia consensus statement on preoperative selection of adult patients with obstructive sleep apnea scheduled for ambulatory surgery. Anesth Analg. 2012 Nov;1 15(5):1060-8. https://doi.org/10.1213/ANE.0b013e318269cfd7 PMID:22886843
18. Nicolini A, Ferrando M, Solidoro P, Di Marco F, Facchini F, Brai- do F. Non-invasive ventilation in acute respiratory failure of patients with obesity hypoventilation syndrome. Minerva Med. 2018 Dec;109(6 Suppl 1):1-5. https://doi.org/10.23736/S0026-4806.18.05921-9 PMID:30642143
19. Nathan N. Super Morbid Obesity: Implications of BMI for Ambulatory Surgery. Anesth Analg. 2021 Dec;133(6):1365-1365. https://doi.org/10.1213/ANE.0000000000005793 PMID:34784320
20. Tian C, Hawryluck L, Tomlinson G, Chung F, Beattie S, Miller M, et al. Impact of a continuous enhanced cardio-respiratory monitoring pathway on cardio-respiratory complications after bariatric surgery: A retrospective cohort study. J Clin Anesth. 2022 May;77:110639. https://doi.org/10.1016/j.jclinane.2021.110639 PMID:34953279

 ORCID
ORCID