Luis Brunet L. 1
Rev Chil Anest Vol. 39 Núm. 2 pp. 110-115|doi:
PDF|ePub|RIS
Introducción
Una de las tareas más importantes de los anestesiólogos durante la anestesia, la cirugía y en el período postoperatorio inmediato, es asegurar la permeabilidad de la vía aérea y mantener la función respiratoria para lograr una oxigenación adecuada. La dificultad en el manejo de la vía aérea, incluidos los problemas de ventilación y de intubación traqueal, aunque poco frecuentes, constituye la primera causa de morbilidad y mortalidad anestésica 1 . Las recomendaciones para evaluar la vía aérea en el preoperatorio, el reconocimiento de predictores y las guías para el manejo de la vía aérea difícil, son el resultado de los esfuerzos organizados por reducir el problema 2 . A pesar del impacto positivo que han tenido estas medidas, la vía aérea difícil inesperada continúa siendo un problema real en la práctica anestésica. Con objeto de predecir y prepararse para enfrentar este problema, se ha tratado de identificar a grupos de pacientes de riesgo, entre los cuales se ha mencionado a los obesos y a los portadores de síndrome de apnea obstructiva del sueño (SAOS), entre otros.
El aumento sostenido de la obesidad en la población mundial es un problema importante de salud pública, que ha llevado a denominarla como la “Epidemia del Siglo XXI” 3 . El reconocimiento del éxito de la cirugía bariátrica en el tratamiento de la obesidad, sumado al incremento del número de pacientes obesos y de las patologías asociadas a la obesidad que requieren de tratamiento quirúrgico, han aumentado las probabilidades de que los anestesiólogos tengan que enfrentar a este tipo de pacientes en su práctica habitual 4 , 5 . Como aún hay controversias entre los propios anestesiólogos respecto del manejo de la vía aérea en los pacientes obesos, es necesario resolver algunas preguntas pendientes en relación con este tema (Tabla 1).
Tabla 1 Controversias pendientes en relación a la vía aérea en el obeso
| 1. ¿Son más difíciles la ventilación e intubación en el paciente obeso? |
| 2. ¿Qué parámetros son útiles para predecir una vía aérea difícil en los obesos? |
| 3. ¿Cómo debe manejarse la vía aérea del obeso? |
| 4. ¿Existe alguna relación entre la obesidad, el SAOS y la dificultad de manejo de la vía aérea? |
| 5. ¿Cómo deben evaluarse y manejarse los pacientes con SAOS? |
-
Ventilación e intubación traqueal en el obeso
Los obesos han sido catalogados como pacientes difíciles de intubar y de ventilar con máscara facial, prueba de esto son las afirmaciones hechas en tal sentido en los textos clásicos de anestesia y el temor por parte de los anestesiólogos e intensivistas al manejo de la vía aérea en este grupo de pacientes 5 , 6 . La relación establecida entre obesidad y vía aérea difícil probablemente se basa en el reporte de casos aislados durante un período, donde el número de pacientes obesos sometidos a anestesia era escaso, como ocurría hasta el inicio de los años noventa. Recientemente, el aumento de la cirugía bariátrica ha influido en el desarrollo de la anestesia para los obesos y ha permitido el estudio de distintos aspectos de la especialidad en ellos.
Existen estudios que han confirmado la mayor dificultad en la ventilación con la máscara facial en los obesos, lo cual se debería al aumento del tejido graso en el cuello y la cara, limitando la adaptación de la máscara 7 . La mayor dificultad en la intubación traqueal del paciente obeso, por el contrario, sigue siendo un tema controvertido. Algunos investigadores han demostrado que existe una relación entre el aumento del peso corporal o del índice de masa corporal (IMC) y una mayor dificultad en la intubación. La dificultad en la intubación es variable, pudiendo llegar a ser 2 a 10 veces mayor en los obesos, en comparación con los pacientes eutróficos en algunos trabajos 8 , 9 . Otros estudios no han logrado establecer que exista una relación entre la obesidad y una intubación traqueal difícil 10 , 11 . Se ha especulado que esta controversia puede tener su origen en la falta de consenso para definir “vía aérea difícil”. Con frecuencia se utiliza el grado de dificultad en la visión de la glotis durante la laringoscopia, de acuerdo a la clasificación de Cormack-Lehane, como equivalente de intubación difícil 11 . En otros trabajos, se utilizan distintos índices de “intubación difícil”, basados en el número de intentos realizados para intubar la tráquea, el número de operadores, y el tiempo necesario para intubar, entre otros. También se han usado como indicadores, diversas combinaciones de laringoscopia difícil, intubación difícil e intubación fallida 12 . Al parecer y como lo muestran diversos estudios, la laringoscopia e intubación en los pacientes con sobrepeso u obesidad no serían más complejas que en los pacientes eutróficos, en ausencia de otros predictores reconocidos de una vía aérea difícil.
El reconocimiento de predictores de una vía aérea difícil permite la preparación y planificación de la anestesia, y ha permitido además la construcción de algoritmos para enfrentar tanto las situaciones esperadas como las inesperadas en el manejo de la vía aérea. Entre los algoritmos, el más conocido y utilizado es el de la Sociedad Americana de Anestesiología (ASA) 2 . En el grupo de pacientes obesos, la anticipación de una vía aérea difícil es de especial importancia, debido a que tienen una baja tolerancia a la apnea como consecuencia de las alteraciones funcionales pulmonares que acompañan a la obesidad: la hipoxemia es más intensa y aparece en un menor período de tiempo que en los pacientes eutróficos 13 , 14 . Además, se presume que tendrían un mayor riesgo de aspiración de contenido gástrico durante el período previo a la intubación, hecho que no ha sido clínicamente demostrado 15 . Junto a los predictores conocidos en los individuos eutróficos (Tabla 2), en los obesos también se han asociado a la dificultad de intubación la circunferencia del cuello mayor de 40 cm, y el antecedente de SAOS 10 , 12 . De acuerdo a Brodsky y cols, una circunferencia del cuello mayor a 44 cm medida a nivel del cartílago tiroides, aumenta progresivamente la probabilidad de una intubación difícil, hasta llegar a un 35% con una circunferencia de 60 cm o más 11 .
Tabla 2 Predictores de intubación difícil en individuos eutróficos
|
Predictores Vía Aérea Alta |
| 1. Visión Faríngea – Mallampati |
| 2. Distancia Tiro – Mentoneana |
| 3. Distancia Mento – Esternal |
| 4. Tamaño de Lengua |
| 5. Apertura Bucal |
| 6. Movilidad Articulación Atlantoccipital |
| 7. Función Articulación Temporomandibular |
-
Posición e intubación en obesos
En la práctica anestésica se destaca la importancia que tiene la posición del paciente y en especial la posición de la cabeza, de modo de condiciones adecuadas para la laringoscopia y la intubación traqueal. En individuos eutróficos la “posición olfatoria”, que consiste en la elevación de la cabeza en relación al tronco utilizando una almohada bajo el occipucio, junto a la hiperextensión del cuello y a la elevación de la mandíbula, permiten alinear los ejes de la vía aérea superior, facilitando la laringoscopia y la intubación traqueal. Una publicación reciente mostró que la posición “olfatoria” no era suficiente para lograr las condiciones óptimas durante la laringoscopia en los pacientes obesos mórbidos (IMC > 40 kg/m2), debido al depósito de tejido graso en las regiones del tronco y cuello (Figura 1).
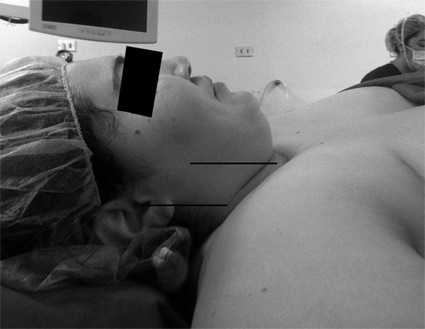
Figura 1 Paciente con IMC de 40 Kg/m2 en decúbito supino y “posición olfatoria”. Cojín cefálico de 10 cm.
La elevación de la cabeza, el cuello y la parte alta del tórax en un ángulo de 20 a 30° por sobre el resto del tronco, demostró permitir una mejor visión durante la laringoscopia y, por lo tanto, facilitar la intubación en estos pacientes16. Esta posición, llamada “en rampa”, se puede lograr colocando además de la almohada bajo la cabeza, cojines o almohadas bajo la región torácica alta, cervical y cefálica. El grupo de investigadores que realizó este estudio observó que la posición “en rampa” a diferencia de la posición “olfatoria”, producía la alineación del hueco supra-esternal con el meato auditivo externo en el plano horizontal, y recomendó esta alineación, previo a la laringoscopia en los individuos obesos mórbidos (Figura 2).
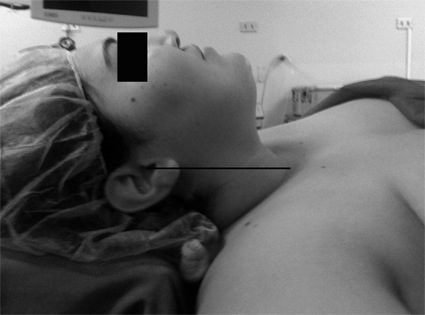
Figura 2 “Posición en rampa” con la utilización de cojines para elevar la porción alta del tórax y cabeza. Se observa la alineación del meato auditivo externo y el hueco supraesternal.
Experiencias posteriores han confirmado la utilidad de la posición “en rampa”, tanto en la intubación como en la ventilación con máscara facial. La angulación de una mesa quirúrgica articulada produce el mismo efecto logrado con el uso de los cojines 17 . La descripción de la posición en rampa probablemente marca un “antes y un después” en el manejo de la vía aérea del paciente obeso, y los próximos trabajos en el área, así como el manejo anestésico de estos pacientes, deberían incluirla. Además de alinear ejes, el uso de la posición en rampa en el período previo a la inducción de la anestesia mejora la mecánica respiratoria, permite una mejor oxigenación sanguínea y retarda la desaturación por apnea, si al paciente se le permite respirar oxígeno 100% a través de una máscara facial durante 3 minutos 18 , 19 .
-
Máscara laríngea en obesos
Una alternativa para el manejo de la vía aérea en los obesos es la utilización de la máscara laríngea de intubación (ILMA = sigla del inglés “intubating laryngeal mask airway”), que ha demostrado en algunos trabajos recientes su utilidad tanto en la ventilación, como en la intubación en obesos mórbidos. Los estudios muestran una ventilación exitosa a través de la ILMA en el 100% de los casos antes de la intubación, lo cual implica la posibilidad de ventilar adecuadamente a pacientes que, por colapso u obstrucción de la vía aérea alta posterior a la inducción de la anestesia, son difíciles o imposibles de ventilar con una máscara facial 20 . También se demostró que en un 96% de los pacientes obesos mórbidos fue posible intubar la tráquea a ciegas a través de la ILMA 20 , 21 .
La máscara laríngea (LMA = sigla del inglés “laryngeal mask airway”) también ha demostrado ser útil y fácil de usar en pacientes obesos mórbidos difíciles de ventilar con la máscara facial 22 . En base a estos estudios, se ha sugerido que la ILMA y la LMA deberían ser consideradas como alternativas para el manejo de la vía aérea de los obesos, cuando se sospecha una vía aérea difícil o en presencia de una ventilación y/o una intubación fallida.
Otra alternativa utilizada en el manejo de la vía aérea de los pacientes obesos es la intubación vigil electiva con un fibrobroncoscopio. Esta técnica se recomienda para la intubación de pacientes con grados extremos de obesidad, cuando la obesidad se asocia a alguna malformación facial o cervical, o cuando existe el antecedente de una intubación difícil o fallida previa 5 . Para algunos grupos de anestesistas, la intubación por fibrobroncoscopia sigue siendo la técnica elegida para los pacientes hiperobesos 23 . En nuestra experiencia, en más de dos mil pacientes obesos mórbidos sometidos a cirugía bariátrica, no ha sido necesario intubar a ningún caso con esta técnica, ni ha habido intubaciones fallidas en los últimos diez años.
-
Obesidad y síndrome de apnea obstructiva del sueño
El Síndrome de Apnea Obstructiva del Sueño (SAOS) que se asocia con frecuencia a la obesidad, se relaciona con un aumento en la incidencia de ventilación e intubación traqueal difícil y fallida en los pacientes obesos, y es considerado un predictor independiente de intubación difícil en este grupo, por lo que debe ser pesquisado en el preoperatorio 10 . El SAOS es la alteración funcional más frecuente del sueño y tiene una incidencia 12 a 30 veces mayor en los obesos que en los individuos eutróficos 24 . Esta alteración, de etiología desconocida, produce episodios repetitivos de obstrucción parcial o total de la vía aérea superior durante el sueño, asociados a hipoxemia e hipercarbia, trastornos cardiovasculares, sueño interrumpido y descanso inadecuado, acompañado de hipersomnia y trastornos conductuales durante el día. Aparentemente se debe a un desequilibrio entre la musculatura inspiratoria, que supera la acción de la musculatura dilatadora de la vía aérea superior 25 . El SAOS sin diagnóstico y tratamiento apropiado aumenta la morbilidad, la mortalidad y reduce la expectativa de vida.
La incidencia real del SAOS moderado a severo dentro la población se desconoce; se estima en 11% de los hombres 26 y 5% de las mujeres 27 , y más del 80% de los casos no tiene diagnóstico 28 , 29 . Junto a la mayor dificultad en el manejo de la vía aérea, la literatura sostiene un riesgo elevado de complicaciones perioperatorias como producto de la cirugía, la modificación de la arquitectura del sueño, y la utilización de anestésicos, analgésicos y sedantes, que agravan las alteraciones propias del SAOS durante este período 30 , 31 . Con objeto de reducir el riesgo perioperatorio, es necesario diagnosticar el SAOS antes de la cirugía. La mayoría de los pacientes quirúrgicos obesos no tienen una evaluación formal tendiente a reconocer si son portadores de un SAOS, motivo por el cual se ha discutido la utilidad de realizar estudios preoperatorios a todos los pacientes que van a ser sometidos a cirugía bariátrica 29 . La polisomnografía (PSG), considerada el gold standard en el diagnóstico del SAOS es impracticable con este objetivo, debido a problemas de disponibilidad de recursos económicos, médicos y técnicos 32 . Como alternativa, las guías de consenso de la ASA basadas en la opinión de expertos, recomiendan la pesquisa del SAOS a través del uso de diferentes cuestionarios y sugiere una estrategia de manejo perioperatorio para los casos sospechosos 33 . Entre los diferentes cuestionarios conocidos, el “STOP-BANG” parece ser uno de los más útiles y fáciles de usar en el preoperatorio, aún cuando sus resultados requieren ser validados en la práctica clínica (Tabla 3) 34 , 35 .
Tabla 3 Cuestionario STOP-BANG (Modificado de Chung F. y cols.) 34
| S | Snore | Roncar |
| T | Tired | Cansancio |
| P | Stop | Dejar de respirar |
| O | Pressure | Hipertensión arterial |
| B | BMI | IMC > 35 Kg/m2 |
| A | Age | Edad > 50 años |
| N | Neck | Cuello > 40 cm |
| G | Gender | Masculino |
| *Dos o más respuestas positivas, riesgo de SAOS | ||
Una reciente revisión sistemática de la literatura, demuestra que aparte de las guías de la ASA, no existen actualmente recomendaciones basadas en evidencias para el tratamiento de los pacientes con SAOS sometidos a cirugía y anestesia 36 .
Recomendaciones para el manejo de la vía aérea en los pacientes obesos y obesos con SAOS asociada:
-
1. Evaluación Preoperatoria:
-
Historia previa de intubación traqueal y su relación temporal con el aumento de peso, antecedentes de intubación difícil o fallida.
-
Antecedentes de ser roncador severo o de presentar un SAOS.
-
Examen exhaustivo de la vía aérea superior, incluyendo: distancia tiromentoneana, apertura bucal, condiciones de la dentadura, tamaño de la lengua, visión faríngea según Mallampati, función de la articulación témporo-mandibular y movilidad cervical.
-
Medición de la circunferencia cervical a nivel del cartílago tiroides.
-
Pesquisa de SAOS con el uso de alguno de los cuestionarios conocidos.
-
Descartar poliglobulia, hipoxemia o desaturación sin compensación ventilatoria (PaCO2> 35 mmHg). Detección de elementos sugerentes de hipertensión pulmonar y sobrecarga del corazón derecho, y arritmias sin una causa aparente. Todas estas alteraciones pueden ser producidas por un SAOS.
-
Estudio de SAOS en pacientes electivos con elementos sospechosos de apnea del sueño moderada y severa. Evaluar uso preoperatorio de equipo de CPAP o BiPAP.
-
Evitar el uso de opioides y sedantes, en especial benzodiacepinas, en la premedicación anestésica sin vigilancia continua.
-
2. Manejo Intraoperatorio:
-
Durante la intubación y extubación de la tráquea deberán estar presentes en el pabellón al menos dos operadores entrenados en el manejo de la vía aérea. Además, se sugiere la presencia de un tercer operador experto, disponible en el área del pabellón, en caso de que no se pueda ventilar o intubar.
-
El pabellón debe disponer de máscaras faciales de distintos tamaños y perfiles, máscaras laríngeas y máscaras laríngeas de intubación (ILMA), laringoscopio con hojas de diferentes tamaños. En el área de pabellón debe haber un carro equipado con todos los elementos necesarios para el manejo de una vía aérea difícil.
-
El pabellón quirúrgico debe estar equipado con una mesa quirúrgica articulada, adecuada al peso del paciente, que permita fácilmente el cambio de posición del paciente.
-
El paciente debe mantenerse permanentemente en posición semisentada desde su ingreso a pabellón hasta después de la intubación y previo a la extubación de la tráquea.
-
Colocar al paciente en “posición en rampa”, elevando la porción superior del tronco y la cabeza 20 a 30°, con objeto de alinear el meato auditivo externo y el hueco supraesternal, antes de la inducción e intubación traqueal.
-
Oxigenación con FiO2 de 100% a través de máscara facial durante 3 a 5 minutos antes de la inducción de la anestesia general y la intubación.
-
Monitorización del bloqueo neuromuscular con un estimulador de nervio periférico, dotado de un método cuantitativo de medición de las respuestas musculares.
-
Reversión completa del bloqueo neuromuscular (Relación de TOF > 0,9) previo a la extubación.
-
Extubación traqueal con paciente despierto en posición semisentada o en decúbito lateral, para mejorar la mecánica ventilatoria, reducir el ascenso diafragmático y evitar el colapso de la vía aérea superior.
-
Iniciar analgesia multimodal (AINES, infiltración de herida con anestésicos locales, bloqueos neuroaxiales o regionales) durante la anestesia, para reducir las alteraciones respiratorias secundarias al dolor postoperatorio al despertar.
-
Trasladar al paciente desde el pabellón a la sala de recuperación, unidades de atención intermedia o intensiva en posición semisentada, con suplemento de oxígeno, sólo si cumplen las siguientes condiciones: el paciente está despierto, ventila en forma adecuada, mantiene una SaO2 > 90% y la hemodinamia es estable.
-
3. Cuidados Postoperatorios:
-
Manejo en unidades que permitan control médico y de enfermería continuo, monitorización, terapia respiratoria y oxigenoterapia, durante las primeras 24 a 48 horas del postoperatorio.
-
Posición semisentada permanente.
-
Aporte de oxígeno en la cantidad y por el tiempo necesario para mantener los niveles de saturación preoperatorios. Limitar el suplemento de oxígeno en los pacientes con SAOS puede ser útil para reducir el número y la duración de los episodios de apnea.
-
Monitorización continua con oximetría de pulso.
-
Analgesia efectiva con esquemas multimodales, para evitar o reducir el uso de opioides y sedantes en los pacientes con SAOS.
-
Reinicio precoz de la utilización de los dispositivos de CPAP durante el sueño de los pacientes que los utilizaban en el preoperatorio. Uso de CPAP en presencia de episodios frecuentes de apnea en el postoperatorio.
Resumen
La obesidad mórbida, reconocida históricamente como uno de los factores de riesgo de vía aérea difícil, hoy, a la luz de la experiencia en cirugía bariátrica, no constituye un factor de riesgo por sí misma, excepto en presencia de predictores de dificultad reconocidos y de SAOS. Debido a la repercusión de la obesidad en la función respiratoria y de los efectos devastadores que podría tener una vía aérea difícil durante la anestesia, es necesario reconocer previamente a los pacientes obesos con riesgo elevado de presentar el problema, realizando una exhaustiva evaluación preoperatoria, descartando un SAOS y disponiendo de los elementos y personal necesarios para evitarlo. Además de contar con personas experimentadas y capacitadas, es de gran utilidad disponer de recomendaciones y guías de manejo de la vía aérea para los pacientes obesos.
Bibliografía
- Caplan RA, Posner KL, Cheney F. Adverse Respiratory Events in Anesthesia: A Close Claims Analysis. Anesthesiology 1990; 71: 828-833.
- Practice Guidelines for Management of the Difficult Airway. An Update Report by the American Society of Anesthesiologists Task Force on Management of the Difficult Airway. Anesthesiology 2003; 98: 1269-1277.
- Deitel M. The Obesity Epidemic. Obes Surg 2006; 16: 377-378.
- National Institute Health Consensus Developement Conference Statement. Gastrointestinal Surgery for Severe Obesity. (2 Suppl). Am J Clin Nutr 1992; 55: S615-619.
- Adams JP, Murphy PC. Obesity in Anaesthesia and Intensive Care. Br J Anaesth 2000; 85: 91-108.
- Donlon, JV Jr. Anesthesia for Eye, Ear, Nose, and Throat. En Miller RD. Anesthesia. New York: Churchill Livingstone 1986; 3: 1837-1894.
- Langeron O, Masso E, Hureaux C, et al. Prediction of Difficult Mask Ventilation. Anesthesiology 2000; 92: 1229-1236.
- Juvin P, Lavaut E, Dupont H, et al. Difficult Tracheal Intubation is more Common in Obese than in Lean Patients. Anesth Analg 2003; 97: 595-600.
- Voyagis GS, Kyriakis P, Dimirtiou V, Vettrou I. Value of Oropharyngeal Mallampati Classification in Predicting Difficult Laryngoscopy among Obese Patients. Eur J Anaesthesiol 1998; 15: 330-334.
- Ezri T, Medalion B, Weisenberg M, et al. Increased Body Mass Index per se is not a Predictor of Difficult Laryngoscopy. Can J Anaesth 2003; 50: 179-183.
- Brodsky JB, Lemmens HJ, Brock-Utne J, et al. Morbid Obesity and Tracheal Intubation. Anesth Analg 2002; 94: 732-736.
- González H, Minville V, Delanoue K, et al. The Importance of Increased Neck Circumference to Intubation Difficulties in Obese Patients. Anesth Analg 2008; 106: 1132-1136.
- Biring MS, Lewis MI, Liu JT, et al. Pulmonary Physiologic Changes of Morbid Obesity. Am J Med Sci 1999; 318: 293-297.
- Kaw R, Aboussouan L, Auckley D, et al. Challenges in Pulmonary Risk Assessment and Perioperative Management in Bariatric Surgery Patients. Obes Surg 2008; 18: 134-138.
- Ebert TJ. Bariatric Medicine: Clinical Implications of Morbid Obesity. [ed.] Schwartz A J. The ASA Refresher Courses in Anesthesiology 2007; 35: 6.
- Collins JS, Lemmens H, Brodsky JB, et al. Laryngoscopy and Morbid Obesity: a Comparison of the “Sniff” and “Ramped” Positions. Obes Surg 2004; 14: 1171-1175.
- Rao SL, Kunselman AR, Schuler AG, Des Harnais S. Laryngoscopy and Tracheal Intubation in the Head-Elevated Position in Obese Patients: A Randomized, Controlled, Equivalence Trial. Anesth Analg 2008; 107: 1912-1918.
- Dixon BJ, Dixon JB, Carden JR, et al. Preoxygenation Is More Effective in the 25° Head-up Position Than in the Supine Position in Severely Obese Patients. Anesthesiology 2005; 102: 1110-1115.
- Altermatt FR, Muñoz HR, Delfino AE, Cortinez LI. Pre-oxygenation in the Obese Patient: Effects of Position on Tolerance to Apnoea. Br J Anaest 2005; 95: 706-709.
- Combes X, Sauvat S, Leroux B, et al. Intubating Laryngeal Mask Airway in Morbidly Obese and Lean Patients. 2005, Anestthesiology 2005; 102: 1106-1109.
- Frappier J, Guenoun T, Journois D, et al. Airway Management Using the Intubating Laryngeal Mask Airway for the Morbidly Obese Patient. Anesth Analg 2003; 96: 1510-1515.
- Abdi W, Dhonnheur G, Amathieu R, et al. LMA Supreme™ Versus Facemask Ventilation Performed by Novices: A Comparative Study in Morbidly Obese Patients Showing Difficult Ventilation Predictors. Obes Surg 2009; 19: 1624-1630.
- Sinha AC. Some Anesthetic Aspects of Morbid Obesity. Curr Opin Anaesthesiol 2009; 22: 442-446.
- Peiser J, Lavie P, Ovnat A, et al. Sleep Apnea Syndrome in the Morbidly Obese as an Indication for Weight Reduction Surgery. Ann Surg 1984; 199: 112-115.
- Jordan AS, White DP, Lo Y, et al. Airway Dilator Muscle Activity and Lung Volume During Stable Breathing in Obstructive Sleep Apnea. Sleep 2009; 32: 361-368.
- Bixler EO, Vgontzas AN, Ten HT, et al. Effects of Age on Sleep Apnea in Men: I. Prevalence and Severity. Am J Respir Crit Care Med 1998; 157: 144-148.
- Bixler EO, Vgontzas AN, Lihn HM, et al. Prevalence of Sleep-disordered Breathing in Women: Efects of Gender. Am J Respir Crit Care Med 2001; 163: 608-613.
- Young T, Evans L, Finn L, Palta M. Estimation of the Clinically Diagnosed Proportion of Sleep Apnea Syndrome in Middleaged Men and Women. Sleep 1997; 20: 705-706.
- O’Keeffe T, Patterson EJ. Evidence Supporting Routine Polysomnography before Bariatric Surgery. Obes Surg 2004; 14: 23-26.
- Kaw R, Michota F, Jaffer A, et al. Unrecognized Sleep Apnea in the Surgical Patient: Implications for the Perioperative Setting. Chest 2006; 129: 198-205.
- Liao P, Yegneswaran B, Vairavanathan S, et al. Postoperative Complications in Patients with Obstructive Sleep Apnea: A Retrospective Matched Cohort Study. Can J Anaesth 2009; 56: 819-828.
- Kushida CA, Littner MR, Morgenthaler T, et al. Practice Parameters for the Indications for Polysomnography and Related Procedures: an Update for 2005. Sleep 2005 28: 499-521.
- Practice Guidelines for the Perioperative Management of Patients with Obstructive Sleep Apnea. A Report by the American Society of Anesthesiologists Task Force on. Anesthesiology 2006; 104: 1081-1093.
- Chung F, Yegneswaran B, Liao P, et al. STOP Questionnaire: A Tool to Screen Patients for Obstructive Sleep Apnea. Anesthesiology 2008. 108: 812-821.
- Chung F, Yegneswaran B, Liao P, et al. Validation of the Berlin Questionnaire and American Society of Anesthesiologists Checklist as Screening Tools for Obstructive Sleep Apnea in Surgical Patients. Anesthesiology 2008; 108: 822-830.
- Chung SA, Yuan H, Chung F. A Systemic Review of Obstructive Sleep Apnea and Its Implications for Anesthesiologists. Anesth Analg 2008; 107: 1543-1563.
