Ingrid Del Pilar Chitiva MD.1,2, Carlos Quintero MD.1, Juan Sebastián González MD.1,2,3, Laura Daniela Aponte Camacho1,2, Tatiana Andrea Bernal1,2, Ricardo Salamanca Parra1,2
Recibido: 12-04-2023
Aceptado: 23-04-2023
©2023 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 52 Núm. 5 pp. 459-473|https://doi.org/10.25237/revchilanestv52n5-04
PDF|ePub|RIS
Anesthetic and perioperative management of thermal trauma in pediatrics
Abstract
The management of burn patients has always been a multidisciplinary challenge in which anesthesiologists play a crucial role, with their intervention having a great impact on the patient and their clinical outcome. Burn injuries have long been a public health problem in Colombia due to the high incidence, limited availability of specialized care, and the scant information on their management. This type of injury produces vast physiological responses, which can lead to fatal complications if an adequate approach is not undertaken. The burnt patient presents clinical variables that will determine the structure of the treatment, creating a wide and varied therapeutic spectrum with different management options. This narrative review explores articles and studies that describe the perioperative, anesthetic, and analgesic management of burn injuries in pediatric patients, with the aim of describing the appropriate approach in this population, thus helping nurture future analgesia and anesthesia recommendations.
Resumen
Desde siempre el manejo de pacientes quemados ha sido un desafío multidisciplinar, en el cual los anestesiólogos juegan un papel crucial, por ende su intervención tiene un gran impacto en el paciente e inclusive en su desenlace clínico. Hace décadas en Colombia, las quemaduras han sido un problema de salud pública, por su alta incidencia, la poca disponibilidad de atención especializada, y la escasa información sobre su manejo. Este tipo de lesiones producen respuestas fisiológicas que pueden generar complicaciones mortales si no se realiza un abordaje adecuado. El paciente quemado presenta variables clínicas que van a determinar la estructura del tratamiento, por lo que, el espectro terapéutico es amplio y variado con varias opciones de manejo. Esta es una revisión narrativa donde se tomaron artículos que describieron el manejo perioperatorio, anestésico y analgésico de las quemaduras en pacientes pediátricos, por ende, pretende describir el abordaje en esta población, con el objetivo de nutrir futuras guías de analgesia y anestesia.
-
Introducción
El manejo de pacientes con trauma térmico es un reto a nivel mundial, tanto en los servicios de urgencias como en los quirófanos, pues representa desafíos por la complejidad fisiopatológica y la extensión de las lesiones que se presentan. Es por esto que el anestesiólogo juega un papel crucial en el abordaje perioperatorio del paciente.
Actualmente, no existen recomendaciones establecidas en el abordaje perioperatorio del paciente pediátrico quemado, haciendo necesario una revisión de la literatura en adultos, en la cual se extrapolen las recomendaciones que se obtienen en esta población, pero haciendo especial énfasis en los aspectos fisiológicos característicos del paciente pediátrico, como la evaluación de la vía aérea, accesos venosos y el uso de medicamentos para el manejo analgésico transoperatorio.
La siguiente revisión tiene como fin agrupar evidencia disponible que sea útil para efectuar sugerencias en el manejo anestésico del paciente pediátrico con trauma térmico, y que a su vez ésta se considere como pilar para la profundización y producción de estudios con mayor evidencia que propongan el mejor pronóstico, disminuyendo costos en los distintos sistemas de salud.
La Organización Mundial de la Salud (OMS) estima que las heridas por quemaduras en la infancia representan aproximadamente 180.000 muertes anualmente, y países como Bangladesh, Egipto, Pakistán y Colombia representan el 17% de discapacidades temporales asociada a quemaduras y el 18% de discapacidades permanentes, convirtiendo a las quemaduras en la principal causa de muerte accidental y discapacidad en la infancia a nivel mundial[1]. Según los diferentes censos realizados globalmente, las quemaduras ocurren principalmente en países de medianos y bajos ingresos, considerando el ámbito laboral y el hogar como los lugares de mayor ocurrencia[2].
Las quemaduras han sido un tema de salud con gran impacto en Colombia desde hace décadas, por lo que se debe hacer especial énfasis en su epidemiología, tanto en población adulta, como en población pediátrica, esto para estimar estrategias de prevención[3]. Según el primer estudio de análisis de mortalidad de quemados en la infancia que se realizó en Colombia, se estimó que durante 2000-2009 la tasa de mortalidad ajustada fue de 0,912 por 100.000 habitantes por año, siendo los menores de 5 años los más afectados, con un porcentaje de 59,5% de un total de 1.197 pacientes fallecidos por quemaduras[4].
De forma paralela, en el informe anual del centro de excelencia de quemados de la Unidad de Servicios de Salud Simón Bolívar, se describe que durante el período 2013-2018, se presentaron 5.439 pacientes en estancia hospitalaria a causa de quemaduras[3], con una proporción de 65% y 35%, para hombres y mujeres respectivamente, siendo la causa principal líquidos hirvientes, seguidos de llama, electricidad, químicos, sólidos caliente y pólvora[3]. Por otra parte, en el período de 2016-2018 de 2.725 pacientes quemados 57,61% eran menores de 15 años, demostrando que más de la mitad del grupo etario de quemados corresponde a pacientes pediátricos[3]. Entre los departamentos con más mortalidad a causa de las quemaduras están Bogotá, Antioquia, Valle del Cauca, y Santander, sumando entre estos la mayoría de las fallecidos en el país por esta causa en 48%[3].
Con respecto al impacto en la salud pública, es claro que las secuelas psicosociales y emocionales, junto con las sesiones de recuperación, presentan un importante factor económico para los sistemas de salud del mundo, dado que en promedio, estos pacientes requieren alrededor de un año para la recuperación física de la misma[3]. Adicionalmente, el trauma térmico genera un gran costo al estado, por las hospitalizaciones prolongadas, incapacidades físicas y funcionales severas, e incapacidades laborales extensas, y en el caso de la población pediátrica se aplica igualmente, pero debido a su fisiología y su área de superficie corporal, pueden estar cursando por situaciones más críticas que generan retos a nivel clínico que por ende generan costos más elevados[2],[3].
En general, la información disponible es escasa y en muchos caso no es actualizada, ya que Colombia no tiene estadísticas nacionales de quemaduras[3] por no ser éstas un evento de notificación obligatoria, lo cual genera que no se tenga una incidencia real de los casos totales y que su impacto no se vea reflejado en programas y protocolos de promoción, prevención y tratamiento. Adicionalmente, y con respecto al manejo, también existe escasa información que no es muy clara, y no expone lineamientos o protocolos que guíen la atención de los pacientes pediátricos quemados con la rigurosidad con la que se requiere.
Es por esto que la presente investigación pretende describir el manejo inicial de un paciente pediátrico quemado, con el propósito de nutrir futuras guías de analgesia y anestesia sobre esta población. Además, también se enfoca en exhibir las principales diferencias entre la población general quemada y la pediátrica, entendiendo que se deben hacer cambios y modificaciones terapéuticas según el escenario al que el clínico se enfrente.
-
Metodología de la investigación
La investigación es una revisión narrativa con elementos de revisión sistemática, sin embargo, no pretende ser una revisión sistemática de la literatura y por ende no contará con la descripción de criterios de inclusión, exclusión ni el flujograma de información de selección de artículos. Lo que se incluirá serán los algoritmos de búsqueda y bases de datos usadas.
Para comenzar, se normalizaron los siguientes términos en los tesauros MeSH y DeCS: “Quemaduras pediátricas”, “pacientes pediátricos”, “cuidado perioperatorio”, “manejo anestésico”, “anestesia general”, “anestesia pediátrica”, “unidad de quemados”. “Pediatric burns”, “pediatric patients”, “perioperative care”, “anesthetic management”, “general anesthesia”, “pediatric anesthesia”, “burn unit”. Luego de esto, se crearon algoritmos de búsqueda para realizar la pesquisa en las siguientes bases de datos: PubMed, Scopus, Medline, Embase y ProQuest.
Los algoritmos utilizados fueron los siguientes:
• ((“Anesthetic management” OR “Anesthesia”) AND (“pediatric burns” OR (“pediatrics” AND “burns”) AND “perioperative care”).
• ((“Anesthetic management” OR “Anesthesia”) AND (“pediatric burns” OR (“pediatrics” AND “burns”) AND “burn unit”).
• (((“Anesthetic management” OR “Anesthesia”) OR (“pediatric anesthesia”)) AND ((“pediatric burns” OR (“pediatrics” AND “burns”) OR (“pediatric patients” AND “burns”)) AND “burn unit” AND “perioperative care”).
• ((“quemaduras pediátricas” OR (“quemaduras” AND “pacientes pediátricos”) AND (“manejo anestésico” OR “anestesia general” OR “anestesia pediátrica”) AND “unidad de quemados”).
• ((“quemaduras pediátricas” OR (“quemaduras” AND “pacientes pediátricos”) AND (“manejo anestésico” OR “anestesia general” OR “anestesia pediátrica”) AND “unidad de quemados” AND “cuidado perioperatorio”).
Se tomaron los artículos que describieron el abordaje anestésico, manejo perioperatorio y analgésico de los pacientes gran quemados pediátricos, incluyendo los cambios fisiopato-
lógicos relevantes, recomendaciones y evidencia actual, usando artículos en español e ingles desde, 2000 a 2022, en las bases de datos.
-
Resultados
-
Cambios fisiológicos en el gran quemado pediátrico
En el paciente gran quemado se alteran casi todos los sistemas orgánicos según el tamaño y la profundidad de la lesión por quemadura[2]. En la Tabla 1 se encuentran descritos los cambios fisiológicos más importantes en los quemados pediátricos. Se ha especificado que en las quemaduras extensas se desencadenan respuestas fisiológicas por los mediadores circulantes, perpetuando la inflamación local e inflamación sistémica, generando de esta manera la liberación de prostaglandinas, leucotrienos, bradiquininas, óxido nítrico, histamina, factor estimulante de colonias de granulocitos, proteína quimioatrayente de monocitos 1, interleucina (IL) 1, IL-6, IL-8, IL-10, factor de necrosis tumoral y radicales libres de oxígeno[5],[6]. Además, la activación de células presentadoras de antígenos y de la inmunidad adaptativa como T-helper (Th) -1, Th-2, Th-17 y células T citotóxicasT[6].
Los cambios fisiológicos y manifestaciones clínicas en el quemado son amplios y variables, coexisten varios factores que producen la inflamación y aquí están implicadas múltiples células, receptores, mediadores proinflamatorios y antiinflamatorios, que a su vez desempeñan un papel importante en la respuesta inmunitaria a la lesión por quemadura[6]. En la Tabla 1 se describen sistema por sistema las respuestas que existen debido al estrés térmico[6],[7],[8].
-
Clasificación de las quemaduras
La clasificación de las quemaduras se puede realizar dependiendo de la gravedad y profundidad de la misma. En el Gráfico 1 se encuentra una diferenciación basada en las capas anatómicas de la piel que permite establecer una escala de tiempo probable de curación[19].
-
Estimación del área de superficie corporal afectada por quemaduras
El área total de superficie corporal permite valorar la extensión de la quemadura, la regla tradicional de los nueve es menos exacta en niños, quienes tienen, relativamente una cabeza más grande y extremidades pequeñas comparados con los adultos como se describe en la Figura 1. Sin embargo, esta regla permite estimar de forma más rápida si el paciente debe ser transferido a un centro especializado. Lund y Browder en el 2019, reportaron un algoritmo basado en la edad que considera estas diferencias[19]. También se puede usar la regla de los uno, con la palma del paciente independiente de la edad, puede ser usada para estimar 1% de área de superficie corpo- ral[19].
La aplicación Mersey Burns app permite estimar el tamaño de la quemadura y podría ayudar a calcular la cantidad de líquidos para reanimación, ingresando la edad, peso del paciente y las áreas de la quemadura de espesor parcial. The National Institute for Health and Care Excellence (NICE) sugiere que podría ser una herramienta útil para reducir el tiempo de evaluación y facilitar así el manejo temprano de reanimación hídrica en estos pacientes para médicos no especialistas en quemados[20].
-
Criterios de remisión a unidad de quemados
La mayoría de quemaduras pueden ser valoradas y manejadas por los servicios de pediatría, pero es importante conocer los criterios de remisión a unidad de quemados, aquí se destacan los siguientes: Quemaduras mayores al 5%, cualquier quemadura que implique áreas especiales (cara, manos pies, y genitales) o que se encuentren sobre alguna articulación, pacientes donde se sospeche quemadura de vía área o que ésta sea secundaria a maltrato infantil, las quemaduras eléctricas y por agentes químicos[21]. Sin embargo, se debe considerar la estabilidad y la gravedad de las lesiones presentadas que puedan tolerar un traslado a un centro de referencia debido a que la mortalidad por trauma térmico mejora en centros especializados por el tratamiento específico que se ofrece. Se tiene en cuenta que la estancia puede llegar a ser prolongada, el Cuadro 1 describe los criterios para remisión a centros especializados en quemaduras[21].
Por su parte, la escala de Baux diseñada en 1960 para predecir la mortalidad de pacientes quemados, la cual utiliza como variables (edad + % de superficie corporal) en el que un puntaje mayor de 100 tiene una valor predictivo de mortalidad del 100%. Por lo cual, algunas instituciones toman como referencia el valor inicial para definir si el paciente es aceptado[21].
-
Evaluación preoperatoria
Los cambios fisiopatológicos en la fase inicial de la lesión, como el déficit del estado mental, hipovolemia, arritmias, edema, lesión renal aguda, inmunodeficiencias, entre otras[22], representan un reto en la evaluación preanestésica puesto que afectarán, directamente, el manejo del paciente pediátrico en el ámbito intraoperatorio. Durante esta fase son llevados frecuentemente, a procedimientos quirúrgicos como la escisión temprana de tejido necrótico con cobertura temporal o permanente de las áreas expuestas, disminuyendo así la posibilidad de colonización de heridas y sepsis sistémica. Estos procedimientos hacen parte de la atención durante el período agudo de la quemadura, cuando el paciente presenta inestabilidad hemodiná- mica y/o ventilatoria[23].
Dentro de la valoración preoperatoria estándar existen variables que se deben tomar en cuenta, especialmente, en los pacientes pediátricos, y que son listados en la Tabla 2. Teniendo en cuenta que la valoración se lleva a cabo sobre un procedimiento planeado con antelación, es necesario evaluar y manejar adecuadamente la vía aérea, la alimentación por sonda nasogástrica o nasoyeyunal, conocer el plan quirúrgico con el fin de estimar las pérdidas sanguíneas y, si es necesario, reserva de hemoderivados, dependiendo de la extensión de la quemadura. Simultáneamente evaluar el requerimiento de monitoria invasiva al igual que contemplar el uso de inotrópicos, estar en comunicación directa con el equipo quirúrgico y de cuidados intensivos para la planificación de la atención perioperatoria[23]. En el escenario de pacientes pediátricos, algunos procedimientos, como el cuidado de heridas por quemaduras mayores del
Tabla 1. Cambios fisiológicos en el gran Quemado

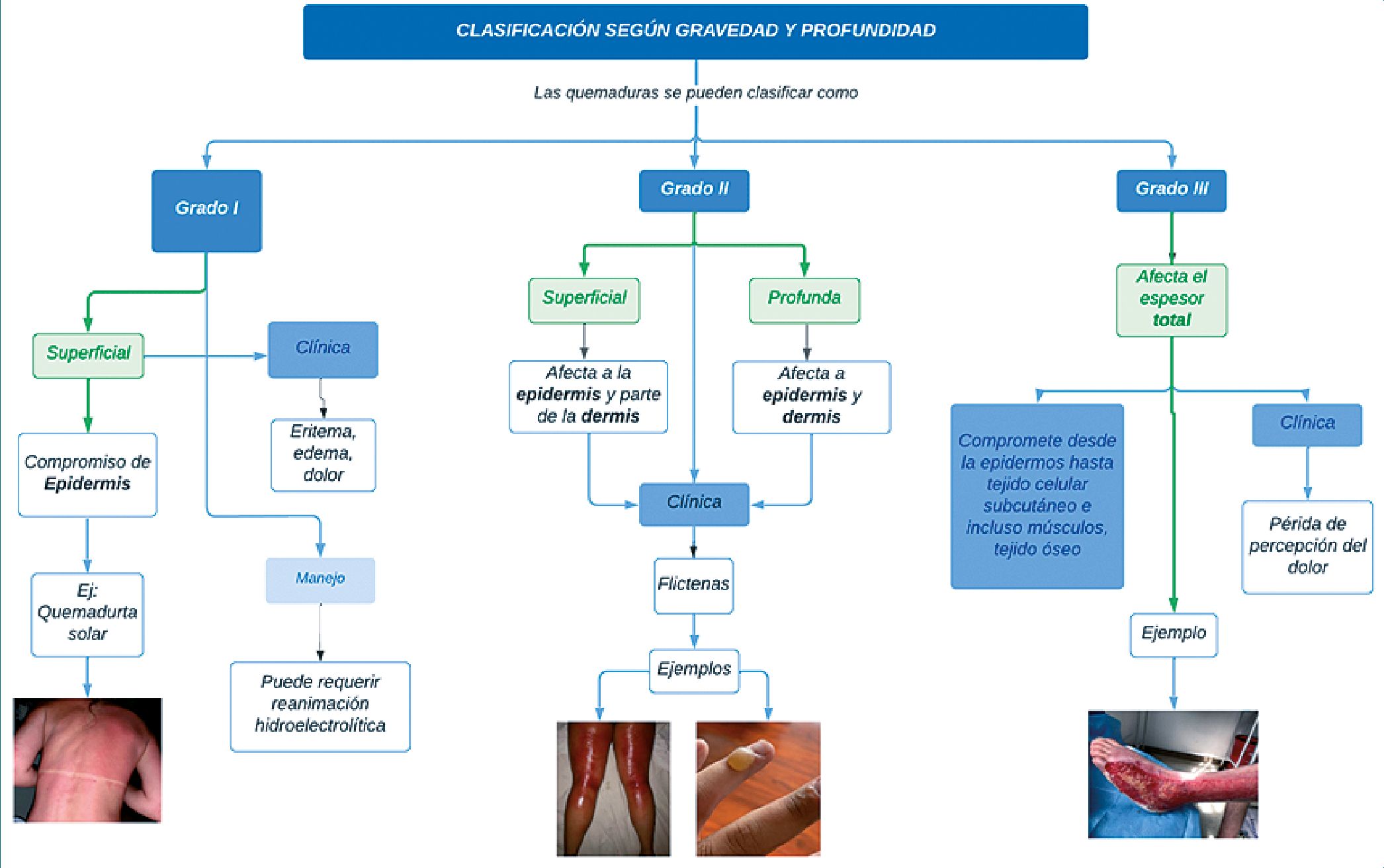
Gráfico 1. Clasificación de las quemaduras según su gravedad y profundidad. Elaboración propia.
5% TBSA o en manos o pies, pueden llegar a ser tan dolorosos que requieren sedación o anestesia general[24]. Finalmente, el uso de antibiótico en contexto de evitar una bacteriemia por desbridamiento, usando cefalosporinas (cefazolina) 50 mg/kg/ dosis por vía intravenosa. La clindamicina 20 mg/kg es el agente preferido en pacientes sensibles a la penicilina[35].
Sumado a esto, parte del proceso del paciente involucra a sus padres o responsables directos, por ende, se debe explicar y preparar en ellos el papel que se espera que desempeñen[35]. El niño debe sentirse lo más cómodo posible dentro del ambiente hospitalario y dentro de su contexto actual como paciente quemado, por lo que los esfuerzos de querer normalizar los espacios donde se encuentra, son completamente válidos. Esto ayuda a fomentar la seguridad mental del niño, permitiendo que se sienta más seguro y con menor ansiedad[41]. Son medidas no farmacológicas que son, significativamente, satis
factorias para el niño, por la oscuridad al dormir, música, videos o programas de televisión, ambientar la habitación con colores u objetos que le sean familiares al niño, ya que al estar en una cama de UCI o en una hospitalización prolongada el niño puede perder el sentido del Yo[41].
-
Ayuno preoperatorio
El soporte nutricional es fundamental para el manejo de pacientes con quemaduras moderadas a severas, dado que los requerimientos calóricos aumentan por el estado hipercatabólico que desarrollan los pacientes quemados por la respuesta al estrés, la respuesta inflamatoria, la extension de la quemadura, edad y sexo[25]. Algunos investigadores no recomiendan un ayuno prolongado en estos pacientes, pues el déficit calórico puede causar una desnutrición, lo cual tendría un impacto negativo en la recuperación[26], como el aumento de la incidencia de atrofia de la mucosa intestinal, virulencia de la sub-flora, translocación microbiana, catabolismo proteico, pérdida de peso, infecciones oportunistas, sepsis y multiorgánica falla[27].
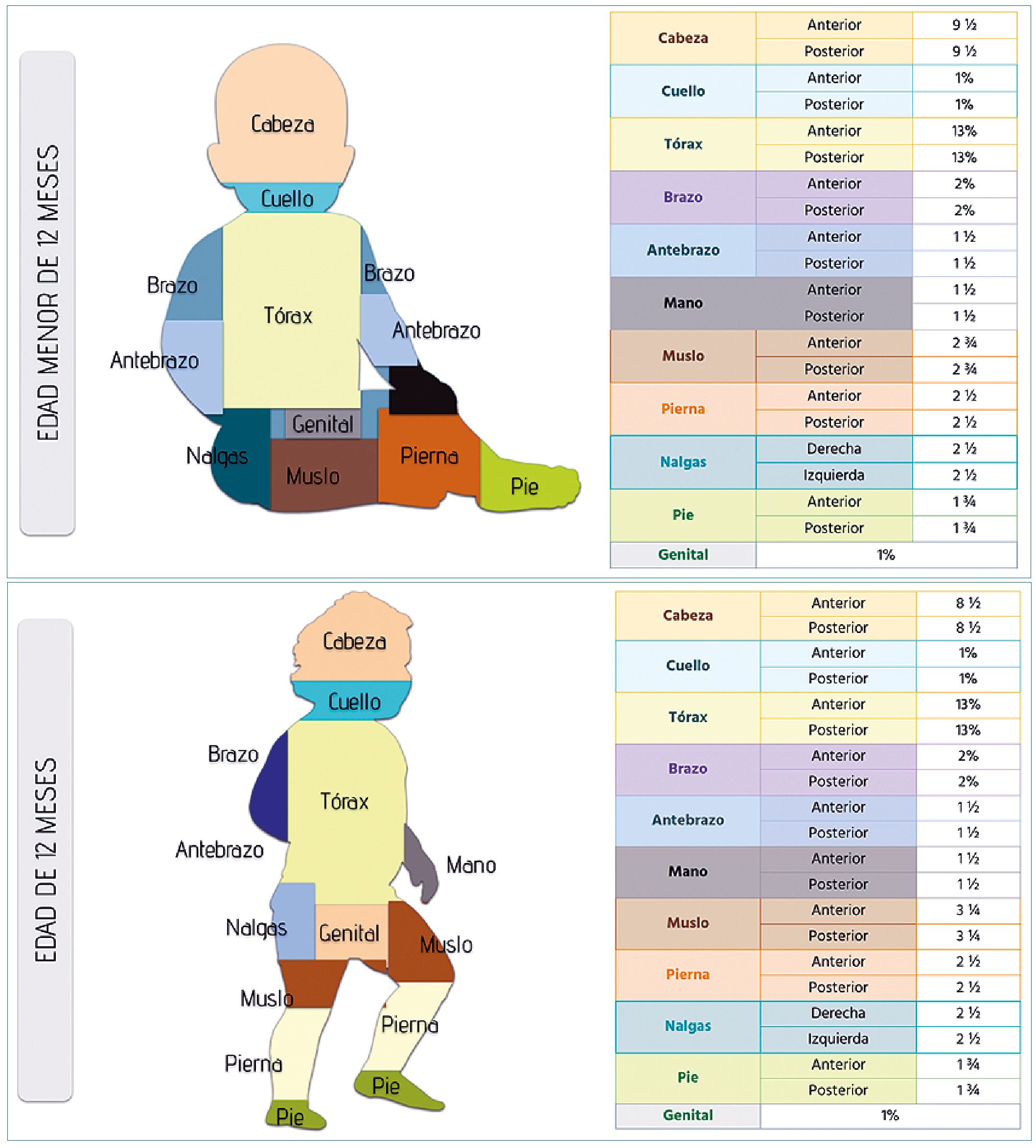
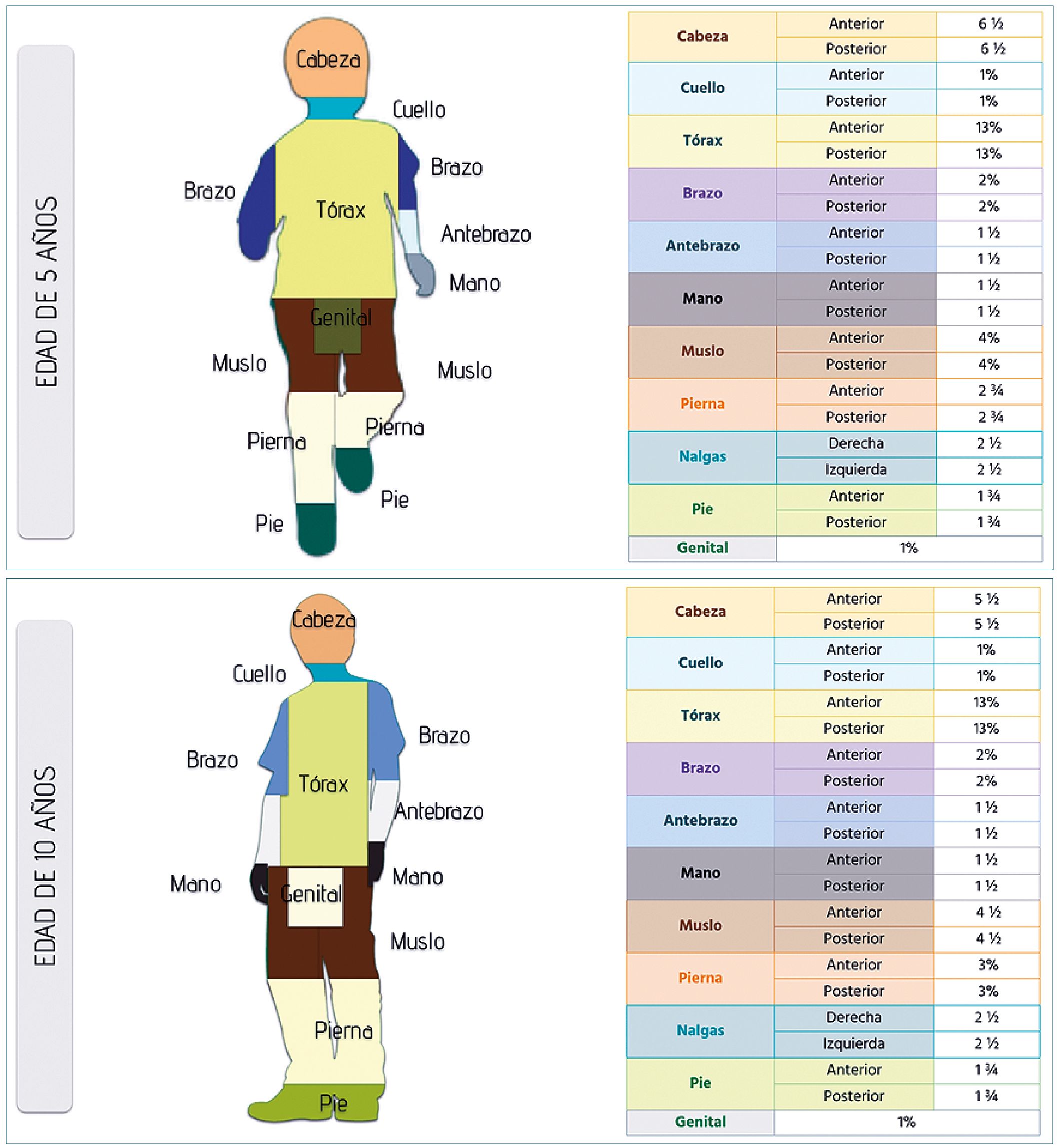
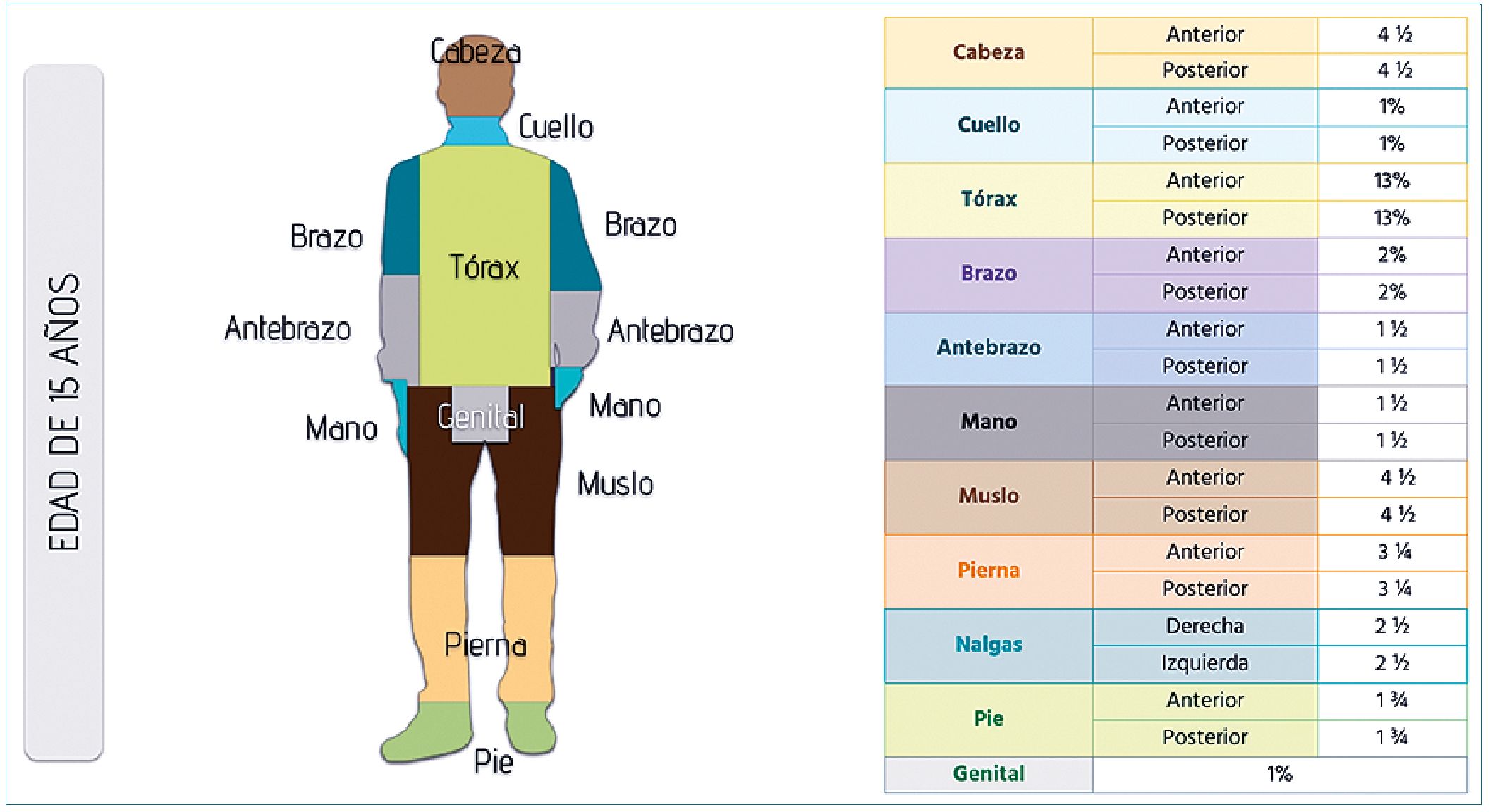
Figura 1. Ilustración del porcentaje de quemadura total en la superficie corporal en niños. Modificado de: Total Burn Care. 2018. 5th Edition.
Cuadro 1. Criterios para remisión a centro especializado en quemaduras

Aún existen muchos interrogantes acerca de una óptima nutrición, volumen y composición de la dieta para el paciente quemado, aunque algunos autores coinciden en sus posiciones. En el contexto de una quemadura grande/severa, el tracto gastrointestinal (TGI) se encuentra en estrés por las lesiones y por el mismo tratamiento requerido para preservar la vida[28]. Por ejemplo, la reanimación con líquidos genera edema generalizado, eso incluye al TGI, por lo que si no es estimulado desde el comienzo pueden existir complicaciones como íleo paralítico[28], por lo cual, se elige la alimentación por vía enteral temprana en pacientes con quemaduras moderadas a graves, pues se asocia con ventajas clínicas y biológicas, como la disminución de la respuesta metabólica, de los niveles de cortisol, reducción de úlceras por estrés y al mismo tiempo, se previene la desnutrición y el déficit energético[28].
Adicionalmente, estos pacientes requieren múltiples procedimientos quirúrgicos que interrumpen con frecuencia la nutrición. Se ha demostrado que los períodos de ayuno de 8 horas dificultan el cumplimiento de los altos requerimientos calóricos. Para tratar de corregir esto, la alimentación pospilórica ha demostrado ser exitosa[14] en pacientes con la vía aérea asegurada con tubo endotraqueal o traqueostomía, evitando así su interrupción durante el período perioperatorio. Sin embargo, si existe riesgo de incremento de la presión abdominal (posición prona durante la cirugía) o cuando se realizará un procedimiento de vía aérea como la traqueostomía, sería prudente suspenderla[14]. Es importante resaltar que todos los pacientes quemados se consideran estómago lleno por el íleo y la disminución del vaciamiento gástrico, por lo tanto, siempre se debe abordar con secuencia de inducción e intubación rápida.
Tabla 2. Valoración preoperatoria

Manejo intraoperatorio
a. Vía aérea
El abordaje de la vía aérea por el anestesiólogo puede ser requerido en cualquier estadío de la quemadura por lo que la disponibilidad de diferentes tamaños de laringoscopio, videolaringoscopio, equipo de fibra-óptica y dispositivos supraglóticos, es esencial, ya que la anatomía puede estar alterada por la quemadura. Generalmente, estos pacientes se consideran vía aérea difícil anticipada cuando presentan lesiones en cara o cuello o de inhalación, por lo que se debe priorizar el mantenimiento de la ventilación espontánea. Dada la incapacidad de cooperación del paciente pediátrico para técnicas de vía aérea difícil en paciente despierto, el abordaje seguro incluye el uso de intubación por fibra óptica bajo sedación o anestesia asegurando la ventilación espontánea. El uso de medicamentos como ketamina, dexmedetomidina para sedación, tienen la ventaja de mantener los reflejos protectores de la vía aérea y la respiración espontánea. La anestesia general con sevoflurano o una infusión intravenosa de propofol podría también mantener la ventilación espontánea[29]. La selección del tubo endotraqueal con neumotaponador en pacientes pediátricos es de vital importancia[30]. La fijación debe realizarse sin cintas en áreas quemadas, puede ser necesaria la fijación a encías o dientes para disminuir el riesgo de extubaciones accidentales.
La presencia de quemadura en cara y cuello incrementa el riesgo de la reducción del calibre de la vía aérea superior o la disminución de la movilidad de las estructuras anatómicas profundas del cuello. Se debe prestar especial atención al edema lingual, de faringe y laringe[22]. La consideración de valoración por nasofibroscopia en pacientes pediátricos quemados es importante, dado que el diámetro de las vías respiratorias es mucho menor por el edema causando obstrucción por lo que la intubación temprana no debe ser retrasada[31].
Por otro lado, la oxigenación, ventilación y mecánica respiratoria pueden estar comprometidas si hay presencia de lesión por inhalación, la cual podría ocasionar falla ventilatoria incrementando así la morbimortalidad. La patofisiología de la falla respiratoria por inhalación de humo se da porque la Compliance pulmonar se ve afectada y aumenta el volumen (de cierre), disminuye la capacidad residual y esto produce atelectasia y cortocircuito resultando en hipoxia[22]. La vía aérea se ve reducida en calibre por aumento de secreción de moco y pobre actividad ciliar del epitelio respiratorio. Análogamente, la inhalación de humo puede conducir a intoxicación por dióxido de carbono y/o productos cianógenos si se han quemado plásticos, es por esto que se deben tomar niveles de carboxihemoglobina, buscar signos y síntomas como cefalea, déficit del estado mental, letargia, adinamia, entre otros, además de iniciar soporte ventilatorio con aporte de oxígeno elevado[22].
La lesión de vía aérea inferior se puede sospechar con evidencia de quemaduras faciales, esputo carbonáceo, vellos nasales quemados y la ronquera los cuales son indicadores de necesidad de una vía aérea definitiva[19].
b. Monitorización
En pacientes pediátricos, con quemaduras extensas, se puede dificultar la ubicación estándar de la monitoria. Para la colocación de los electrodos del ECG se pueden necesitar suturas para que haya contacto, además el pulsioxímetro y el tensiómetro pueden resultar difíciles de posicionar, junto con sitios limitados para poner una línea arterial[22]. Además, se puede considerar medir la presión venosa central, gases arteriales, electrolitos y gasto urinario (GU)[32]. La medición de producción de orina es una medida de la perfusión de los órganos y de la adecuación de la resucitación hídrica, claro que esto depende de la edad y del tamaño del niño. Actualmente, se sugiere un GU de 1 ml/kg/h para niños con peso menor a 30 kg y de 0,5 ml/kg/h en niños con más de 30 kg[15].
La frecuencia de pulso, de respiración y la PAS son parámetros importantes que nos pueden sugerir estabilidad hemo- dinámica, pero debemos saber que el estado hipermetabólico de los pacientes quemados nos puede confundir[30]. En estos pacientes es de vital importancia monitorear la temperatura y la pérdida de sangre, ya que puede ser hasta de 3,4% de pérdida de volumen total sanguíneo por cada 1% de TBSA quemada. Los riesgos de sangrado son exacerbados cuando hay infecciones subyacentes, quemaduras muy profundas y tiempos quirúrgicos prolongados, en estos casos se deberían considerar alternativas como torniquetes de extremidades, administración de adrenalina tópica, compresas y en algunos casos es de utilidad tener la capacidad de realizar una tromboelastografía para identificar alteraciones de coagulación[22].
c. Acceso vascular
Los infantes y niños con quemaduras de más del 10% TBSA y adolescentes con más del 15% TBSA requieren hidratación endovenosa, mientras que con porcentajes menores son tratados con hidratación oral[15]. En el gran quemado es esencial no retrasar la resucitación hídrica ya que puede resultar en incremento de tasas de complicaciones tales como falla renal, estancia hospitalaria prolongada y la mortalidad[33], por lo que es necesario tener accesos vasculares periféricos para poder realizar administración de líquidos, medicamentos, toma de muestras y monitoreo hemodinámico y evaluar qué tan eficaz ha sido la reanimación con líquidos previa[22]. Sin embargo, por la extensión de las quemaduras no siempre es posible, por lo que se decide muchas veces realizar una cateterización de vía central y en una región de piel que no esté afectada, preferible mente con varias vías[22].
El uso de la ultrasonografía para localización de las venas periféricas o centrales es de gran utilidad en pacientes con difícil acceso venoso[23]. Adicionalmente, debido a la vasoconstricción e hipovolemia es difícil acceder a los compartimentos vasculares y, constantemente, se necesitará cambiar el punto de punción si son catéteres periféricos, y en el caso de las vías centrales, no siempre son aptas para infusiones rápidas de líquidos y productos sanguíneos[22]. Debido a esto, pueden haber complicaciones como trombosis en las vías periféricas que puedan generar eventos tromboembólicos, además de infecciones locales[22]. En caso tal de no lograrse ningún acceso se puede utilizar de manera temporal la vía intraósea, pero debe ser reemplazada a las 24 horas[23].
d. Control de temperatura
El control de la temperatura es especialmente importante y desafiante para los pacientes pediátricos quemados. Por la quemadura hay una pérdida de la integridad de la piel que hace que pierdan más fácilmente calor, por lo cual es esencial la medición de la temperatura central[20]. La hipotermia en estos pacientes provoca un aumento exagerado del consumo de oxígeno, exacerba la respuesta catabólica a las lesiones, durante cirugía puede incrementar la pérdida de sangre y a su vez la morbimortalidad.
Algunas estrategias como la elevación de la temperatura en el quirófano cirugía por encima de 28°C[23], la disponibilidad de dispositivos para el calentamiento de líquidos y/o sangre, mantas térmicas, el cubrimiento de áreas no quemadas, envolver la cabeza minimizando el área de superficie corporal expuesta, el uso de calentadores de aire forzado y cubiertas de plástico[34].
Una de las complicaciones posteriores a las quemaduras es la pirexia, que puede aparecer de 24 – 48 h después de la lesión, aumentando la tasa metabólica basal y el gasto energético y en los casos más severos puede requerir hemofiltración. No suele ser ocasionada por infección, sin embargo, hay que descartarla[20].
-
Consideraciones farmacológicas
Existen alteraciones tanto farmacocinéticas como farmacodinámicas en el paciente quemado y es por esto que se debe ajustar la dosis del fármaco para evitar intoxicaciones o para mejorar su eficacia[22]. Los cambios fisiopatológicos afectan la unión a proteínas, el volumen de distribución y el aclaramiento, lo cual afecta directamente la dosis-efecto del fármaco.
En la fase inicial o período hipovolémico de la quemadura, el gasto cardíaco está, dramáticamente, disminuido por una rápida disminución del volumen vascular, efectivo secundario al incremento de la permeabilidad vascular dado a la liberación de mediadores inflamatorios como respuesta a las quemaduras extensas. Durante esta fase, hay una fuga capilar de líquido y proteínas como la albúmina, disminuyendo la presión oncótica, lo que favorece la salida del líquido intravascular al espacio intersticial. Adicionalmente, el metabolismo hepático y la eliminación renal pueden estar disminuidos como consecuencia de la reducción de la perfusión de estos órganos, secundario a que el gasto cardíaco es bajo y la combinación de anestésicos puede resultar en hipotensión grave[22].
Luego de 48 h de la lesión, se instaura la fase hipermetabólica o catabólica e hiperdinámica que, generalmente, se acompaña de un gasto cardíaco aumentado, mayor consumo de oxígeno y temperatura corporal elevada[22]. El volumen de distribución se ve incrementado con los grandes volúmenes de líquidos administrados durante la reanimación, por lo cual mayores dosis medicamentosas son necesarias para alcanzar la concentración sérica.
Asimismo, aumenta la perfusión a los riñones e hígado que generarán el efecto contrario al anterior mencionado, incrementando la tasa de filtración glomerular, por lo tanto, la eliminación y metabolismo de los fármacos, ocasionando una necesidad de dosis más altas y menor tiempo de intervalos en la administración del medicamento. Los niveles plasmáticos de albúmina se encuentran, severamente, disminuidos y la producción de proteínas de fase aguda como la alfa-1-glicoproteína ácida incrementa casi al doble[36]. Durante esta fase la unión a las proteínas plasmáticas se encuentra alterada.
La disminución de unión a proteínas incrementa la fracción libre, por lo tanto, su efecto farmacológico y viceversa[16]. Existen algunos fármacos con alta unión a proteínas, como de pH ácido que se unen a la albúmina, la cual está reducida debido al edema, por lo tanto, mayor fracción libre del medicamento y las de pH básico tienden a unirse a la alfa-1-glicoproteína ácida, que está elevada por ser reactante de fase aguda, con una consecuente disminución de la fracción libre. Se debe prever que haya una amplia variabilidad interindividual de la respuesta a los fármacos que se le van a administrar al paciente, por lo tanto, se recomienda una titulación cuidadosa a la hora de buscar un efecto deseado[16],[22].
-
Manejo anestésico
Con respecto al manejo anestésico en pacientes pediátricos se pueden considerar alternativas como TIVA (anestesia total intravenosa) y agentes inhalados, sin embargo, no hay suficiente evidencia sobre cuál se usa con más frecuencia en pacientes quemados. Además de esto, son más seguros hepática y cardiovascularmente, tienen pocos efectos adversos y las respuestas esperadas según la MAC son más predecibles y manejables que con anestésicos intravenosos[37].
En pacientes quemados, la técnica de inducción anestésica debe ser basada según factores como dilatación ventricular, hipertrofia ventricular, hipertensión pulmonar, arritmias y el riesgo-beneficio debe ser personalizado para cada paciente[37]. Por otra parte, los eventos adversos que sí son comunes cuando la inducción es dada con agentes volátiles son: movimiento, laringoespasmo, tos, náusea y vómito posoperatorios que según el Journal of Cardiac Critical Care no son, significativamente, mayores a los causados por TIVA[35].
La elección del agente anestésico debe basarse en el estado hemodinámico y ventilatorio del paciente, recordando que la vía aérea en ellos puede estar comprometida por quemaduras[23]. Se necesita de mayores dosis de anestésicos, por ejemplo el propofol, para que se alcance su efecto hipnótico. Esto se debe a que los pacientes cuando están en el estado hipermetabólico generan un clearance mayor del medicamento[23]. Sin embargo, se debe ser prudente a la hora de su administración pues sus efectos depresores hemodinámicos seguirán presentes. En varios lugares la ketamina es el anestésico preferido en pacientes quemados por su buen perfil de seguridad y eficacia[23]. Este fármaco preserva la hemodinamia, la vía aérea y la función ventilatoria, lo que la hace ideal en los grandes quemados, se puede administrar en una dosis de 0,5 – 2,0 mg/kg teniendo en cuenta el contexto del paciente[38]. La ketamina puede ser administrada con otros anestésicos con un efecto analgésico potente y es comúnmente usada en sedación, lo cual resulta óptimo para el desbridamiento quirúrgico[38].
Otro aspecto relevante a tener en cuenta es el uso de anestesia general en cierto contextos posteriores a la cirugía como lo es el cambio de apósitos, en la mayoría de escenarios no es necesario llevar a la anestesia general, sin embargo, en el caso de tener un paciente con quemaduras mayores del 20% de superficie de área corporal total comprometida por la lesión, quemaduras en cara, las manos, los pies y el perineo, o en zonas que requieran la manipulación de articulaciones, niños con problemas mentales, dificultad para la comunicación, o con trastorno de estrés postraumático, lo ideal para llevar a cabo el cambio de apósitos es la anestesia general[34].
Por otra parte, la anestesia regional ha demostrado ser útil en estos pacientes debido a que ha mejorado el dolor posoperatorio y mejorado los desenlaces de rehabilitación[37]. Dentro de las técnicas más usadas se encuentran los bloqueos neuroaxiales, tanto como anestésico único y como coadyuvante en modulación dolorosa, se recomienda usar anestesia epidural o anestesia caudal cuando los procedimientos son solo en los miembros inferiores. En pacientes adultos se puede considerar epidural o anestesia intratecal para miembros inferiores y bloqueo del plexo braquial como anestesia para el procedimiento o para la analgesia posoperatoria[37].
-
Relajantes musculares
La farmacología de los medicamentos cambia en los pacientes quemados, como se ha expuesto anteriormente. En el caso del uso de la succinilcolina no se debería administrar después de las primeras 48 h posteriores a la quemadura debido a que existe un incremento en la sensibilidad de la misma que puede terminar en una respuesta hiperkalemica exagerada que se puede prolongar hasta 2 años después de la lesión[35]. El efecto de los relajantes musculares no despolarizantes se ve disminuido, necesitando mayores dosis para lograr el efecto terapéutico requerido[35], lo cual también está relacionado con el incremento de receptores de acetilcolina. En estos casos, la dosis recomendada para secuencia de intubación rápida con rocuronio en los quemados sería de 1,2 a 1,5 mg/kg y que se llegaría a su efecto en un tiempo de 90 segundos a diferencia de los 60 segundos esperados normalmente[35].
-
Administración de líquidos
El manejo de líquidos en pacientes pediátricos con trauma térmico siempre va a ser un reto, se considera que la hidrata- ción oral en paciente con quemaduras superficiales y menores del 5% son aceptables, sin embargo, infantes y niños con quemaduras mayores al 10%, o adolescentes con más del 15% de la superficie de área corporal requiere de reposición hídrica endovenosa, como se mencionó anteriormente. La pérdida de la integridad de la piel lleva a un aumento en la permeabilidad capilar, que desencadena una depleción de volumen y puede resultar rápidamente en hipovolemia y shock[15]. Por lo anterior, es fundamental no subestimar el área de superficie corporal en los niños, ya que el volumen requerido por porcentaje de superficie corporal quemada es mayor comparado con los adultos[15].
Otro aspecto importante en el manejo de líquidos en infantes es el riesgo de hipoglucemia, debido a sus reservas limitadas de glucógeno. La resucitación debe iniciar con lactato de ringer sin importar la edad y adicionar soluciones dextrosadas en niños con menos de 30 kg de peso o menores de 5 años[33].
Basados en estas diferencias fisiológicas, existen varias fórmulas pediátricas que se encuentran relacionadas en la Tabla 3. La más conocida y usada es la fórmula de Parkland, la fórmula modificada de Brook con regímenes más restrictivos[33]. Las fórmulas de Cincinnati y Galveston están basadas en el área de superficie corporal quemada en función de volúmenes estimados de reanimación con líquidos y los líquidos de mantenimiento que contienen dextrosa y albúmina[33].
En un estudio randomizado por Müller et al., se describe que la administración de albúmina de manera temprana en niños con quemaduras de más del 15% de superficie de área corporal, podría reducir la cantidad de cristaloides al momento de realizar la reanimación, disminuyendo también la extravasación masiva de líquidos y logrando una menor estancia hospitalaria[34]. Antes se relacionaba el uso de coloides con aumento de mortalidad. En estudios posteriores se encontró que no se podía asociar la sola administración de estos fluidos con este desenlace sino que dependía de las comorbilidades del paciente[34]. Del mismo modo, se describe que los coloides, como la albúmina, puede usarse para reducir el riesgo de desarrollar Fluid Creep, especialmente, en los grandes quemados[34].
En los grandes quemados se realiza una administración de líquidos importante para lograr una normalización hemodinámica. Los criterios de valoración de la reanimación del gran quemado son el gasto urinario monitorizado por horario. Los hallazgos del examen físico, como son la perfusión periférica, el sensorio y monitoreo hemodinámico con el fin evitar una resucitación con líquidos inadecuada o complicaciones asociada a la sobre resucitación o “fluid creep”[15]. El riesgo de edema pulmonar, síndrome compartimental abdominal o de las extremidades pueden ser gestionados mediante la monitorización de forma temprana, lo cual en pacientes pediátricos es de vital importancia[30].
Tabla 3. Fórmulas de administración de líquido endovenoso en pacientes pediátricos

Pérdidas sanguíneas y necesidad de hemoderivados
Las pérdidas sanguíneas son inevitables durante cirugía, sin embargo, se pueden intentar mitigar, inicialmente, con técnicas quirúrgicas y/o farmacológicas como con el uso de antifibrinolíticos, los cuales han sido exitosamente usados en cirugía craneofacial, en la cual la pérdida sanguínea puede ser similar en velocidad y extensión[19].
Algunos estudios han demostrado que quemaduras de más del 20% TBSA en pacientes pediátricos puede ser un predictor de transfusión[39]. Existen múltiples diferencias con los adultos a la hora del abordaje para la transfusión que varía con la edad, como en los más jóvenes tiene mayor área de superficie corporal por masa que el adulto, la frecuencia cardíaca, la función cardíaca, el volumen sanguíneo que varía según los grupos de edad. Los niveles de hemoglobina también son dependientes de la edad. Los niños más pequeños tienen mayor riesgo de complicaciones asociadas a la transfusión como la hiperkalemia en quienes reciben un volumen mayor de 20 ml/kg, por lo tanto, los niveles de potasio deben ser monitoreados. Se puede disminuir el riesgo de paro cardíaco hiperkalémico usando UGRE jóvenes de menos de 7 días, eritrocitos lavados antes de la transfusión y evitar transfundir sangre total. Una tasa de infusión menor de 1 ml/kg/min puede disminuir el efecto hipocalcémico de la transfusión[40].
Los criterios de transfusión en pacientes críticos y pediátricos quemados siguen siendo debatibles. Algunos estudios han sugerido que los protocolos de transfusión restringida son más seguros y eficaces, reduciendo riesgos médicos y menor carga económica. Los umbrales restrictivos para transfusión sanguínea en este estudio retrospectivo fueron de 7 g/dl, mostrando menor mortalidad[40]. La guía alemana recomienda un umbral de 7 g/dl en pacientes hemodinámicamente estables y de 10 g/ dL en pacientes hemodinámicamente inestables para niños mayores de 4 meses con sangrado activo, sin embargo, este valor no es específico en niños con lesiones de quemaduras[40].
La óptima relación de plasma fresco congelado y glóbulos rojos empaquetados en sangrado masivo no ha sido definido, sin embargo, un estudio prospectivo en niños quemados sugiere que una relación 1:1 puede mejorar resultados[40]. Para calcular el volumen máximo permitido de pérdidas sanguíneas durante una cirugía sin transfusión sanguínea, puede ser calculado a través de la siguiente fórmula[40].
(Hct inicial – Hct final)/Hct inicial) x VSE
Hct = hematocrito VSE = Volumen sanguíneo estimado
No hay que olvidar que la transfusión de glóbulos rojos debe ser realizada teniendo en cuenta el estado general y metabóli- co del paciente y consideraciones en las que el paciente sigue perdiendo sangre más que por los valores del hemograma[23]. Adicionalmente, la transfusión masiva incrementa el riesgo de mortalidad temprana, ya que puede resultar en hipotermia, acidosis y coagulopatía, la triada de la muerte[39].
Analgesia
En el paciente pediátrico quemado, la sedación y la analgesia juegan un papel importante ya que el dolor puede estar exacerbado por la ansiedad, miedo a extraños, separación de sus padres, temor a lo que pueda pasar después de la lesión, lo cual hace que la evaluación sea más difícil en las edades más tempranas[23]. Adicionalmente, casi todo el manejo de las quemaduras como las escisiones, los desbridamientos, cambios de vendajes, terapia física, entre otras, son dolorosas[23]. Teniendo en cuenta que el dolor por quemadura es una de las formas más severas de dolor agudo[41], debe ser tratado adecuadamente ya que puede resultar en desorden de estrés postraumático, secuelas psicológicas o incluso dolor crónico[41].
Los opioides son el tratamiento a elección para el dolor derivado de quemaduras, entre ellos la morfina es el más usado y se ha demostrado que la analgesia controlada por el paciente con opioides es segura y efectiva tanto en adultos como niños[23],[38]. Estos se deben administrar de forma controlada, en dosis bajas y titulados según el efecto en el paciente por la tolerancia que pueden generar. Asimismo, la evaluación constante de la función ventilatoria es importante, puesto que los opioides son depresores respiratorios fuertes[23],[38]. Se ha demostrado que su administración contínua puede conducir hiperalgesia inducida por opioides y por esto hay que estratificar de manera adecuada el dolor para no sobrepasar las dosis terapéuticas y poder transicionar entre varios opioides y hacer uso de otras alternativas[23].
También existe la alternativa de utilizar como tratamiento coadyuvante, analgésicos como acetaminofen, siendo éste el más usado, o AINES, gabapentina, o antidepresivos tricíclicos, ya que se ha demostrado que mejoran el dolor neuropático y nociceptivo perioperatorio. Inclusive la anestesia regional como el bloqueo de nervios periféricos, ayudan a reducir también el dolor posoperatorio y tener una mejor evolución clínica, especialmente cuando se trata de procedimientos reconstructivos secundarios a las quemaduras[23]. De la misma manera, una revisión sistemática de manejo no farmacológico en manejo de dolor secundario a procedimientos en pacientes pediátricos demostró ser efectiva como manejo adjunto, con mayor efectividad con los juegos de realidad virtual, con una reducción del dolor hasta de 68,3%, seguido de dispositivos de distracción no tecnológicos y terapia infantil[40].
-
Discusión de resultados
Abstrayendo toda la búsqueda realizada, y las consideraciones clínicas de las quemaduras en pacientes pediátricos, se tienen en cuenta variadas apreciaciones como que existe muy poca información acerca del manejo anestésico de pacientes pediátricos quemados y, junto a ello, los limitantes epidemiológicos también son una constante, lo que hace de su tratamiento un reto importante desde cualquier esfera humana.
Se evidenciaron muchas consideraciones especiales sobre el manejo de quemaduras en esta población, y las diferencias de tratamiento en contraste con los adultos, que se hacen mucho más relevantes cuando comparamos la anatomía, la fisiología, o inclusive aspectos sociales y económicos. Por ejemplo, la tráquea con diámetro más pequeño en la población pediátrica, esto en específico puede causar edema e influir, significativamente, en el flujo de oxígeno a través de las vías aéreas, causando una obstrucción mucho más rápida. La pérdida de calor por quemaduras es también más rápida en niños por la superficie de área corporal, que es evidentemente más reducida que la de un adulto.
Ahora bien, si centramos nuestra atención en los aspectos psicosociales, podemos ver que de cualquier punto de vista el tratamiento es un reto, aún más cuando los factores que influyen en el dolor quirúrgico deben ser atendidos tempranamente y eficazmente para evitar el dolor crónico, el cual es una complicación que afecta directamente la calidad de vida del paciente.
En cuanto al impacto en salud pública que tiene este tema, podemos concluir que sin duda se generan costos a corto y a largo plazo en temas de salud, lo cual podría ser gestionado de mejor manera si se tuvieran mayores fuentes de evidencia y algoritmos terapéuticos para esta población.
-
Conclusión
El trauma térmico genera un gran impacto fisiológico derivado de múltiples complicaciones que pueden terminar en falla multiorgánica y en algunos casos la muerte del paciente. Algunos de los principales retos en el manejo perioperatorio del paciente pediátrico quemado, que es sometido a múltiples intervenciones quirúrgicas es lograr la disminución de la ansiedad y el dolor mediante medidas farmacológicas y no farmacológicas. En el abordaje de la vía aérea, va depender de la distorsión de la anatomía dado por quemadura extrínseca e intrínseca de la misma, mientras los accesos vasculares pueden estar afectados de acuerdo a la extensión de la quemadura. Finalmente, el manejo anestésico va a modificarse teniendo en cuenta, principalmente, los cambios fisiológicos generados de acuerdo a la fase de la quemadura.
Con esta revisión, concluimos que hace falta mayor cantidad de estudios en este grupo de pacientes que permitan emitir recomendaciones sólidas basadas en mayores grados de evidencia.
Referencias
1. Jordan KC, Di Gennaro JL, von Saint André-von Arnim A, Stewart BT. Global trends in pediatric burn injuries and care capacity from the World Health Organization Global Burn Registry [Internet]. Frontiers in pediatrics. U.S. National Library of Medicine; 2022 [cited 2022Nov11]. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9343701/
2. Aldana M, Castellanos L, Osorio L, Navarrete N. Las quemaduras en la población pediátrica colombiana: del desconocimiento hacia la prevención. 2022.
3. Castellano J, Santamaría N, Patiño C, Hernandez A, Popo C. Georreferenciación de las quemaduras en Bogotá, Colombia. 2019 https://www.ciplastica.com/ojs/index.php/rccp/article/view/116.
4. Aldana MC, Navarrete N. Epidemiology of a decade of pediatric fatal burns in Colombia, South America [Internet]. Burns: journal of the International Society for Burn Injuries. U.S. National Library of Medicine; 2015 [cited 2022Nov10]. Available from: https://pubmed.ncbi.nlm.nih.gov/26059049/
5. Ferro, A. Ospino, C. Conceptos Actuales en Quemaduras: Un Manual Basado en la Evidencia. 2019
6. Lang TC, Zhao R, Kim A, Wijewardena A, Vandervord J, Xue M, et al. A Critical Update of the Assessment and Acute Management of Patients with Severe Burns. Adv Wound Care (New Rochelle). 2019 Dec;8(12):607–33. https://doi.org/10.1089/wound.2019.0963 PMID:31827977
7. Castellanos-Bueno R. La respuesta inmunitaria. Revista Colombiana De Endocrinología, Diabetes & Amp. Metabolismo. 2020;7 2S:55–61. https://doi.org/10.53853/encr.7.2S.584.
8. Valero González N. Valor de los biomarcadores en el diagnóstico diferencial entre síndrome de respuesta inflamatoria sistémica y sepsis en el paciente gran quemado. Universidad Autónoma de Madrid. 2017. oai:repositorio.uam.es:10486/680155
9. Ross, Michael H., y Wojciech Pawlina. Histología: Texto Y Atlas Color Con Biología Celular Y Molecular. 6a. ed https://user-biackli.cld.bz/Ross-Histologia-Texto-y-Atlas/18/
10. Chavarría Z. Caracterización de los pacientes pediátricos quemados ingresados en el hospital Dr. Fernando Vélez Paiz Enero 2018 a Diciembre 2020 (Doctoral dissertation, Universidad Nacional Autónoma de Nicaragua, Managua). 2021
11. Pino RM. Manual de Procedimientos de Anestesia Clínica Del Massachusetts General Hospital. Philadelphia: Wolters Kluwer; 2017.
12. Jeschke M. Baar, M. Choudhry, M. Chung, K. Gibran, N. Logsetty, S. Burn Injury. Nature Reviews; 2020. https://doi.org/10.1038/s41572-020-0145-5.
13. Tzika AA, Mintzopoulos D, Mindrinos M, Zhang J, Rahme LG, Tompkins RG. El análisis de microarrays sugiere que la lesión por quemadura da como resultado una disfunción mitocondrial en el músculo esquelético humano [Crossref, Medline]. Int J Mol Med. 2009;24:387–92. PMID:19639232
14. Fuzaylov G. Fidkowski C. Anesthetic considerations for major burn injury in pediatric patients. 2009. Pediatric Anesthesia 2009 19: 202–211. https://doi.org/10.1111/j.1460-9592.2009.02924.x.
15. Arbuthnot MK, Garcia AV. Early resuscitation and management of severe pediatric burns. Semin Pediatr Surg. 2019 Feb;28(1):73–8. https://doi.org/10.1053/j.sempedsurg.2019.01.013 PMID:30824139
16. BRIAN J. ANDERSON, JERROLD LERMAN, AND CHARLES J. COTÉ. Pharmacokinetics and Pharmacology of Drugs Used in Children
17. ERIK S. SHANK, CHARLES J. COTÉ, AND J.A. JEEVENDRA MARTYN. Burn Injuries
18. Moreno, P. Gaviria, G. Paciente Quemado: Conceptos Básicos en la Práctica Anestésica
19. Preston D, Ambardekar A. The Pediatric Burn: Current Trends and Future Directions. Anesthesiol Clin. 2020 Sep;38(3):517–30. https://doi.org/10.1016/j.anclin.2020.05.003 PMID:32792181
20. Suman A, Owen J. Update on the management of burns in paediatrics. BJA Educ. 2020 Mar;20(3):103–10. https://doi.org/10.1016/j.bjae.2019.12.002 PMID:33456937
21. Advanced Burn life support course, UPDATE 2018 ABA
22. McGovern C, Puxty K, Paton L. Major Burns: part 2. Anaesthesia, intensive care and pain management. 2022
23. Bittner EA, Shank E, Woodson L, Martyn JA. Acute and perioperative care of the burn-injured patient. Anesthesiology. 2015 Feb;122(2):448–64. https://doi.org/10.1097/ALN.0000000000000559 PMID:25485468
24. Gill P, Falder S. Early management of paediatric burn injuries. 2017 https://doi.org/10.1016/j.paed.2017.03.011.
25. Togo H, Lopes E. Preoperative fasting reduction in burned patients: A systematic review. Burns Open. 2020;4(4):176–82. https://doi.org/10.1016/j.burnso.2020.06.004.
26. Winckworth S, Allorto NL, Clarke DL, Aldous C. Perioperative fasting i36n burn patients: are we doing it right? [Internet]. S Afr J Surg. 2015 Jul;53(2):65–6. [cited 2022 Jun 15] Available from: http://www.scielo.org.za/scielo.php?script=sci_arttext&pid=S0038-23612015000200011&lng=en https://doi.org/10.7196/sajsnew.7743.
27. Morgan Johnson, Rajan K. Thakkar, Sheila Giles, Teresa Capello, Renata Fabia. Safety and efficacy of uninterrupted perioperative enteral feeding in pediatric burn patients Folasade Imeokparia.
28. Rousseau AF, Losser MR, Ichai C, Berger MM. ESPEN endorsed recommendations: nutritional therapy in major burns. Clin Nutr. 2013 Aug;32(4):497–502. https://doi.org/10.1016/j.clnu.2013.02.012 PMID:23582468
29. Krishna SG, Bryant JF, Tobias JD. Management of the Difficult Airway in the Pediatric Patient. J Pediatr Intensive Care. 2018 Sep;7(3):115–25. https://doi.org/10.1055/s-0038-1624576 PMID:31073483
30. Sofia J, Ambardekar A. Pediatric burn resuscitation, management, and recovery for the pediatric anesthesiologist. Curr Opin Anaesthesiol. 2020 Jun;33(3):360–7. https://doi.org/10.1097/ACO.0000000000000859 PMID:32371635
31. Strobel AM, Fey R. Emergency Care of Pediatric Burns. Emerg Med Clin North Am. 2018 May;36(2):441–58. https://doi.org/10.1016/j.emc.2017.12.011 PMID:29622333
32. Pizano LR, Davies J, Corallo JP, Cantwell PG. Critical care and monitoring of the pediatric burn patient. J Craniofac Surg. 2008 Jul;19(4):929–32. https://doi.org/10.1097/SCS.0b013e318175f3cd PMID:18650714
33. Romanowski and Palmieri. Burns & Trauma. Pediatric burn resuscitation: past, present, and future, (2017) 5:26 DOI https://doi.org/10.1186/s41038-017-0091-y.
34. Müller Dittrich MH, Brunow de Carvalho W, Lopes Lavado E. Evaluation of the “early” use of albumin in children with extensive burns. Pediatr Crit Care Med. 2016 Jun;17(6):e280–6. https://doi.org/10.1097/PCC.0000000000000728 PMID:27077832
35. Thomas JM, Bester K. Pediatric burns anesthesia: the things that make a difference. Southern African Journal of Anesthesia and Analgesia. 2014;20(5):190–6. https://doi.org/10.1080/22201181.2014.979630.
36. Blanchet B, Jullien V, Vinsonneau C, Tod M. Influence of burns on pharmacokinetics and pharmacodynamics of drugs used in the care of burn patients. Clin Pharmacokinet. 2008;47(10):635–54. https://doi.org/10.2165/00003088-200847100-00002 PMID:18783295
37. Kashav R, Kohli J, Magoon R. TIVA versus Inhalational Agents for Pediatric Cardiac Intensive Care. Journal of Cardiac Critical Care TSS. 2021;5(02):134–41. https://doi.org/10.1055/s-0041-1732834.
38. Chinchilla, P. A., & Moyano, J. (2021). Efficacy of opioids and non-opioid analgesics in the treatment of post procedure pain of burned patients: a narrative review. Brazilian journal of anesthesiology (Elsevier), S0104-0014(21)00303-1. Advance online publication. https://doi.org/10.1016/j.bjane.2021.07.022.
39. Wittenmeier E, Katharina A, Schmidtmann I, Griemert EV, Kriege M, König T, et al. Intraoperative transfusion practice in burned children in a university hospital over four years: a retrospective analysis. BMC Anesthesiol. 2021 Apr;21(1):118. https://doi.org/10.1186/s12871-021-01336-3 PMID:33858338
40. Palmieri TL. Children are not little adults: blood transfusion in children with burn injury. Burns Trauma. 2017 Aug;5:24. https://doi.org/10.1186/s41038-017-0090-z PMID:28815186
41. Fagin A, Palmieri TL. Considerations for pediatric burn sedation and analgesia. Burns Trauma. 2017 Oct;5:28. https://doi.org/10.1186/s41038-017-0094-8 PMID:29051890

 ORCID
ORCID