https://doi.org/10.25237/congreso-2022-21 | PDF
Wilbaldo Salas Morales (1), Rodrigo López Barreda (1), Esteban Del Rio Otto (2), César Godoy (3), Ady Giordano (4), Victor Contreras Ibacache (5), Natalia Calderón
(5), Esteban Godoy Zumaeta (6), Luis Ignacio Cortinez (7)
-
Anestesiología Cardiovascular. Pontificia Universidad Católica de Chile
-
Residente Anestesiología Cardiovascular. Pontificia Universidad Católica de Chile
-
E.U. Perfusionista Clínico Pontificia Universidad Católica de Chile
-
Bioquímica Pontificia Universidad Católica de Chile
-
E.U. Anestesiología Pontificia Universidad Católica de Chile
-
Alumno Medicina. Pontificia Universidad Católica de Chile
-
Anestesiología. Pontificia Universidad Católica de Chile
Introducción
La metadona tiene características que la hacen atractiva para el tratamiento del dolor postoperatorio tras la cirugía cardíaca. Sin embargo, a pesar de ser un fármaco relativamente antiguo, su uso en este escenario es relativamente reciente y los escasos trabajos publicados reportan resultados positivos en términos de analgesia postoperatoria(1-3). Se sabe que la instauración del bypass cardiopulmonar (CPB) implica cambios profundos que pueden alterar la farmacocinética y la respuesta clínica a los fármacos(4-11). Hasta la fecha, no existen estudios farmacocinéticos de metadona en pacientes sometidos a cirugía cardíaca con CPB.
Objetivo General
Describir la farmacocinética (PK) de una dosis intravenosa en bolo de metadona en pacientes adultos sometidos a cirugía cardíaca con CPB.
Material y Métodos
El estudio se registró en clinicaltrials.gov NCT05075265. Tras obtener la aprobación del Comité de Ética Clínica (ID 200323005) y el consentimiento informado del paciente, se estudiaron prospectivamente 18 pacientes de entre 45 y 75 años programados para cirugía cardíaca con CPB. Se administró una dosis única en bolo de 0,2 mg/kg de metadona al final de la inducción anestésica. Se tomaron muestras de sangre arterial (n=10) durante 24 h de cada paciente: 3 muestras en el período pre-CPB, 3 muestras durante el período CPB y 4 muestras durante el período post-CPB. El análisis de la concentración plasmática de metadona se realizó mediante un método espectrofluorométrico de cromatografía líquida de alto rendimiento (HPLC). El análisis farmacocinético poblacional se realizó con el programa NONMEM (NONMEM 7.4, ICON Development Solutions, USA). Se utilizaron modelos unicompartimentales y bicompartimentales para describir el perfil temporal de las concentraciones plasmáticas de metadona. Una disminución de la función objetivo de NONMEM de 6,63 para un parámetro adicional del modelo se consideró una mejora significativa del ajuste del modelo al nivel P < 0,01. (distribución Chi2).
Resultados
Los 18 pacientes completaron el estudio. El perfil temporal de las concentraciones de metadona en plasma se muestra en la figura 1. Un modelo estructural de dos compartimentos produjo un mejor ajuste de los datos que un modelo de un compartimento. (Disminución del OFV de 297 puntos, p<0,01) La influencia del CPB en la farmacocinética de la metadona se describió mejor mediante un incremento del aclaramiento de eliminación durante el CPB. La incorporación de este nuevo parámetro mejoró en gran medida el ajuste del modelo con una disminución del OFV de 43 puntos. (P<0.01). Las estimaciones finales de los parámetros poblacionales y sus coeficientes de variación (CV%) se muestran en la tabla 1.
Conclusiones y/o Implicaciones
El uso del CPB altera la farmacocinética de la metadona. Estos cambios se caracterizaron adecuadamente por un aumento del aclaramiento de eliminación durante el CPB utilizando un modelo de 2 compartimentos con eliminación lineal. El impacto clínico de los cambios observados durante la CPB en la farmacocinética de la metadona es probablemente insignificante con el esquema de dosificación actual.
Figura 1
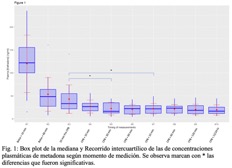
Tabla 1