María Mora-Aznaro1,*
Recibido: 01-09-2022
Aceptado: 11-09-2022
©2022 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 51 Núm. 6 pp. 757-759|https://doi.org/10.25237/revchilanestv5106101126
PDF|ePub|RIS
Case report: Massive obstetric hemorrhage
Abstract
Obstetric bleeding is a frequent complication within the Gynecology and Obstetrics Services, but it is somewhat more anecdotal in the Intensive Care Units, however, it must be considered for its approach as a possible etiological diagnosis of hypovolemic shock and for quick handling. Its cause can be of hemostatic or organic origin, and its anticipation allows different support-therapeutic measures to be taken (both conservative and surgical). In the reviewed case, there is the particularity of presentation of a critical hemorrhage in a parturient, difficult to control, and whose origin is due to two complications that occur successively: first, secondary to uterine atony, with treatment failure initial conservative and need for final surgical treatment. And secondly, the origin of the bleeding is located in an arterial injury secondary to the previous urgent puerperal hysterectomy. In any of its presentations, it is essential to establish a Service protocol, as well as multidisciplinar/ work for its optimal approach.
Resumen
El sangrado obstétrico se trata de una complicación frecuente dentro de los Servicios de Ginecología y Obstetricia, pero es algo más anecdótico en las Unidades de Cuidados Intensivos, no obstante, se ha de tener en cuenta para su planteamiento como posible diagnóstico etiológico de un shock hipovolémico y para su rápido manejo. Su causa puede ser de origen hemostático u orgánico, y su anticipación permite tomar distintas medidas de soporte-terapéuticas (tanto conservadoras como quirúrgicas). En el caso revisado se da la particularidad de presentación de una hemorragia crítica en una parturienta, de difícil control, y cuyo origen se debe a dos complicaciones que se presentan de forma sucesiva: en primer lugar, secundaria a una atonía uterina, con fracaso del tratamiento conservador inicial y necesidad de tratamiento quirúrgico final. Y en segundo lugar, el origen del sangrado se localiza en una lesión arterial secundaria a la histerectomía puerperal urgente previa. En cualquiera de sus presentaciones, es fundamental el establecimiento de un protocolo de servicio, así como un trabajo multidisciplinar para su abordaje óptimo.
-
Introducción
Presentación de un caso de una gestante con hemorragia obstétrica primaria masiva difícil control, sin respuesta a la aplicación de medidas conservadoras, con requerimiento de tratamiento quirúrgico urgente con histerectomía total y doble salpinguectomía. Persistencia del sangrado, con revisión quirúrgica posterior y necesidad de abordaje por cirugía vascular para realización de arteriografía con embolización selectiva por complicación quirúrgica secundaria.
-
Material y Métodos
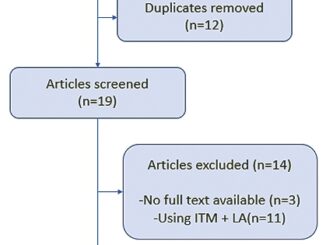
Estudio descriptivo-retrospectivo de historia clínica de paciente sangrante con seguimiento en distintos escenarios: des
de paritorio, quirófano, unidad de cuidados intensivos (UCI) y traslado. Revisión de bibliografía disponible.
-
Resultados
Se presenta el caso de una gestante de 37 años, secundípara, gestación actual en seguimiento por su ginecóloga, sin complicaciones.
Ingresa en nuestro Centro Hospitalario a término para parto vaginal. Inducción del parto con correcta progresión, y finalización del mismo mediante instrumentación vía vaginal en sala de paritorio. Tras alumbramiento inicio de sangrado abundante, se revisa canal del parto y resto de estructuras sin hallazgo de punto sangrante, se instauran medidas conservadoras que resultan ineficaces (20 U oxitocina intravenosa + 1.000 mg mi- soprostol rectal + 0,25 mg metilergometrina intramuscular + 0,5 mg carboprost intramuscular, e implantación posterior de balón de Bakri® ante persistencia de hemorragia posparto); sangrado continuo con inestabilidad hemodinámica, disminución del nivel de conciencia y situación de shock hipovolémico, por lo que se avisa a anestesia y somete a intervención quirúrgica urgente.
En quirófano se objetiva atonía uterina, realizando histerec- tomía total con doble salpinguectomía. Durante intervención la paciente se mantiene con coagulopatía con anemia, por lo que se inician transfusión masiva de hemoderivados y tratamiento hemostático con aparente control del débito hemático.
A su ingreso en UCI en posoperatorio inmediato, empeoramiento de inestabilidad hemodinámica con hipotensión y taquicardia, acidosis metabólica láctica y de coagulopatía. Por lo que se mantiene conectada a ventilación mecánica invasiva, sedoa- nalgesiada y se realiza resucitación inicial con fluidoterapia intensiva guiada por monitorización invasiva con catéter PICCO® venoso femoral, manteniendo durante las primeras horas de ingreso un índice cardíaco inferior a 2 l/min/m2. De acuerdo con hallazgos se inicia noradrenalina hasta 1 mcg/kg/min y dobu- tamina hasta 5 mcg/kg/min, prosiguiendo con administración de fármacos hemostáticos con ácido tranexámico y factor VII recombinante activado.
Ante falta de respuesta se reinterviene en quirófano para laparotomía exploradora urgente, revisando hemostasia y evidenciando leve sangrado a nivel de cúpula vaginal, reforzando y dando puntos hemostáticos a este nivel.
En su reingreso en UCI, estabilización progresiva tras administración de 6 concentrados de hematíes, 4 bolsas de plasma y dos de plaquetas, con posibilidad de suspensión de dobuta- mina a las 24 h de ingreso en la Unidad y descenso de noradre- nalina hasta 0,3 mcg/kg/min a las 48 h con último control de hemoglobina en 7,9 g/dl. A las 8 h de este control, distensión brusca de abdomen sin débito sanguíneo por drenajes quirúrgicos, por lo que se realiza nueva analítica donde se objetiva caída brusca de hemoglobina a 5,1 g/dl, se realiza ecografía abdominal urgente: gran cantidad de líquido libre. Por lo que, se hace control TC abdominal: hemoperitoneo de distribución difusa, colecciones hemorrágicas pélvicas con extensión hasta región perianal siguiendo vasos iliacos derechos y fuga del medio de contraste por extravasado sanguíneo a nivel de la unión de arteria iliaca común-externa-interna difundiéndose el mismo hacia las colecciones hemorrágicas pélvicas descritas.
Dados hallazgos se intensifica tratamiento con fluidotera- pia, vasopresores, transfusiones y fármacos coagulantes-hemostáticos y se comenta caso para radiología vascular intervencionista.
Traslado a centro de referencia donde se realiza arteriogra- fía selectiva de arteria iliaca común-externa sin visualización de fuga, evidenciando sangrado a nivel de arteria hipogástri- ca izquierda, con embolización de su rama distal. Control de hemorragia, con buena evolución posterior en UCI. Paciente estabilizada a las 24 h tras embolización.
Siendo dada de alta de UCI al mes de su ingreso, sin incidencias en seguimientos posteriores.
-
Discusión
El motivo de revisión y análisis de este caso es porque se presentan dos sangrados consecutivos con distintas etiologías, que de forma prospectiva impresionaban de ser una única hemorragia posparto masiva no controlada. Por un lado, encontramos una hemorragia obstétrica mayor-grave inmediata al alumbramiento y secundaria a la atonía uterina[1], donde se establecen una serie de medidas conservadoras iniciales para aumentar las contracciones musculares (como la ergometrina, la oxitocina y las prostaglandinas), un tratamiento no farmacológico ante el fracaso de las medidas anteriores (balón intrauterino y suturas de estructuras), y dada la situación de shock se decide finalmente intervención quirúrgica con histerectomía[2]. Una vez controlado este primer sangrado, a las 48 h del parto se manifiesta de nuevo una hemorragia grave posquirúrgica con hemoperitoneo secundario a lesión de arteria hipogástrica izquierda en contexto de histerectomía puerperal urgente[3]. Para el anestesista supone un desafío puesto que implica el manejo de una situación de shock hipovolémico ante la incertidumbre de la etiología que desencadena e cuadro. Un manejo en distintos escenarios como son el quirófano y la UCI.
El sangrado obstétrico masivo se presenta en 5%-15% de todos los partos. A pesar de las precauciones establecidas en distintos protocolos obstétricos, el sangrado con riesgo para la vida se observa en hasta 7 por cada mil partos y la hemorragia es responsable de hasta un tercio de las muertes maternas, siendo la primera causa de muerte materna en el mundo y la tercera en países desarrollados[4]. El sangrado crítico puede aparecer en cualquier momento durante la gestación, siendo más frecuente y grave aquél que ocurre intraparto o inmediatamente posparto como ocurre en nuestro caso. Se define como una pérdida estimada mayor a 500 ml para un parto vaginal o mayor a 1.000 ml para una cesárea; no obstante, el deterioro hemodinámico suele aparecer más tardíamente[5],[6]. Las causas de sangrado obstétrico pueden ser orgánicas o hemostáticas. Las primeras se explican por la falta de tono uterino después del parto, el trauma al útero o al canal de parto o la retención uterina de tejidos o coágulos. Requieren de una solución primariamente obstétrica conservadora o quirúrgica según la respuesta[7].
El sangrado de causa hemostática se debe ya sea a la incapacidad para formar cantidades adecuadas de trombina (por ejemplo, en la coagulopatía dilucional que sigue a la resucitación del sangrado masivo) o bien a la formación de trombina endovascular seguida de la activación de la coagulación y el consumo, por ejemplo, en caso de coagulación intravascular diseminada (CID)[8]. Idealmente, los factores de riesgo para sangrado deben identificarse anteparto, utilizando todos los métodos de imagen disponibles así como un enfoque multidisciplinar. Recursos como la ecografía permiten el diagnóstico prenatal de una placentación anómala[9]. La anticipación del sangrado permite tomar distintas medidas de soporte quirúrgicas, transfusionales y aún la colocación preventiva de un catéter-balón, en las arterias uterinas. Sin embargo, en hasta el 60% de las pacientes que requirieron una histerectomía por sangrado incohercible, el sangrado no fue previsto[10].
Cualquier sangrado de causa orgánica, localizado y suficientemente prolongado, desembocará en un sangrado difuso, de causa hemostática, debido al agotamiento de factores por consumo o a la dilución por la transfusión masiva o al desarrollo de una CID por hipoperfusión tisular, shock persistente, acido- sis e hipotermia. En estas condiciones, el soporte transfusional sostenido ya no bastará para detener el sangrado ni logrará mejorar los controles analíticos y la cirugía usualmente fracasará, apareciendo un sangrado difuso dentro del campo operatorio, de ahí la importancia de estabilización inicial urgente y control de las causas desencadenantes[11].
El tratamiento inicial del sangrado obstétrico masivo ha consistido en restablecer el tono uterino, reemplazar la pérdida de volumen intravascular y de sangre y reestablecer la hemostasia, reparando toda causa orgánica de sangrado y diagnosticando y tratando una coagulación alterada[12].
La cirugía incluye la reparación del tracto genital, la remoción de restos retenidos y el empleo de diferentes medios físicos para detener el sangrado del lecho placentario. La terapéutica debe instituirse lo antes posible recordando que el sangrado sostenido lleva a una coagulopatía muy difícil de revertir. Ante el fracaso del tratamiento conservador, las alternativas terapéuticas incluyen la ligadura arterial, las suturas compresivas, la embolización selectiva y aún la histerectomía[13].
En ocasiones, y a pesar de haberse adoptado todas las provisiones ya enunciadas, el sangrado se vuelve pertinaz o no se logra la estabilidad hemodinámica. En este punto se debe realizar revisión quirúrgica, y como en nuestro caso por la situación clínica y la ausencia de cirugía vascular en nuestro Hospital ya se había realizado la histerectomía con anexectomía, se derivó a Centro de referencia para realización de arteriografía para estudio y tratamiento de la causa[14],[15].
Finalmente, la falta de un protocolo institucional y la poca comunicación entre especialistas coadyuvan para que, en la atención de estas emergencias complejas, pocas veces participen los médicos más experimentados o un equipo mutidiscipli- nar de obstetra-hematólogo-anestesista[16].
Agradecimientos: Agradecimientos al Servicio de Ginecología del Hospital Santa Bárbara de Soria, por su ayuda en la elaboración de este caso.
Referencias
1. Guasch E, Gilsanz F. Hemorragia masiva obstétrica. Protocolos asistenciales en anestesia y analgesia obstétrica. Madrid: SEDAR; 2013.
2. Butwick AJ, Goodnough LT. Transfusion and coagulation management in major obstetric hemorrhage. Curr Opin Anaesthesiol. 2015 Jun;28(3):275–84. https://doi.org/10.1097/ACO.0000000000000180 PMID:25812005
3. Howard TF, Grobman WA. The relationship between timing of postpartum hemorrhage interventions and adverse outcomes. Am J Obstet Gynecol. 2015 Aug;213(2):239.e1–3. https://doi.org/10.1016/j.ajog.2015.04.017 PMID:25912302
4. Combs CA, Laros RK Jr. Prolonged third stage of labor: morbidity and risk factors. Obstet Gynecol. 1991 Jun;77(6):863–7. PMID:2030858
5. Rojas J, Cogollo M, Miranda J, Ramos E, Fernández JC, Bello A. Morbilidad materna extrema en cuidados intensivos obstétricos. Cartagena (Colombia) 2006– 2008. Rev Colomb Obstet Ginecol. 2011;62(2):131–40. https://doi.org/10.18597/rcog.223 .
6. Lalonde A; International Federation of Gynecology and Obstetrics. Prevention and treatment of postpartum hemorrhage in low-resource settings. Int J Gynaecol Obstet. 2012 May;117(2):108–18. https://doi.org/10.1016/j.ijgo.2012.03.001 PMID:22502595
7. Sentilhes L, Gromez A, Razzouk K, Resch B, Verspyck E. Mar- peau L. B-Lynch suture for massive persistent postpartum hemorrhage following stepwise uterine devascularisation. Acta Obstet Gynecol Scand. 2009;88:489–90.
8. Kozek-Langenecker SA, Afshari A, Albaladejo P, Aldecoa-Santullano CA, De robertis E, Filipescu DC, et al. Management of severe perioperative bleeding: Guidelines from the European Society of Anaesthesiology. Eur J Anaesthesiol. 2013;30:270—382.
9. Rath WH. Postpartum hemorrhage—update on problems of definitions and diagnosis. Acta Obstet Gynecol Scand. 2011 May;90(5):421–8. https://doi.org/10.1111/j.1600-0412.2011.01107.x PMID:21332452
10. El-Hamamy E, B-Lynch C. A worldwide review of the uses of the uterine compression suture techniques as alternative to hysterectomy in the management of severe post-partum haemorrhage. J Obstet Gynaecol. 2005 Feb;25(2):143–9. https://doi.org/10.1080/01443610500040752 PMID:15814393
11. Llau JV, Acosta FJ, Escolar G, Fernández-Mondéjar E, Guasch E, Marco P, et al. Multidisciplinary consensus document on the management of massive haemorrhage (HEMOMAS document). Med Intensiva. 2015;39:483—504.
12. Leal-Noval SR, Muñoz M, Asuero M, Contreras E, García-Erce JA, Llau JV. Documento Sevilla de Consenso sobre Alternativas a la Transfusión de Sangre Alogénica. Actualización del Documento Sevilla. Rev Esp Anestesiol Reanim. 2013;60:263e1-25.
13. Chelli D, Boudaya F, Dimassi K, Gharbi B, Najjar I, Sfar E, et al. [Hypogastric artery ligation for post-partum hemorrhage]. J Gynecol Obstet Biol Reprod (Paris). 2010 Feb;39(1):43–9. https://doi.org/10.1016/j.jgyn.2009.10.002 PMID:19962252
14. Evans S, McShane P. The efficacy of internal iliac artery ligation in obstetric hemorrhage. Surg Gynecol Obstet. 1985 Mar;160(3):250–3. https://doi.org/10.1097/00006254-198511000-00008 PMID:3871975
15. Unal O, Kars B, Buyukbayrak EE, Karsidag AY, Turan C. The effectiveness of bilateral hypogastric artery ligation for obstetric hemorrhage in three different underlying conditions and its impact on future fertility. J Matern Fetal Neonatal Med. 2011 Oct;24(10):1273–6. https://doi.org/10.3109/14767058.2011.574751 PMID:21557692
16. Gallos G, Redai I, Smiley RM. The role of the anesthesiologist in management of obstetric hemorrhage. Semin Perinatol. 2009 Apr;33(2):116–23. https://doi.org/10.1053/j.semperi.2008.12.005 PMID:19324241

 ORCID
ORCID