José Benito Parra-Maldonado1,*, Pía Carolina Gallardo-Astorga1, Alberto Gómez-González1, Miguel Fernández-Chavez2, Santiago Nicolás Saavedra3
Recibido: 13-06-2022
Aceptado: 03-07-2022
©2023 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 52 Núm. 2 pp. 165-169|https://doi.org/10.25237/revchilanestv5221121445
PDF|ePub|RIS
From mechanical ventilation to decannulation
Abstract
The patient with tracheostomy could has a functional progression as soon as possible if the clinical stability allow the intervention in the critical ill patient. It is important to remove the mechanical ventilation quickly and safety. Every day is needed to make evaluation and interventions for progress thinking in a tracheostomy protocol decannulation.
Resumen
El paciente con traqueostomía puede ser progresado de manera funcional desde el primer día que se realice dicho procedimiento siempre y cuando la estabilidad del paciente lo permita. Es necesario realizar evaluaciones e intervenciones con el objetivo de desvincular de la ventilación mecánica lo antes posible y poder comenzar con el protocolo de decanulación de manera personalizada y segura para evitar el fracaso de la misma.
-
Introducción
La realización de traqueostomía ha tomado un rol importante en los pacientes mecanicamente ventilados en la Unidad de Cuidados Intensivos (UCI), ya que podría disminuir los días de ventilación mecánica (VM), así como los días de estancia hospitalaria permitiendo mejores resultados en la funcionalidad del paciente, esto se debe a la mayor accesibilidad que existe a la rehabilitación en estos pacientes.
Existen diferentes criterios para considerar la realización de una traqueostomía como la necesidad de ventilación mecánica invasiva prolongada, fracaso a la extubación por mal manejo de secreciones, protección de la vía aérea, entre otros. Ante la necesidad de la realización de traqueostomía, existen dos tec- nicas para llevarla a cabo, la quirúrgica y la percutánea, que, al compararlas estadísticamente, no se ha encontrado diferencia una de la otra en los beneficios para el paciente crítico (PC)[1].
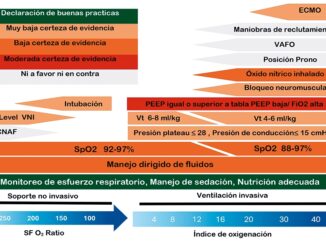
En el contexto del PC, se cuestiona la definición de una traqueostomía “precoz”, así como el momento oportuno para realizarla ya que, en la UCI, la diversidad de enfermedades (neurológicas, cardíacas, respiratorias, quirúrgicas etc.) que se abordan, dificultan realizar un protocolo homogéneo para decidir el momento “óptimo” de traqueostomizar, por ello, se trata de personalizar cada situación y contexto clínico del paciente (Tabla 1) con el objetivo de obtener mejores resultados[2],[3]. Es importante recalcar que no se ha encontrado disminución de la mortalidad entre una traqueostomía temprana y tardía.
Tabla 1. Traqueostomía temprana y tardía
| Tipo de paciente | Traqueostomia temprana (días) | Traqueostomia tardía (días) |
| Trauma | Antes del día 8 de VM | Después de 28 días de VM |
| Neurológico | Antes del día 3 de VM | 7 a 14 días de VM |
| Quirúrgico | Antes del día 3 de VM | 15 días de VM |
| Neumología (COVID-19) | Antes del día 14 de VM | Después del día 14 de VM |
| Poscirugía cardíaca | Antes del día 5 posoperatorio | Después del día 15 de VM |
Una vez traqueostomizado y resuelta la causa por la cual el paciente requirió VM, se comenzará con el proceso de desvinculación de la asistencia respiratoria siempre y cuando cumpla con los principales criterios para el retiro comenzando con un Índice de Respiraciones rápidas superficiales (RBSI) < 105 resp/L/min[4], tolerancia a la prueba de ventilación espontánea sin repercutir en lo hemodinámico y/o respiratorio, presión ins- piratoria máxima (Pimax) de -20 a -30 cmH2O, engrosamiento diafragmático de más del 30%[5] y un pico flujo tosido por más de 60-70 L/min. Si el paciente no tolera la desvinculación por debilidad de musculatura respiratoria, es importante encaminar la rehabilitación en el weaning[6]. Posterior a la desvinculación de la VM, comienza una serie de cuidados y puntos a seguir con el objetivo de cumplir ciertos requisitos para retirar la cánula de traqueostomía, a este acto se le llamará, decanulación. La decisión de decanular, será por el equipo multidisciplinario en la UCI conformado por médico tratante, fonoaudiólogo, kine- siólogo, nutriólogo y enfermería[7]. Es fundamental mencionar, que no existen guías o recomendaciones de expertos con pasos a seguir para la retirada de cánula de traqueostomía, esto dependerá de protocolos de cada equipo de trabajo y terapia intensiva[8].
Es importante que para llegar al punto de la decanulación el paciente necesita realizar un entrenamiento previo de todas aquellas estructuras que estuvieron en desuso, como es la vía aérea superior y con esto estimular las funciones perdidas como son la voz, deglución, tos y manejo de secreciones[9]. Este en- trenamieto puede comenzar desde el día que se realiza la tra- queostomía, si el paciente y su situación clínica lo permiten. Inicialmente se puede comenzar con trabajo a fuga, el cual se realiza cuando el paciente se encuentra bajo asistencia respiratoria mecánica, este trabajo consiste en el desinflado de balón de neumotaponamiento paulatino, con el objetivo de que la columna de aire fluya hacia vía aérea superior y permita estimular estas estructuras permitiendo la fonación, deglución y el manejo de secreciones, aunque el paciente aún se encuentre bajo ventilación mecánica[10]. Es fundamental que previo al desinflado del globo de neumotaponamiento se realice higiene oral exahustiva y aspiración de secreciones orofaríngeas y traqueales para mantener una vía aérea permeable, así mismo, el paciente debe estar en una modalidad espontánea en la VM.
Paulatinamente, se comenzará hacer la desvinculación de la ventilación mecánica y posteriormente, se debe comenzar el trabajo de reeducar la respiración por vía aérea superior con la oclusión digital intermitente, válvulas de fonación y/o occlusion completa de la traqueostomía[10]. Para saber que dispositivo tolerará el paciente es necesario realizar medición de presión traqueal para determinar si la vía aérea superior es permeable y si tolerará algún dispositivo de los previamente mencionados.
La medición de presión traqueal se debe realizar cuando el paciente ya se encuentra desvinculado de la ventilación mecánica, para esto los primeros pasos deben ser la aspiración de secreciones tanto orofaríngeas como traqueales, luego se debe desinflar el balón de neumotaponamiento en su totalidad. Y finalmente colocaremos en la traqueostomía un conector “L” en donde se conectará el manometro en el puerto del conec- tor y el dispositivo seleccionado u oclusión en el otro extremo. Algunos autores sugieren realizar esta medición con válvula de fonación y otros con oclusión completa, independiente del dispositivo utilizado, los resultados no varían ya que se mide la presión en la fase espiratoria (Figura 1). Es importante recalcar que la válvula de fonación presenta menor resistencia al flujo aéreo y es mejor tolerada por los pacientes en primera instancia y posiblemente esta evaluación sea mejor tolerada con este dispositivo.
Para obtener un resutado se debe mantener la válvula u oclusión durante un minuto y en el manometro se mostrarán presiones negativas durante la inspiración y positivas durante la espiración. El paciente no debe hablar ni toser para que no aumenten la presiones en la vía aérea en la fase espiratoria. Los resultados demuestran que una presión mayor a 10 cmH2O se sugiere reducir el diámetro de la cánula de traqueostomía, ya que posiblemente este ocupando la totalidad de la luz traqueal y/o evaluar vía aérea mediante endoscopía para determinar si existe alguna alteración orgánica que este provocando obstrucción en la vía aérea. Una presión entre 5 – 10 cmH2O sugiere utilización de válvula de fonación por lapsos breves de tiempo con fines de entrenamiento de vía aéra superior y también sugiere revisar el diámetro de la cánula de traqueostomía. Y finalmente, un resultado menor a 5 cmH2O el paciente tolerará la ultilización de válvula de fonación e incluso oclusión completa de cánula de traqueostomía, lo cual se sugiere realizar de manera paulatina hasta alcanzar los tiempos necesarios para la decanulación[11].
Con estos resultados ya se podrá definir el dispositivo que tolerará el paciente para comenzar el protocolo de decanulación, para el cual debe cumplir ciertos criterios como son: resuelta la causa que lo llevo a la traqueostomía, sin necesidad de VM en las últimas 48 h, integridad neurológica que será definida con la escala coma de Glasgow > 12 puntos, estabilidad hemodinámica, integridad y funcionalidad de vía aérea superior e inferior, manejo adecuado de secreciones, reflejo deglutorio y tusigeno presentes y eficientes, tolerar oclusión de cánula > 24 h, entre otros[7],[12],[13].
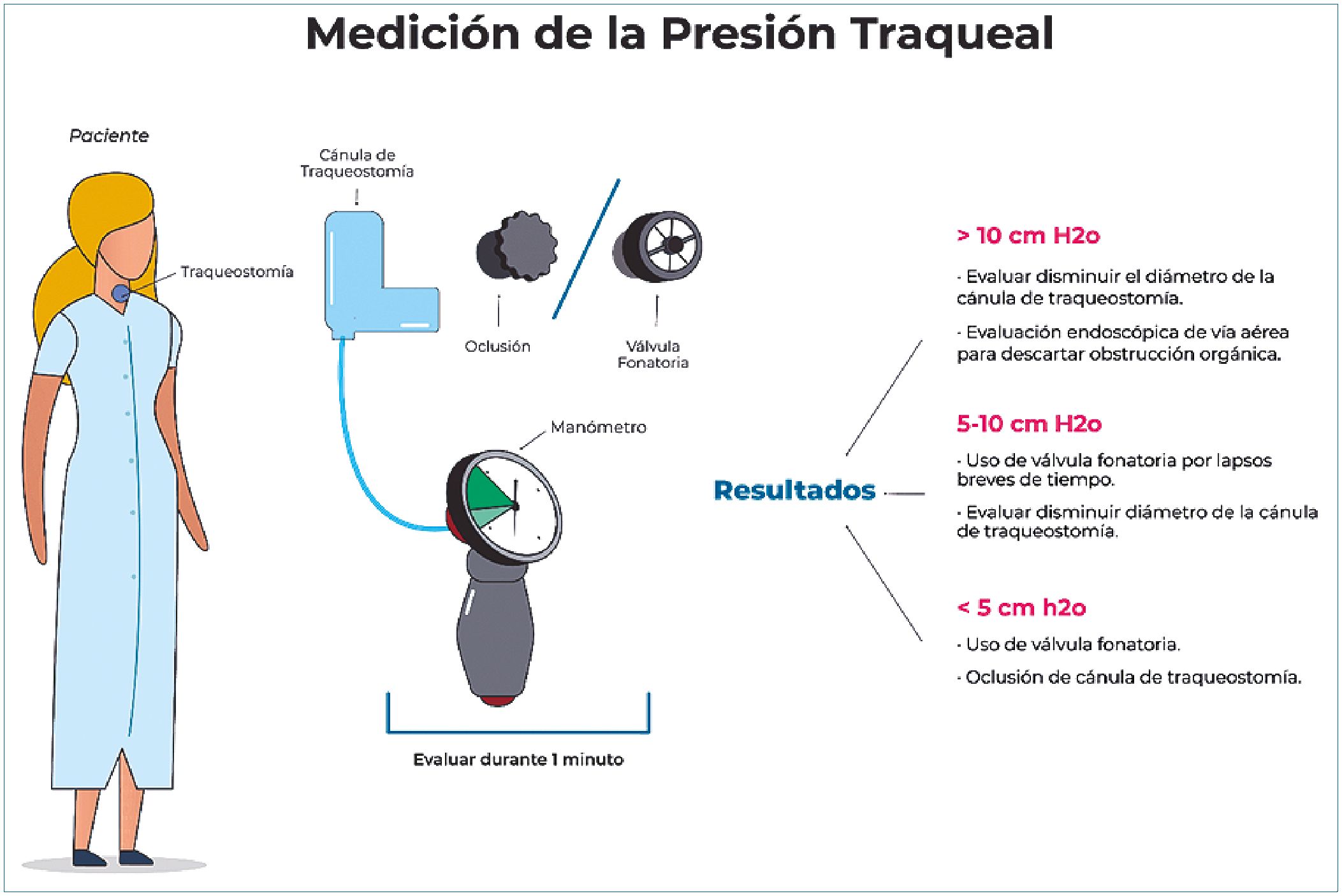
Figura 1. Medición de la presión traqueal.
Otro punto importante a valorar en el paciente traquosto- mizado es la deglución, esta evaluación es bastante subestimada en la UCI[14] y es de gran importancia para un adecuado resultado en la decanulación. Para evaluar esta función existen pruebas clínicas y pruebas instrumentales, siendo estas últimas el gold estándar para la evaluación de la deglución[15]. La evaluación clínica utilizada en estos pacientes es el blue dye test, la cual tiene dos modalidades de realización, si el objetivo es valorar el manejo de secreciones orofaríngeas se debe realizar tinción de la cavidad oral del paciente con colorante vegetal de color azul y esperar el manejo deglutorio de su saliva durante 24 h. En cambio si el objetivo es valorar el manejo de diferentes consistencias, se debe realizar tinción de los alimentos con colorante vegetal azul[7]. Se recomienda que esta prueba (secreciones y/o alimentos) se realice con globo de neumotaponamiento desinflado y con la utilización de algún dispositivo como válvula de fonación u oclusión de cánula para favorecer el proceso de deglución y permitir una adecuada coordinación respiración- deglución, por este motivo es fundamental el entrenamiento de las estructuras de vía aérea superior y utilización de dispositivos mencionados previo a la evaluación de deglución. Una vez realizada la prueba se deben aspirar secreciones traqueales y observar la coloración de estas, si hay presencia de colorante en las secreciones aspiradas y/o pericánula, la prueba es considerada positiva y refiere que el paciente esta presentando aspiración traqueal del contenido orofaríngeo, en cambio si en las secreciones y/o pericánula no se evidencia colorante, la prueba se considera negativa y refiere que el paciente pudiera presentar una deglución segura. Al ser una prueba clínica, puede presentar falsos negativos[16]. Por este motivo, se recomienda hacer evaluaciones instrumentales para la valoración de la deglución, en estos pacientes la elegida es la evaluación fibroscópica de la deglución por sus siglas en inglés FEES, la cual permite visualizar la anatomía, funcionalidad laríngea, manejo de secreciones, sensibilidad y función deglutoria. Es importante mencionar que el paciente debe presentar un adecuado manejo de secreciones para la decanulación[7], y aunque exista alteración de la deglución con alguna consistencia pero el paciente presenta un adecuado manejo de secreciones, podría ser decanulado.
Una vez que el paciente cumple con estos requisitos se podría pensar en la decanulación (Figura 2) y se debe realizar un monitoreo intrahospitalario en las próximas 24 – 48 h pues es el tiempo que se tiene para considerar una decanulación exitosa[17].
La determinación para el fracaso de la decanulación del paciente con traqueostomía es importante para el desenlace y pronóstico a corto y largo plazo. Aquellos pacientes que fracasan a dicho precedimiento y deben ser recanulados, la mortalidad incrementa hasta 30%. Por ello es necesario la consideración de diferentes aspectos tales como los factores de riesgo que son la edad, género, en particular el masculino, antecedentes respiratorios previos, sepsis, problemas neurológicos, obstrucciones de la vía aérea superior o neumonía, protocolo inadecuado de decanulación y uso prolongado de cánula[8]. Este último se asocia a mayor fracaso, debido a que puede generar estenosis traqueal, traqueomalasias, granulomas, fistulas e infecciones. Además, se deben considerar predictores de éxito de decanulación, de lo contrario aumenta el riesgo de recanular al paciente. Dentro de esos predictores son la oclusión total mínimo por 24 h, sin presentar dificultad respiratoria, adecuado manejo de secreciones por vía aérea superior, FEES y pruebas de cultivos de esputo previos a la decanulacion (Figura 2).
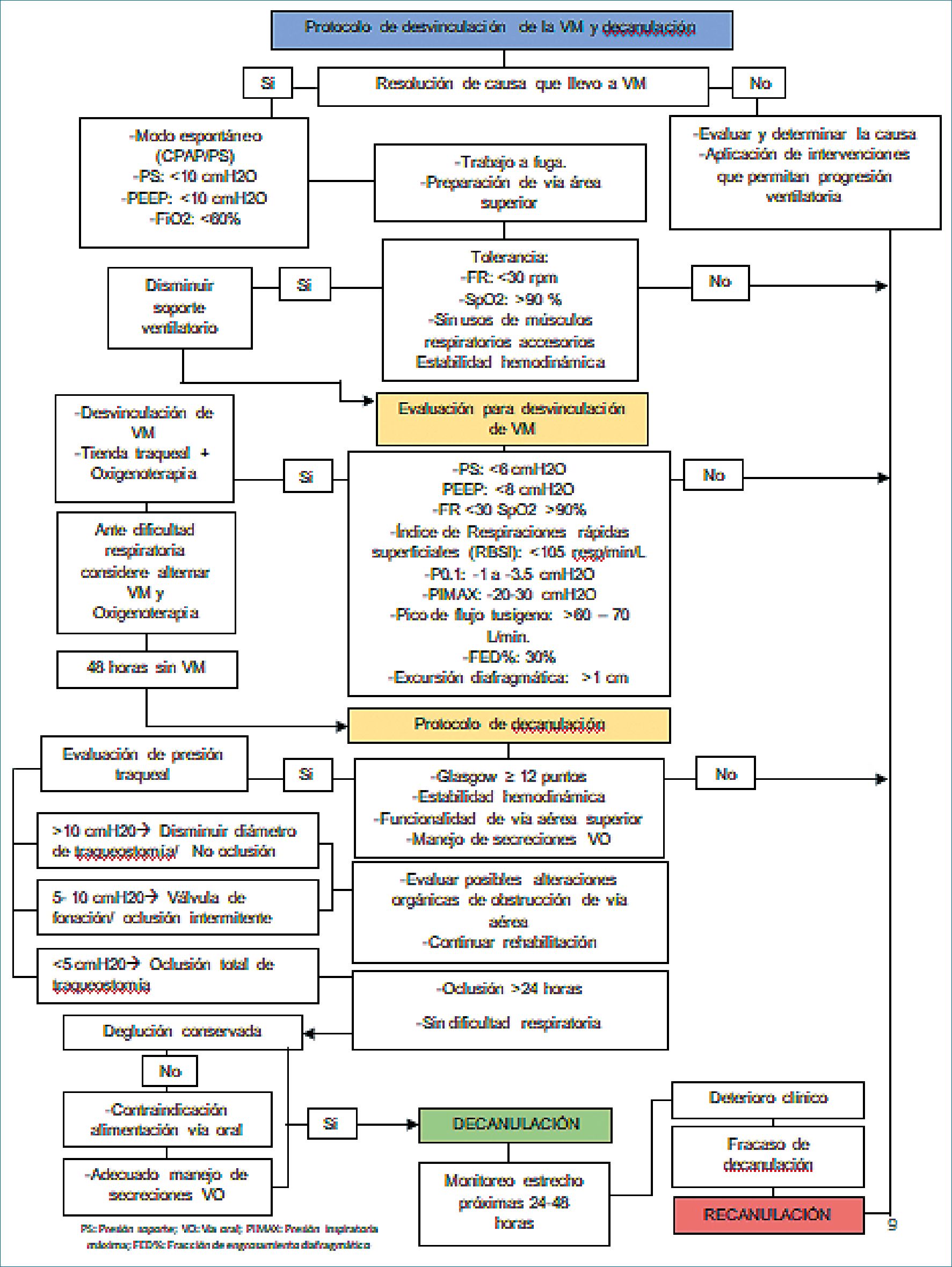
Figura 2. Algoritmo de desvinculación de ventilación mecánica y decanulación.
-
Conclusión
Es importante recalcar que no existe unificación de criterios para la decanulación, por este motivo es fundamental crear protocolos de decanulación de cada institución tomando en cuenta a la población que atiende y en lo posible evaluar diferentes aspectos antes de la decanulación con el objetivo de reducir el fracaso a la decanulación.
Referencias
1. Adly A, Youssef TA, El-Begermy MM, Younis HM. Timing of tracheostomy in patients with prolonged endotracheal intubation: a systematic review. Eur Arch Otorhinolaryngol. 2018 Mar;275(3):679–90. https://doi.org/10.1007/s00405-017-4838-7 PMID:29255970
2. Raimondi N, Vial MR, Calleja J, Quintero A, Cortés Alban A, Celis E, et al. Guías basadas en la evidencia para el uso de traqueostomía en el paciente crítico. Med Intensiva. 2017 Mar;41(2):94–115. https://doi.org/10.1016/j.medin.2016.12.001 PMID:28188061
3. Ferro A, Kotecha S, Auzinger G, Yeung E, Fan K. Systematic review and meta-analysis of tracheostomy outcomes in COVID-19 patients. Br J Oral Maxillofac Surg. 2021 Nov;59(9):1013–23. https://doi.org/10.1016/j.bjoms.2021.05.011 PMID:34294476
4. Palacios EM, De J, Cruz López L, Sigfrido H, Flavio R, Mendoza M. Medigraphic.com. [citado el 6 de abril de 2022]. Disponible en: https://www.medigraphic.com/pdfs/medcri/ti-2007/ti074f.pdf
5. Haaksma, ME, Smit, JM, Boussuges, A. et al. Consenso de expertos sobre ultrasonografía de diafragma en pacientes críticos (EXODUS): una declaración de consenso de Delphi sobre la medición de los parámetros derivados de la ecografía del diafragma en un entorno de cuidados intensivos. Cuidado crítico 26, 99 (2022). https://doi.org/10.1186/s13054-022-03975-5 .
6. Hernández-López GD, Cerón-Juárez R, Escobar-Ortiz D, et al. Weaning from mechanical ventilation. Med Crit. 2017;31(4):238–45.
7. Villalba D, Lebus J, Quijano A, Bezzi M, Plotnikow G. RETIRADA DE LA CÁNULA DE TRAQUEOSTOMÍA. REVISIÓN BIBLIOGRÁFICA. Rev Arg de Ter Int. [Internet]. 20 de marzo de 2014 [citado 6 de abril de 2022];31(1). Disponible en: //revista.sati.org.ar/index.php/MI/article/view/365
8. Saavedra-Mendoza AG, Akaki-Caballero M. Puntos esenciales en el protocolo de decanulación traqueal. Otorrinolaringología. 2014;59(4):254–61.
9. Fernández-Carmona A, Peñas-Maldonado L, Yuste-Osorio E, Díaz-Redondo A. Exploración y abordaje de disfagia secundaria a vía aérea artificial. Med Intensiva [Internet]. 2012;36(6):423–33. Disponible en: https://doi.org/10.1016/j.medin.2011.09.006 .
10. Hess DR. Facilitating speech in the patient with a tracheostomy. Respir Care. 2005 Apr;50(4):519–25. PMID:15807915
11. Johnson DC, Campbell SL, Rabkin JD. Tracheostomy tube manometry: evaluation of speaking valves, capping and need for downsizing. Clin Respir J [Internet]. 2009;3(1):8–14. Disponible en: https://doi.org/10.1111/j.1752-699X.2008.00100.x .
12. Medeiros GC de, Sassi FC, Lirani-Silva C, Andrade CRF de. Critérios para decanulação da traqueostomia: revisão de literatura. CoDAS [Internet]. 2019;31(6). https://10.1590/2317-1782/20192018228 PMID: 31800881.
13. Christopher KL. Tracheostomy decannulation. Respir Care. 2005 Apr;50(4):538–41. PMID:15807918
14. Parra MJ, Martínez CM, Gallardo AP, Boy SM. Disfagia en el paciente crítico. ¿Un problema ignorado? Acta Med Grupo Ángeles. 2021;19(4):566–7. https://doi.org/10.35366/102550 .
15. Arteaga J. Patricia, Olavarria L Christian, Naranjo D Benjamin, Elgueta L Francisca, Espinóla M Daniella. Cómo realizar una evaluación de deglución completa, eficaz y en corto tiempo. Rev. Otorrinolaringol. Cir. Cabeza Cuello [Internet]. 2006 Abr [citado 2022 Mayo 31]; 66 (1) : 13-22. Disponible en: http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0718-48162006000100003&lng=es . https://doi.org/10.4067/S0718-48162006000100003 .
16. Béchet S, Hill F, Gilheaney Ó, Walshe M. Diagnostic Accuracy of the Modified Evan’s Blue Dye Test in Detecting Aspiration in Patients with Tracheostomy: A Systematic Review of the Evidence. Dysphagia. 2016 Dec;31(6):721–9. https://doi.org/10.1007/s00455-016-9737-3 PMID:27530728
17. Stelfox HT, Hess DR, Schmidt UH. A North American survey of respiratory therapist and physician tracheostomy decannulation practices. Respir Care. 2009 Dec;54(12):1658–64. PMID:19961631

 ORCID
ORCID