Daniel Rivera Tocancipá1,2, César D. Galindo3, Valentina Gutiérrez Perdomo4*
Recibido: 09-11-2022
Aceptado: 20-12-2022
©2023 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 52 Núm. 4 pp. 419-421|https://doi.org/10.25237/revchilanestv52n04-16
PDF|ePub|RIS
Spinal anesthesia in a preterm infant
Abstract
Spinal anesthesia is generally used in pediatrics for postoperative analgesia; however, its use as an anesthetic technique in neonates, especially with high risk of complications (prematurity, pulmonary pathologies, among others) has been increasing exponentially in the last decade in order to avoid the risks generated by general anesthetics and airway manipulation. We present a case of a patient born at 30 weeks, with hyaline membrane disease, and subsequently, he must be taken for a rectal biopsy due to clinical suspicion of Hirschsprung’s disease, applying spinal anesthesia as an anesthetic technique, without complications.
Resumen
La anestesia espinal en general es utilizada en pediatría para analgesia posoperatoria; sin embargo, su uso como técnica anestésica en neonatos, especialmente con alto riesgo de complicaciones (prematuridad, patologías pulmonares, entre otros) ha ido aumentando de forma exponencial en la última década con el fin de evitar los riesgos generados por los anestésicos generales y la manipulación de la vía aérea. Se presenta un caso de un paciente nacido a las 30 semanas, y con enfermedad de membranas hialinas, y posteriormente, debe ser llevado a toma de biopsia rectal por sospecha clínica de enfermedad de Hirschsprung, aplicando anestesia espinal como técnica anestésica, sin complicaciones.
-
Introducción
En términos generales, los neonatos representan el grupo con mayor morbilidad durante el manejo anestésico, bien sea por dificultad en el manejo de la vía aérea, apnea posanestésica, y/o por falta de experiencia en este grupo poblacional[1].
Si bien la anestesia neuroaxial en pediatría se ha usado desde el año 1900[2]; existe un auge de la anestesia espinal en la última década, debido a los potenciales beneficios reportados, especialmente en pacientes con factores de riesgo para complicaciones asociadas, tales como: prematuridad, uso de oxígeno, síndrome de dificultad respiratoria aguda, y/o vía aérea difícil[3]. Actualmente, se ha implementado la anestesia espinal en los recién nacidos para un gran número de procedimiento quirúrgicos: herniorrafia inguinal, cirugía abdominal, biopsias rectales, cirugía ortopédica, entre otros[1].
Presentamos un caso de recién nacido pretérmino de 30 semanas, que cursó con enfermedad de membrana hialina, y posteriormente fue llevado a toma de biopsias rectales para descartar enfermedad de Hirschsprung.
-
Descripción del caso
Neonato masculino nacido a las 30 semanas vía cesárea, hijo de primera gestación de madre de 35 años quien cursaba con preeclampsia severa, y con adecuado peso para la edad gestacional. Fue llevado a unidad neonatal bajo ventilación con presión positiva por tubo en T, y posteriormente, ventilación mecánica no invasiva a través de cánula nasal de alto flujo. Desarrolló enfermedad de enfermedad de membrana hialina, manejada con surfactante (#2 dosis), ecocardiograma sin hallazgos de cardiopatía, y tomografía de cráneo sin lesiones.
Antropometría al nacer: Peso: 1.238 g; talla: 38 cm; perímetro cefálico: 29 cm; perímetro torácico: 24 cm; perímetro abdominal: 25,5 cm.
Durante su estancia hospitalaria el paciente debuta con distensión abdominal y ausencia de deposiciones. Fue valorado por cirugía pediátrica, quienes realizan sospecha diagnóstica de enfermedad de Hirschsprung, y programan toma de biopsias rectales. Paraclínicos: tiempo de protrombina 13,1, tiempo parcial de tromboplastina 46,4, INR 1,22, hemoglobina 10,9 g/dl, y plaquetas 687.000. Valoración preanestésica sin otros hallazgos.
Tres días previos al procedimiento se retira oxígeno por cánula de alto flujo. El día del procedimiento, el paciente tenía edad cronológica de 32 días, y edad corregida de 34 semanas y 4 días; y un peso calculado el mismo día de 1.580 g. Se ingresa a salas de cirugía en compañía de neonatólogo y anestesiólogo, bajo monitoría no invasiva, calentador neonatal, cánula nasal de bajo flujo a 0,5 L/min, y acceso venoso periférico en dorso de pie izquierdo.
Se posicionó en decúbito lateral derecho, con paciente despierto y bajo monitoría no invasiva, se realizó asepsia y antisepsia de región lumbar. Se ubicó manualmente línea entre las crestas ilíacas, y el espacio intervertebral L4-L5 (Figura 1) Posteriormente, con aguja hipodérmica #25 (aguja espinal neonatal/ pediátrico en la institución de salud), se ingresó al espacio subdural; y se administró bupivacaína 0,5% hiperbárica a 1 mg/k de peso, mediante jeringa de insulina. Se posiciona el paciente en decúbito supino, y se continúa vigilancia hemodinámica, respiratoria y neurológica; continuando aporte de oxígeno durante todo el perioperatorio.
Durante el procedimiento, los signos vitales estuvieron estables; no se presentó llanto ni irritabilidad posterior al estímulo quirúrgico; y se finalizó la cirugía sin complicaciones y con sangrado mínimo. No se administró medicación para sedación, ni intervenciones en la vía aérea por parte del servicio de anestesiología. Paciente tranquilo y sonriente durante el procedimiento. El paciente fue trasladado nuevamente a unidad neonatal.
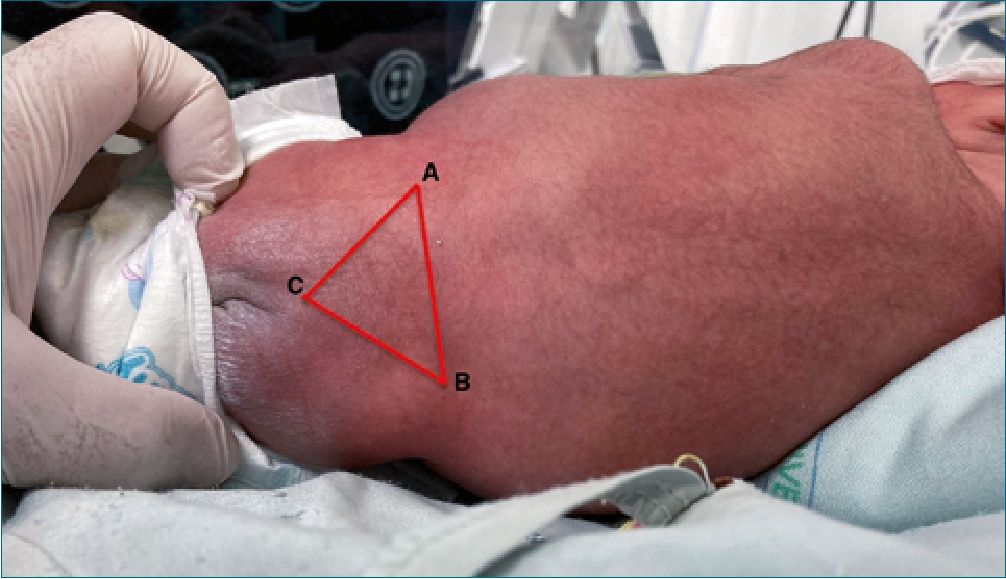
Figura 1. Ubicación de neonato en decúbito lateral derecho. Los puntos A y B corresponden a las apófisis ilíacas posterosuperiores (línea de Tuffier) y, punto C el hiato sacro, formando un triángulo equilátero. El punto de punción corresponde al punto C.
-
Discusión
La anestesia espinal es una alternativa segura y efectiva frente a la anestesia general para procedimientos quirúrgicos dolorosos en neonatos de alto riesgo anestésico (como prematuros, y antecedente compromiso pulmonar). Su aplicación clínica ha venido en aumento exponencial durante la última década, dado una disminución del consumo de opioides, evita el efecto nocivo de los anestésicos generales, y la manipulación invasiva de la vía aérea, la presentación de apnea posoperatoria, y tiene menores efectos sobre la estabilidad hemodinámica[4].
Un aspecto clave en la aplicación de anestesia espinal en neonatos es la estabilidad hemodinámica[5]. Fisiológicamente, los recién nacidos poseen un tono basal simpático disminuido, y un bajo volumen sanguíneo venoso en los miembros inferiores; por lo cual en raras ocasiones presentan hipotensión arterial asociada a bloqueo neuroaxial[6].
Si bien la anestesia espinal brinda una menor respuesta simpática y metabólica, y menor estrés global al trauma quirúrgico; también posee limitaciones: el primero es la dificultad en técnica (por lo cual se debe contar con el suficiente entrenamiento para realizar movimiento finos y precisos); dado los espacios milimétricos y las pequeñas estructuras. Para ello, se han diseñado fórmulas para medición de la longitud entre la piel y el espacio subaracnoideo, incluida la que utilizó en nuestro caso: (Peso (kg) + 10) * 0,8[1]-[7], y un espacio subaracnoideo entre 6 a 8 milímetros. Por ende, la elección de una aguja fina y corta, permite una mejor manipulación y realización de movimientos finos; se recomienda una aguja de Quincke de 25G en neonatos y una jeringa de 1 ml para la administración del medicamento, con el fin de otorgar mayor seguridad[8].
Otro tema, es el cálculo preciso de la dosis del anestésico local, para evitar toxicidad. En el uso de bupivacaína hiperbárica al 0,5% la dosis recomendada es 1 mg/kg[9]. En infantes menores de 6 meses de edad, dada la inmadurez del metabolismo y de la síntesis de alfa 1 glicoproteína ácida, se genera una mayor cantidad de fármaco libre, y mayor riesgo de intoxicación. Sin embargo; esta complicación tiene una baja tasa de presentación[10].
Finalmente, en los recién nacidos el tiempo de anestesia espinal es relativamente menor en comparación con los adultos, se estima que se encuentra entre 40 a 60 minutos[7]. Esto es debido a varios factores: 1. un mayor volumen de líquido espinal en relación con el peso; 2. mayor circulación del mismo; y 3. mayor vasculatura de la piamadre. Ello conduce a mayor distribución y absorción de anestésico local, y repercute en el tiempo de anestesia efectiva. En cuanto a la posición del paciente, la técnica en decúbito lateral es de elección (con flexión de cuello y articulación de las caderas), por lo que ofrece un mejor manejo de la vía aérea en caso de necesitarlo; aunque también se ha descrito la técnica en sedestación[8]. En nuestro paciente se definió por una técnica en decúbito lateral debido a una enfermedad pulmonar pulmonar de base que podría generar complicaciones de ventilación y/o oxigenación durante la inducción anestésica o realización de la punción lumbar.
La principal desventaja es el corto tiempo de duración anestésica, pese a ello, se ha descrito que podría ser el “estándar de oro” en técnica anestésica para procedimientos abdominales inferiores y de extremidades inferiores, con una estimación de tiempo quirúrgico menor a 90 minutos[8].
Es importante aclarar que posterior al bloqueo neuroaxial, los neonatos tienden a dormir sin uso de medicamentos sedantes. Este efecto se ha explicado por la desaferenciación al sistema de activación reticular, lo cual facilita la realización de las intervenciones quirúrgicas y menor estrés emocional para el paciente[11].
-
Conclusión
La anestesia espinal es una técnica que ha venido en un crecimiento exponencial de su aplicación clínica para realización de procedimientos quirúrgicos de corta duración, debido a que evita los riesgos hemodinámicos de la anestesia general y la manipulación activa e invasiva de la vía aérea, sin generar alteración emocional en el paciente y riesgos para la oxigenación (y consiguiente hipoxia con daño neurológico cerebral), y poca repercusión hemodinámica; especialmente, en pacientes de alto riesgo (como el caso de las patologías pulmonares). Siempre teniendo en cuenta los riesgos y la precisión técnica que implica, para lo cual se debe contar con la suficiente experticia y entrenamiento médico.
Consideraciones éticas: Se obtuvo consentimiento informado firmado por la madre del paciente para realización de técnica anestésica y toma de fotos con fines académicos e investigativos del área del dorso, con respeto de la identidad.
Fuente de financiamiento: Se declara que no existe patrocinio de ninguna entidad.
Declaración conflicto de interés: Los autores no tienen conflictos de interés para reportar, son independientes a instituciones financiadoras y de apoyo.
Referencias
1. Whitaker EE, Williams RK. Epidural and Spinal Anesthesia for Newborn Surgery. Clin Perinatol. 2019 Dec;46(4):731–43. https://doi.org/10.1016/j.clp.2019.08.007 PMID:31653305
2. Gray HT. A study of spinal anesthesia in children and infants: from a series of 200 cases. Lancet. 1909;174(4491):913–7. https://doi.org/10.1016/S0140-6736(01)61506-X.
3. Jones LJ, Craven PD, Lakkundi A, Foster JP, Badawi N. Regional (spinal, epidural, caudal) versus general anaesthesia in preterm infants undergoing inguinal herniorrhaphy in early infancy. Cochrane Database Syst Rev. 2015 Jun;2015(6):CD003669. https://doi.org/10.1002/14651858.CD003669.pub2 PMID:26058963
4. Ing C, Sun LS, Friend AF, Roh A, Lei S, Andrews H, et al. Adverse events and resource utilization after spinal and general anesthesia in infants undergoing pyloromyotomy. Reg Anesth Pain Med. 2016;41(4):532–7. https://doi.org/10.1097/AAP.0000000000000421 PMID:27281725
5. McCann ME, Withington DE, Arnup SJ, Davidson AJ, Disma N, Frawley G, et al.; GAS Consortium. Differences in blood pressure in infants after general anesthesia compared to awake regional anesthesia (GAS study-a prospective randomized trial). Anesth Analg. 2017 Sep;125(3):837–45. https://doi.org/10.1213/ANE.0000000000001870 PMID:28489641
6. Ing C, Sun LS, Friend AF, Kim M, Berman MF, Paganelli W, et al. Differences in intraoperative hemodynamics between spinal and general anesthesia in infants undergoing pyloromyotomy. Paediatr Anaesth. 2017 Jul;27(7):733–41. https://doi.org/10.1111/pan.13156 PMID:28419639
7. Johnson C, Gibson C. Regional Anesthesia for Infants and Children. In: Sims C, Weber D, Johnson C, editors. A Guide to Pediatric Anesthesia. Cham: Springer; 2020. https://doi.org/10.1007/978-3-030-19246-4_10.
8. Gupta A, Saha U. Spinal anesthesia in children: A review. J Anaesthesiol Clin Pharmacol. 2014 Jan;30(1):10–8. https://doi.org/10.4103/0970-9185.125687 PMID:24574586
9. Suresh S, Ecoffey C, Bosenberg A, et alThe European Society of Regional Anaesthesia and Pain Therapy/American Society of Regional Anesthesia and Pain Medicine Recommendations on Local Anesthetics and Adjuvants Dosage in Pediatric Regional AnesthesiaRegional Anesthesia &. Pain Med. 2018;43:211–6.
10. Walker BJ, Long JB, Sathyamoorthy M, Birstler J, Wolf C, Bosenberg AT, et al.; Pediatric Regional Anesthesia Network Investigators. Complications in pediatric regional anesthesia: an analysis of more than 100,000 blocks from the pediatric regional anesthesia Network. Anesthesiology. 2018 Oct;129(4):721–32. https://doi.org/10.1097/ALN.0000000000002372 PMID:30074928
11. Hermanns H, Stevens MF, Werdehausen R, Braun S, Lipfert P, Jetzek-Zader M. Sedation during spinal anaesthesia in infants. Br J Anaesth. 2006 Sep;97(3):380–4. https://doi.org/10.1093/bja/ael156 PMID:16816395

 ORCID
ORCID