Priscilla Ulloa1
Recibido: 2025-08-10
Aceptado: 2025-09-08
©2026 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 55 Núm. 2 |https://doi.org/10.25237/revchilanestv55n2-16
PDF
Anesthetic management of patients with Klippel-Trenaunay syndrome: A case report
Abstract
Klippel-Trenaunay syndrome (KTS) is a rare congenital disorder, corresponding to an angioosteohypertrophic syndrome characterized by venous malformations, capillary malformations, and hypertrophy of bones or soft tissues in the affected limbs, with or without lymphatic involvement. These patients present comorbidities such as coagulopathies, thrombosis, and chronic pain. Patients with KTS may require various surgical interventions, where perioperative management is challenging in terms of airway management, hemodynamic alterations, and an increased risk of bleeding and thrombosis in the perioperative period. Knowledge of this syndrome and its implications allows us to be prepared for possible perioperative complications, thus providing greater safety in the management of these patients. We present the case of a 38-year-old patient with KTS, who was electively admitted for total knee arthroplasty.
Resumen
El síndrome de Klippel Trenaunay (SKT) es un trastorno congénito infrecuente, corresponde a un síndrome angioosteohipertrófico, caracterizado por malformaciones venosas, malformaciones capilares, e hipertrofia de huesos o tejidos blandos en las extremidades afectadas, con o sin malformación linfática. Estos pacientes presentan comorbilidades tales como coagulopatías, trombosis y dolor crónico. Los pacientes con SKT pueden requerir diversas intervenciones quirúrgicas, donde el manejo perioperatorio es desafiante en cuanto al manejo de vía aérea, alteraciones hemodinámicas, y riesgo de sangrado y trombosis que está aumentado en el perioperatorio. Conocer este síndrome y sus implicancias nos permite estar preparados frente a las posibles complicaciones perioperatorias, pudiendo así otorgar una mayor calidad y seguridad en el manejo de estos pacientes. Se presenta el caso de una paciente de 38 años, portadora de SKT, que ingresó de forma electiva para una artroplastía total de rodilla.
Introducción
El síndrome de Klippel-Trenaunay (SKT) es infrecuente, con una incidencia de 1/27.500 nacidos vivos. Se caracteriza por la tríada de malformaciones venosas, malformaciones capilares e hipertrofia de huesos o tejidos blandos en extremidades afectadas, con o sin malformación linfática[1]-[4].
Los pacientes con SKT pueden requerir diversas intervenciones quirúrgicas, planteando desafíos anestésicos importantes debido al riesgo aumentado de sangrado, trombosis, dificultades en el control hemodinámico y de la vía aérea[4],[5]. La planificación anestésica cuidadosa y el manejo multidisciplinario son fundamentales para minimizar complicaciones y optimizar resultados.
En este contexto, presentamos el caso de una paciente con SKT sometida a artroplastia total de rodilla.
Descripción del caso
Mujer, 38 años, con gonartrosis severa, programada para prótesis total de rodilla izquierda. Sin alergias. Portadora del SKT, tuvo una trombosis venosa profunda (TVP) hace 16 años. Usa paracetamol, celecoxib, tramadol y pregabalina para manejo del dolor crónico por patología articular y vascular. Ha sido sometida a liberación del anillo del tercer aductor (5 años), liberación del anillo del sóleo (9 años), liberación de arteria y vena femoral con esclerosis de venas superficiales (15 años), y esclerosis del golfo venoso en la pierna (17 años), bajo anestesia general, sin incidentes, salvo requerimiento de transfusiones bien toleradas.
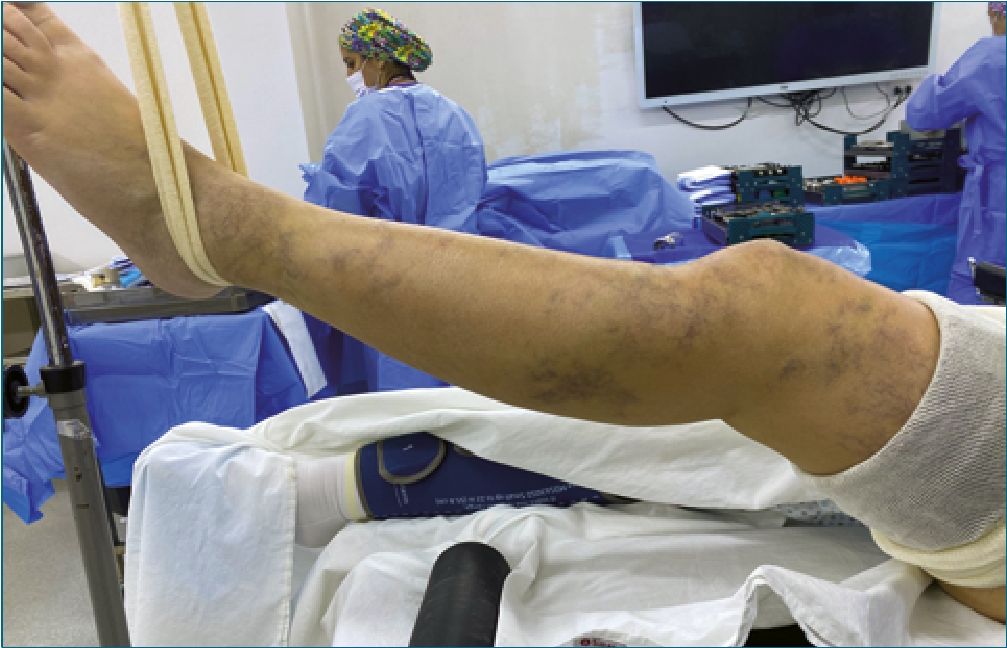
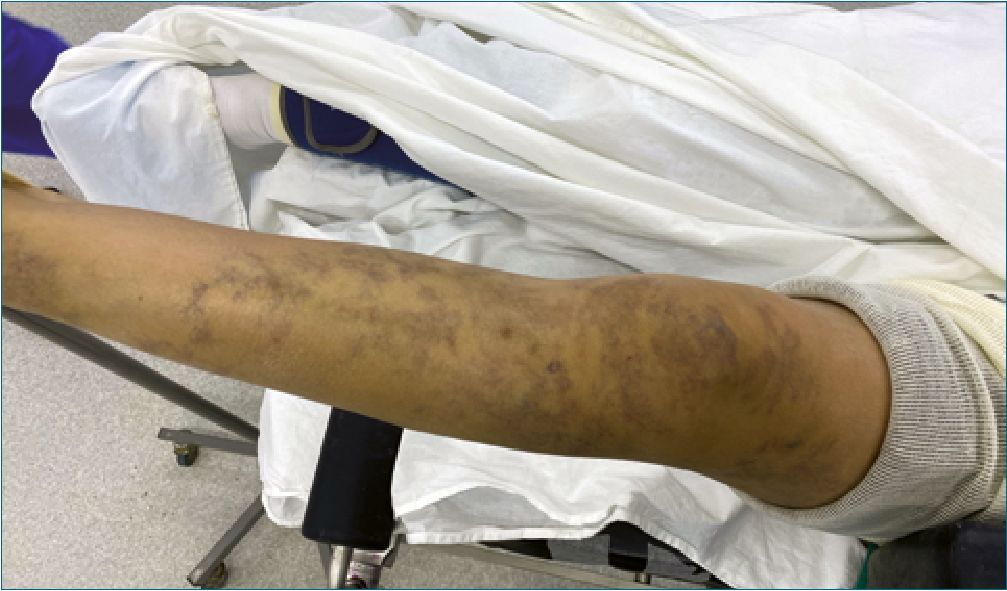
Al examen físico: índice de masa corporal de 26, sin predictores de vía aérea difícil (VAD), y abundantes telangiectasias, manchas vasculares y várices en la extremidad inferior izquierda (Figuras 1 y 2).
En sus exámenes preoperatorios presentó un hematocrito de 40%, hemoglobina 13,6 g/dL, plaquetas 238.000, PT 97%, TTPa 31 seg, INR 1,02, fibrinógeno 133 mg/dL y dímero D 12,77 ng/mL. Ecocardiograma normal. La resonancia magnética (RM) describió una gonartrosis tricompartimental y malformaciones arteriovenosas en celular subcutáneo. La angiotomografía computarizada informó: estructuras varicosas dependientes de vena safena, sin patología arterial. La ecografía doppler venosa detalló cambios postquirúrgicos/post flebíticos en la vena femoral, insuficiencia venosa y formación de várices, con importante cantidad en el aspecto anterior de la rodilla, muslo distal y pierna proximal.
La paciente fue clasificada como ASA II. Se reservó 6 unidades de glóbulos rojos y se solicitó cama en la unidad de tratamiento intermedio (UTI) para el posoperatorio. Se inició tromboprofilaxis con enoxaparina 40 mg/día subcutáneo, una semana previa a la intervención (Caprini 13 pts).
La paciente ingresó de forma ambulatoria, recibió 75 mg de pregabalina, se instaló dos vías venosas periféricas (18 G y 16 G) y medias antitrombóticas.
En pabellón se monitorizó con electrocardiograma continuo, pulsioximetría, presión arterial invasiva, monitor de bloqueo neuromuscular, índice biespectral (BIS), termómetro esofágico y diuresis mediante sonda Foley. Se mantuvo con un dispositivo de compresión neumática y calefactor de aire forzado.
Figura 1.
Figura 2.
Recibió anestesia total intravenosa con propofol al 1% (modelo Marsh) y remifentanilo (modelo Minto), titulando según BIS, y rocuronio 0,6 mg/kg. Se intubó mediante laringoscopía directa (Cormack 1) con un tubo endotraqueal N° 7.0, sin incidentes.
Durante el intraoperatorio se administró: 1 g de ácido tranexámico, 40 mg de omeprazol, metadona 0,1 mg/kg, ketamina 0,5 mg/kg, dexametasona 8 mg, ketorolaco 60 mg, paracetamol 1 g y metamizol 1 g, además de una infusión de nitroglicerina para mantener una presión arterial media (PAM) alrededor de 60 mmHg.
Durante la cirugía se mantuvo con isquemia a 280 mmHg a nivel del muslo. El sangrado quirúrgico fue de 300 cc aproximadamente. El equipo quirúrgico realizó una infiltración periarticular con bupivacaína 150 mg, morfina 8 mg, epinefrina 0,3 mg, ketorolaco 60 mg y depomedrol 40 mg, en un total de 100 cc que se distribuyó alrededor del sitio quirúrgico, además, se realizó un bloqueo del canal de los aductores con bupivacaína 50 mg y lidocaína 200 mg en un total de 20 cc tras finalizar la cirugía.
Tras 1 h y 3 min se detuvo la infusión de nitroglicerina y se liberó la isquemia, momento en que la paciente presentó una marcada y brusca hipotensión (PAM 40 mmHg) y taquicardia (hasta 110 lpm), se administró 100 mcg de fenilefrina y 1.000 cc de suero Ringer Lactato, logrando PAM alrededor de 60 mmHg.
Finalmente, la paciente fue extubada y trasladada a UTI para su posoperatorio, donde permaneció con medias antitrombóticas y compresión neumática. Se inició tromboprofilaxis con enoxaparina 40 mg/día sc a las 8 h posoperatorias.
La paciente fue trasladada a sala básica en su segundo día posoperatorio donde presentó dolor EVA 9-10/10 en la extremidad operada, el cual cedió con sus botas de compresión de uso habitual y vendas elásticas. Fue dada de alta en su tercer día posoperatorio.
Discusión
El SKT es una malformación congénita infrecuente, su severidad varía desde mínima hasta potencialmente mortal[1]. Lo más común es que afecte solo una extremidad inferior, pero podría involucrar ambas, además de las extremidades superiores, tórax y estructuras abdomino-pélvicas[1]. Su diagnóstico clínico se caracteriza por manchas vasculares cutáneas, malformaciones venosas, hipertrofia del tejido blando y/o del hueso de la extremidad afectada, pudiendo presentar anomalías linfáticas[5]. Presentan estructuras venosas avalvulares que originan várices tortuosas y dilatadas, además, puede existir aplasia o hipoplasia en el sistema venoso profundo, formación o dilatación de aneurismas, incompetencia valvular, y compresión por bandas fibróticas o vasculatura anómala[5]. La paciente del caso presentaba alteraciones sólo en la extremidad inferior izquierda, y no tenía afectación del sistema linfático, pudiendo considerarse un caso leve, sin embargo, nunca se buscó, dirigidamente, afectación de otras zonas.
Como exámenes complementarios, se recomienda realizar un ultrasonido y una RM. En cuanto al laboratorio, se debe realizar un hemograma, dímero D, fibrinógeno, tiempo de protrombina y tromboplastina parcial activada periódicamente para evaluar la presencia de coagulopatías[3],[5].
El manejo del SKT es multidisciplinario. Se prefieren las medidas conservadoras, centradas en la prevención y manejo de complicaciones, como terapia compresora y cuidados de las heridas, esto, porque los síntomas persisten o incluso empeoran hasta en el 90% de los pacientes tratados quirúrgicamente[7]. Dentro de los tratamientos farmacológicos, bajas dosis de aspirina logran una mejora del edema y dolor, sumado a los analgésicos para el dolor crónico. También, existen terapias dirigidas con sirolimus y alpelisib, que pueden estar indicados en pacientes con SKT sintomático o con notorio deterioro funcional[6]. En cuanto a las terapias quirúrgicas, las técnicas menos invasivas como terapia láser, ablación endovascular, radiofrecuencia o escleroterapia suelen ser superiores[1]. También, puede realizarse extirpación de venas, ligadura alta o flebectomía ambulatoria[7],[8]. La paciente era usuaria de vendas elásticas y botas de compresión en su domicilio, además de analgésicos. También, había sido sometida a la liberación de estructuras vasculares, lo que contribuyó a un mejor pronóstico, disminuyendo su riesgo quirúrgico.
Los pacientes con SKT pueden presentar diversas complicaciones. Destaca el riesgo de coagulopatía: coagulación intravascular localizada en las malformaciones venosas, mayor riesgo de tromboflebitis superficial, y riesgo de trombosis venosa profunda (TVP) y tromboembolismo pulmonar (TEP), incluso TEP crónico llevando a hipertensión pulmonar. El riesgo de sangrado está dado por la coagulación intravascular local que causa depleción de los factores de coagulación en el flujo distal, sin embargo, a menudo se asocia con coagulación intravascular diseminada y Síndrome de Kasabach-Merrit (coagulopatía de consumo y trombocitopenia)[2]. Pueden presentar desde episodios menores hasta casos severos de coagulación intravascular diseminada y sangrado mayor tras procedimientos invasivos. Este riesgo suele estar relacionado con la extensión de la enfermedad venosa, y se debe sospechar en pacientes con niveles elevados de Dímero D, bajo fibrinógeno, y, ocasionalmente, trombocitopenia[5],[8]. La paciente del caso tenía un dímero D elevado con bajo fibrinógeno.
En estos pacientes, el dolor crónico tiene una prevalencia de 88%. Su etiología es multifactorial (insuficiencia venosa crónica, tromboflebitis superficial, TVP, celulitis, afectación intraósea, artritis, contracturas por la afectación intraarticular y dolor neuropático)[5],[9]. Por esto, es primordial el manejo multimodal del dolor perioperatorio, considerar premedicar con gabapentinoides, usar técnicas de analgesia regional, además de analgésicos con diferentes mecanismos de acción.
El manejo anestésico de los pacientes con SKT es complejo y desafiante, además de las comorbilidades señaladas, se debe poner especial atención en el manejo de vía aérea, hemodinamia y riesgo de sangrado y trombosis que está aumentado en el perioperatorio[4]. En la evaluación preoperatoria se debe considerar la necesidad de evaluación por cardiología, dado las posibilidades de TEP y consiguiente hipertensión pulmonar y falla ventricular derecha. En el caso presentado, la paciente no poseía sintomatología cardíaca, además, contaba con ecocardiograma normal por lo que se desestimó esta evaluación.
En relación a las técnicas anestésicas, la presencia de hemangiomas y malformaciones arteriovenosas espinales, dilataciones venosas y tendencia a la coagulopatía, hacen de la anestesia neuroaxial una técnica poco segura por el riesgo de hematoma peridural. Sin embargo, su uso es seguro en ausencia de lesiones cutáneas sobre el sitio de punción y con imagen previa (TAC o RM) que demuestre la ausencia de malformaciones vasculares en el sistema nervioso central y estructuras circundantes[1],[2]. Al no contar con estas imágenes, se optó por la anestesia general.
Se ha descrito que debido a la hipertrofia de tejidos blandos y posible presencia de hemangiomas en la vía aérea se debería anticipar una VAD. Sin embargo, en los reportes de caso existentes no se ha descrito dificultad en el manejo de la vía aérea[1]-[4]. Así como tampoco hubo dificultad en nuestra paciente.
En el intraoperatorio, se debe considerar la monitorización invasiva de la presión arterial, sobre todo en situaciones en que se anticipe una pérdida sanguínea importante y consecuente inestabilidad hemodinámica. En este caso, el riesgo de alteraciones hemodinámicas estaba aumentado, por un lado, por las malformaciones vasculares concentradas en el sitio quirúrgico, y, por otro, los cambios hemodinámicos asociados al mango de isquemia se ven exacerbados por el mayor territorio vascular en la extremidad afectada, explicando la notoria hipotensión que se presentó tras liberar la isquemia. Además, es perentorio contar con la disponibilidad de drogas vasoactivas e insumos para reposición de volumen[3]. En este caso se utilizó nitroglicerina para una hipotensión permisiva durante la cirugía, disminuyendo el riesgo de sangrado intraoperatorio, además, se contaba con disponibilidad de efedrina, fenilefrina y noradrenalina.
En caso de requerir un catéter venoso central, se debe descartar la presencia de malformaciones vasculares en el sitio de inserción y la tromboflebitis de miembros inferiores, en cuyo caso se debe evitar canular la vena femoral[3].
En toda intervención quirúrgica en pacientes con SKT se debe considerar el potencial de hemorragia masiva intraoperatoria, aunque lo más común es que el sangrado sea mínimo, puede ser masivo en formas severas del síndrome[2]-[3]. También, se debe tener en cuenta que el sitio de sangrado puede involucrar no solo las extremidades, sino también otros órganos afectados, por esto deben evitarse las variaciones bruscas de hemodinamia que exacerban el riesgo[1],[4]. Es importante el uso de isquemia cuando sea posible, aunque este no elimina el riesgo de un sangrado significativo. En cuanto al uso de ácido tranexámico, este está recomendado como dosis profiláctica única en el intraoperatorio, estando contraindicado en el posoperatorio dado el riesgo aumentado de trombosis.
Otro punto a destacar es el riesgo ya mencionado de enfermedad tromboembólica, que es aún mayor en el contexto quirúrgico, este es especialmente elevado en pacientes con niveles elevados de dímero D, trombocitopenia e historia familiar o personal de trombosis, factores que estaban presentes en la paciente. Se recomienda iniciar, profilácticamente, heparina de bajo peso molecular 2 semanas previo a cualquier procedimiento invasivo, así como también en las 2 semanas posteriores[10]. En este caso, se inició profilaxis con clexane una semana previa a la intervención, manteniéndose posteriormente con anticoagulación. Además, se enfatizó el uso estricto de medias antitrombóticas desde preparación de paciente, y el uso de compresión neumática en pabellón y UTI.
En cuanto al posoperatorio, el nivel de monitorización debe ajustarse según el estado preoperatorio, la intervención y las complicaciones intraoperatorias[3]. En este caso, dado el riesgo de sangrado en relación al sitio quirúrgico, sumado a las alteraciones hemodinámicas posteriores a la liberación de la isquemia, se decidió monitorizar en UTI.
Conclusión
El conocimiento del SKT es fundamental para proporcionar una atención segura. La planificación meticulosa del manejo perioperatorio puede prevenir complicaciones potencialmente graves asociadas con las anomalías características del SKT. Los casos reportados son escasos y no existe un consenso sobre la estrategia anestésica óptima, por lo que el manejo debe individualizarse según cada paciente.
Referencias
1. Barbara DW, Wilson JL. Anesthesia for surgery related to Klippel-Trenaunay syndrome: a review of 136 anesthetics. Anesth Analg. 2011 Jul;113(1):98-102. https://doi.org/10.1213/ANE.0b013e31821a03c2 PMID:21467557
2. George SE, Sreevidya A, Asokan A, Mahadevan V. Klippel Trenaunay syndrome and the anaesthesiologist. Indian J Anaesth. 2014;58(6):775-7. https://doi.org/10.4103/0019-5049.147161 PMID:25624555
3. George SE, Lee MG, Hannawi S. Anaesthesia recommendations for patients suffering from Klippel-Trénaunay syndrome [Internet]. Ophananesthesia. 2017 [citado 2024]. Disponible en: https://www.orphananesthesia.eu/es/rare-diseases-2/recomenda-ciones-online/klippel-tr%C3%A9naunay-syndrome/307-klippel-tr%C3%A9naunay-syndrome/file.html
4. Dwivedi D, Sheshadri K, Tandon U, Chakraborty S. Klippel-Trenaunay syndrome: a rare entity with anesthesia concerns. J Clin Anesth. 2016 Dec;35:233-4. https://doi.org/10.1016/jjdina-ne.2016.09.004 PMID:27871531
5. Ilona J. Frieden, Derek H Chu. Klippel-Trenaunay syndrome: Clinical manifestations, diagnosis, and management [Internet]. uptodate. 2024. Disponible en: https://www.uptodate.com
6. DeMaio A, New C, Bergmann S. Medical treatment of vascular anomalies. Dermatol Clin [Internet]. 2022;40(4):461-71. Disponible en: https://doi.org/10.1016/j.det.2022.06.013
7. Glovkzki P, Driscoll DJ. Klippel-Trenaunay syndrome: Current management. Phlebology [Internet]. 2007;22(6):291-8. Disponible en: https://doi.org/10.1177/026835550702200611
8. Mazoyer E, Enjolras O, Bisdorff A, Perdu J, Wassef M, Drouet L. Coagulation disorders in patients with venous malformation of the limbs and trunk: a case series of 118 patients: A case series of 118 patients. Arch Dermatol [Internet]. 2008;144(7):861-7. Disponible en: https://doi.org/10.1001/archderm.144.7.861
9. Harvey JA, Nguyen H, Anderson KR, Schoch JJ, Bendel EC, Driscoll DJ, et al. Pain, psychiatric comorbidities, and psychosocial stressors associated with Klippel-Trenaunay syndrome. J Am Acad Dermatol [Internet]. 2018;79(5):899-903. Disponible en: https://doi.org/10.1016/j.jaad.2018.05.1245
10. John PR. Klippel-Trenaunay syndrome. Tech Vasc Interv Radiol [Internet]. 2019;22(4):100634. Disponible en: https://doi.org/10.1016/j.tvir.2019.100634

 ORCID
ORCID