Gustavo Galleguillos Coloma 1 ,2,*, Gianpaolo Cecioni P. 1 , Fabian Pereira P. 3 , Francisca Álvarez H. 1
Recibido: 05-03-2022
Aceptado: 12-06-2022
©2022 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 51 Núm. 5 pp. 510-520|https://doi.org/10.25237/revchilanestv5124061412
PDF|ePub|RIS
Cardiac risk assessment prior to noncardiac surgery
Abstract
The preoperative evaluation is a fundamental weapon for the anesthesiologist. Its objective is to identify conditions that modify the anesthetic plan and perioperative care, considering that cardiovascular pathologies are the greatest predictors of morbidity and mortality. Based on the guidelines described below, perioperative management should include preoperative risk stratification, functional capacity, type of surgery, cardiovascular risk factors and function. The use of complementary tests must be individualized since, apart from time and cost, they do not improve the postoperative prognosis if they are used indiscriminately. In this work, we will describe the key points for cardiological evaluation for non-cardiac surgery.
Resumen
La evaluación preanestésica es un arma fundamental para el anestesiologo. Su objetivo es identificar condiciones que modifiquen el plan anestésico y el cuidado perioperatorio, considerando que las patologías cardiovasculares son los mayores predictores de morbi y mortalidad. Basado en las guías más adelante descritas, el manejo perioperatorio debe incluir estratificación del riesgo preoperatorio, capacidad funcional, tipo de cirugía, función y factores de riesgo cardiovascular. El uso de exámenes complementarios debe ser individualizado ya que, aparte de tiempo y costo, no tiene mejoría en el pronóstico posoperatorio si son usados de forma indiscriminatoria. En este trabajo, describiremos los puntos claves para la evaluación cardiológica para cirugía no cardiaca.
-
Introducción
La evaluación preanestésica de pacientes con cardiopatías tiene por objetivo establecer la gravedad de la condición, el riesgo de descompensación y, de ser posible, optimización en su tratamiento.
La evaluación cardíaca perioperatoria puede influir en las medidas que se tomen para reducir el riesgo de complicaciones cardíacas o MACE (Mayor adverse cardiac events), pero no deberían tener influencia en la decisión de realizar la intervención. En algunos casos, el riesgo cardíaco puede influir en el tipo de operación y hacer recomendable una intervención menos invasiva o estratificar de mejor manera el riesgo de complicaciones cardíacas perioperatorias y la supervivencia a largo plazo.
La evaluación preoperatoria nos permite:
• Evaluar el riesgo de paciente.
• Optimizar la condición del paciente e identificar los factores
de riesgo que requieren manejo.
• Formular un plan perioperatorio con énfasis en reducción de los riesgos.
• Informar al paciente y sus familiares del proceso.
La forma de abordar esta evaluación es conocida y se efectúa siguiendo algoritmos desarrollados por grupos multidisciplinarios (AHA/ACC USA 2014 – ESC/ESA 2014 y CCS 2017).
En general, podemos resumir que estas guías proponen definir el tipo de cirugía en función de las complicaciones, la urgencia del procedimiento, la presencia de condiciones cardíacas activas (en forma de descompensación clínica) y la definición de factores de riesgo para la aparición de eventos o MACE (Major adverse cardiac events). Existen elementos propios de cada guía y conciliar todos ellos es difícil (Figura 1)[1].
Intervenciones basadas en evaluación preoperatoria[1]:
• Decisión proceder con la cirugía.
• Modificación del procedimiento.
• Retrasar la cirugía por tratamiento de condiciones inestables.
• Modificación en terapia medica preoperatoria.
• Inicio de terapias como beta bloqueo, estatinas, hipertensión arterial.
• Plan de cuidados postoperatorios y monitorización (ejemplo Unidad de cuidados intensivos).
• Revascularización coronaria (PCI – CABG).
• Derivación centro mayor complejidad.
• Cuidados paliativos.
¿Cuáles son condiciones cardíacas de riesgo elevado?[2]
• Infarto agudo miocardio en el último mes.
• Angina inestable.
• Insuficiencia cardíaca aguda.
• Insuficiencia cardíaca crónica en fase descompensada.
• Arritmia cardiaca con frecuencia ventricular elevada (> 100 lat/min) en reposo.
• Bradicardia sintomática.
• Enfermedad valvular cardíaca sintomática.
• Estenosis mitral asintomática con área valvular < 1,5 cm2.
• Estenosis aortica asintomática con área valvular < 1,0 cm2.
• Cardiopatía con hipertensión pulmonar grave.
-
Enfermedad coronaria
La angina inestable o severa (CCS III – IV) y el infarto miocardio reciente (30 días) deben considerarse como condiciones activas y de riesgo (Figura 2).
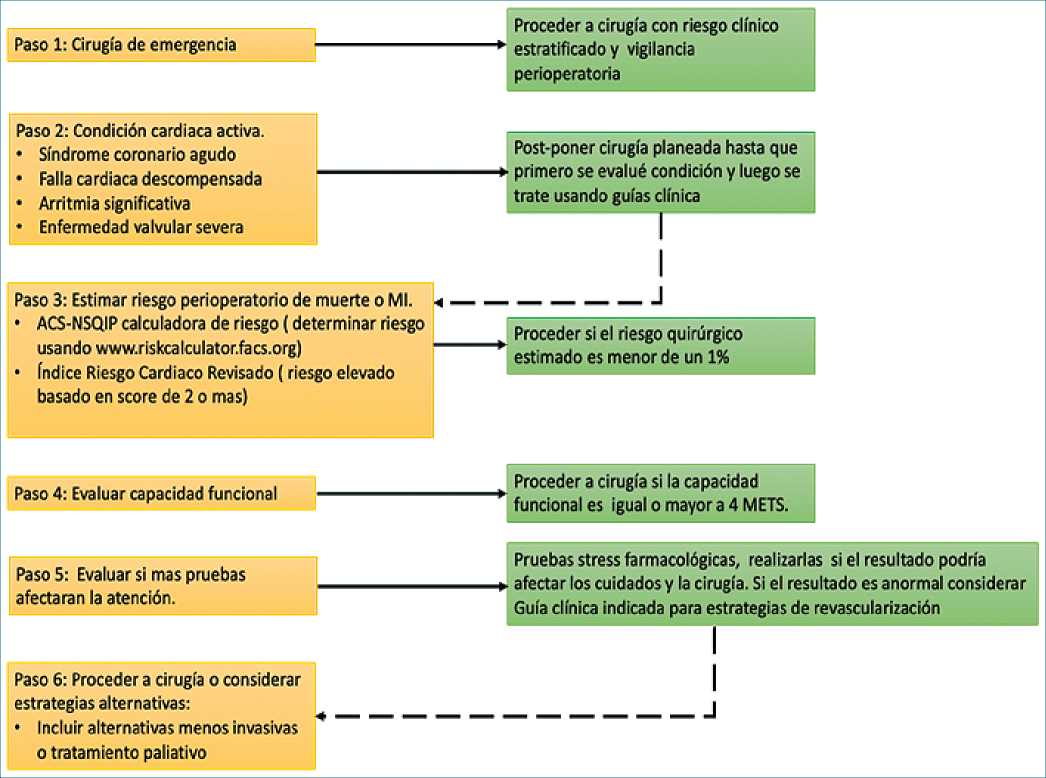
Figura 1. Adaptado del original: Nathaniel R. Smilowitz, MD, MS; Jeffrey S. Berger, MD, MS -Perioperative Cardiovascular Risk Assessment and Management for Noncardiac Surgery A Review,JAMA. 2020;324(3):279-290. doi:10.1001/jama.2020.7840
Deben transcurrir > 60 días después de un infarto de miocardio antes de una cirugía no cardíaca en ausencia de una intervención coronaria (Stent o CABG). En función de disminuir el riesgo de MACE[3].
Un infarto de miocardio reciente, ocurrido dentro de los 6 meses posteriores a la cirugía no cardíaca, también resultó ser un factor de riesgo independiente de ACV perioperatorio, que se asoció con un aumento de 8 veces en la tasa de mortalidad perioperatoria[4].
Los adultos mayores tienen mayor carga de enfermedad con presencia de enfermedad coronaria, cerebrovascular y diabetes mellitus. Se ha observado una mayor tasa de incidencia de ACV en mayores de 65 años[5] (Figura 4).
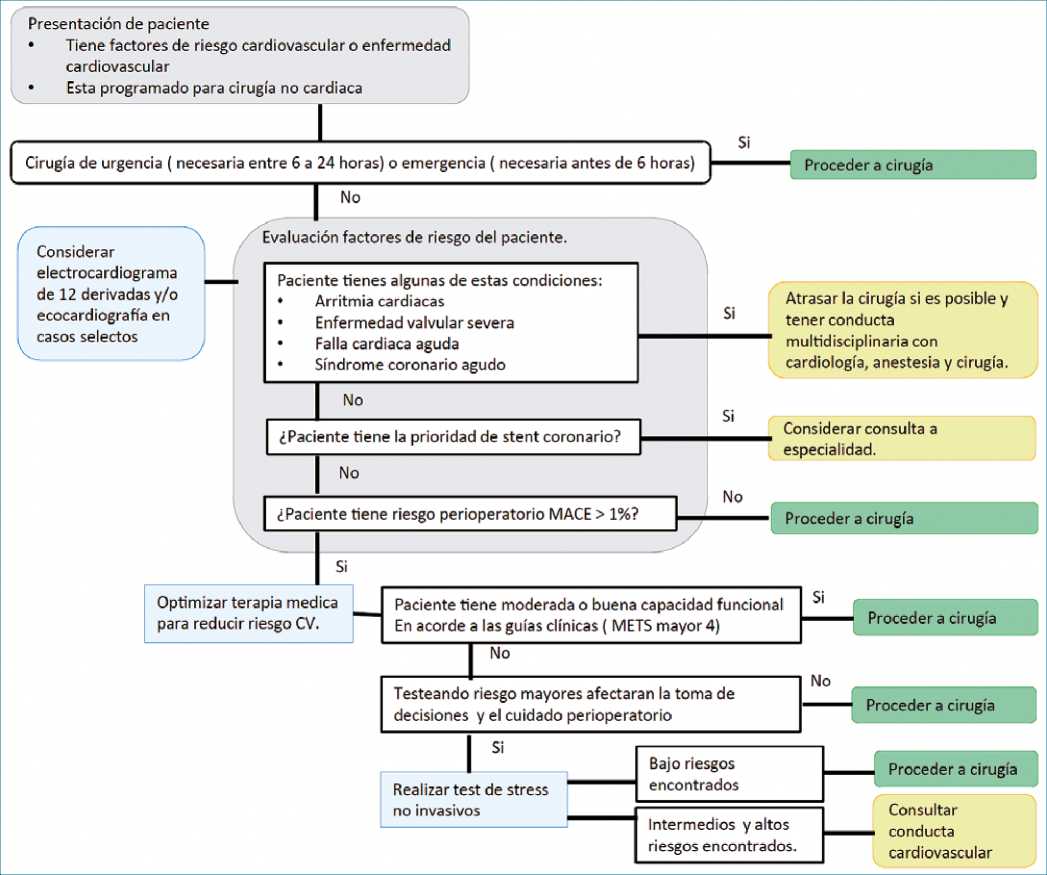
Figura 2. Adaptado del original: Nathaniel R. Smilowitz, MD, MS; Jeffrey S. Berger, MD, MS -Perioperative Cardiovascular Risk Assessment and Management for Noncardiac Surgery A Review,JAMA. 2020;324(3):279-290. doi:10.1001/jama.2020.7840
-
Insuficiencia cardíaca
Consideramos la insuficiencia cardíaca como un estado fisiopatológico en el que algún tipo de disfunción del corazón provoca su incapacidad para bombear sangre en la cantidad necesaria para suplir los requerimientos metabólicos del organismo.
Los pacientes con insuficiencia cardíaca clínica (IC) (síntomas de IC activa o hallazgos en el examen físico de edema periférico, distensión venosa yugular, estertores, tercer ruido cardíaco o radiografía de tórax con redistribución vascular pulmonar o edema pulmonar) o antecedentes de IC están en riesgo significativo de complicaciones perioperatorias[6].
La insuficiencia cardíaca es un potente predictor de eventos adversos no cardíacos en los pacientes como morbilidad, reoperación, readmisión e incremento en la mortalidad a 30 días[7].
-
Enfermedad valvular[8]
La enfermedad cardíaca valvular significativa aumenta el riesgo cardíaco para los pacientes que se someten a una cirugía no cardíaca. Los pacientes con sospecha de enfermedad valvular cardíaca deben someterse a una ecocardiografía para cuantificar la gravedad de la estenosis o regurgitación, calcular la función sistólica y estimar las presiones del corazón derecho. También se justifica la evaluación de enfermedad coronaria concurrente.
Se recomienda que los pacientes con sospecha clínica de enfermedad valvular (moderada a severa) se sometan a una ecocardiografía preoperatoria: (recomendación grado 1 LOE C).
• Si no tiene una ecocardiografía previa dentro 1 año.
• Presenta un cambio significativo en el estado clínico o examen físico desde la última evaluación.
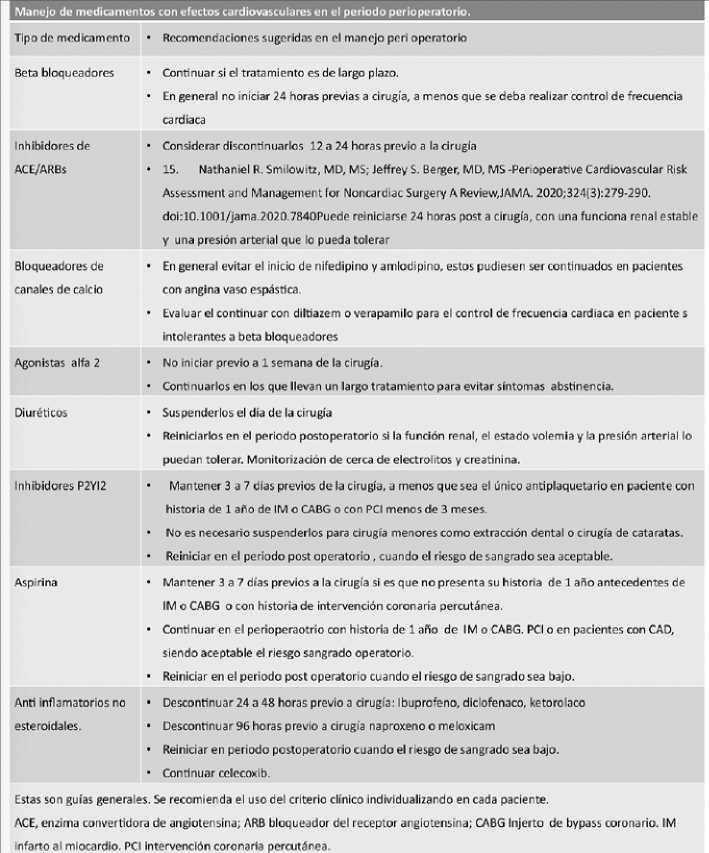
Figura 3. Adaptado del original: Ravindra Ganesh y otros -Perioperative Cardiac Risk Reduction in Noncardiac Surgery Crossref DOI link: https://doi.org/10.1016/J. MAYOCP.2021.03.014 Published Print: 202108
En el grupo de pacientes que cumplen con la indicación para recibir intervención valvular (reemplazo – reparación) en base a su cuadro clínico. La intervención valvular antes de la cirugía no cardíaca electiva es efectiva para reducir el riesgo peri operatorio. (Recomendación grado 1 LOE C).
En este contexto existen recomendaciones específicas para la enfermedad valvular por estenosis e insuficiencia basadas en guías de práctica clínica.
-
Arritmias y trastornos de la conducción[8]
Las arritmias cardíacas y los trastornos de la conducción son hallazgos comunes en el período perioperatorio, particularmente con el aumento de la edad. Se han identificado dentro del grupo de condiciones cardíacas activas (del RCRI), arritmias por bradicardia, alteraciones de la conducción y taquicardias.
• Bloqueo AV de alto grado, bloqueo AV mobitz II y AV 3er grado.
• Arritmias supraventriculares con respuesta ventricular no
controlada (fibrilación auricular – flutter auricular).
• Bradicardia sintomática.
• Taquicardia ventricular recientemente conocida.
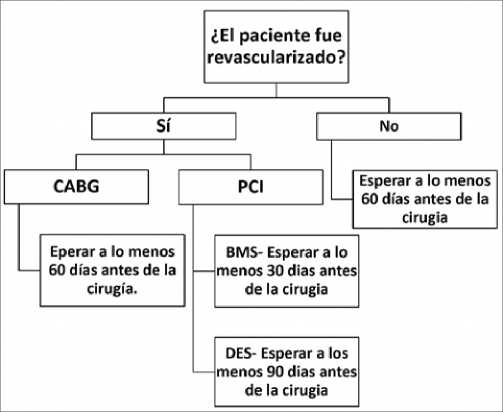
Figura 4.
Los pacientes con antecedentes preoperatorios de FA que se encuentran clínicamente estables, generalmente, no requieren modificación del manejo médico o evaluación especial en el período perioperatorio, aparte del ajuste de la anticoagulación.
La presencia de extrasístoles ventriculares prematuros frecuentes y la taquicardia ventricular no sostenida son factores de riesgo para el desarrollo de arritmias perioperatorias, aunque no se asocian claramente a un riesgo mayor de MACE[9].
Tabla 1. Medicación empleada para frenar y prevenir los paroxismos, así como para el tratamiento sintomático[10]
| Fármaco | Dosis | Efecto deseado | Efectos secundarios |
| Morfina | Bolo 2-8 mg ev | – Aborto crisis
– Tratamiento sintomático |
– Depresión respiratoria
– Sedación – Hipotensión – Ileo paralítico – Emesis – Liberación histamina – Tolerancia |
| Propofol | Bolo 10-20 mg ev o Infusión continua hasta 80 mcg/kg/min | – Los bolos abortan las crisis y la perfusión las previene
– Tratamiento sintomático |
– Sedación profunda
– Síndrome de infusión prolongada por propofol |
| Benzodiacepinas | – Diazepam 5-10 mg ev bolo – Lorazepam 1-4 mg ev bolo – Midazolam 2-5 mg ev bolo – Clonazepam 0,5-2 mg/8 h | – Aborto y prevención (clonazepam) de las crisis
– Tratamiento sintomático |
– Sedación
– Depresión respiratoria – Tolerancia |
| Dexmedetomidina | 0,2-1,5 mcg/kg/h en perfusión ev | – Aborto y prevención de crisis
– Tratamiento sintomático de la taquicardia e hipertensión |
– Bradicardia
– Hipotensión – Sedación |
| Clonidina | 0,1-0, mg 7 6-8 h enteral | – Aborto y prevención de las crisis
– Tratamiento sintomático de la taquicardia e hipertensión |
– Bradicardia
– Hipotensión – Sedación |
| Propanolol | 20-80mg/4-6 h enteral | – Prevención
– Tratamiento sintomático de la taquicardia, hipertensión, diaforesis y distonía |
– Bradicardia
– Hipotensión – Alteraciones del sueño |
| Gabapentina | 100-300 mg/8 h enteral
Aumentar hasta máximo 3.600-4,800 mg al día |
– Prevención
– Tratamiento sintomático |
– Sedación |
| Bromocriptina | 1,25 mg/12 h enteral Dosis total máxima 40 mg | – Prevención
– Escaso y retardado efecto |
– Confusión
– Agitación – Discinesia – Emesis – Hipotensión ortostática |
| Baclofeno | 5 mg/8 h enteral
Se puede aumentar hasta máximo 80 mg al día |
– Prevención
– Tratamiento de la hipertonía y distonía |
– Sedación
– Debilidad muscular |
| Dantroleno | 0,5-2 mg/kg ev/6-12 h Máximo 10 mg/kg al día | – Aborto de las crisis
– Mejora la hipertonicidad y distonía |
– Hepatotoxicidad
– Depresión respiratoria – Debilidad muscular |
-
Herramientas de evaluación riesgo cardiovascular[8]
RCRI (índice de riesgo cardiaco revisado):
El RCRI es una herramienta simple, validada y aceptada para evaluar el riesgo peri operatorio de complicaciones cardíacas mayores (infarto miocardio, edema pulmonar, fibrilación ventricular o paro cardíaco primario y bloqueo cardíaco completo -MACE). Tiene 6 predictores de riesgo de complicaciones cardíacas mayores.
*ev: endovenoso.
• Antecedentes de cardiopatía isquémica.
• Antecedentes de insuficiencia cardiaca congestiva.
• Antecedentes de enfermedad cerebrovascular.
• Diabetes insulino-dependiente.
• Creatinina mayor de 2 mg/Dl.
El RCRI revisado permite discriminar moderadamente bien a los pacientes con bajo riesgo, de los pacientes con alto riesgo de eventos cardíacos tras diferentes tipos de cirugía no cardiaca, pero su, comportamiento fue peor en la predicción de eventos cardiacos tras la cirugía vascular no cardíaca y en la predicción de la muerte[10].
NSQIP-ACS:
El índice de riesgo quirúrgico NSQIP del American College of Surgeons, incluye variables clínicas y quirúrgicas para determinar riesgo. Se identificaron cinco variables predictivas de infarto de miocardio/parada cardíaca perioperatorios:
• Tipo de cirugía.
• Estado funcional.
• Niveles elevados de creatinina (> 1,5 mg/dl).
• Tipo o clase ASA.
• Edad.
NSQIP-ACS proporciona una estimación del riesgo según modelo de probabilidad de infarto de miocardio o parada cardíaca para un paciente individual. Además de los riesgos específicos del procedimiento para un grupo diverso de resultados[11)].
Ambos modelos proporcionan perspectivas diagnósticas complementarias que pueden ayudar al médico en el proceso de toma de decisiones.
-
Capacidad de ejercicio y capacidad funcional[8]
El estado funcional es un predictor confiable de eventos cardíacos perioperatorios y a largo plazo. Los pacientes con un estado funcional reducido antes de la operación tienen un mayor riesgo de complicaciones. Por el contrario, aquellos con buen estado funcional antes de la operación tienen un riesgo menor. El estado funcional, generalmente, se puede estimar a partir de las actividades de la vida diaria o a través de herramientas específicas como DASI[12].
La capacidad funcional se clasifica como excelente (> 10 MET), buena (7 MET a 10 MET), moderada (4 MET a 6 MET), deficiente (< 4 MET) o desconocida. (1 MET = 3,5 ml O2 x min). Los riesgos cardíacos y a largo plazo perioperatorios aumentan en pacientes que no pueden realizar 4 MET de trabajo durante sus actividades diarias.
Si un paciente puede llevar una caminata por más de 2 km sin la aparición de disnea, la probabilidad de enfermedad coronaria extensa es muy baja. Por el contrario, si el paciente ante mínimo esfuerzo físico se vuelve disneico y presenta dolor torácico la probabilidad se hace alta.
En el grupo de pacientes que se sometieron a cirugía no cardíaca, la isquemia miocárdica perioperatoria y los eventos
cardiovasculares fueron más comunes en aquellos con un estado funcional deficiente (definido como la incapacidad para caminar 4 cuadras o subir 2 tramos de escaleras) incluso después de ajustar por otros factores de riesgo.
-
DASI: Duke Activity Score Index
La capacidad funcional (CF) es un concepto que refleja la habilidad de desarrollar actividades de la vida diaria requirentes de metabolismo aeróbico. Una baja CF se asocia a una baja aptitud cardiorrespiratoria, y a mayor riesgo de mortalidad cardiovascular. La CF se relaciona con el consumo de oxígeno máximo (VO2 max), definido como el producto del gasto cardíaco y la diferencia arterio-venosa de oxígeno ante un ejercicio máximo extenuante[13].
El DASI consiste en 12 preguntas sobre actividades de la vida diaria, que evalúan cinco ámbitos: cuidado personal, marcha, cuidado de la casa, actividad sexual y actividades deportivas (Tabla 2).
-
Exámenes complementarios[8]
Las pruebas perioperatorias no invasivas tienen el propósito de entregas información sobre tres factores de riesgo: disfunción ventrículo izquierdo (insuficiencia cardíaca) isquemia miocardio y alteraciones valvulares. Todos estos son determinantes de resultados postoperatorios adversos.
ECG en reposo:[8]
Sachile recomendación 5.3.6.1
Recomendamos la realización de un ECG de reposo de 12 derivadas en pacientes con enfermedad coronaria conocida, enfermedades pulmonares, arritmias, enfermedad arterial periférica, enfermedad cerebrovascular y otras enfermedades cardíacas estructurales, como también en pacientes diabéticos insulino-requirientes o aquellos con enfermedad renal (creatinina > 2 mg/dl o clearence de creatinina < 60 ml/min/1,73 m2), así como en aquellos con signos o síntomas cardiovasculares activos y que serán sometidos a cirugías de riesgo cardíaco elevado (> 1%)[14].
Sachile recomendación 5.3.6.3
Sugerimos la realización de un ECG de reposo en pacientes con factores de riesgo (> 1 FR), incluso cuando serán sometidos a cirugías de bajo riesgo[14].
Sachile recomendación 5.3.6.4
En pacientes mayores de 65 años, sin factores de riesgo, que serán sometidos a cirugías de riesgo intermedio y alto[14].
Podemos comentar respecto a estos dos últimos puntos que el ECG en reposo tiene como característica mostrarnos un “período acotado” de la actividad eléctrica del corazón y por ello al anestesiólogo le sirve en ciertas circunstancias contar con este examen como una referencia ante cambios en los pacientes con riesgo CV.
Sachile recomendación 5.3.6.2
No recomendamos la realización de un ECG de reposo en pacientes sin factores de riesgo que serán sometidos a cirugías
de bajo riesgo[14].
Esta afirmación queda fuertemente respaldada para las guías AHA -ACC 2014 (USA) y ESC ESA 2014 (Europa).
| Tabla 2. Cuestionario DASI versión en Español adaptado a población chilena: formulación de 12 preguntas con puntaje estimado frente a respuesta positiva | |
| Actividad | Valor estimado |
| 1. ¿Puede Usted realizar sus actividades de autocuidado, tales como alimentarse, vestirse, bañarse, o usar el baño? | 2,75 |
| 2. ¿Puede Usted caminar dentro de su casa y alrededor de ésta? | 1,75 |
| 3. ¿Puede Usted caminar una o dos cuadras, sin pendiente? | 2,75 |
| 4. ¿Puede subir un tramo de escalones (ej: dos pisos de escaleras) sin detenerse? | 5,50 |
| 5. ¿Puede correr una pequeña distancia? | 8,00 |
| 6. ¿Puede realizar trabajos livianos en su casa tales como sacudir el polvo, o lavar platos? | 2,70 |
| 7. ¿Puede realizar trabajo moderado en su casa tal como pasar la aspiradora, barrer los pisos, o acarrear comestibles desde una | 3,50 |
| tienda o mercado? | |
| 8. ¿Puede realizar trabajo pesado en su casa tal como el fregado de piso, o levantar o desplazar muebles pesados? | 8,00 |
| 9. ¿Puede hacer trabajos en el jardín tales como rastrillar las hojas, desmalezar o empujar una cortadora de pasto? | 4,50 |
| 10. ¿Puede tener relaciones sexuales? | 5,25 |
| 11. ¿Puede participar en actividades recreacionales físicas de intensidad moderada como baile entretenido, zumba, jugar tenis | 6,00 |
| (en dobles), jugar golf o lanzar pelotas? | |
| 12. ¿Puede participaren deportes intensos como natación, tenis individual, fútbol, baloncesto o esquí? | 7,50 |
| Puntaje total sumatorio | |
| Cálculo V02max = puntaje total DASI x 0,43 + 9,6 / METs = puntaje total DASI x 0,43 + 9,6 / 3,5 | |
Adaptación del original:[13].
-
Evaluación función ventricular izquierda[8]
Las guías AHA -ACC (USA) 2014 hacen hincapié en la evaluación sistólica del VI. Existe asociación entre la disminución de la función sistólica del VI y las complicaciones perioperatorias, en particular, insuficiencia cardíaca posoperatoria. El mayor riesgo es para pacientes con FEVI en reposo < 35%.
La FE es un parámetro de función sistólica que relaciona el volumen de tele diastólico con el volumen tele sistólico y puede ser obtenido a través de múltiples modalidades de imagen cardíaca. (Ecocardiografía en reposo, angioTAC cardíaco, RNM cardíaca, SPECT miocárdico, etc.)
| Función sistólica del ventrículo | Fracción eyección del ventrículo |
| izquierdo | izquierdo |
| Normal | Mayor e igual 55% |
| Disfunción leve | 45% a 54% |
| Disfunción moderada | 36% a 44% |
| Disfunción severa | Menor 35% |
-
Evaluación función diastólica del VI[8]
La disfunción diastólica del VI ocurre debido a la alteración en el llenado y relajación (distensibilidad) de la cavidad ventricular. La insuficiencia cardíaca diastólica involucra el lado izquierdo del
corazón. Provoca un ventrículo izquierdo rígido que impide que el corazón se relaje entre latidos. Esto significa que el corazón no puede bombear una cantidad adecuada de sangre por todo el cuerpo o tiene que bombear con una presión mayor.
La ecocardiografía es crucial en su determinación. Aunque no existe un parámetro ecográfico único, simple y preciso para su diagnóstico. Se requiere del uso de herramientas ecográficas como eco 2d, Doppler pulsado y Doppler tisular.
El VI se llena en dos etapas: una etapa de llenado temprano (E) y luego ocurre el llene tardío (A) a consecuencia de la contracción auricular.
Una de las formas de medir este proceso de llenado ventricular es obteniendo las velocidades de onda pulsada (Doppler) a través de la válvula mitral, en el cual las ondas A y onda E representan las dos etapas de llenado (temprano – tardío). En un corazón sano la velocidad de la onda E es mayor que la velocidad de la onda A. Por tanto, la relación E/A es > 1. Cuando el VI pierde distensibilidad (como en insuficiencia cardíaca FEVI preservada) la onda E se reduce alterando y disminuyendo la relación E/A un valor < de 1.
En estados más avanzados de disfunción la relación E/A puede revertir a un patrón que asemeja el normal, llamado pseudonormal. Con ello se agrega la necesidad de otros índices eco cardiográficos (Velocidad tisular del anillo mitral, ondas de flujo venoso pulmonar, volumen de aurícula izquierda, velocidad de reflujo tricúspide).
Es importante para los anestesiólogos conocer el grado de disfunción diastólica (disfunción diastólica de grado I – II – III en función de mayor presión en aurícula izquierda, reflejo de mayor presión intraventricular del VI. En el escenario clínico de insuficiencia cardíaca (FE reducida y FE preservada) cobra más importancia el grado de disfunción diastólica[15].
-
Pruebas de isquemia miocárdica – test esfuerzo, eco stress y MPI[8]
Las pruebas de esfuerzo o provocación para isquemia miocárdica agrupan al ECG en ejercicio (test esfuerzo propiamente tal o ergometría), la ecocardiografía de stress y las imágenes de perfusión miocárdica (MPI) con radio nucleótidos a partir de los datos disponibles, los pacientes capaces de lograr aproximadamente 7 MET a 10 MET tienen un riesgo bajo de eventos cardiovasculares perioperatorios y aquellos que logran < 4 MET a 5 MET tienen un mayor riesgo de eventos cardiovasculares perioperatorios.
Las imágenes cardíacas con esfuerzo o stress no son solicitadas de rutina por los anestesiólogos. Lo que ocurre en la mayoría de los centros, es el paciente referido a un manejo multidisciplinario donde cardiólogos clínicos, cardiólogos de hemodinamia, especialistas en ecocardiografía y cardiocirujano pueden contribuir al manejo con este tipo de pacientes, en donde por supuesto el anestesiólogo juega un rol fundamental.
Ante pruebas de esfuerzo negativas o imágenes de perfusión (MPI) con pequeñas áreas de isquemia lo correcto es proceder con la cirugía bajo la óptima terapia médica (basado en guías de práctica clínica).
En la situación que se presenten alteraciones en pruebas de esfuerzo o imágenes MPI entra a jugar esta evaluación multidisciplinaria tras realizar una coronariografía que puede indicar la necesidad de revascularización (PCI/Stent o CABG) o limitar intervenciones invasivas mayores.
-
Test esfuerzo – ergometría[8]
Las pruebas de esfuerzo muestran cómo responde el corazón a la actividad física. Cuando se somete al ejercicio, el corazón bombea con más rapidez y fuerza. En una prueba de esfuerzo, se examina cómo funciona el corazón mientras se hace ejercicio en una cinta rodante o una bicicleta estática. Se realiza durante un episodio inducido de aumento de la demanda cardíaca para poder identificar áreas isquémicas con riesgo de infarto. La frecuencia cardíaca se incrementa hasta 85% del valor máximo estimado para la edad (frecuencia cardíaca objetivo) o hasta que se desarrollan los síntomas de angina.
El diagnóstico se fundamenta en la evaluación de la respuesta del segmento ST (que representa la isquemia subendocárdica global), la respuesta de la tensión arterial y los síntomas del paciente. La sensibilidad promedio es de 67% y la especificidad promedio es de 72%. El pronóstico empeora con la profundidad del desnivel del segmento ST.
Se puede considerar la prueba de ejercicio cardiopulmonar para pacientes sometidos a procedimientos de alto riesgo en quienes se desconoce la capacidad funcional (Clase IIb, Nivel de evidencia: B)[8]
-
Ecocardiograma de stress
-
(DSE, Dobutamine stress echo)[8]
Consiste en efectuar una ecocardiografía durante la infusión por vía endovenosa de un medicamento inótropo (dobutamina) que mediante el aumento de la frecuencia y contractilidad cardíaca simula la realización de un ejercicio. Se monitoriza
frecuencia cardíaca, ritmo cardíaco y presión arterial antes, durante y después del examen.
La ecocardiografía detecta anomalías del movimiento de la pared que son un signo de isquemia regional. Usando técnicas Doppler, ayuda a evaluar los trastornos valvulares que pueden contribuir al desarrollo de isquemia o valvulopatías primarias o ser el resultante de la isquemia, pero que merecen una evaluación concomitante. La ecocardiografía de estrés presenta un valor predictivo similar al de las MPI.
Es razonable que los pacientes que tienen un riesgo elevado de cirugía no cardíaca y una capacidad funcional deficiente (< 4 MET) se sometan a una prueba de estrés farmacológica no invasiva (ya sea ecocardiograma de estrés con dobutamina [DSE] o MPI de estrés farmacológico) si cambiará el tratamiento. (Clase IIa, Nivel de evidencia: B)[8].
-
Imágenes de perfusión miocárdica con radio nucleótidos MPI[8]
Cintigrafía cardíaca y SPECT miocárdico
La cintigrafía o gammagrafía del corazón es particularmente útil para el diagnóstico de un dolor torácico cuando la causa es desconocida. Si las arterias coronarias están ocluidas, se utiliza la gammagrafía para determinar en qué medida la oclusión está afectando el aporte de sangre al corazón y su funcionamiento. La gammagrafía también se usa para valorar el aumento de la irrigación sanguínea coronaria después de un bypass coronario u otros procedimientos similares, y puede utilizarse como ayuda para determinar el pronóstico después de un infarto de miocardio.
La tomografía computarizada por emisión de fotón único (SPECT) es una técnica de imagen topográfica de medicina nuclear que utiliza rayos gamma. Proporciona más información sobre la funcionalidad, el flujo sanguíneo y las anomalías que la imagen convencional obtenida con radionúclidos o gammagrafía.
La mayoría de los estudios de MPI muestran que los defectos de perfusión reversibles de moderados a grandes, que reflejan isquemia miocárdica, conllevan el mayor riesgo de muerte cardíaca perioperatoria o infarto.
Las pruebas MPI de estrés farmacológico, (dipiridamol/ adenosina/regadenosón) pueden usarse en pacientes sometidos a cirugía no cardiaca que no pueden realizar ejercicio para detectar isquemia miocárdica inducida por estrés y enfermedad coronaria.
La presencia de áreas moderadas a grandes de isquemia miocárdica se asocia con un mayor riesgo de infarto de miocardio perioperatorio y/o muerte.
Un estudio normal de MPI tiene un valor predictivo negativo muy alto, para IAM perioperatorio y/o muerte cardíaca.
La presencia de un IAM antiguo identificado en imágenes de reposo tiene poco valor predictivo de IAM perioperatorio o muerte cardíaca.
En general, un defecto de perfusión miocárdica reversible predice eventos perioperatorios, mientras que un defecto de perfusión fijo predice eventos cardíacos a largo plazo.
Un estudio de perfusión miocárdica normal predice un desenlace benigno con un riesgo de eventos adversos inferior al 1%.
-
Angiografía coronaria
La coronariografía no está indicada en forma rutinaria antes de la cirugía no cardíaca. Debe considerarse en pacientes con test de esfuerzo o imágenes de stress que indiquen la posibilidad de isquemia miocárdica y siempre que el resultado afecte los cuidados perioperatorios. (ej implante de Stent o CABG).
Una alternativa interesante es la utilización por la cardiología del AngioTAC coronario (CCTA). En un metaanálisis de 11 estudios evaluando CCTA previo a la cirugía, la severidad y extensión de la enfermedad coronaria fue asociado con MACE perioperatorio.
Sin embargo, la enfermedad coronaria evaluada con CCTA sobreestima el riesgo y su utilización aun no es recomendada en guías de práctica clínica para estratificar el riesgo preoperatorio en cirugía no cardíaca[16].
La revascularización (PCI/CABG) preoperatoria no ha mostrado disminución de la aparición de MACE. Sin embargo, ante situaciones impostergables como síndrome coronario agudo debe realizarse precozmente independiente de la cirugía no cardíaca.
-
Pacientes que requieren cirugía urgente o de emergencia
La cirugía no cardíaca urgente (requerida entre 6 a 24 h) y de emergencia (antes de 6 h por amenaza vital o compromiso de extremidad) ambas están, independientemente asociadas a incremento del riesgo de morbilidad (13,8% de emergencia,
12,3% de urgencia y 6,7% electiva) y mortalidad quirúrgica (3,7% de emergencia, 2,3% de urgencia y 0,4% electiva).
La evaluación preoperatoria cardiovascular debe considerar los beneficios de la cirugía y las alternativas de tratamiento en el contexto del riesgo de las cardiopatías.
Cuando la cirugía urgente compromete riesgo vital, es posible no poder realizar una evaluación cardiovascular detallada, especialmente, si el resultado sea poco probable que vaya a cambiar el tratamiento del paciente. Las guías de práctica clínica recomiendan que la evaluación cardiovascular sería apropiada previo a la cirugía urgente para excluir condiciones activas que contraindican la cirugía cardiaca y de ser necesario optimizar su manejo.
Si se dispone es sugerido la participación de anestesistas cardiovasculares y el manejo de monitorización hemodinámica avanzada en el perioperatorio.
-
Biomarcadores en estratificación del riesgo perioperatorio
Los biomarcadores son pequeñas moléculas (polipéptidos u otros) que pertenecen a la maquinaria intracelular de los miocardiocitos. Su funcionamiento y regulación están ligados a mecanismos de señalización intracelular de segundos mensajeros y regulación genómica (como ARN mensajeros) (Figura 5).
Distinguimos dos grandes grupos los péptidos natriuréticos (más bien relacionados con la insuficiencia cardíaca) y las troponinas (relacionados con injuria e isquemia miocárdica).
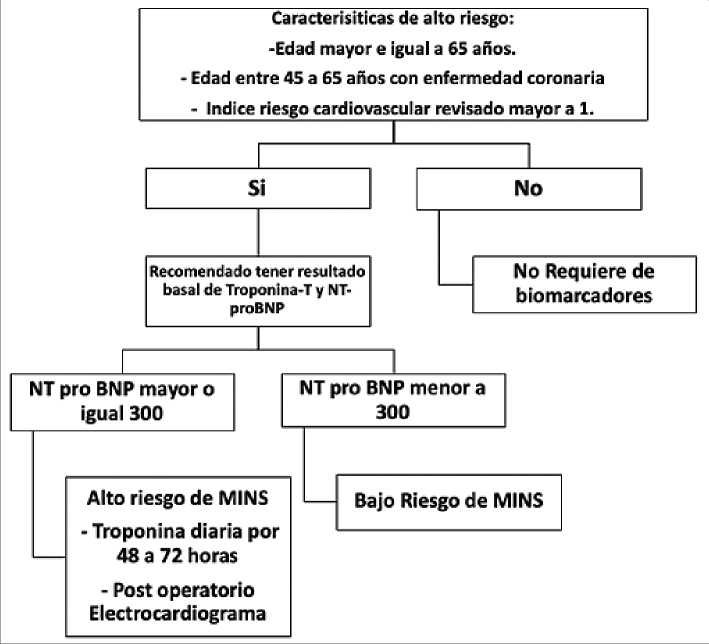
Figura 5. Adaptado del original: (17).
Artículo de Revisión
-
Péptido natriurético cerebral (BNP)
Es una hormona natriurética que se libera principalmente del corazón. Está elevado en muchas condiciones patológicas. Son hormonas que se encuentran en distintos tejidos, pero principalmente son sintetizadas y almacenadas en los miocitos auriculares y ventriculares. Su acción está vinculada a segundos mensajeros intracelulares como GMPc. Algunos de sus efectos fisiológicos son: el incremento del filtrado glomerular, la excreción de sodio, la vasodilatación periférica y la atenuación de los sistemas renina-angiotensina aldosterona, adrenérgico y endotelinérgico.
Actualmente, se utilizan como marcadores en el manejo de insuficiencia cardíaca (IC) y contribuyen al pronóstico de esta. La medición de biomarcadores, especialmente los péptidos natriuréticos, puede ser útil para evaluar a los pacientes con IC y para diagnosticar la IC como una complicación posoperatoria en pacientes con alto riesgo de IC. (Estrategia de guías CCS) [17].
Las pautas anteriores de ESC/ESA o AHA/ACC no recomendaban el uso de biomarcadores en procedimientos preoperatorios y posoperatorios, pero las guías ESC/ESA 2014 sugieren que las troponinas cardíacas en pacientes de alto riesgo pueden evaluarse tanto antes como 48 a 72 h después de una cirugía mayor.
Sin embargo, debe tenerse en cuenta que no se recomienda el muestreo de biomarcadores preoperatorios de rutina en todos los pacientes para la estratificación del riesgo y para prevenir eventos cardíacos. Aún debe determinarse el impacto de dicha medición de biomarcadores en el manejo perioperatorio de pacientes de cirugía no cardíaca, pero estas recomendaciones iniciales establecen a los biomarcadores como parte del manejo perioperatorio[8],[18].
En pacientes con arteriopatía periférica sometidos a cirugía vascular mayor, el mecanismo probable de IAM perioperatorio parece ser el estrés hemodinámico relacionado con el tipo y la duración de la cirugía. El biomarcador NT-proBNP fue un predictor independiente útil de eventos (MACE) y, por lo tanto, puede servir como un biomarcador importante de la aptitud cardiovascular para la cirugía[19].
No está claro si es útil medir los niveles de péptidos natriuréticos posoperatorios cuando se ha realizado una medición preoperatoria. Aún cuando estudios muestran que podría ser beneficioso en estratificación (MACE) falta desarrollo de evidencia de potencia a estas afirmaciones[20].
-
Troponinas (Tn) en perioperatorio
Las troponinas son parte importante de los filamentos contráctiles del esqueleto en miocardiocitos y musculo estriado esquelético. Estas moléculas facilitan la acción entre la actina y miosina. Comprenden tres subunidades:
TnT que une el complejo de troponina a la actina, TnC que comprende un sitio de unión al calcio iónico, y TnI que inhibe la acción entre la actina y las cabezas de miosina.
La troponina TnC es idéntica en el miocardio y musculo estriado, mientras que TnT y TnI se diferencian entre sí.
Recordemos que las troponinas y los exámenes de medición de éstas han permitido evaluar la injuria miocárdica producida por la isquemia jugando un rol fundamental en los síndromes
coronarios agudos. (Parte de la 4ta definición universal de IAM) [21].
El uso preoperatorio de Tn hay estudios sugieren que un valor elevado de troponinas (ultrasensibles) estarían asociados con mortalidad temprana y mayor incidencia de eventos tipo MACE[22].
Las guías clínicas AHA/ACC 2014 y CCS 2016 comentan sobre el uso de troponinas preoperatorias en grupos de mayor riesgo[8],[17].
Actualmente, existe un vacío en la evidencia ante protocolos estandarizados para manejar pacientes con alza preoperatoria de Tn. Además, debemos tener en cuenta de algunas condiciones que producen alzas en troponinas y que pueden tener un papel confundente, ej Sepsis[22].
Respecto al uso posoperatorio las Tn son una herramienta valiosa para identificar el IAM (síndromes coronarios agudos) y la injuria miocárdica (MINS). En estudios como VISION[23] la elevación postoperatoria peak de Tn se asocia al aumento de la mortalidad a 30 días en un patrón de dosis – respuesta (mayor peak, mayor mortalidad)[22].
Cuando nos encontramos con MINS (lesión miocárdica asociada con cirugía no cardíaca) observamos un aumento en la mortalidad a 30 días posoperatorios (CHASE study)[24].
Tiene importancia, sin duda encontrarnos con injuria tipo MINS, aunque la evidencia del manejo de esta es limitada. Algunos autores relacionan esta condición con IAM tipo 2[21], en la cual se produciría un desbalance entre el aporte y demanda de oxígeno miocárdico. Esta condición es muy importante para los anestesiólogos, ya que intervenciones como el control de hipotensión, taquicardia, hipovolemia y anemia podrían ser tratadas[25].
El manejo de la isquemia coronaria (IAM sin SDST) en sus distintos escenarios es abordado de acuerdo con las guías de práctica clínica respectivas[26].
Referencias
1. L.A F. Preoperative Assessment of the Patient with Cardiac Disease Undergoing Noncardiac Surgery. 2016.
2. Jordi Casademont Pou JMPPJACMASOaEMR. Medicina perioperatoria. Elsevier; 2013.
3. Livhits M, Ko CY, Leonardi MJ, Zingmond DS, Gibbons MM, de Virgilio C. Risk of surgery following recent myocardial infarction. Ann Surg. 2011 May;253(5):857–64. https://doi.org/10.1097/SLA.0b013e3182125196 PMID:21372685
4. Mashour GA, Shanks AM, Kheterpal S. Perioperative stroke and associated mortality after noncardiac, nonneurologic surgery. Anesthesiology. 2011 Jun;114(6):1289–96. https://doi.org/10.1097/ALN.0b013e318216e7f4 PMID:21478735
5. Bateman BT, Schumacher HC, Wang S, Shaefi S, Berman MF. Perioperative acute ischemic stroke in noncardiac and nonvascular surgery: incidence, risk factors, and outcomes. Anesthesiology. 2009 Feb;110(2):231–8. https://doi.org/10.1097/ALN.0b013e318194b5ff PMID:19194149
6. van Diepen S, Bakal JA, McAlister FA, Ezekowitz JA. Mortality and readmission of patients with heart failure, atrial fibrillation, or coronary artery disease undergoing noncardiac surgery: an analysis of 38 047 patients. Circulation. 2011 Jul;124(3):289–96. https://doi.org/10.1161/CIRCULATIONAHA.110.011130 PMID:21709059
7. Turrentine FE, Sohn MW, Jones RS. SMJR. Congestive heart failure and noncardiac operations: risk of serious morbidity, readmission, reoperation, and mortality. J Am Coll Surg. 2016 Jun;222(6):1220–9. https://doi.org/10.1016/j.jamcollsurg.2016.02.025 PMID:27106641
8. Fleisher LA, Fleischmann KE, Auerbach AD, Barnason SA, Beckman JA, Bozkurt B, et al.; American College of Cardiology; American Heart Association. 2014 ACC/AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines. J Am Coll Cardiol. 2014 Dec;64(22):e77–137. https://doi.org/10.1016/j.jacc.2014.07.944 PMID:25091544
9. Mahla E, Rotman B, Rehak P, Atlee JL, Gombotz H, Berger J, et al. Perioperative ventricular dysrhythmias in patients with structural heart disease undergoing noncardiac surgery. Anesth Analg. 1998 Jan;86(1):16–21. https://doi.org/10.1213/00000539-199801000-00004 PMID:9428844
10. Ford MK, Beattie WS, Wijeysundera DN. Systematic review: prediction of perioperative cardiac complications and mortality by the revised cardiac risk index. Ann Intern Med. 2010 Jan;152(1):26–35. https://doi.org/10.7326/0003-4819-152-1-201001050-00007 PMID:20048269
11. Gupta PK, Gupta H, Sundaram A, Kaushik M, Fang X, Miller WJ, et al. Development and validation of a risk calculator for prediction of cardiac risk after surgery. Circulation. 2011 Jul;124(4):381–7. https://doi.org/10.1161/CIRCULATIONAHA.110.015701 PMID:21730309
12. Reilly DF, McNeely MJ, Doerner D, Greenberg DL, Staiger TO, Geist MJ, et al. Self-reported exercise tolerance and the risk of serious perioperative complications. Arch Intern Med. 1999 Oct;159(18):2185–92. https://doi.org/10.1001/archinte.159.18.2185 PMID:10527296
13. Pea VA. Evaluación y Utilidad del Cuestionario DASI (Duke Activity Score Index) para la Estimación de Capacidad Funcional en Población Chilena. Rev Chil Cardiol. 2021;40(2):104–13. https://doi.org/10.4067/S0718-85602021000200104.
14. Merino Nea. Recomendaciones Evaluacion preoperatoria. Revista Chilena de Anestesia. ; 48(2): p. 182-193.
15. A. Agatha Crerar-Gilbert MM. Core Topics in Preoperative Anaesthetic Assessment and Management: Cambridge Medicine.
16. Koshy AN, Ha FJ, Gow PJ, Han HC, Amirul-Islam FM, Lim HS, et al. Computed tomographic coronary angiography in risk stratification prior to non-cardiac surgery: a systematic review and meta-analysis. Heart. 2019 Sep;105(17):1335–42. https://doi.org/10.1136/heartjnl-2018-314649 PMID:31018953
17. Duceppe E. PJMPLKMMSSGMTVSKBASDBGDP. Canadian Cardiovascular Society Guidelines on Perioperative Cardiac Risk Assessment and Management for Patients Who Undergo Noncardiac Surgery. Can J Cardiol. 2017;1(33):17–32. https://doi.org/10.1016/j.cjca.2016.09.008 PMID:27865641
18. Stefan De Hert M. SSGFJHAA. Pre-operative evaluation of adults undergoing elective noncardiac surgery. Eur J Anaesthesiol. 2018;6(35):407–65. https://doi.org/10.1097/EJA.0000000000000817.
19. Chan W, Kingwell BA, Schneider HG, Cox G, Natoli A, Starr J, et al. Preoperative biomarker evaluation for the prediction of cardiovascular events after major vascular surgery. J Vasc Surg. 2019 Nov;70(5):1564–75. https://doi.org/10.1016/j.jvs.2019.02.041 PMID:31653377
20. Rodseth RN, Biccard BM, Le Manach Y, Sessler DI, Lurati Buse GA, Thabane L, et al. BBM,LMY,SDI,LBGA,TL,SRC,BD,CL,CD,CCP,CR,CM,DSS,FR,LWK,ME,MR. The prognostic value of pre-operative and post-operative B-type natriuretic peptides in patients undergoing noncardiac surgery a systematic review and individual patient. J Am Coll Cardiol. 2014;2(63):170–80. https://doi.org/10.1016/j.jacc.2013.08.1630 PMID:24076282
21. ESC. Consenso ESC 2018 sobre la cuarta definición universal del infarto. Rev Esp Cardiol. 2019;1(72):72.e1–27.
22. De Hert SG, Lurati Buse GA. Cardiac Biomarkers for the Prediction and Detection of Adverse Cardiac Events After Noncardiac Surgery: A Narrative Review. Anesth Analg. 2020 Jul;131(1):187–95. https://doi.org/10.1213/ANE.0000000000004711 PMID:32102011
23. Devereaux PJ, Chan MT, Alonso-Coello P, Walsh M, Berwanger O, Villar JC, et al.; Vascular Events In Noncardiac Surgery Patients Cohort Evaluation (VISION) Study Investigators. Association between postoperative troponin levels and 30-day mortality among patients undergoing noncardiac surgery. JAMA. 2012 Jun;307(21):2295–304. https://doi.org/10.1001/jama.2012.5502 PMID:22706835
24. van Waes JA, Grobben RB, Nathoe HM, Kemperman H, de Borst GJ, Peelen LM, et al.; Cardiac Health After Surgery (CHASE) Investigators. One-Year Mortality, Causes of Death, and Cardiac Interventions in Patients with Postoperative Myocardial Injury. Anesth Analg. 2016 Jul;123(1):29–37. https://doi.org/10.1213/ANE.0000000000001313 PMID:27111647
25. Wesselink EM, Kappen TH, Torn HM, Slooter AJ, van Klei WA. Intraoperative hypotension and the risk of postoperative adverse outcomes: a systematic review. Br J Anaesth. 2018 Oct;121(4):706–21. https://doi.org/10.1016/j.bja.2018.04.036 PMID:30236233
26. Collet JP, Thiele H, Barbato E, Barthélémy O, Bauersachs J, Bhatt DL, et al.; ESC. Guía ESC 2020 sobre el diagnóstico y tratamiento del síndrome coronario agudo sin elevación del segmento ST. Rev Esp Cardiol. 2021;74(6):544.e1–73. https://doi.org/10.1016/j.recesp.2020.12.024.
27. Ganesh R, Kebede E, Mueller M, Gilman E, Mauck KF, Mauck MM. Perioperative Cardiac Risk Reduction in Noncardiac Surgery. Mayo Clin Proc. 2021 Aug;96(8):2260–76. https://doi.org/10.1016/j.mayocp.2021.03.014 PMID:34226028

 ORCID
ORCID