Héctor J. Lacassie 1 , Mario E. Guerrero 1 y Rodrigo Montaña 1
Rev Chil Anest Vol. 39 Núm. 4 pp. 292-298|doi:
PDF|ePub|RIS
Introducción
La cirugía laparoscópica ginecológica se desarrolló al menos diez años antes que en otras especialidades. En sus inicios no fue más que un procedimiento diagnóstico, para rápidamente pasar a ser terapéutica. El desarrollo de las técnicas, equipos y experiencia de los operadores han ayudado a demostrar los innegables beneficios que aporta a las pacientes, aunque, no está libre de riesgos. La presente revisión pretende evaluar el impacto de la técnica en los diferentes sistemas corporales, describir situaciones particulares de ella, su forma de enfrentarlas y la relación con el uso de técnicas anestésicas modernas.
-
Alteraciones respiratorias
Hoy en día, el dióxido de carbono (CO2) es el principal gas utilizado en la cirugía laparoscópica por tener propiedades que lo acercan al gas ideal para este tipo de técnica. Entre ellas: su transparencia, no combustibilidad y ser muy difusible. Esta última propiedad es un arma de doble filo ya que su absorción aumenta los niveles corporales, con potenciales repercusiones sistémicas.
Los máximos niveles de absorción sistémica se alcanzan alrededor de los quince minutos de insuflación, lo que se traduce en un aumento en los niveles de CO2 espirado (ETCO2) y plasmático 1 . Este efecto es más marcado en pacientes que sufren patología concomitante y que se consideran categoría II o III de la Sociedad Americana de Anestesiología (ASA) 2 . Más aún, en estos pacientes se puede producir una gradiente mayor entre los niveles de CO2 arterial y pulmonar que en pacientes sanos. De todos modos, el CO2 absorbido no superaría el 10% del CO2 total. El principal mecanismo de hipercarbia va a estar dado por los fenómenos restrictivos pulmonares generados por una ventilación alveolar inadecuada debido a la distensión abdominal por el gas (y consecuente elevación del diafragma) y la posición de Trendelemburg que exacerbará más la restricción pulmonar. En el pulmón, se producen atelectasias que se traducen en una alteración de la relación ventilación/perfusión del tipo cortocircuito, que determinará una potencial caída de la saturación de oxígeno e hipercarbia. Por lo anterior no se recomienda para el capnoperitoneo* presiones de insuflación mayores a 15 mmHg en forma mantenida. Puede aumentarse la presión en forma transitoria, con riesgo de exacerbar los problemas respiratorios.
Los mecanismos compensatorios del aumento de los niveles de CO2 son básicamente tres: 1) compresión capilar por aumento de la presión abdominal, lo que reduce el área vascular de absorción, disminuyendo la posibilidad de difusión del gas al plasma. Esto explicaría el aumento transitorio del ETCO2 al desinflar el abdomen (disminuyendo la presión intraperitoneal); 2) aumento en la ventilación alveolar, lo que demanda aumentar en aproximadamente 30% los parámetros del ventilador mecánico (volumen corriente y frecuencia respiratoria) y 3) la capacidad del organismo de tamponar CO2, ya sea como anhídrido carbónico (H2CO3), unido a la hemoglobina (carboxihemoglobina) o ligado a proteínas plasmáticas.
Los problemas respiratorios más frecuentes suelen ser iatrogénicos, entre los que destacan: i) enfisema subcutáneo de CO2 (ocurre en alrededor de un 20% de los casos, secundario a una incorrecta instalación de la aguja de Veress); ii) neumotórax (capnotórax, cuando se comunican la cavidad peritoneal y la cavidad torácica, o neumotórax clásico si es por ruptura de bulas pulmonares); iii) neumomediastino y neumopericardio/mediastino (en estricto rigor es un capnomediastino, habitualmente secundario a un capnotórax) y iv) embolia gaseosa.
La embolia gaseosa es un problema que requiere un análisis por separado dada su gravedad.
La dosis letal 50% (DL50) de CO2 intravascular en perros es de 25 ml•kg-1 3 , a diferencia de la DL50 de aire que es de 5 ml•kg-1. Esta es la principal razón por la que se recomienda revisar acuciosamente que la línea de insuflación esté previamente cebada con CO2 y que la insuflación inicial sea a flujos bajos (1 lt•min-1). Con volúmenes de 2 ml•kg-1 de CO2 intravasculares se pueden producir arritmias e hipotensión y a la auscultación se puede evidenciar el signo semiológico de “rueda de molino”. Existen métodos más sensibles para detectar embolias como el uso de un detector doppler precordial que puede detectar volúmenes de hasta 0,5 ml•kg-1 o bien la ecocardiografía transesofágica (ETE) cuyo límite inferior de detección es de 0,02 ml•kg-1 4 . Lo más frecuentemente utilizado en el quirófano es la medición en línea del CO2 espirado (ETCO2), que da una muy buena aproximación de lo que está ocurriendo, sin necesidad de invadir a las pacientes. Este monitor revela una potencial embolia de CO2 al mostrar una caída brusca en los valores y aplanamiento de la curva del ETCO2, sin que otra causa la explique. En un estudio reciente, Kim y cols. detectaron por medio de ETE que la ocurrencia de embolia de CO2 en pacientes sanas sometidas a histerectomía laparoscópica fue de 100% comparada con la técnica abierta, en que sólo fue de 15% 5 . Todas las embolias detectadas fueron asintomáticas desde el punto de vista clínico, sin embargo, frente a esto, siempre existe el riesgo potencial de una complicación hemodinámica o bien un accidente cerebro-vascular si se produce una embolia paradojal (traspaso desde las cavidades derechas hacia las izquierdas por un cortocircuito intracardiaco, donde el más frecuente es foramen oval permeable).
El tratamiento de la embolia de CO2 masiva incluye los siguientes pasos:
-
Vaciar el capnoperitoneo.
-
Poner a la paciente en posición de Durant (posición de Trendelemburg y en decúbito lateral izquierdo): Esto busca elevar el ápex del ventrículo de manera que las burbujas de CO2 no obstruyan el tracto de salida ventricular derecho y por lo tanto el débito cardiaco no se afecte.
-
Ventilar con oxígeno 100%. Esto favorece el intercambio del CO2 por el O2 en el torrente circulatorio, minimizando el efecto de aquel en la circulación.
-
Aumentar la ventilación alveolar, para favorecer la eliminación de CO2.
-
Introducir un catéter venoso central hasta la cavidad ventricular derecha para aspirar gas que obstruya su tracto de salida.
-
Soporte hemodinámico en base a volumen y drogas vasoactivas.
-
Alteraciones cardiovasculares
El principal parámetro hemodinámico que determina la perfusión de los órganos es el débito cardíaco. La insuflación abdominal a presión positiva puede disminuir el débito cardíaco hasta en 50%, secundario a: i) compresión de la vena cava inferior; ii) secuestro sanguíneo por disminución del retorno venoso; iii) disminución del volumen de fin de diástole y iv) contribución de los anestésicos, que pueden deprimir la función miocárdica y por lo tanto, afectar el débito cardíaco. Por otra parte, factores neurohumorales (catecolaminas y CO2) y la resistencia vascular de los órganos intra abdominales producen un aumento de la resistencia vascular sistémica, lo que disminuirá más aún el débito cardíaco. Cabe hacer notar que la precarga con volumen intravascular atenúa la respuesta hipotensiva del capnoperitoneo 1 .
Las alteraciones hemodinámicas serán mayores en las pacientes cardiópatas y éstas tendrán mayor susceptibilidad a la hipercarbia, acidosis y a cambios en la presión intra abdominal, lo que determinará que estas pacientes requieran una monitorización más exhaustiva. El capnoperitoneo puede desencadenar o aumentar una disfunción diastólica.
-
Alteraciones en otros sistemas
El flujo sanguíneo a los diferentes órganos intra abdominales puede ser afectado por el aumento de la presión intra abdominal y por el tiempo quirúrgico. Así, el flujo del parénquima renal puede disminuir hasta en 50% cuando la presión intra abdominal alcanza los 20 mmHg y la circulación mesentérica disminuye en 70% cuando la presión es de 40 mmHg.
La insuflación de la cavidad abdominal compromete muy poco la circulación hepática. A nivel cerebral, las alteraciones son principalmente por el aumento en el CO2, lo que se traduce en aumento del flujo sanguíneo el que eventualmente puede aumentar la presión intracraneana. Por esta razón, la cirugía laparoscópica está contraindicada en pacientes con aumento de la presión intracraneana.
De las alteraciones del tracto digestivo que son relevantes para el anestesiólogo, la más importante son las náuseas y vómitos postoperatorios (NVPO). La cirugía de histerectomía es una de las que tiene el mayor riesgo de ocurrencia de NVPO 6 , principalmente por el tipo de cirugía. Se han ideado procedimientos laparoscópicos sin insuflación de CO2 (laparolift) 7 o bien utilizando otros gases (óxido nítrico), sin embargo, sus resultados han sido desalentadores o bien con beneficios marginales, que por ahora no justifican su incorporación en la práctica clínica.
-
Cirugía laparoscópica y embarazo
En la embarazada, la laparoscopía se ha transformado en una herramienta cada vez más común para el diagnóstico y tratamiento de las patologías no obstétricas. Aproximadamente un 2% de éstas requieren algún tipo de intervención quirúrgica durante la gestación 8 . Las intervenciones más frecuentes son la apendicectomía 9 , colecistectomía 10 y cirugía por obstrucción intestinal 11 .
A pesar de los evidentes beneficios que la cirugía laparoscópica podría tener en la embarazada, los efectos que esta técnica pudiera producir en el feto no han sido del todo aclarados. Por el momento, los estudios en animales y análisis epidemiológicos en humanos no han demostrado diferencias en los desenlaces obstétricos y neonatales, al comparar cirugía laparoscópica versus abierta 8 , aunque sí ha demostrado ventajas maternas al disminuir el dolor y el tiempo de recuperación postoperatoria 12 . Sin embargo, estas ventajas aún deben ser demostradas con evidencia más sólida. Así, lo más claro es que el resultado obstétrico dependerá de dos factores fundamentales: la condición basal de la paciente y el grado de manipulación uterina 13 , 14 .
Si bien, técnicamente el segundo trimestre del embarazo es el período más propicio para realizar un procedimiento laparoscópico, este puede ser realizado en cualquier momento si así lo amerita la situación 15 . La ubicación de los trócares estará determinada por el tamaño uterino y por la facilidad de acceso al abdomen con ellos. La presión de insuflación habitualmente utilizada es de 10 mmHg, la que puede ser aumentada hasta 15 mmHg, idealmente manteniéndola no más allá de 12 mmHg para evitar la compresión de los vasos sanguíneos que irrigan el útero y el consiguiente deterioro del flujo útero placentario 15 .
La técnica anestésica más utilizada es la anestesia general con gases halogenados. Estos últimos tienen el beneficio agregado de la tocolisis, en concentraciones mayores a una concentración alveolar mínima (MAC). McClaine y cols, demostraron en un modelo animal que la anestesia general aumenta la oxigenación sistémica y cerebral en los fetos 16 .
Con respecto a los efectos del capnoperitoneo durante el embarazo, los reportes de casos aislados de cirugía laparoscópica en pacientes embarazadas no han demostrado mayor alteración gasométrica materna 17 . Estudios en animales menores (ratas) y mayores (ovejas) han mostrado que el capnoperitoneo produce acidosis materna y fetal, a pesar de haberse incrementado la ventilación materna. Uemura y cols, demostraron en un modelo de ovejas cursando el equivalente al segundo trimestre de gestación, que el capnoperitoneo redujo el flujo útero-placentario, produciendo hipercapnia y acidosis, seguidas de hipoxia fetal y depresión cardiovascular prolongada 18 . Si bien esta información es relevante, no se pueden hacer extrapolaciones a largo plazo. Hasta el momento, la única evidencia disponible es un estudio en ratas cursando el segundo trimestre de embarazo a las que se les indujo un capnoperitoneo. En éstas, no hubo alteración en la duración del embarazo, tasa de abortos o peso al nacimiento, sin embargo, los animales expuestos al gas, mostraron mayor nivel de actividad locomotora que los controles, lo que ha sido correlacionado como un indicador de una alteración prenatal 19 . Por el momento, esta evidencia no es extrapolable al ser humano 15 y por lo tanto el embarazo per se no constituye una contraindicación de cirugía laparoscópica.
Finalmente, debido a la amplia disponibilidad de cirugía laparoscópica, la Asociación Europea de Cirugía Endoscópica (EAES) 20 y la Sociedad Americana de Cirujanos Gastrointestinales y Endoscópicos (SAGES) 15 han publicado las guías para el uso de cirugía laparoscópica durante el embarazo (Tabla 1).
Tabla 1 Recomendaciones para la realización de laparoscopía durante el embarazo 15 , 20
|
|
|
|
|
|
|
|
-
Analgesia post laparoscopía
Comentario sobre género y dolor
Múltiples estudios recientes en población anglosajona sobre género y percepción de dolor han notado que la mayoría de las condiciones dolorosas parecen ser mayores en mujeres que en hombres 21 , 22 . De hecho, el dolor de órganos viscerales sexo-específicos puede ser el resultado de la naturaleza más compleja de la región pélvica femenina y de un mayor número de condiciones fisiopatológicas asociadas directa o indirectamente a las funciones reproductivas femeninas 23 . Desde el punto de vista anatómico, existen receptores de hormonas esteroidales gonadales ubicadas en forma ubicua en las áreas del sistema nervioso central involucradas en la percepción e inhibición del dolor, tales como el área gris periaqueductal, bulbo raquídeo y el asta posterior de la médula espinal 24 . Gran parte del esfuerzo investigativo se ha concentrado en la sensibilidad somática, sin embargo, el conocimiento sobre las diferencias sexuales y hormonales ha aumentado en el campo del dolor de órganos internos 25 .
Cuando se analizan las diferencias sexuales en términos de respuesta a tratamientos analgésicos, las mujeres normales y aquéllas con dolor crónico responden mejor a la analgesia con opioides (agonistas mu y kappa) 26 y analgesia colinérgica, principalmente por el componente nicotínico a nivel espinal 27 ,28 . En cambio, los hombres responden mejor a los antiinflamatorios no esteroidales 26 .
Dolor en cirugía laparoscópica ginecológica
El dolor secundario a los procedimientos laparoscópicos es multifactorial, derivado de las incisiones cutáneas en los accesos de los trócares, la irritación peritoneal por el gas insuflado (CO2) y por la injuria quirúrgica intraperitoneal. Esto implica que los tipos de dolor que enfrentaremos son variados, encontrando dolor de tipo somático, visceral y eventualmente neuropático.
El dolor de los portales cutáneos es de tipo somático, el que puede ser bien bloqueado con la infiltración de anestésicos locales, idealmente antes de la incisión, con la finalidad de realizar una analgesia anticipatoria (preemptive). Esta práctica no se ha demostrado más eficaz que la infiltración al final de la cirugía, sin embargo, es razonable pensar que pudiese ser beneficioso, aunque sea marginal. Diferente es el uso de anestésicos locales instilados en la cavidad peritoneal al final de la cirugía. Varios autores han demostrado un descenso en el consumo de morfina al despertar y a las 24 hrs, asociado a una disminución en la incidencia de náuseas y vómitos post operatorios (NVPO) 29 y una disminución en el consumo total de morfina 30 . Otros autores han descrito beneficios en términos analgésicos si se vacía completamente el capnoperitoneo. Abbott y cols, han demostrado que vaciarlo resulta en menor omalgia a las 4 y 48 hrs post operatorias, además de requerir menos analgésicos después del alta 31 . Por su parte, vaciar el CO2 y además instilar anestésicos locales logra un beneficio analgésico a las 2 y 4 hrs post operatorias 32 . Finalmente, frente a la disyuntiva de alterar las propiedades físicas del gas, tales como temperatura y humedad, Kissler y cols, no encontraron diferencias al utilizar el gas frío y seco (el estándar hoy en día) versus la alternativa de gas tibio y húmedo 33 .
Recientemente han aparecido estudios en que se ha utilizado lidocaína sistémica en cirugía de colon por vía laparoscópica, evidenciándose una disminución en los consumos de anestésicos intraoperatorios y opiáceos post operatorios, reinicio del tránsito intestinal más precoz y estadías hospitalarias menores que los controles 34 . Lo anterior ha sido corroborado en un metanálisis que consideró cirugías intraabdominales abiertas y laparoscópicas, donde el uso de lidocaína favoreció una mejor recuperación postoperatoria (menor consumo de opiáceos y menor incidencia de NVPO), reinicio del tránsito intestinal más rápido y una menor estadía intrahospitalaria 35 . Aunque esto no ha sido aún demostrado en cirugía ginecológica, es altamente probable que así sea. Otros coadyuvantes sistémicos como los alfa-2 agonistas (dexmedetomidina) también podrían disminuir el uso de opioides intraoperatorios, favoreciendo una recuperación más corta y de mejor calidad. Aún está pendiente su evaluación en estudios de buena calidad metodológica.
Recomendaciones prácticas
Las pacientes habitualmente se ponen en posición de litotomía y Trendelemburg. Las piernas deben apoyarse en soportes anatómicos del estilo de las pierneras Allen® o similares (Figura 1). La correcta posición de ellas es alineando las articulaciones del tobillo y rodilla unilateral con el hombro contralateral. La flexión de la rodilla y cadera no debe ser de menor a 90˚ y 45˚ respectivamente (Figura 2). Habitualmente se utiliza un tope acolchado en los hombros, apoyándolo en la apófisis coracoides, para evitar que la paciente se desplace hacia cefálico en los momentos que está en posición de Trendelemburg extremo. Esto implica el riesgo de una lesión neurológica por compresión del plexo braquial, por lo que la posición debe ser adoptada cuidadosamente.

Figura 1 Pierneras para posición de litotomía.
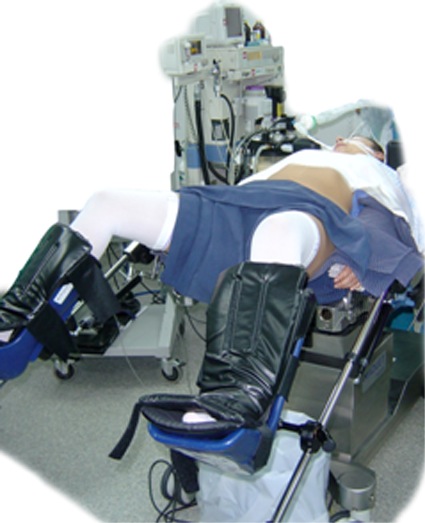
Figura 2 Alineación de las articulaciones del tobillo, rodilla y hombro contralateral.
Antes de iniciar la insuflación, se recomienda utilizar una sonda gástrica para vaciar el estómago de aire u otro contenido, ya que la instalación de la aguja de Veress puede perforar una víscera hueca dilatada, en especial en el acceso por el punto de Palmer (Palmer point o acceso subcostal izquierdo).
La utilización de capnografía en línea es un estándar de monitorización para este tipo de procedimientos, especialmente si el CO2 es el gas insuflador. Tiene el valor agregado de permitir monitorizar la ventilación alveolar en tiempo real.
La medición de temperatura es importante dado que la insuflación de gas presurizado produce un descenso en la temperatura corporal en forma significativa, que es tiempo-dependiente. Al pasar un gas de alta a baja presión, consume energía en forma de temperatura, disminuyendo ésta en el gas resultante, por lo que el peritoneo recibirá un gas frío. Los métodos de profilaxis térmica son la utilización de frazadas de aire caliente (Bair Hugger® o similar) además de la infusión de soluciones endovenosas y de irrigación entibiadas, ya sea con un sistema comercial del tipo Hotline® o bien entibiando soluciones cristaloídeas (no glucosadas) en baño maría o en un microondas.
El tromboembolismo venoso (TEV) es una importante causa de morbilidad y mortalidad en pacientes quirúrgicos. En el período perioperatorio, la inmovilidad, la injuria quirúrgica, la anestesia y la respuesta a estrés, predisponen a la ocurrencia de TEV. La cirugía ginecológica laparoscópica por patología benigna se considera de bajo riesgo, sin embargo, la tendencia hoy en día es a hacer procedimientos cada vez más complejos por vía laparoscópica, incluyendo la cirugía por cáncer. Es en este subgrupo donde la tromboprofilaxis se hace cada vez más relevante. Las recomendaciones del American College of Chest Physicians (ACCP) en lo que respecta a tromboprofilaxis en cirugía ginecológica se puede ver en la Tabla 2.
Tabla 2 Tromboprofilaxis en Cirugía Ginecológica. Tomado de Hirsh y cols 36 . HBPM: heparina de bajo peso molecular; HNFDB: heparina no fraccionada en dosis bajas; Grado 1: Beneficio del tratamiento supera claramente el riesgo y costo de la intervención. Evidencia tipo A: Evidencia de alta calidad; Evidencia tipo B: Evidencia de calidad moderada; Evidencia tipo C: Evidencia de mala calidad
| Factores de Riesgo | Recomendación para Tromboprofilaxis |
| Cirugía laparoscópica en pacientes con bajo
riesgo de TEV |
Deambulación (precoz y frecuente) (Grado 1B) |
| Cirugía laparoscópica y con factores de riesgo
para TEV |
Uno o la combinación de HBPM, HNFDB,
tromboprofilaxis mecánica (Grado 1C) |
| Cirugía extensa oncológica en pacientes con
factores de riesgo para TEV |
HBPM (Grado 1A), o HNFDB tres veces al día (Grado
1A) o compresión neumática intermitente, inmediatamente previo a la cirugía y hasta la deambulación (Grado 1A). Consideraciones alternativas: combinación de HBPM o HNFDB más tromboprofilaxis mecánica, o fondaparina (todas Grado 1C) |
Finalmente, como la histerectomía aumenta el riesgo para presentar NVPO 6 , es prácticamente un estándar utilizar profilaxis antiemética para estos procedimientos. Hoy en día se recomienda utilizar un antiemético profiláctico (dexametasona 4 mg u ondansetron 4 mg, endovenosos) si existiesen 2 a 3 factores de riesgo (factores de riesgo son: sexo femenino, historia de cinetosis, ser no-fumadora, uso de opiáceos perioperatorios, cirugía laparoscópica y antecedentes de NVPO previos) o bien doble profilaxis si tiene más de 3 factores. Además se recomienda evitar el uso de óxido nitroso (N2O) y gases halogenados a favor de una anestesia endovenosa total (TIVA) si los factores de riesgo de NVPO son altos 6 ,37 .
Conclusión
Si bien la técnica laparoscópica ha demostrado ser una técnica segura y que proporciona beneficios claros para las pacientes al compararla con su contraparte abierta, no está exenta de complicaciones. Un alto grado de vigilancia y de sospecha permite prevenir y corregir prontamente alteraciones iatrogénicas que cada vez están siendo mejor identificadas y pesquisadas.
Bibliografía
- Joris JL. Anesthesia for Laparoscopic Surgery, Anesthesia, 6 Edition. Edited by Miller R. Philadelphia, Elsevier Churchill Livingstone 2005; pp 2285-2306.
- Wittgen CM, Andrus CH, Fitzgerald SD, Baudendistel LJ, Dahms TE, Kaminski DL. Analysis of the hemodynamic and ventilatory effects of laparoscopic cholecystectomy. Arch Surg 1991; 126: 997-1000; discussion 00-1.
- Graff TD, Arbegast NR, Phillips OC, Harris LC, Frazier TM. Gas embolism: a comparative study of air and carbon dioxide as embolic agents in the systemic venous system. Am J Obstet Gynecol 1959; 78: 259-265.
- Furuya H, Suzuki T, Okumura F, Kishi Y, Uefuji T. Detection of air embolism by transesophageal echocardiography. Anesthesiology 1983; 58: 124-129.
- Kim CS, Kim JY, Kwon JY, Choi SH, Na S, An J, et al. Venous air embolism during total laparoscopic hysterectomy: comparison to total abdominal hysterectomy. Anesthesiology 2009; 111: 50-54.
- Apfel CC, Korttila K, Abdalla M, Kerger H, Turan A, Vedder I, et al. A factorial trial of six interventions for the prevention of postoperative nausea and vomiting. N Engl J Med 2004; 350: 2441-2451.
- Goldberg JM, Maurer WG. A randomized comparison of gasless laparoscopy and CO2 pneumoperitoneum. Obstet Gynecol 1997; 90: 416-420.
- Mazze RI, Kallen B. Reproductive outcome after anesthesia and operation during pregnancy: a registry study of 5405 cases. Am J Obstet Gynecol 1989; 161: 1178-1185.
- Halvorsen AC, Brandt B, Andreasen JJ. Acute appendicitis in pregnancy: complications and subsequent management. Eur J Surg 1992; 158: 603-606.
- Scott LD. Gallstone disease and pancreatitis in pregnancy. Gastroenterol Clin North Am 1992; 21: 803-815.
- Gurbuz AT, Peetz ME. The acute abdomen in the pregnant patient. Is there a role for laparoscopy? Surg Endosc 1997; 11: 98-102.
- Hart RO, Tamadon A, Fitzgibbons RJ, Jr., Fleming A. Open laparoscopic cholecystectomy in pregnancy. Surg Laparosc Endosc 1993; 3: 13-16.
- Al-Fozan H, Tulandi T. Safety and risks of laparoscopy in pregnancy. Curr Opin Obstet Gynecol 2002; 14: 375-379.
- Obstetric Anesthesia, Obstetric Anesthesia. Principles and Practice. Edited by Chestnut. D. St Louis, MO, Mosby-Year Book Inc., 1994, pp 262.
- Guidelines for Diagnosis, Treatment, and Use of Laparoscopy for Surgical Problems during Pregnancy, 2007. Diciembre 2009 (fecha de acceso). http://www.sages.org/publications/publication.php?id=23.
- McClaine RJ, Uemura K, de la Fuente SG, Manson RJ, Booth JV, White WD, et al. General anesthesia improves fetal cerebral oxygenation without evidence of subsequent neuronal injury. J Cereb Blood Flow Metab 2005; 25: 1060-1069.
- Bhavani-Shankar K, Steinbrook RA, Brooks DC, Datta S. Arterial to end-tidal carbon dioxide pressure difference during laparoscopic surgery in pregnancy. Anesthesiology 2000; 93: 370-373.
- Uemura K, McClaine RJ, de la Fuente SG, Manson RJ, Campbell KA, McClaine DJ, et al. Maternal insufflation during the second trimester equivalent produces hypercapnia, acidosis, and prolonged hypoxia in fetal sheep. Anesthesiology 2004; 101: 1332-1338.
- de la Fuente SG, Pinheiro J, Gupta M, Eubanks WS, Reynolds JD. Early postnatal behavior deficits after maternal carbon dioxide pneumoperitoneum during pregnancy. Surg Endosc 2003; 17: 1823-1825.
- Neudecker J, Sauerland, S, Neugebauer E, et al. The European Association for Endoscopic Surgery clinical practice guideline on the pneumoperitoneum for laparoscopic surgery. Surg Endosc 2002; 1121-1143.
- LeResche L. Epidemiologic Perspectives on Sex Differences in Pain, Progress in pain research and management; v. 17. Edited by Fillingim RB. Seattle, IASP Press, 2000, pp 233-250.
- Fillingim RB, King CD, Ribeiro-Dasilva MC, Rahim-Williams B, Riley JL, 3rd. Sex, gender, and pain: a review of recent clinical and experimental findings. J Pain 2009; 10: 447-485.
- Bonica JJ. The Management of Pain, 2nd Edition. Philadelphia, Lea & Febiger, 1990.
- Sternberg WF, Wachterman MW. Experimental Studies of Sex-Related Factors Influencing Nociceptive Responses: Nonhuman Animal Research, Sex, gender, and pain. Progress in pain research and management; v. 17. Edited by Fillingim RB. Seattle, IASP Press, 2000, pp 71-88.
- Berkley KJ. Sex differences in pain. Behav Brain Sci 1997; 20: 371-80; discussion 435-513.
- Miaskowski C, Gear RW, Levine JD. Sex-Related Differences in Analgesic Response, Sex, gender, and pain. Progress in pain research and management; v. 17. Edited by Fillingim RB. Seattle, IASP Press, 2000, pp 209-230.
- Chiari A, Tobin JR, Pan HL, Hood DD, Eisenach JC. Sex differences in cholinergic analgesia I: a supplemental nicotinic mechanism in normal females. Anesthesiology 1999; 91: 1447-1454.
- Lavand’homme PM, Eisenach JC. Sex differences in cholinergic analgesia II: differing mechanisms in two models of allodynia. Anesthesiology 1999; 91: 1455-1461.
- Goldstein A, Grimault P, Henique A, Keller M, Fortin A, Darai E. Preventing postoperative pain by local anesthetic instillation after laparoscopic gynecologic surgery: a placebo-controlled comparison of bupivacaine and ropivacaine. Anesth Analg 2000; 91: 403-407.
- Buck L, Varras MN, Miskry T, Ruston J, Magos A. Intraperitoneal bupivacaine for the reduction of postoperative pain following operative laparoscopy: a pilot study and review of the literature. J Obstet Gynaecol 2004; 24: 448-451.
- Abbott J, Hawe J, Srivastava P, Hunter D, Garry R. Intraperitoneal gas drain to reduce pain after laparoscopy: randomized masked trial. Obstet Gynecol 2001; 98: 97-100.
- Readman E, Maher PJ, Ugoni AM, Gordon S. Intraperitoneal ropivacaine and a gas drain: effects on postoperative pain in laparoscopic surgery. J Am Assoc Gynecol Laparosc 2004; 11: 486-491.
- Kissler S, Haas M, Strohmeier R, Schmitt H, Rody A, Kaufmann M, et al. Effect of humidified and heated CO2 during gynecologic laparoscopic surgery on analgesic requirements and postoperative pain. J Am Assoc Gynecol Laparosc 2004; 11: 473-477.
- Kaba A, Laurent SR, Detroz BJ, Sessler DI, Durieux ME, Lamy ML, et al. Intravenous lidocaine infusion facilitates acute rehabilitation after laparoscopic colectomy. Anesthesiology 2007; 106: 11-8; discussion 5-6.
- Marret E, Rolin M, Beaussier M, Bonnet F. Meta-analysis of intravenous lidocaine and postoperative recovery after abdominal surgery. Br J Surg 2008; 95: 1331-1338.
- Hirsh J, Raschke R. Heparin and low-molecular-weight heparin: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest 2004; 126: 188S-203S.
- Gan TJ, Meyer T, Apfel CC, Chung F, Davis PJ, Eubanks S, et al. Consensus guidelines for managing postoperative nausea and vomiting. Anesth Analg 2003; 97: 62-71.