Ricardo Fuentealba Ramírez1,2,3,*, Luciano Bravo Pérez4.
Recibido: 19-08-2022
Aceptado: 24-08-2022
©2022 El(los) Autor(es) – Esta publicación es Órgano oficial de la Sociedad de Anestesiología de Chile
Revista Chilena de Anestesia Vol. 51 Núm. 6 pp. 636-642|https://doi.org/10.25237/revchilanestv5127091639
PDF|ePub|RIS
Hemodynamic inestability in obstetric patient
Abstract
The hemodynamic instability in the pregnant patient is a challenge for the treating team, due to the physiological peculiarities of her condition and the emotional impact of her care. Considering the increase in the mortality of pregnant women worldwide in developed countries due to múltiple factors associated with an inadequate level of care, anesthesiologists have an essential role within this team. Early recognition and timely treatment of a pregnant or postpartum patient is required. The evaluation of the hemodynamic status only with the clinic in changing situations may be insufficient in the obstetric patient for an adequate management, especially in pathophysiological conditions and with the impact of the pharmacological action of anesthesia. Therefore, monitoring at the patient’s bedside, mainly through monitoring of cardiac output (CO), myocardial response and volemia status with minimally invasive cardiac output monitors, cardiac and pulmonary ultrasound evaluation allow a management that has an impact on survival.
Resumen
La inestabilidad hemodinámica en la paciente gestante constituye un desafío para el equipo tratante, por las peculiaridades fisiológicas que ofrece su condición y por el impacto emocional que genera su atención. Considerando el aumento de la mortalidad de la embarazada a nivel mundial en países desarrollados debido a factores múltiples asociados a un nivel de cuidados no adecuados, es que los anestesiólogos cumplen un rol fundamental dentro de este equipo. Se requiere la detección precoz y tratamiento oportuno de una paciente gestante o puérpera. La evaluación del estado hemodinámico solo con la clínica en situaciones cambiantes puede ser insuficiente en la paciente obstétrica para un adecuado enfrentamiento, especialmente en condiciones fisiopatológicas y con impacto de la acción farmacológica de la anestesia. Es por esto que la monitorización al lado del paciente, principalmente a través de la vigilancia del gasto cardíaco (GC); la respuesta miocárdica y el estado de la volemia con monitores de gasto cardíaco mínimamente invasivos; la evaluación ecográfica cardíaca y pulmonar permiten un enfrentamiento que impacta en la sobrevida.
-
Introducción
La inestabilidad hemodinámica en la paciente gestante constituye un desafío para el equipo que participa en su atención, debido a las particulares condiciones fisiológicas que ofrece su condición y por el impacto emocional que genera su atención. Los anestesiólogos cumplen un papel fundamental dentro de este equipo, por su formación y por el rol que cumplen nuestra especialidad; durante la asistencia anestésica del fin de la gestación, nos vamos a ver expuestos a enfrentarnos a la compleja situación que significa la reanimación de una paciente, gestante o puérpera, críticamente enferma.
-
Realidad mundial
Durante el año 2014, se publicó un análisis multicéntrico realizado por la organización mundial de la salud en 115 países con datos recopilados desde el año 2003 al 2012 en donde se analizaron más de 2,6 millones de muertes maternas en países con distinto nivel de desarrollo y distinto nivel de cuidado obstétrico. Las hemorragias como causa global, los trastornos hipertensivos en todo su espectro y la sepsis constituyen más de la mitad de las causas de mortalidad materna. Se agregan las enfermedades crónicas descompensadas, enfermedades pulmonares y miocardiopatías específicas[1].
Si bien las tasas de mortalidad materna aún siguen presentando disparidad dependiendo del acceso a cuidados obstétricos de alto estándar, ha ido descendiendo a nivel mundial en forma persistente desde el siglo pasado tanto en países con alto como con bajo nivel de cuidado obstétrico.
En países desarrollados se observa con preocupación el estancamiento de las tasas de mortalidad materna o un leve incremento en las mismas que se adjudica a varios factores; el aumento del número de mujeres con enfermedades crónicas estables, bajo tratamiento, con el objetivo de ser madres, incremento del número de primíparas añosas y técnicas de fertilización asistida que posibilitan el embarazo más allá del período de fertilidad natural[2].
En cuanto a la realidad en países latinoamericanos la tasa de mortalidad materna presenta valores muy disimiles. En nuestro país, durante las ultimas décadas la mortalidad materna se posiciona alrededor de 10 por cada 100.000 nacimientos, siendo en el período entre 2002 y 2015 en donde se describieron las siguientes causas: 1) enfermedades concurrentes; 2) hipertensión arterial; 3) embarazo ectópico; 4) hemorragia y 5) embolias. A su vez, el análisis por edad muestra que la razón de mortalidad materna asociada a enfermedades concurrentes, hipertensión arterial, aborto y hemorragia posparto aumenta en los extremos de edad materna, siendo mayor en el quinquenio superior[3].
En el caso particular de la sepsis, desde la década de los 90 sigue afectando aproximadamente de 4 a 10 de cada 10.000 nacimientos vivos. La mortalidad y la incidencia parecen estar aumentando a pesar de la estandarización de los cuidados. Los estudios y análisis de causa muestran que en más del 60% de los casos de fallecimiento se observaron cuidados subóptimos. En todas estas situaciones, como anestesiólogos, nos veremos involucrados en algún punto de la atención de la paciente gestante, y por lo tanto, nuestras decisiones y acciones serán fundamentales para aumentar la sobrevida[4].
-
Consideraciones fisiológicas cardiovasculares propias del embarazo
El sistema cardiovascular presenta cambios fisiológicos durante el embarazo que lo preparan para aumentar su gasto cardíaco, disminuir las resistencias vasculares sistémicas y preparar la hemodinámia materna para asimilar un nuevo lecho vascular, como el placentario, tolerar el influjo hormonal sobre el tono vascular y compensar las pérdidas hemáticas durante parto. A pesar de que es una condición normal dentro del ciclo de vida de la mujer, puede considerarse una condición fisiopatológica debido al mayor riesgo que implican estos cambios y la labilidad potencial que presentan frente a agresiones, es por esto que la ASA ha clasificado al embarazo como categoría II.
Cuando se analiza el comportamiento del corazón de la embarazada sana es útil analizar la relación entre presión y volumen a nivel del ventrículo izquierdo (VI). Inicialmente, la dis- tensibilidad del VI es semejante a la distensibilidad normal de la persona no gestante. Sin embargo, el cierre de la válvula mitral en la embarazada ocurre con un volumen de fin de diástole 40% mayor a la paciente no embarazada, la apertura de la válvula aórtica se produce a una presión menor que la no embarazada, fundamentalmente, por una menor resistencia vascular sistémica y a una presión arterial sistémica menor a la no embarazada. Es importante destacar que el volumen telesisto- lico no se modifica, por lo que el aumento en el gasto cardíaco es secundario a un mayor volumen eyectivo (± 25%) en conjunto a una mayor frecuencia cardíaca (± 25%). Estos cambios son producidos durante el período que dura el embarazo, por lo que el estiramiento crónico de la fibra no representa mayor contractilidad miocárdica (la pendiente de la curva no se modifica en el gráfico de presion volumen del VI) a diferencia de una condición aguda que, según la ley de Frank Starling, un mayor estiramiento determina mayor contractilidad. Todos estos cambios determinan que la paciente obstétrica sea dependiente del gasto cardíaco para sostener su presión de perfusión.
En cuanto a las resistencias vasculares sistémicas, la actividad hormonal mediada por progesterona y estrógenos circulantes determina vasodilatación periférica, aumento de la actividad de la NO sintetasa y una caída del 50% de la actividad del eje renina angiotensina aldosterona[5]. Estos cambios generan como consecuencia un estado hemodinámico dominado por la vasodilatación y el aumento del gasto cardíaco que, a pesar de que no constituye un estado fisiopatológico, como la sepsis, pero compartiendo las mismas características, sí alteran las escalas de detección precoz, teniendo que modificarse para no sobrediagnosticar o subestimar una entidad grave como la sepsis, como se describe en el SOS (Sepsis in Obstetric Score)[6].
La respuesta hemodinámica que puede observarse con el aumento de la precarga, en la mujer no gestante, está limitada por la compresión del útero grávido, siendo mayor a medida que se acerca al final de la gestación, situación que también puede influir en la evaluación de la paciente y en la subesti- macion de signos clínicos de gravedad que permitan la detección de alguna patología potencialmente grave. La suma de condiciones, normales en una gestante, pero exclusivas de este grupo, determinan que deba recurrirse a elementos como la evaluación de la precarga, gasto cardíaco y resistencia con métodos diagnósticos a lado de la paciente[7].
-
Evaluación clínica y escalas de gravedad
La clínica va a depender de la condición patológica (Tabla 1) que determine el colapso hemodinámico materno[8]. En caso de predominar una caída de las resistencias periféricas, incrementando el estado de vasodilatación propia de la condición, o una caída del gasto cardíaco, ya sea por caida de la precarga que condicione una caída del volumen telediastólico o una caída de la contractilidad, va a determinar la presencia de signos clínicos de baja perfusión, incluso si por mecanismos compensatorios es sostenida la macrohemodinamia, ya que el aumento del consumo de oxígeno basal de la paciente gestante, generará en forma precoz una deuda de oxígeno que determinará una redistribución del flujo y aumento del trabajo respiratorio para aumentar el aporte de oxígeno. Si no hay detección precoz, esto llevará inevitablemente a la hipoperfusión sistémica, al deterioro del binomio feto placentario y al fallo multiorgánico de la madre.
Con el objetivo de dar respuesta dentro de la evaluación clínica de una gestante o de una puérpera con signos clínicos de deterioro, es que las escalas de gravedad de patologías que determinan riesgo de morbimortalidad y que se expresan en forma de inestabilidad hemodinámica han sido modificadas, incorporando los cambios por sistemas, propios de la condición gravídica, con el objeto de detectar de forma precoz el deterioro clínico.
Una de las escalas más importantes de la MEOWS, cuya aplicación basada en elementos de la evaluación física ha demostrado 89% de sensibilidad y 78% de especificidad de detectar la posibilidad de morbimortalidad de las pacientes gestantes. Ésta escala de fácil aplicación divide los signos clínicos, encontrados en la evaluación de la paciente en colores rojo, verde, amarillo, permitiendo identificar en forma simple la posibilidad de presentar deterioro clínico[9].
En el caso de la sepsis, en el consenso de sepsis III de 2016[10], se modificó en forma significativa la evaluación inicial del paciente, dando importancia a la aplicación del SOFA y del quickSoFA para la detección precoz de la sepsis, simplificando además la presencia de shock con un criterio perfusional y eliminando el concepto de sepsis severa. Este criterio de deteccion precoz, fue refrendando y mantenido en la última edición de la campaña para sobrevivir a la sepsis del 2021[11]. Ésta valiosa herramienta fue adaptada, incorporando los cambios fisiológicos propios del embarazo, por las guías SOMANZ[8]. Ésta adaptación a las escalas SOFA y qSOFA han permitido aumentar la capacidad de detactar a la paciente críticamente enferma por sepsis. Dado que la aplicación de las escalas originales no te- nian suficiente evidencia durante el embarazo y el puerperio, ésta adaptacion permitió hacer un enfrentamiento precoz y así tomar medidas terapéuticas dirigidas a disminuir la mortalidad en este caso por sepsis materna.
Signos clínicos frecuentemente encontrados en entidades patológicas durante la gestación y puerperio.
Tabla 1. Posibles causas de deterioro clínico en la gestante y puérpera y sus signos clínicos[8]
| Embolia pulmonar aguda | Hipotensión, taquipnea, taquicardia, febrícula |
| Embolia de líquido amniótico | Hipotensión, taquicardia, hemorragia |
| Pancreatitis aguda | Fiebre, náuseas, vómitos, dolor abdominal |
| Hígado graso agudo del embarazo | Fatiga, náuseas, vómitos, dolor abdominal, ictericia, alteración del nivel de consciencia |
| Reacciones adversas a medicamentos, fiebre por medicamentos | Hipotensión, bradicardia relativa, fiebre, exantema, angioedema |
| Insuficiencia hepática aguda relacionada con fármacos o viral | Ictericia, náuseas, vómitos, alteración del nivel de conciencia, dolor abdominal |
| Insuficiencia suprarrenal aguda | Debilidad, fatiga, náuseas, anorexia, pérdida de peso, hipotensión, fiebre |
| Insuficiencia pituitaria aguda | Hipotensión, bradicardia relativa, poliuria, polidipsia |
| Condiciones autoinmunes | Fiebre leve, erupción cutánea, artritis, ojos o boca seca, úlceras en la boca, serología diagnóstica |
| Hemorragia oculta incluyendo embarazo ectópico | Hipotensión, taquicardia, febrícula |
| Neoplasia maligna diseminada | Fiebre de bajo grado, pérdida de peso |
| Trombosis pélvica | Dolor pélvico, fiebre |
| Reacciones transfusionales | Fiebre alta, escalofríos, arritmias, taquipnea, hipotensión, erupción cutánea, hemorragia, hematuria |
-
Evaluación hemodinámica al lado del paciente
Aparte de los cambios propios del embarazo, uno de los elementos a considerar para evaluar correctamente el volumen intravascular y volumen sistólico, con sus territorios estresables y no estresables, es lo rápido que pueden producirse los cambios hemodinámicos. Una paciente séptica durante el parto o cesárea puede sangrar presentando compromiso de la macro- hemodinamia de rápida instalación, cambiando en cosa de minutos el modelo de choque, desde distributivo a hipovolémico, debido a una pérdida del volumen sistólico por una disminución brusca de la precarga por sangrado que superó las fases iniciales de compensación. Si se agrega el efecto que tiene la anestesia neuroaxial o general sobre los vasos de capacitancia y en el tono vascular, nos entrega una situación fisiopatológica en que la sola evaluación clínica de la paciente nos puede generar error al estimar el componente predominante del choque y así definir la necesidad de volemizacion o de vasoconstrictores para poder normalizar la macrohemodinamia, manteniendo la perfusión tisular y preservando la función cardíaca. La literatura recomienda evaluar metas hemodinámicas dinámicas para decidir este dilema. Entre ellas, la variabilidad de la pletismografía; el delta de presión de pulso (Delta Pp) o la elevación pasiva de las piernas para generar una autotransfusión del territorio venoso, ésta acción diagnóstica para evaluar la respuesta a un aumento brusco de la precarga, puede verse alterada por la compresion del útero grávido.
Para una evaluación completa debemos, además, evaluar la función cardíaca, evaluando no solo la necesidad de volemización, sino también la tolerancia a ésta. En el caso de una paciente que padece preeclamsia severa que desarrolla durante la evolución de su enfermedad una disfunción diastólica del ventrículo izquierdo, una volemización no juiciosa podría conducir a un aumento del agua libre intratorácica y con el consecuente edema pulmonar agudo con compromiso de la oxigenación. Es por eso que como especialistas debemos disponer de elementos que nos permitan complementar la clínica del paciente, con elementos de mayor objetividad, siempre que nos enfrentamos a una embarazada con hemodinamia inestable.
-
Monitores de gasto cardiaco mínimamente invasivos
Existen varios tipos de monitores de gasto cardíaco mínimamente invasivos, que se clasifican según la forma de medir, basados en modelos matemáticos y físicos distintos, el gasto cardíaco, el volumen stroke (VS) y las resistencias periféricas.
Durante las últimas 2 décadas estos monitores han ganado importancia en obstetricia, a pesar de su alto costo y que han sido transferido desde la esfera de la medicina crítica y cardiovascular, han ganado su espacio en pacientes con patología cardíaca previa. Lorello et al[12], publicó el manejo de 2 pacientes portadoras de miocardiopatía periparto con resultados favorables, en quienes la vigilancia continua del gasto cardíaco permitió evaluar en forma precoz la caída del gasto cardíaco y el aumento de la resistencia periférica, lo que permitió tomar medidas precoces frente al compromiso hemodinámico.
Los monitores basados en bioimpedancia, son de fácil uso, pero su dispersion con el gold estándar, puede llegar a cerca de 30% en la paciente obstétrica. El monitor LIDCO, permite evaluar el GC por análisis de la curva de pulso, pero requiere calibración a través de una inyección de litio.
El monitor PICCO, funciona bajo el principio de la termodilución transpulmonar, es de raro uso en obstetricia, ya que requiere la instalación de una línea arterial femoral y de un CVC. Es de utilidad en la UCI cuando no necesitamos medir la saturación venosa mixta ni saber la presión de eclavamiento pulmonar. Su uso logra mayor utilidad en pacientes sépticos con aumento del agua torácica extrapulmonar.
El monitor basado en el análisis matemático de la integral de curva de pulso en una línea arterial radial llamado Flotrac (Edwars), permite el uso al lado del paciente, ya que no requiere CVC, no requiere calibración y permite tener el VS en forma precoz frente a los cambios hemodinámicos que se pueden observar tanto en una gestante sana en contexto de una urgencia obstétrica como en una paciente con patología cardíaca previa o del ámbito séptico que se someta a un trabajo de parto o una cesárea. A pesar de que este dispositivo fue creado para pacientes con anestesia general y bloqueo neuromuscular, su uso se ha extendido a pacientes en obstetricia con anestesia neuroaxial.
En la paciente sana, los cambios hemodinámicos más importantes ocurren en la induccion de la anestesia regional, la compresion aortocava por el útero grávido, el uso de drogas oxitócicas, y los efectos del uso de vasoactivos durante la operación cesárea.
En estudios pequeños que describen la posición de la paciente, estos monitores permitieron vigilar en directo el VS , RVS y el gasto cardíaco, usando los fluidos de precarga y asociado al uso racional de medicamentos vasopresores, permitiendo así, preservar el glicocálix, que es dañado por la sobrevolemización. Esta es una de las bases fisiopatologicas y bioquímicas del daño al endotelio vascular y fuga capilar de fluidos al intersticio[13],[14].
En un trabajo publicado por Rosseland et al.[15], utilizando el monitor LIDCOplus, comparó el uso de uterotónicos en dosis equipotentes, 5UI de oxitcina eran equivaletes a 100 microgramos de carbetocina en cuanto a la respuesta hemodiná- mica. Dentro de los resultados destaca la constante caída de las RVS, un aumento compensatorio de la frecuencia cardíaca y el consecuente aumento de GC lo interesante de este estudio es que en el grupo control hubo un aumento del VS posterior al nacimiento por liberación de la compresion aortocava, en los grupos de ensayo este efecto fue mínimo, esto sería explicable por efecto hemodinamico del uterotonico oxitocico.
En otro pequeño, pero interesante estudio, Otavio et al.[16], evaluaron mediante el uso del monitor por análisis de onda de pulso, Flotrac, el efecto hemodinámico de la anestesia espinal, con precarga y uso de vasopresores según necesidad, esto per- mitio concluir, que posterior al uso de AE para cesárea se produce una importante caída del VS y la-RVS con aumento de la frecuencia cardíaca. Estos efectos serían atenuados con el uso de precarga de fluidos y vasoactivos, es interesante que vuelve a producirse en forma constante, una importante fluctuación del VS luego del nacimiento.
Los monitores de gasto cardíaco minimimante invasivos, por lo tanto, son prometedores en la evaluación de pacientes con cambios rápidos hemodinámicos, en pacientes obstétricas sanas y pacientes con patología agregada que determinen por sí sola alteración de la hemodinamia (Figura 1).
-
Ecografía cardíaca y pulmonar al lado del paciente
La ecocardiografía representa uno de los avances más importantes en la monitorización de paciente crítico, tanto en el contexto perioperatorio como en UCI, siendo un monitor no invasivo en tiempo real. La ecografía al lado del paciente, con sus distintas aplicaciones, ha ganado un espacio en la toma de decisiones clínicas, que en este momento en medicina critica y anestesia es indiscutible. Su uso, entrenamiento y aplicabilidad ha tenido un aumento explosivo.
En la embarazada normal se producen cambios a nivel cardiovascular desde el inicio del embarazo, estos cambios anatómicos y hemodinámicos pueden ser visualizados por la ecocar- diografía (Tabla 2)[17].
Existen distintos protocolos para evaluar al paciente en el lugar de atención a través de dispositivos cada vez más porta- tiles, que varían de complejidad para su aplicación en cuanto a si entregan valores cuantitativos y/o cualitativos, cuyo objetivo es dar respuestas sobre el estado hemodinámico, evaluar la respuesta cardíaca, evaluar la respuesta a fluidos y realizar imagen pulmonar evaluando causas de alteración de la oxigenación y del trabajo respiratorio. En una publicacion reciente de Cabrera y cols.[18], se analizó compromiso hemodinámico con ecocardiografía intraoperatoria en 124 pacientes, en los cuales en todos, al menos se logro obtener una ventana que permitió tomar una decisión o un cambio en la terapeutica , la causa mas frecuente de inestabilidad en este grupo fue la hipovolemia. Lo interesante es que permitió detectar a través de la medición del gasto cardíaco situaciones de origen cardiogénico que cambiaron el manejo y el resultado.
La idea es, frente a desafíos hemodinámicos, buscar una respuesta con la ecoscopia y así decidir la terapia más adecuada. ¿Cuál es el estado de la volemia?; ¿Cómo se contrae el corazón?; ¿Existe otra causa que explique el problema en el estado hemodinámico (por ejemplo, derrame o taponamiento cardíaco)?. Existe un paradigma aplicado a la generalidad de los pacientes, incluidas las pacientes obstétricas, como en estado crítico y es que cada vez que un paciente está hipotenso su tratamiento es, a todo evento, la administración de fluidos de cualquier tipo. Esto en los enfermos que realmente requieren volumen o un sangrado evidente puede ser beneficioso, pero en los casos en que el paciente está normovolémico o hipervolémico la administración de volumen puede ser ineficaz o francamente deletérea. Así que un punto muy importante que ha enseñado la ecocardiografía focalizada es que hipotensión no es sinónimo de hipovolemia[19].
-
Protocolos ecocardiográficos
El protocolo POCUS permite obtener en forma cualitativa la contractilidad, la relación entre las cavidades y el estado del intravascular a través de la medición de la vena cava inferior. Distintos protocolos más avanzados, como RUSH y FATE, permiten obtener mediciones cuantitativas para obtener el gasto cardíaco y estimar las presiones de llenado a través de la medición del doppler pulsado del flujo a traves de las válvulas auri- culoventriculares.
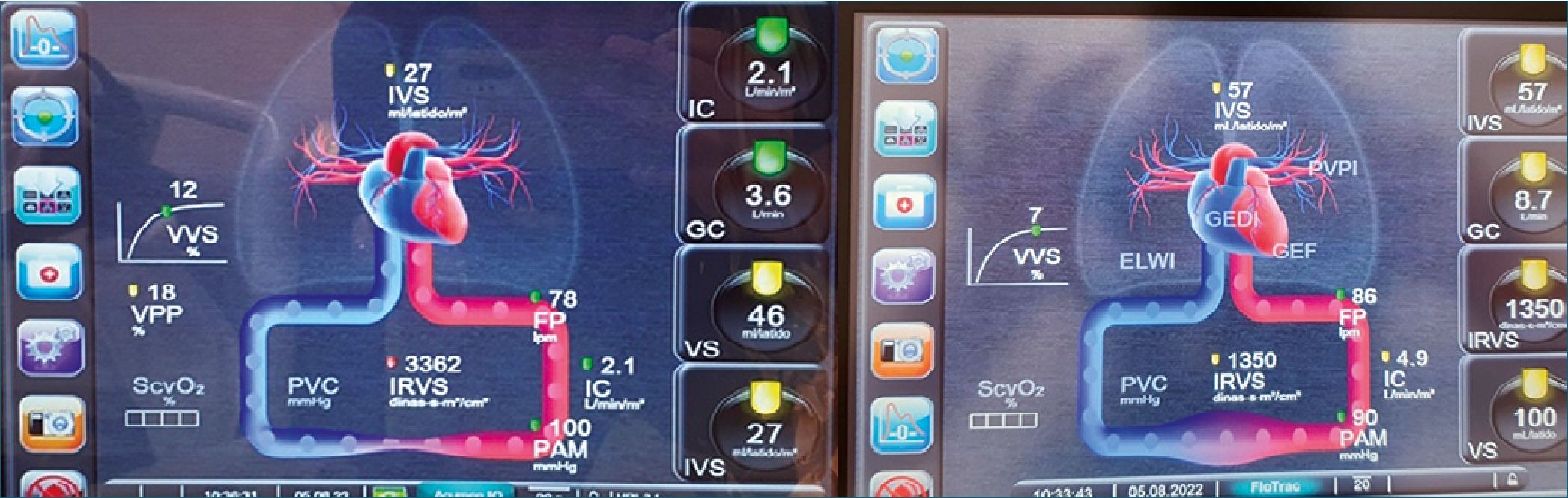
Figura 1. Ejemplos de vigilancia hemodinámica con monitor de gasto cardíaco mínimamente invasivo. En la imagen 1 se observa a la izquierda el ejemplo de choque hipovolémico, con IRVS altas, volumen stroke (VS) bajos y con VVS (variabilidad de volumen sistolico) y DPP (delta presión de pulso) en rangos de respuesta a volumen. En la imagen de la derecha, se observa un patrón distinto con IRVS bajas, VVS en rangos de no respuesta a volumen, y patrón hipervolemico con GC y VS altos, típicos de un patrón distributivo.
Tabla 2. Cambios ecográficos normales en la embarazada
| Sin cambios en el embarazo | Aumentado en el embarazo | Normativo en el embarazo |
| Fracción de eyección | Volumen ventrículo izquierdo al final de diástole | Derrame pericárdico (a menudo leve) |
| Fracción de acortamiento
Peak de velocidad sistólica miocárdica Strain longitudinal Índice E/E’ Estimación presión arterial sistólica pulmonar |
Masa ventrículo izquierdo
Gasto cardíaco Área diastólica ventrículo derecho Volumen aurícula izquierda Tamaño aurícula izquierda Tamaño aurícula derecha Dimensión de los anillos valvulares Integral de tiempo de velocidad aortica y pulmonar |
Pseudodiscinecia |
| Cuadro comparativo de los cambios que pueden ser considerados normales en la evaluacion ecográfica de una gestante sana, estos cambios fuera del contexto del embarazo suelen verse en condiciones patológicas. | ||
Otra herramienta de fácil aplicación es el doppler tisular, que a través de la interpretación de las. ondas a’, e’ y s’ se puede estimar la función sistólica y diastólica de ambos ventrículos. En un estudio[20] se evaluó la función del ventrículo derecho después de una anestesia espinal a través de la medición de s’, resultando en una disminución significativa de ésta posterior de una anestesia espinal en pacientes no obstétricas. Se debe considerar que de una buena función del ventrículo derecho depende la precarga del ventriculo izquierdo. A pesar de que éste estudio es pequeño, propone una interesante herramienta para evaluar el VD cuando el clínico se enfrenta a una patología obstétrica que comprometa la hemodinamia en forma aguda. En un reporte de caso, decrito por Fuentealba y cols[21], en una paciente con colapso súbito hemodinámico, la ecocardiografía realizada al lado del paciente permitió detectar signos ecográficos de choque obstructivo como dilatación del ventrículo derecho, alteración de las presiones de llenado, además de aumento de la FE del VI con signos clásicos de cavidades izquierdas de tamaño disminuido , que en conjunto con la clínica permitieron plantear la sospecha diagnóstica de embolia amniótica y planificar su manejo posterior en UCI con resultado favorable.
En pacientes con patología agregada, como preeclampsia, el uso de ecocardiografía y ecografía pulmonar permite una valoración adecuada de las presiones de llenado del ventrículo izquierdo, de la contractilidad y de la volemizacion adecuada. Además, podemos evaluar la presencia de líneas b, sugerente de congestión pulmonar en el mapeo ecográfico pulmonar. Para el diagnóstico diferencial con tromboembolismo pulmonar ésto cobra especial importancia en el paciente con preeclampsia severa con inestabilidad hemodinámica que presenta disnea asociada al cuadro[22].
En la paciente con preeclampsia severa, la alteración del endotelio vascular, la alteración de la función renal, el estado intravascular con tendencia a la hipovolemia, y la alteración de la relajación ventricular, genera una condición clínica en la cual es extremadamente difícil y arriesgado tomar decisiones solo con la clínica. En este contexto la ecocardiografía al lado del paciente y los monitores de GC mínimamente invasivos ofrecen elementos fundamentales en la toma de decisiones clínicas, frente a una paciente con inestabilidad hemodinámica, considerando el impacto negativo que tiene sobre este grupo de pacientes una volemizacion no controlada.
-
Conclusiones
Las pacientes obstétricas constituyen un desafío para el anestesiólogo, considerando la mortalidad de la embarazada a nivel mundial y en los países desarrollados que se ha ido incrementando por factores múltiples y que se asocia a un nivel de cuidados no adecuados. Es por ésto que se requiere la detección precoz y tratamiento oportuno de una paciente gestante o puerpera que presenta compromiso hemodinámico. Los cambios cardiovaculares fisiológicos del embarazo deben ser considerados para la correcta evaluación de la situación de riesgo. Debido a los cambios rápidos entre modelos fisiopatológicos de choque en una paciente obstétrica, es necesario tener a disposición para un adecuado enfoque, monitores al lado del paciente, que permitan inclinar el beneficio hacia la volemiza- ción o al uso de medicamentos vasoactivos. Es en este contexto en donde los monitores de GC mínimamente invasivos y la ecocardiografía al lado del paciente (POCUS) logran reforzar o cambiar la decisión clínica en un momento crítico.
Referencias
1. Say L, Chou D, Gemmill A, Tunçalp Ö, Moller AB, Daniels J, et al. Global causes of maternal death: a WHO systematic analysis. Lancet Glob Health. 2014 Jun;2(6):e323–33. https://doi.org/10.1016/S2214-109X(14)70227-X PMID:25103301
2. Girotra V, Mushambi M. Cuidado crítico materno. 2013; Tutorial 310. University Hospitals, Leicester, UK
3. Héctor J, Lacassie H, Cárdenas A. Anestesia para emergencias en obstetricia. Revista Chilena de Anestesia; 2021. p. 50.
4. Ali A, Lamont RF. Recent advances in the diagnosis and management of sepsis in pregnancy. F1000 Res. 2019 Aug;8:1546. https://doi.org/10.12688/f1000research.18736.1 PMID:31508205
5. Chestnut D, Wong C. Tsen L y cols. 6º Edición. Elsevier España; 2020. pp. 13–77.
6. Albright CM, Has P, Rouse DJ, Hughes BL. Internal Validation of the Sepsis in Obstetrics Score to Identify Risk of Morbidity From Sepsis in Pregnancy. Obstet Gynecol. 2017 Oct;130(4):747–55. https://doi.org/10.1097/AOG.0000000000002260 PMID:28885400
7. Dyer RA, James MF. Maternal hemodynamic monitoring in obstetric anesthesia. Anesthesiology. 2008 Nov;109(5):765–7. https://doi.org/10.1097/ALN.0b013e31818a3825 PMID:18946283
8. Bowyer L, Robinson HL, Barrett H, Crozier TM, Giles M, Idel I, et al. SOMANZ guidelines for the investigation and management sepsis in pregnancy. Aust N Z J Obstet Gynaecol. 2017 Oct;57(5):540–51. https://doi.org/10.1111/ajo.12646 PMID:28670748
9. Vasco M, Pandya S, Van Dyk D, Bishop DG, Wise R, Dyer RA. Maternal critical care in resource-limited settings. Narrative review. Int J Obstet Anesth. 2019 Feb;37:86–95. https://doi.org/10.1016/j.ijoa.2018.09.010 PMID:30482717
10. Shankar-Hari M, Phillips GS, Levy ML, Seymour CW, Liu VX, Deutschman CS, et al.; Sepsis Definitions Task Force. Developing a new definition and assessing new clinical criteria for septic shock: for the Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA. 2016 Feb;315(8):775–87. https://doi.org/10.1001/jama.2016.0289 PMID:26903336
11. Evans L, Rhodes A, Alhazzani W, Antonelli M, Coopersmith CM, French C, et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock 2021. Crit Care Med. 2021 Nov;49(11):e1063–143. https://doi.org/10.1097/CCM.0000000000005337 PMID:34605781
12. Lorello G, Cubillos J, McDonald M, Balki M. Peripartum cardiomyopathy: postpartum decompensation and use of non-invasive cardiac output monitoring. Int J Obstet Anesth. 2014 Feb;23(1):66–70. https://doi.org/10.1016/j.ijoa.2013.10.008 PMID:24360329
13. Castro OJ, Hernández PG, Romero C. Sepsis y falla multiorganica. 3rd ed. Santiago: Ed. Mediterráneo; 2011.
14. Langesæter E, Gibbs M, Dyer RA. The role of cardiac output monitoring in obstetric anesthesia. Curr Opin Anaesthesiol. 2015 Jun;28(3):247–53. https://doi.org/10.1097/ACO.0000000000000190 PMID:25915203
15. Rosseland LA, Hauge TH, Grindheim G, Stubhaug A, Langesæter E. Changes in blood pressure and cardiac output during cesarean delivery: the effects of oxytocin and carbetocin compared with placebo. Anesthesiology. 2013 Sep;119(3):541–51. https://doi.org/10.1097/ALN.0b013e31829416dd PMID:23598289
16. Auler JO Jr, Torres ML, Cardoso MM, Tebaldi TC, Schmidt AP, Kondo MM, et al. Clinical evaluation of the flotrac/Vigileo system for continuous cardiac output monitoring in patients undergoing regional anesthesia for elective cesarean section: a pilot study. Clinics (São Paulo). 2010 Jun;65(8):793–8. https://doi.org/10.1590/S1807-59322010000800010 PMID:20835557
17. Afari HA, Davis EF, Sarma AA. Echocardiography for the Pregnant Heart. Curr Treat Options Cardiovasc Med. 2021;23(8):55. https://doi.org/10.1007/s11936-021-00930-5 PMID:34075291
18. Cabrera Schulmeyer M, Straub A. Utilidad de la ecocardiografía transtorácica focalizada en emergencias hemodinámicas intraoperatorias. Revista Chilena de Anestesia. 2020;49(4):521–7. https://doi.org/10.25237/revchilanestv49n04-08 .
19. Cabrera Schulmeyer M. Ecocardiografía en la sala de urgencias, intensivo y perioperatorio. Revista Chilena de Anestesia. 2021;50(1).
20. Cabrera Schulmeyer M, Araya C. Evaluación ecocardiográfica de la función del ventrículo derecho con doppler tisular luego de una anestesia espinal. Revista Chilena de Anestesia. 2020;49(2):271–6. https://doi.org/10.25237/revchilanestv49n02.12 .
21. Bravo P L, Colmenarez LD, Zambrano Ramón B, Villanueva Gredilla J, Vargas C, Fuentealba R R. Embolia de líquido amniótico. Revista Chilena de Anestesia. 2022;51(2):225–30. https://doi.org/10.25237/revchilanestv5110020951 .
22. Dennis AT. Transthoracic echocardiography in women with preeclampsia. Curr Opin Anaesthesiol. 2015 Jun;28(3):254–60. https://doi.org/10.1097/ACO.0000000000000182 PMID:25812006

 ORCID
ORCID